E2F1 - E2F1
Эта статья может быть слишком техническим для большинства читателей, чтобы понять. Пожалуйста помогите улучшить это к сделать понятным для неспециалистов, не снимая технических деталей. (Декабрь 2018 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
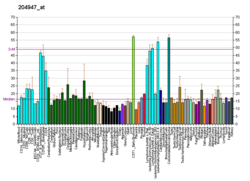
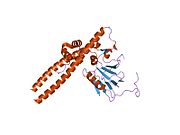
Фактор транскрипции E2F1 это белок что у людей кодируется E2F1 ген.[5]
Функция
Белок, кодируемый этим геном, является членом семейства E2F факторы транскрипции. Семейство E2F играет решающую роль в управлении клеточный цикл и действие подавитель опухолей белков, а также является мишенью для трансформирующих белков небольших ДНК опухолевых вирусов. Белки E2F содержат несколько эволюционно консервативных доменов, обнаруженных у большинства членов этого семейства. Эти домены включают ДНК-связывающий домен, домен димеризации, который определяет взаимодействие с регулируемыми дифференцировкой белками факторов транскрипции (DP), доменом трансактивации, обогащенным кислыми аминокислотами, и доменом ассоциации белка-супрессора опухоли, который встроен в домен трансактивации. Этот белок и еще 2 члена, E2F2 и E2F3, имеют дополнительный связывающий циклин домен. Этот белок связывается преимущественно с белок ретинобластомы pRB в зависимости от клеточного цикла. Он может опосредовать как пролиферацию клеток, так и p53 -зависимый / независимый апоптоз.[6]
Транскрипция
Промотор E2F1 [PAX8] => E2F1 PMID 21602887
Взаимодействия
E2F1 был показан взаимодействовать с:
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000101412 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000027490 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Нойман Э., Селлерс В. Р., Макнил Дж. А., Лоуренс Дж. Б., Келин В. Г. (декабрь 1996 г.). «Структура и частичная геномная последовательность гена E2F1 человека». Ген. 173 (2): 163–9. Дои:10.1016/0378-1119(96)00184-9. PMID 8964493.
- ^ «Ген Entrez: фактор транскрипции E2F1 E2F 1».
- ^ а б Сузуки М., Окуяма С., Окамото С., Ширасуна К., Накадзима Т., Хачия Т., Нодзима Х., Секия С., Ода К. (август 1998 г.). «Новый связывающий E2F белок с мотивом HLH Myc-типа стимулирует E2F-зависимую транскрипцию путем образования гетеродимера». Онкоген. 17 (7): 853–65. Дои:10.1038 / sj.onc.1202163. PMID 9780002.
- ^ а б Марти А., Вирбелауэр С., Шеффнер М., Крек В. (май 1999 г.). «Взаимодействие между убиквитин-протеинлигазой SCFSKP2 и E2F-1 лежит в основе регуляции деградации E2F-1». Nat. Cell Biol. 1 (1): 14–9. Дои:10.1038/8984. PMID 10559858. S2CID 8884226.
- ^ Ян Р., Мюллер С., Хюин В., Фунг Ю.К., Йи А.С., Кёффлер Х.П. (март 1999 г.). «Функции циклина A1 в клеточном цикле и его взаимодействия с фактором транскрипции E2F-1 и белками семейства Rb». Мол. Клетка. Биол. 19 (3): 2400–7. Дои:10.1128 / mcb.19.3.2400. ЧВК 84032. PMID 10022926.
- ^ Сюй М., Шеппард К.А., Пэн С.Й., Йи А.С., Пивница-Вормс Х. (декабрь 1994 г.). «Циклин A / CDK2 связывается непосредственно с E2F-1 и ингибирует ДНК-связывающую активность E2F-1 / DP-1 путем фосфорилирования». Мол. Клетка. Биол. 14 (12): 8420–31. Дои:10.1128 / MCB.14.12.8420. ЧВК 359381. PMID 7969176.
- ^ Вандель Л., Кузаридес Т. (август 1999 г.). «Остатки, фосфорилированные TFIIH, необходимы для разложения E2F-1 во время S-фазы». EMBO J. 18 (15): 4280–91. Дои:10.1093 / emboj / 18.15.4280. ЧВК 1171504. PMID 10428966.
- ^ Strachan GD, Jordan-Sciutto KL, Rallapalli R, Tuan RS, Hall DJ (февраль 2003 г.). «Фактор транскрипции E2F-1 негативно регулируется своим взаимодействием с белком MDMX». J. Cell. Биохим. 88 (3): 557–68. Дои:10.1002 / jcb.10318. PMID 12532331. S2CID 38805122.
- ^ Kong HJ, Yu HJ, Hong S, Park MJ, Choi YH, An WG, Lee JW, Cheong J (ноябрь 2003 г.). «Взаимодействие и функциональное сотрудничество усиливаемого раком транскрипционного коактиватора, активирующего сигнал коинтегратора-2 и E2F-1 в пролиферации клеток». Мол. Рак Res. 1 (13): 948–58. PMID 14638867.
- ^ а б Таниура Х., Танигучи Н., Хара М., Йошикава К. (январь 1998 г.). «Некдин, постмитотический нейрон-специфический супрессор роста, взаимодействует с вирусными трансформирующими белками и клеточным фактором транскрипции E2F1». J. Biol. Chem. 273 (2): 720–8. Дои:10.1074 / jbc.273.2.720. PMID 9422723.
- ^ Кувако К., Таниура Х, Йошикава К. (январь 2004 г.). «Связанные с некдином белки MAGE по-разному взаимодействуют с фактором транскрипции E2F1 и рецептором нейротрофина p75». J. Biol. Chem. 279 (3): 1703–12. Дои:10.1074 / jbc.M308454200. PMID 14593116.
- ^ Sansal I, Dupont E, Toru D, Evrard C, Rouget P (октябрь 2000 г.). «NPDC-1, регулятор пролиферации и дифференцировки нервных клеток, взаимодействует с E2F-1, снижает его связывание с ДНК и модулирует его транскрипционную активность». Онкоген. 19 (43): 5000–9. Дои:10.1038 / sj.onc.1203843. PMID 11042687.
- ^ Дарбинян Н., Галлия Г.Л., Кунду М., Щербик Н., Третьякова А., Джордано А., Халили К. (ноябрь 1999 г.). «Ассоциация Pur alpha и E2F-1 подавляет транскрипционную активность E2F-1». Онкоген. 18 (46): 6398–402. Дои:10.1038 / sj.onc.1203011. PMID 10597240.
- ^ Джоши Б., Ко Д., Ордонез-Эркан Д., Челлаппан С. П. (декабрь 2003 г.). «Предполагаемого спирального домена запретитина достаточно для репрессии опосредованной E2F1 транскрипции и индукции апоптоза». Biochem. Биофиз. Res. Сообщество. 312 (2): 459–66. Дои:10.1016 / j.bbrc.2003.10.148. PMID 14637159.
- ^ Fusaro G, Dasgupta P, Rastogi S, Joshi B, Chellappan S (ноябрь 2003 г.). «Prohibitin индуцирует транскрипционную активность p53 и экспортируется из ядра при передаче сигналов апоптоза». J. Biol. Chem. 278 (48): 47853–61. Дои:10.1074 / jbc.M305171200. PMID 14500729.
- ^ Ван С., Чжан Б., Фаллер Д.В. (июнь 2002 г.). «Prohibitin требует Brg-1 и Brm для подавления E2F и роста клеток». EMBO J. 21 (12): 3019–28. Дои:10.1093 / emboj / cdf302. ЧВК 126057. PMID 12065415.
- ^ Ван С., Нат Н., Фусаро Г., Челлаппан С. (ноябрь 1999 г.). «Rb и запретитин нацелены на отдельные области E2F1 для репрессии и отвечают на различные восходящие сигналы». Мол. Клетка. Биол. 19 (11): 7447–60. Дои:10.1128 / mcb.19.11.7447. ЧВК 84738. PMID 10523633.
- ^ а б Дайсон Н., Дембски М., Фаттей А., Нгву С., Юэн М., Хелин К. (декабрь 1993 г.). «Анализ p107-ассоциированных белков: p107 ассоциирует с формой E2F, которая отличается от pRB-ассоциированного E2F-1». Дж. Вирол. 67 (12): 7641–7. Дои:10.1128 / JVI.67.12.7641-7647.1993. ЧВК 238233. PMID 8230483.
- ^ Николас Э., Айт-Си-Али С., Труш Д. (август 2001 г.). «Гистондеацетилаза HDAC3 нацеливает RbAp48 на белок ретинобластомы». Нуклеиновые кислоты Res. 29 (15): 3131–6. Дои:10.1093 / nar / 29.15.3131. ЧВК 55834. PMID 11470869.
- ^ Пардо П.С., Люнг Дж. К., Луччези Дж. К., Перейра-Смит О. М. (декабрь 2002 г.). «MRG15, новый белок хромодомена, присутствует в двух различных мультибелковых комплексах, участвующих в активации транскрипции». J. Biol. Chem. 277 (52): 50860–6. Дои:10.1074 / jbc.M203839200. PMID 12397079.
- ^ а б Choubey D, Li SJ, Datta B, Gutterman JU, Lengyel P (октябрь 1996 г.). «Ингибирование E2F-опосредованной транскрипции с помощью p202». EMBO J. 15 (20): 5668–78. Дои:10.1002 / j.1460-2075.1996.tb00951.x. ЧВК 452311. PMID 8896460.
- ^ Fajas L, Paul C, Zugasti O, Le Cam L, Polanowska J, Fabbrizio E, Medema R, Vignais ML, Sardet C (июль 2000 г.). «pRB связывается и модулирует трансрепрессирующую активность E1A-регулируемого фактора транскрипции p120E4F». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 97 (14): 7738–43. Bibcode:2000PNAS ... 97.7738F. Дои:10.1073 / pnas.130198397. ЧВК 16614. PMID 10869426.
- ^ а б Ву С.Л., Цукерберг Л.Р., Нгву К., Харлоу Е., Лис Дж. А. (май 1995 г.). «Связь in vivo белков семейства E2F и DP». Мол. Клетка. Биол. 15 (5): 2536–46. Дои:10.1128 / mcb.15.5.2536. ЧВК 230484. PMID 7739537.
- ^ а б c d Rotheneder H, Geymayer S, Haidweger E (ноябрь 1999 г.). «Факторы транскрипции семейства Sp1: взаимодействие с E2F и регуляция промотора мышиной тимидинкиназы». J. Mol. Биол. 293 (5): 1005–15. Дои:10.1006 / jmbi.1999.3213. PMID 10547281.
- ^ Lin SY, Black AR, Kostic D, Pajovic S, Hoover CN, Azizkhan JC (апрель 1996 г.). «Регулируемая клеточным циклом ассоциация E2F1 и Sp1 связана с их функциональным взаимодействием». Мол. Клетка. Биол. 16 (4): 1668–75. Дои:10.1128 / MCB.16.4.1668. ЧВК 231153. PMID 8657142.
- ^ Карлседер Дж., Ротенедер Х., Винтерсбергер Э. (апрель 1996 г.). «Взаимодействие Sp1 с фактором транскрипции E2F, регулируемым ростом и клеточным циклом». Мол. Клетка. Биол. 16 (4): 1659–67. Дои:10.1128 / mcb.16.4.1659. ЧВК 231152. PMID 8657141.
- ^ Сардет К., Видал М., Кобриник Д., Гэн Й., Онуфрик С., Чен А., Вайнберг Р.А. (март 1995 г.). «E2F-4 и E2F-5, два члена семейства E2F, экспрессируются на ранних фазах клеточного цикла». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 92 (6): 2403–7. Bibcode:1995PNAS ... 92.2403S. Дои:10.1073 / пнас.92.6.2403. ЧВК 42492. PMID 7892279.
- ^ Хелин К., Ву К.Л., Фаттей А.Р., Лис Дж. А., Динлахт Б. Д., Нгву К., Харлоу Э. (октябрь 1993 г.). «Гетеродимеризация факторов транскрипции E2F-1 и DP-1 приводит к совместной трансактивации». Genes Dev. 7 (10): 1850–61. Дои:10.1101 / gad.7.10.1850. PMID 8405995.
- ^ Лю К., Линь Ф.Т., Рупперт Дж. М., Линь В. К. (май 2003 г.). «Регулирование E2F1 с помощью белка TopBP1, содержащего домен BRCT». Мол. Клетка. Биол. 23 (9): 3287–304. Дои:10.1128 / mcb.23.9.3287-3304.2003. ЧВК 153207. PMID 12697828.
- ^ Yu X, Chini CC, He M, Mer G, Chen J (октябрь 2003 г.). «Домен BRCT представляет собой домен, связывающий фосфо-белок». Наука. 302 (5645): 639–42. Bibcode:2003Наука ... 302..639Y. Дои:10.1126 / science.1088753. PMID 14576433. S2CID 29407635.
- ^ Чжоу Ф, Чжан Л., Ван А, Сонг Б., Гонг К., Чжан Л., Ху М., Чжан Х, Чжао Н., Гонг Y (май 2008 г.). «Связь GSK3 beta с E2F1 способствует дифференцировке нервных клеток, индуцированной фактором роста нервов». J. Biol. Chem. 283 (21): 14506–15. Дои:10.1074 / jbc.M706136200. PMID 18367454.
дальнейшее чтение
- Dupont E, Sansal I, Toru D, Evrard C, Rouget P (1997). «[Идентификация NPDC-1, гена, участвующего в контроле пролиферации и дифференцировки нейральных и глиальных предшественников]». C. R. Séances Soc. Биол. Fil. 191 (1): 95–104. PMID 9181131.
- Стивенс К., Ла Танге Н.Б. (2005). «Возникающая роль E2F-1 в ответе на повреждение ДНК и контроле контрольных точек». Ремонт ДНК (Amst.). 3 (8–9): 1071–9. Дои:10.1016 / j.dnarep.2004.03.034. PMID 15279795.
- Чжан З., Ван Х., Ли М., Рейберн Э., Агравал С., Чжан Р. (2006). «Новые р53-независимые функции MDM2, идентифицированные с помощью технологий подавления РНК». Анна. Акад. Наука. 1058 (1): 205–14. Дои:10.1196 / летопись.1359.030. PMID 16394138. S2CID 35683657.
- Шильд С., Вирт М., Райхерт М., Шмид Р.М., Заур Д., Шнайдер Г. (июль 2009 г.). «Передача сигналов PI3K поддерживает экспрессию c-myc для регулирования транскрипции E2F1 в клетках рака поджелудочной железы». Мол. Канцероген. 48 (12): 1149–58. Дои:10.1002 / mc.20569. PMID 19603422. S2CID 41545085.
внешняя ссылка
- E2F1 + белок, + человеческий в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- FactorBook E2F1
Эта статья включает текст из Национальная медицинская библиотека США, который находится в всеобщее достояние.