Этинодиол диацетат - Etynodiol diacetate
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Континуин, Демулен, Фемулен, Лютеонорм, Луто-Метродиол, Метродиол, Овулен и др. |
| Другие имена | Этинодиол диацетат; Диацетат норэтиндрола; 3β-гидроксиноэтистерон, 3β, 17β-диацетат;[1] 17α-этинилэстр-4-ен-3β, 17β-диилдиацетат; CB-8080; SC-11800 |
| Маршруты администрация | Устно |
| Класс препарата | Прогестаген; Прогестин; Эфир прогестагена |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Идентификаторы | |
| |
| Количество CAS |
|
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.005.496 |
| Химические и физические данные | |
| Формула | C24ЧАС32О4 |
| Молярная масса | 384.516 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
Этинодиол диацетат, или же этинодиол диацетат, продается под торговыми марками Демулен и Фемулен среди прочего, это прогестин лекарство, которое используется в противозачаточные таблетки.[2][3][4] Препарат доступен только в сочетании с эстроген.[5] Принято устно.[6]
Этинодиола диацетат - это прогестин или синтетический прогестаген, и, следовательно, является агонист из рецептор прогестерона, то биологическая мишень прогестагенов, таких как прогестерон.[7][8] Имеет слабый андрогенный и эстрогенный активность и ничего другого важного гормональный Мероприятия.[9][10][11] Лекарство - это пролекарство из норэтистерон в теле, с этинодиол происходит как средний.[7][8][12]
Этинодиол, родственное соединение, было открыто в 1954 году, а этинодиол диацетат был представлен для медицинского применения в 1965 году.[13][14] Лекарство остается доступным сегодня только в Соединенные Штаты, Канада, и несколько других стран.[4][5]
Медицинское использование
Этинодиола диацетат используется в сочетании с эстроген Такие как этинилэстрадиол или же местранол в комбинированные оральные контрацептивы для женщин.[6]
Побочные эффекты
Фармакология

Этинодиола диацетат практически неактивен с точки зрения близость для прогестерон и рецепторы андрогенов и действует как быстро преобразованный пролекарство из норэтистерон, с этинодиол происходит как средний.[7][8][12] На пероральное введение и во время метаболизм первого прохождения в печень, диацетат этинодиола быстро превращается эстеразы в этинодиол,[12] за которым следует оксигенация C3 гидроксильная группа производить норэтистерон.[8] Помимо прогестагенной активности, этинодиол диацетат обладает слабым андрогенный Мероприятия,[9][10] и, в отличие от большинства прогестинов, но аналогично норэтистерону и норэтинодрел,[15] также есть некоторые эстрогенный Мероприятия.[10][11]
В фармакокинетика диацетата этинодиола.[16]
| Сложный | Типа | PR | AR | ER | GR | МИСТЕР | SHBG | CBG |
|---|---|---|---|---|---|---|---|---|
| Норэтистерон | – | 67–75 | 15 | 0 | 0–1 | 0–3 | 16 | 0 |
| 5α-дигидроноретистерон | Метаболит | 25 | 27 | 0 | 0 | ? | ? | ? |
| 3α, 5α-тетрагидроноретистерон | Метаболит | 1 | 0 | 0–1 | 0 | ? | ? | ? |
| 3α, 5β-тетрагидроноретистерон | Метаболит | ? | 0 | 0 | ? | ? | ? | ? |
| 3β, 5α-Тетрагидроноретистерон | Метаболит | 1 | 0 | 0–8 | 0 | ? | ? | ? |
| Этинилэстрадиол | Метаболит | 15–25 | 1–3 | 112 | 1–3 | 0 | 0.18 | 0 |
| Норэтистерона ацетат | Пролекарство | 20 | 5 | 1 | 0 | 0 | ? | ? |
| Норэтистерона энантат | Пролекарство | ? | ? | ? | ? | ? | ? | ? |
| Норетинодрел | Пролекарство | 6 | 0 | 2 | 0 | 0 | 0 | 0 |
| Этинодиол | Пролекарство | 1 | 0 | 11–18 | 0 | ? | ? | ? |
| Этинодиол диацетат | Пролекарство | 1 | 0 | 0 | 0 | 0 | ? | ? |
| Линестренол | Пролекарство | 1 | 1 | 3 | 0 | 0 | ? | ? |
| Примечания: Значения указаны в процентах (%). Ссылка лиганды (100%) были промегестон для PR, метриболон для AR, эстрадиол для ER, дексаметазон для GR, альдостерон для МИСТЕР, дигидротестостерон за SHBG, и кортизол за CBG. Сноски: а = Активный или неактивный метаболит, пролекарство, или ни один из норэтистерона. Источники: См. Шаблон. | ||||||||
Химия
Этинодиол диацетат, также известный как 3β-гидрокси-17α-этинил-19-нортестостерон 3β, 17β-диацетат, 3β-гидроксиноэтистерон 3β, 17β-диацетат или 17α-этинилэстр-4-ен-3β, 17β-диол 3β, 17β- диацетат, представляет собой синтетический эстран стероидный препарат и производная из тестостерон.[1][3][4] Это, в частности, производное от 19-нортестостерон и 17α-этинилтестостерон, или из норэтистерон (17α-этинил-19-нортестостерон), в котором C3 кетон группа был дегидрированный в C3β гидроксил группа и ацетат сложные эфиры были прикреплены в положениях C3β и C17β.[3][4] Этинодиола диацетат представляет собой 3β, 17β-диацетат сложный эфир из этинодиол (17α-этинилэстр-4-ен-3β, 17β-диол).[3][4]
Синтез
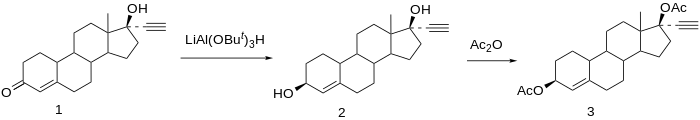
Химический синтез диацетата этинодиола.[16]
Сокращение норэтистерон (1) дает 3,17-диол. 3 -гидроксисоединение является желаемым продуктом; так как реакции на C3 не показывают почти стереоселективность как и у С17, из-за относительного отсутствия стереонаправляющих ближайших заместителей, образование желаемого изомера вызывается использованием объемного восстановителя, три-трет-бутоксиалюминийгидрида лития. Ацетилирование 3β, 17β-диола дает диацетат этинодиола (3).[17]
История
Этинодиол был первым синтезированный в 1954 г., через снижение из норэтистерон, а диацетат этинодиола был введен для использования в медицине в 1965 году.[13][14]
Общество и культура
Родовые имена
Этинодиол диацетат это родовое имя препарата ( ГОСТИНИЦА формы свободного алкоголя этинодиол), пока этинодиол диацетат это его USAN, БАН, и ЯНВАРЬ.[3][4][5] Он также известен под кодовыми названиями CB-8080 и SC-11800.[3][4][5]
Фирменные наименования
Диацетат этинодиола продается или продавался под торговыми марками, включая Conova, Continuin, Demulen, Femulen, Kelnor, Luteonorm, Luto-Metrodiol, Metrodiol, Ovulen, Soluna, Zovia и другие.[3][4][5]
Доступность
Этинодиола диацетат по-прежнему продается только в нескольких странах, включая Соединенные Штаты, Канада, Аргентина, и Оман.[5]
Рекомендации
- ^ а б Шиндлер, Адольф Э; Кампаньоли, Карло; Друкманн, Рене; Хубер, Йоханнес; Паскуалини, Хорхе Р.; Швеппе, Карл В. Тийссен, Джос Х.Х. (2003). «Классификация и фармакология прогестинов». Maturitas. 46: 7–16. Дои:10.1016 / j.maturitas.2003.09.014. ISSN 0378-5122. PMID 14670641.
- ^ Донна Шоуп; Флоренс П. Хазелтин (6 декабря 2012 г.). Контрацепция. Springer Science & Business Media. С. 21–. ISBN 978-1-4612-2730-4.
- ^ а б c d е ж грамм Дж. Элкс (14 ноября 2014 г.). Словарь лекарственных средств: химические данные: химические данные, структуры и библиографии. Springer. С. 522–. ISBN 978-1-4757-2085-3.
- ^ а б c d е ж грамм час Index Nominum 2000: Международный справочник лекарственных средств. Тейлор и Фрэнсис США. 2000. с. 422. ISBN 978-3-88763-075-1. Получено 30 мая 2012.
- ^ а б c d е ж https://www.drugs.com/international/etynodiol.html
- ^ а б Роберт В. Блюм (22 октября 2013 г.). Здравоохранение подростков: клинические вопросы. Elsevier Science. С. 216–. ISBN 978-1-4832-7738-7.
- ^ а б c Хаммерштейн Дж (1990). «Пролекарства: преимущество или недостаток?». Являюсь. J. Obstet. Гинеколь. 163 (6, п. 2): 2198–203. Дои:10.1016 / 0002-9378 (90) 90561-К. PMID 2256526.
- ^ а б c d Рабочая группа МАИР по оценке канцерогенных рисков для человека; Всемирная организация здоровья; Международное агентство по изучению рака (2007 г.). Комбинированные эстроген-прогестагенные контрацептивы и комбинированная эстроген-прогестагеновая терапия менопаузы. Всемирная организация здоровья. С. 146–. ISBN 978-92-832-1291-1.
- ^ а б Армен Геннадьевич Ташджян; Эрин Дж. Армстронг (21 июля 2011 г.). Принципы фармакологии: патофизиологические основы лекарственной терапии. Липпинкотт Уильямс и Уилкинс. С. 523–. ISBN 978-1-4511-1805-6.
- ^ а б c Кеннет Л. Беккер (24 апреля 2001 г.). Принципы и практика эндокринологии и метаболизма. Липпинкотт Уильямс и Уилкинс. п. 1004. ISBN 978-0-7817-1750-2. Получено 30 мая 2012.
- ^ а б Аллан Х. Горолл; Альберт Г. Малли (27 января 2009 г.). Первичная медицина: офисная оценка и ведение взрослого пациента. Липпинкотт Уильямс и Уилкинс. п. 876. ISBN 978-0-7817-7513-7. Получено 30 мая 2012.
- ^ а б c Станчик Ф.З. (2002). «Фармакокинетика и эффективность прогестинов, используемых для заместительной гормональной терапии и контрацепции». Rev Endocr Metab Disord. 3 (3): 211–24. Дои:10.1023 / А: 1020072325818. PMID 12215716. S2CID 27018468.
- ^ а б Прогресс в медицинской химии. Баттерворт-Хайнеманн. 21 сентября 2011. С. 180–. ISBN 978-0-08-086256-9.
- ^ а б Издательство William Andrew (22 октября 2013 г.). Энциклопедия фармацевтического производства, 3-е издание. Эльзевир. С. 1516–. ISBN 978-0-8155-1856-3.
- ^ Бенно Клеменс Руннебаум; Томас Рабе; Людвиг Кизель (6 декабря 2012 г.). Женская контрацепция: новости и тенденции. Springer Science & Business Media. С. 36–. ISBN 978-3-642-73790-9.
- ^ а б Die Gestagene. Springer-Verlag. 27 ноября 2013. С. 14–15, 286. ISBN 978-3-642-99941-3.
- ^ а б Климстра, П .; Колтон, Ф. (1967). «Синтез 3β-гидроксиэстр-4-ен-17-она и 3β-гидроксиандрост-4-ен-17-она». Стероиды. 10 (4): 411–424. Дои:10.1016 / 0039-128X (67) 90119-5. PMID 6064262.
- ^ Sondheimer, F .; Клибанский Ю. (1959). «Синтез 3β-гидроксианалогов стероидных гормонов, биологически активного класса соединений». Тетраэдр. 5: 15–26. Дои:10.1016/0040-4020(59)80066-1.
