Глюкоза - Glucose
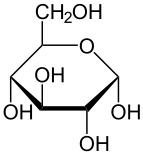
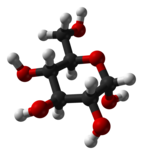
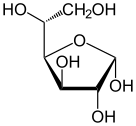
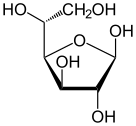
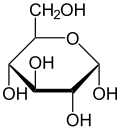 Проекция Хаворта из α-d-глюкопираноза | |
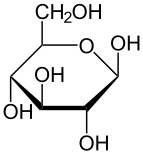
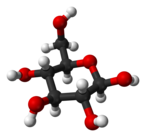
 Проекция Фишера из d-глюкоза | |
| Имена | |
|---|---|
| Произношение | /ˈɡлukoʊz/, /ɡлukoʊs/ |
| Имена ИЮПАК Систематическое название: (2р,3S,4р,5р) -2,3,4,5,6-Пентагидроксигексаналь разрешены тривиальные имена: | |
| Предпочтительное название IUPAC ПИН-коды не используются для натуральных продуктов. | |
| Другие имена Содержание сахара в крови Декстроза Кукурузный сахар d-Глюкоза Виноградный сахар | |
| Идентификаторы | |
3D модель (JSmol ) | |
| 3DMet | |
| Сокращения | Glc |
| 1281604 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| Номер ЕС |
|
| 83256 | |
| КЕГГ | |
| MeSH | Глюкоза |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| |
| |
| Характеристики | |
| C6ЧАС12О6 | |
| Молярная масса | 180.156 г / моль |
| Внешность | белый порошок |
| Плотность | 1,54 г / см3 |
| Температура плавления | α-d-Глюкоза: 146 ° C (295 ° F, 419 K) β-d-Глюкоза: 150 ° C (302 ° F, 423 K) |
| 909 г / л (25 ° C (77 ° F)) | |
| −101.5×10−6 см3/ моль | |
| 8.6827 | |
| Термохимия | |
Теплоемкость (C) | 218,6 Дж / (К · моль)[1] |
Стандартный моляр энтропия (S | 209,2 Дж / (К · моль)[1] |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | −1271 кДж / моль[2] |
| 2,805 кДж / моль (670 ккал / моль) | |
| Фармакология | |
| B05CX01 (ВОЗ) V04CA02 (ВОЗ), V06DC01 (ВОЗ) | |
| Опасности | |
| Паспорт безопасности | ICSC 08655 |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Глюкоза это простой сахар с молекулярная формула C6ЧАС12О6. Глюкоза - самая распространенная моносахарид,[3] подкатегория углеводы. Глюкоза в основном производится растения и большинство водоросли в течение фотосинтез из воды и углекислого газа, используя энергию солнечного света, где он используется для производства целлюлоза в клеточные стенки, который является наиболее распространенным углеводом.[4] В энергетический обмен, глюкоза - самый важный источник энергии во всех организмы. Глюкоза для обмена веществ сохраняется в виде полимер, у растений в основном как крахмал и амилопектин, а у животных как гликоген. Глюкоза циркулирует в крови животных как содержание сахара в крови. Встречающаяся в природе форма глюкозы - это d-глюкоза, а л-глюкоза производится синтетическим путем в сравнительно небольших количествах и имеет меньшее значение. Глюкоза представляет собой моносахарид, содержащий шесть атомов углерода и альдегидную группу, и поэтому альдогексоза. Молекула глюкозы может существовать в форме с открытой цепью (ациклической), а также в кольцевой (циклической) форме. Глюкоза встречается в природе и в свободном состоянии содержится во фруктах и других частях растений. У животных глюкоза высвобождается в результате распада гликогена в процессе, известном как гликогенолиз.
Глюкоза, как внутривенный раствор сахара, на Список основных лекарственных средств Всемирной организации здравоохранения, самые безопасные и эффективные лекарства, необходимые в система здоровья.[5] Он также находится в списке в сочетании с хлоридом натрия.[5]
Название глюкоза происходит от французского от Греческий γλυκός ('глюкос'), что означает «сладкий», в отношении должен, сладкий, первый отжим винограда при изготовлении вино.[6][7] Суффикс "-оза "- химический классификатор, обозначающий сахар.
История
Глюкоза была впервые выделена из изюм в 1747 г. немецким химиком Андреас Маргграф.[8][9] Глюкоза была обнаружена в винограде Иоганн Тобиас Ловиц в 1792 г. и признан отличным от тростникового сахара (сахарозы). Глюкоза - это термин, придуманный Жан Батист Дюма в 1838 г., который преобладал в химической литературе. Фридрих Август Кекуле предложил термин декстроза (от латинского dexter = право), потому что в водном растворе глюкозы плоскость линейно поляризованного света повернута вправо. В отличие, d-фруктоза (кетогексоза) и л-глюкоза повернуть линейно поляризованный свет влево. Прежние обозначения по вращению плоскости линейно поляризованного света (d и л-номенклатура) позже отказались в пользу d- и л-отношение, которое относится к абсолютной конфигурации асимметричного центра, наиболее удаленного от карбонильной группы, и в соответствии с конфигурацией d- или же л-глицеральдегид.[10][11]
Поскольку глюкоза является основной потребностью многих организмов, правильное понимание ее химический макияж и структура внесли большой вклад в общее продвижение органическая химия. Это понимание произошло во многом в результате исследований Эмиль Фишер, немецкий химик, получивший в 1902 г. Нобелевская премия по химии за его находки.[12] Синтез глюкозы установил структуру органического материала и, следовательно, стал первым окончательным подтверждением Якобус Хенрикус ван 'т Хофф теории химической кинетики и расположения химических связей в углеродсодержащих молекулах.[13] Между 1891 и 1894 годами Фишер установил стереохимическую конфигурацию всех известных сахаров и правильно предсказал возможные изомеры, применяя теорию асимметричных атомов углерода Ван 'т Гоффа. Названия изначально относились к натуральным веществам. Их энантиомеры получили одно и то же название с введением систематической номенклатуры с учетом абсолютной стереохимии (например, номенклатура Фишера, d/л номенклатура).
За открытие метаболизма глюкозы Отто Мейерхоф получил Нобелевская премия по физиологии и медицине в 1922 г.[14] Ганс фон Эйлер-Челпин был удостоен Нобелевской премии по химии вместе с Артур Харден в 1929 г. за «исследования ферментации сахара и их доли ферментов в этом процессе».[15][16] В 1947 г. Бернардо Хуссе (за открытие роли гипофиза в метаболизме глюкозы и производных углеводов), а также Карл и Герти Кори (за открытие превращения гликогена из глюкозы) получил Нобелевскую премию по физиологии и медицине.[17][18][19] В 1970 г. Луис Лелуар был удостоен Нобелевской премии по химии за открытие сахарных нуклеотидов, полученных из глюкозы, в биосинтезе углеводов.[20]
Химические свойства
С шестью атомами углерода он классифицируется как гексоза, подкатегория моносахаридов. d-Глюкоза одна из шестнадцати альдогексоза стереоизомеры. В d-изомер, d-глюкоза, также известная как декстроза, широко встречается в природе, но л-изомер, л-глюкоза, не. Глюкозу можно получить гидролиз углеводов, таких как молочный сахар (лактоза ), тростниковый сахар (сахароза ), мальтоза, целлюлоза, гликоген и т. д. Декстроза обычно коммерчески производится из кукурузного крахмала в США и Японии, из картофельного и пшеничного крахмала в Европе и из крахмал тапиоки в тропических регионах.[21] В производственном процессе используется гидролиз путем пропаривания под давлением при контролируемой температуре. pH в струе с последующей ферментативной деполимеризацией.[22] Несвязанная глюкоза - один из основных ингредиентов медовый. Все формы глюкозы бесцветны и легко растворяются в воде, уксусная кислота, и несколько других растворителей. Они мало растворимы в метанол и этиловый спирт.
Структура и номенклатура
Глюкоза - это моносахарид с формулой C6ЧАС12О6 или H− (C = O) - (CHOH)5−H, пять гидроксил (ОН) -группы определенным образом расположены вдоль его шести-углерод назад. Глюкоза обычно присутствует в твердой форме в виде моногидрат с закрытым пиран кольцо (гидрат декстрозы). В водном растворе, с другой стороны, он представляет собой открытую цепь в небольшой степени и присутствует преимущественно в виде α- или β-пираноза, которые частично взаимно сливаются мутаротация. Из водных растворов можно кристаллизовать три известные формы: α-глюкопиранозу, β-глюкопиранозу и гидрат β-глюкопиранозы.[23] Глюкоза - это строительный блок дисахаридов. лактоза и сахароза (тростниковый или свекольный сахар), из олигосахариды Такие как рафиноза и полисахаридов, таких как крахмал и амилопектин, гликоген или же целлюлоза. В температура стеклования глюкозы составляет 31 ° C, а постоянная Гордона – Тейлора (экспериментально определенная константа для предсказания температуры стеклования для различных массовых долей смеси двух веществ)[24] составляет 4,5.[25]
| Различные формы и проекции d-глюкоза в сравнении | ||
|---|---|---|
| Натта проекция | Проекция Хаворта | |
 |  α-d-глюкофураноза | 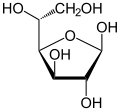 β-d-глюкофураноза |
 α-d-глюкопираноза |  β-d-глюкопираноза | |
| α-d-Глюкопираноза в (1) Толленс / Фишер (2) проекция Хаворта (3) конформация кресла (4) стереохимический вид | ||
 | ||
Форма открытой цепи

В его мимолетном открытая цепь форме молекула глюкозы имеет открытую (в отличие от циклический ) и неразветвленный остов из шести атомов углерода, от C-1 до C-6; где C-1 является частью альдегидная группа H (C = O) -, и каждый из пяти других атомов углерода несет одну гидроксильную группу -OH. Остальные облигации основных углеродов удовлетворяются водород атомы -H. Следовательно, глюкоза является одновременно гексоза и альдоза, или альдогексоза. Альдегидная группа превращает глюкозу в снижения сахара дает положительную реакцию с Тест Фелинга.
Каждый из четырех атомов углерода с C-2 по C-5 является стереоцентр, что означает, что его четыре связи соединяются с четырьмя разными заместителями. (Углерод C-2, например, соединяется с - (C = O) H, -OH, -H и - (CHOH)4З.) В d-глюкоза, эти четыре части должны быть в определенном трехмерном расположении. А именно, когда молекула нарисована в Проекция Фишера, гидроксилы на C-2, C-4 и C-5 должны быть на правой стороне, а гидроксилы на C-3 должны быть на левой стороне.
Положения этих четырех гидроксилов в точности обратны на диаграмме Фишера. л-глюкоза. d- и л-глюкоза - два из 16 возможных альдогексозов; остальные 14 аллозе, Altrose, галактоза, Gulose, идоз, манноза, и таран, в каждом по два энантиомеры, “d-" и "л-”.
Важно отметить, что линейная форма глюкозы составляет менее 0,02% молекул глюкозы в водном растворе. Остальное - одна из двух циклических форм глюкозы, которые образуются, когда гидроксильная группа на углероде 5 (C5) связывается с альдегидным углеродом 1 (C1).
Циклические формы
.
Слева направо: Прогнозы Хаворта и клюшка структуры α- и β- аномеры из D-глюкопираноза (верхний ряд) и D-глюкофураноза (нижний ряд)
В растворах форма глюкозы с открытой цепью (либо "D-" или же "L- ") существует в равновесии с несколькими циклические изомеры, каждая из которых содержит кольцо атомов углерода, замкнутое одним атомом кислорода. Однако в водном растворе более 99% молекул глюкозы в любой момент времени существуют в виде пираноза формы. Форма с открытой цепью ограничена примерно 0,25%, и фураноза формы существуют в незначительных количествах. Термины «глюкоза» и «D-глюкоза »обычно также используются для этих циклических форм. Кольцо образуется из формы с открытой цепью внутримолекулярной нуклеофильное присоединение реакция между альдегидной группой (у C-1) и гидроксильной группой C-4 или C-5 с образованием полуацеталь связь, -C (OH) H-O-.
Реакция между C-1 и C-5 дает шестичленный гетероциклический система, называемая пираноза, которая представляет собой моносахаридный сахар (отсюда «-оза»), содержащий производные пиран скелет. Реакция (гораздо реже) между C-1 и C-4 дает пятичленное кольцо фуранозы, названное в честь циклического эфира. фуран. В любом случае к каждому атому углерода в кольце присоединены один водород и один гидроксил, за исключением последнего атома углерода (C-4 или C-5), где гидроксил заменен остатком открытой молекулы (которая представляет собой - (C ( CH2OH) HOH) -H или - (CHOH) -H соответственно).
Реакция замыкания кольца делает углерод C-1 хиральный также, поскольку его четыре связи приводят к -H, к -OH, к углероду C-2 и кольцевому кислороду. Эти четыре части молекулы могут быть расположены вокруг C-1 ( аномерный углерод ) двумя разными способами, обозначаемыми префиксами «α-» и «β-». Когда молекула глюкопиранозы нарисована в Проекция Хаворта, обозначение «α-» означает, что гидроксильная группа, присоединенная к C-1 и -CH2Группа OH в C-5 лежит по разные стороны от плоскости кольца (a транс расположение), в то время как «β-» означает, что они находятся на одной стороне плоскости (a СНГ расположение). Следовательно, изомер с открытой цепью D-глюкоза дает четыре различных циклических изомера: α-D-глюкопираноза, β-D-глюкопираноза, α-D-глюкофураноза и β-D-глюкофураноза. Эти пять структур существуют в равновесии и взаимопревращаются, и взаимное превращение происходит гораздо быстрее с кислотой. катализ.

Другой изомер с открытой цепью L-глюкоза аналогичным образом дает четыре различных циклических формы L-глюкоза, каждая зеркальное отображение соответствующего D-глюкоза.
Кольца не плоские, а скручены в трех измерениях. Кольцо глюкопиранозы (α или β) может принимать несколько неплоских форм, аналогично конформациям «стул» и «лодочка» у циклогексан. Точно так же кольцо глюкофуранозы может принимать несколько форм, аналогичных конформациям «оболочки» циклопентан.
В твердом состоянии наблюдаются только формы глюкопиранозы, образующие бесцветные кристаллические твердые вещества с высокой растворимый в воде и уксусная кислота но плохо растворим в метанол и этиловый спирт. Они плавятся при 146 ° C (295 ° F) (α) и 150 ° C (302 ° F) (β), и разлагать начиная с 188 ° C с выделением различных летучих продуктов, в конечном итоге оставляя остаток углерод.[26]
Однако некоторые производные глюкофуранозы, такие как 1,2-О-изопропилиден-D-глюкофураноза стабильны и могут быть получены в чистом виде в виде кристаллических твердых веществ.[27][28] Например, реакция α-D-глюкозы с параграф-толилбороновая кислота ЧАС
3C−(C
6ЧАС
4)−В (ОН)
2 преобразует нормальное пиранозное кольцо с образованием 4-кратного сложного эфира α-D-глюкофураноза-1,2∶3,5-бис (п-толилборонат).[29]
Вращательные изомеры
Каждая глюкоза изомер подлежит вращательная изомерия. В циклической форме глюкозы вращение может происходить вокруг O6-C6-C5-O5. угол кручения, названный ω-угол, чтобы сформировать три ступенчатые конформации ротамера, называемые бестактный-бестактный (гг), бестактный-транс (gt) и транс-бестактный (тг).[30] Есть тенденция к ω-угол принять бестактный конформация, тенденция, приписываемая эффект гоша.
Мутаротация

Мутаротация состоит из временного обращения вспять реакции образования кольца, приводящего к форме с открытой цепью, с последующим преобразованием кольца. На этапе замыкания кольца может использоваться группа -OH, отличная от той, которая была воссоздана на этапе раскрытия (таким образом, переключаясь между формами пиранозы и фуранозы), или новая полуацетальная группа, созданная на C-1, может иметь такую же или противоположную направленность, что и исходная. (таким образом переключаясь между формами α и β). Таким образом, хотя форма с открытой цепью практически не обнаруживается в растворе, она является важным компонентом равновесия.
Форма с открытой цепью термодинамически нестабильный, и это спонтанно изомеризуется к циклическим формам. (Хотя реакция замыкания кольца теоретически может создать четырех- или трехатомные кольца, они будут сильно напряженными и не наблюдаются на практике.) В растворах при комнатная температура, четыре циклических изомера взаимно преобразуются в течение часов в процессе, называемом мутаротация.[31] Начиная с любых пропорций, смесь сходится к стабильному соотношению α: β 36:64. Отношение было бы α: β 11:89, если бы не влияние аномерный эффект.[32] Мутаротация происходит значительно медленнее при температурах, близких к 0 ° C (32 ° F).
Оптическая активность
Будь то в воде или в твердой форме, d- (+) - глюкоза правовращающий, то есть он будет вращать направление поляризованный свет по часовой стрелке, если смотреть на источник света. Эффект обусловлен хиральность молекул, и действительно зеркального изомера, л- (-) - глюкоза, есть левовращающий (вращает поляризованный свет против часовой стрелки) на ту же величину. Сила эффекта различна для каждого из пяти таутомеры.
Обратите внимание, что d- префикс не имеет прямого отношения к оптическим свойствам соединения. Это указывает на то, что хиральный центр C-5 имеет такую же хиральность, что и d-глицеральдегид (который был назван так, потому что он правовращающий). Дело в том, что d-глюкоза является правовращающей - это совокупный эффект ее четырех хиральных центров, а не только С-5; и действительно некоторые другие d-альдогексозы левовращающие.
Превращение между двумя аномерами можно наблюдать в поляриметр поскольку чистый α-dглюкоза имеет удельный угол вращения + 112,2 ° · мл / (дм · г), чистая β- D-глюкоза + 17,5 ° · мл / (дм · г).[33] Когда через определенное время за счет мутаротации достигается равновесие, угол поворота составляет + 52,7 ° · мл / (дм · г).[33] При добавлении кислоты или основания это превращение значительно ускоряется. Уравновешивание происходит через альдегидную форму с открытой цепью.
Изомеризация
В разбавленном едкий натр или другие разбавленные основания, моносахариды манноза, глюкоза и фруктоза интерконвертировать (через Преобразование Лобри де Брюйн – Альберда – ван Экенштейна. ), так что между этими изомерами образуется баланс. Эта реакция протекает через эндиол:
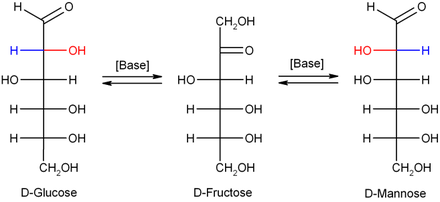
Биохимические свойства
| Метаболизм общего моносахариды и некоторые биохимические реакции глюкозы |
|---|
 |
Глюкоза - самый распространенный моносахарид. Глюкоза также является наиболее широко используемым альдогексоза в большинстве живых организмов. Одно из возможных объяснений этого заключается в том, что глюкоза имеет более низкую тенденцию, чем другие альдогексозы, неспецифически реагировать с амин группы белки.[34] Эта реакция -гликирование - ухудшает или разрушает функцию многих белков,[34] например в гликированный гемоглобин. Низкую скорость гликирования глюкозы можно отнести к более стабильной циклическая форма по сравнению с другими альдогексозами, что означает, что он тратит меньше времени, чем они, в своем реактивном форма с открытой цепью.[34] Причина того, что глюкоза имеет наиболее стабильную циклическую форму из всех альдогексоз, заключается в том, что ее гидроксильные группы (за исключением гидроксильной группы на аномерном углероде d-глюкоза) находятся в экваториальное положение. Предположительно, глюкоза является наиболее распространенным природным моносахаридом, потому что она менее гликирована белками, чем другие моносахариды.[34][35] Другая гипотеза состоит в том, что глюкоза, будучи единственным D-альдогексоза это все пять гидрокси заместители в экваториальный положение в виде β-D-глюкозы, более доступное для химических реакций,[36] например, для этерификация[37] или же ацеталь формирование.[38] По этой причине D-глюкоза также является очень предпочтительным строительным блоком в естественных полисахариды (гликаны). Полисахариды, состоящие исключительно из глюкозы, называются глюканы.
Глюкоза вырабатывается растениями в процессе фотосинтеза с использованием солнечного света, воды и углекислого газа и может использоваться всеми живыми организмами в качестве источника энергии и углерода. Однако большая часть глюкозы встречается не в свободной форме, а в форме ее полимеров, то есть лактозы, сахарозы, крахмала и других веществ, являющихся запасами энергии, а также целлюлозы и хитин, которые являются компонентами клеточной стенки растений или грибы и членистоногие, соответственно. Эти полимеры разлагаются до глюкозы во время приема пищи животными, грибами и бактериями с помощью ферментов. Все животные также могут сами производить глюкозу из определенных прекурсоров по мере необходимости. Нервные клетки, ячейки мозговое вещество почек и эритроциты зависят от глюкозы для производства энергии.[39] У взрослого человека содержится около 18 г глюкозы,[40] из которых около 4 г присутствует в крови.[41] Примерно 180–220 г глюкозы вырабатывается в печени взрослого человека за 24 часа.[40]
Многие из долгосрочных осложнений сахарный диабет (например., слепота, почечная недостаточность, и периферическая невропатия ), вероятно, связаны с гликированием белков или липиды.[42] В отличие, фермент -регулируемое добавление сахаров к белку называется гликозилирование и необходим для функционирования многих белков.[43]
Поглощение
Проглоченная глюкоза изначально связывается с рецептором сладкого вкуса на языке человека. Этот комплекс белков T1R2 и T1R3 позволяет идентифицировать источники пищи, содержащие глюкозу. Глюкоза в основном поступает с пищей - около 300 г в день вырабатывается при переработке пищи,[44] но он также синтезируется из других метаболитов в клетках организма. У человека распад глюкозосодержащих полисахаридов частично происходит уже во время жевать посредством амилаза, который содержится в слюна, а также мальтаза, лактаза и сукраза на кисть границы тонкой кишки. Глюкоза является строительным материалом для многих углеводов и может быть отделена от них с помощью определенных ферментов. Глюкозидазы Подгруппа гликозидаз сначала катализирует гидролиз длинноцепочечных глюкозосодержащих полисахаридов, удаляя концевую глюкозу. В свою очередь, дисахариды в основном разлагаются специфическими гликозидазами до глюкозы. Названия разлагающих ферментов часто происходят от конкретных поли- и дисахаридов; среди прочего, для разложения полисахаридных цепей используются амилазы (названные в честь амилозы, компонента крахмала), целлюлазы (названные в честь целлюлозы), хитиназы (названные в честь хитина) и другие. Кроме того, для расщепления дисахаридов используются мальтаза, лактаза, сахароза, трехалаза и другие. У человека известно около 70 генов, кодирующих гликозидазы. Они выполняют функции переваривания и расщепления гликогена, сфинголипиды, мукополисахариды и поли (АДФ-рибоза). Люди не производят целлюлазы, хитиназы и треалазы, но бактерии в Кишечная флора делать.
Чтобы попасть в клеточные мембраны клеток и мембраны клеточных компартментов или выйти из них, глюкоза требует специальных транспортных белков из суперсемейство основных фасилитаторов. в тонкий кишечник (точнее, в тощая кишка ),[45] глюкоза попадает в кишечник эпителиальные клетки с помощью переносчики глюкозы[46] через вторичный активный транспорт механизм называется ион натрия-глюкоза Симпорт через котранспортер натрия / глюкозы 1.[47] Дальнейшая передача происходит на базолатеральный сторона кишечных эпителиальных клеток через транспортер глюкозы GLUT2,[47] а также их проникновение в клетки печени, клетки почек, ячейки островки Лангерганса, нервные клетки, астроциты и таниоциты.[48] Глюкоза поступает в печень через вена порта и хранится там в виде клеточного гликогена.[49] В клетке печени это фосфорилированный к глюкокиназа в позиции 6 до глюкозо-6-фосфат, который не может покинуть ячейку. С помощью глюкозо-6-фосфатаза глюкозо-6-фосфат при необходимости превращается обратно в глюкозу исключительно в печени, так что он доступен для поддержания достаточной концентрации глюкозы в крови. В других клетках захват происходит путем пассивного транспорта через один из 14 белков GLUT.[47] В других типах клеток фосфорилирование происходит через гексокиназа, после чего глюкоза больше не может диффундировать из клетки.
Транспортер глюкозы GLUT1 продуцируется большинством типов клеток и имеет особое значение для нервных клеток и поджелудочной железы. β-клетки.[47] GLUT3 высоко экспрессируется в нервных клетках.[47] Глюкоза из кровотока поглощается GLUT4 из мышечные клетки (из скелетные мышцы[50] и сердечная мышца ) и жировые клетки.[51] GLUT14 формируется исключительно в яички.[47] Избыточная глюкоза расщепляется и превращается в жирные кислоты, которые хранятся в виде триацилглицериды. в почки глюкоза в моче абсорбируется через SGLT1 и SGLT2 в апикальных клеточных мембранах и передается через GLUT2 в базолатеральных клеточных мембранах.[52] Около 90% реабсорбции глюкозы почками происходит через SGLT2 и около 3% через SGLT1.[53]
Биосинтез
В растения и немного прокариоты, глюкоза является продуктом фотосинтез.[54] Глюкоза также образуется при распаде полимерных форм глюкозы, таких как гликоген (у животных и грибы ) или же крахмал (в растениях). Расщепление гликогена называется гликогенолиз расщепление крахмала называется деградацией крахмала.[55]
Метаболический путь, который начинается с молекул, содержащих от двух до четырех атомов углерода (C), и заканчивается молекулой глюкозы, содержащей шесть атомов углерода, называется глюконеогенезом и происходит во всех живых организмах. Меньшие исходные материалы являются результатом других метаболических путей. В конечном итоге почти все биомолекулы происходят из-за ассимиляции углекислого газа в растениях во время фотосинтеза.[56] Свободная энергия образования α-d-глюкоза составляет 917,2 килоджоулей на моль.[57] У человека глюконеогенез происходит в печени и почках,[58] но также и в других типах клеток. В печени хранится около 150 г гликогена, в скелетных мышцах - около 250 г.[59] Однако глюкоза, высвобождаемая в мышечных клетках при расщеплении гликогена, не может быть доставлена в кровоток, потому что глюкоза фосфорилируется гексокиназой, а глюкозо-6-фосфатаза не экспрессируется для удаления фосфатной группы. В отличие от глюкозы, для глюкозо-6-фосфата нет транспортного белка. Глюконеогенез позволяет организму накапливать глюкозу из других метаболитов, включая лактат или определенные аминокислоты, при этом потребляя энергию. Почечный трубчатые клетки также может производить глюкозу.
Деградация глюкозы
Глюкозосодержащие соединения и изомерный формы перевариваются и усваиваются организмом в кишечнике, в том числе крахмал, гликоген, дисахариды и моносахариды.
Глюкоза хранится в основном в печени и мышцах в виде гликогена. Он распределяется и используется в тканях в виде свободной глюкозы.
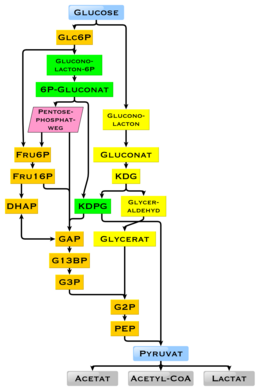
У человека глюкоза метаболизируется путем гликолиза.[60] и пентозофосфатный путь.[61] Гликолиз используют все живые организмы,[62][63] с небольшими вариациями, и все организмы вырабатывают энергию за счет распада моносахаридов.[62] В дальнейшем в процессе метаболизма он может полностью разложиться через окислительное декарбоксилирование, то Цикл Кребса (синоним цикл лимонной кислоты) и дыхательная цепь к воде и двуокиси углерода. Если для этого недостаточно кислорода, разложение глюкозы у животных происходит анаэробно до лактата в результате ферментации молочной кислоты и выделяет меньше энергии. Мышечный лактат попадает в печень через кровоток у млекопитающих, где происходит глюконеогенез (Цикл Кори ). При большом количестве глюкозы метаболит ацетил-КоА из цикла Кребса можно также использовать для синтез жирных кислот.[64] Глюкоза также используется для пополнения запасов гликогена в организме, которые в основном находятся в печени и скелетных мышцах. Эти процессы гормонально регулируется.
В других живых организмах могут происходить другие формы ферментации. Бактерия кишечная палочка могут расти на питательных средах, содержащих глюкозу в качестве единственного источника углерода.[57] У некоторых бактерий, а также в модифицированной форме у архей глюкоза разлагается через Путь Энтнера-Дудорова.[65]
Использование глюкозы в качестве источника энергии в клетках осуществляется либо путем аэробного дыхания, либо анаэробного дыхания, либо путем ферментации. Первым этапом гликолиза является фосфорилирование глюкозы на гексокиназа формировать глюкозо-6-фосфат. Основная причина немедленного фосфорилирования глюкозы состоит в том, чтобы предотвратить ее диффузию из клетки, когда заряженная фосфат группа препятствует легкому переходу глюкозо-6-фосфата через клеточная мембрана.[66] Кроме того, добавление высокоэнергетической фосфатной группы активирует глюкоза для последующего распада на более поздних этапах гликолиза. В физиологические условия, эта первоначальная реакция необратима.
При анаэробном дыхании одна молекула глюкозы дает чистый прирост двух молекул АТФ (четыре молекулы АТФ производятся во время гликолиза посредством фосфорилирования на уровне субстрата, но две необходимы ферментам, используемым во время процесса).[67] При аэробном дыхании молекула глюкозы намного более прибыльна, поскольку генерируется максимальное чистое производство 30 или 32 молекул АТФ (в зависимости от организма) за счет окислительного фосфорилирования.[68]
Нажмите на гены, белки и метаболиты ниже, чтобы ссылки на соответствующие статьи.[§ 1]
- ^ Интерактивную карту путей можно редактировать на WikiPathways: «ГликолизГлюконеогенез_WP534».
Опухоль клетки часто растут сравнительно быстро и потребляют за счет гликолиза количество глюкозы выше среднего,[69] что приводит к образованию лактата, конечного продукта ферментации у млекопитающих, даже в присутствии кислорода. Этот эффект называется Эффект варбурга. Для увеличения поглощения глюкозы опухолями чрезмерно вырабатываются различные SGLT и GLUT.[70][71]
В дрожжи этанол ферментируется при высоких концентрациях глюкозы даже в присутствии кислорода (который обычно приводит к дыханию, но не к ферментации). Этот эффект называется Эффект Крэбтри.
Энергетический ресурс
Глюкоза - повсеместное топливо в биология. Он используется в качестве источника энергии в организмах, от бактерий до людей, через аэробного дыхания, анаэробное дыхание (в бактериях) или ферментация. Глюкоза - ключевой источник энергии человеческого тела, обеспечиваемый аэробным дыханием, обеспечивая около 3,75 энергии.килокалории (16 килоджоули ) из пищевая энергия за грамм.[72] Распад углеводов (например, крахмала) дает мононуклеоз- и дисахариды, большая часть из которых - глюкоза. Через гликолиз а позже в реакции цикл лимонной кислоты и окислительного фосфорилирования, глюкоза окисленный в конечном итоге сформировать углекислый газ и воды, давая энергию в основном в виде АТФ. Реакция на инсулин и другие механизмы регулируют концентрацию глюкозы в крови. Физиологическая калорийность глюкозы, в зависимости от источника, составляет 16,2 килоджоулей на грамм.[73] и 15,7 кДж / г (3,74 ккал / г) соответственно.[74] Высокая доступность углеводов из растительной биомассы привела к появлению множества методов в ходе эволюции, особенно у микроорганизмов, для использования энергии и запаса углерода глюкозы. Существуют различия в том, что конечный продукт больше не может использоваться для производства энергии. Присутствие отдельных генов и их генных продуктов, ферментов, определяет возможные реакции. Метаболический путь гликолиза используется почти всеми живыми существами. Существенным отличием использования гликолиза является восстановление НАДФН как восстановитель для анаболизм которые в противном случае должны были бы быть созданы косвенно.[75]
Глюкоза и кислород поставляют почти всю энергию для мозг,[76] поэтому его доступность влияет психологический процессы. Когда глюкоза низкая психологические процессы, требующие умственных усилий (например, самоконтроль, принятие решений, требующих усилий).[77][78][79][80] В мозге, который зависит от глюкозы и кислорода как основного источника энергии, концентрация глюкозы обычно составляет от 4 до 6 мМ (5 мМ равно 90 мг / дл),[40] но уменьшается до 2–3 мМ при голодании.[81] Путаница встречается ниже 1 мМ и кома на более низких уровнях.[81]
Глюкоза в крови называется содержание сахара в крови. Уровень сахара в крови регулируются связывающими глюкозу нервными клетками в гипоталамус.[82] Кроме того, глюкоза в головном мозге связывается с рецепторами глюкозы система вознаграждений в прилежащее ядро.[82] Связывание глюкозы с рецептором сладкого на языке вызывает высвобождение различных гормонов энергетического метаболизма либо через глюкозу, либо через другие сахара, что приводит к увеличению клеточного поглощения и снижению уровня сахара в крови.[83] Искусственные подсластители не снижают уровень сахара в крови.[83]
Содержание сахара в крови здорового человека при кратковременном голодании, например после ночного голодания составляет от 70 до 100 мг / дл крови (от 4 до 5,5 мМ). В плазма крови, измеренные значения примерно на 10–15% выше. Кроме того, значения в артериальный в крови выше, чем концентрации в венозный кровь, так как глюкоза всасывается в ткани во время прохождения капиллярное русло. Также в капиллярной крови, которая часто используется для определения сахара в крови, значения иногда выше, чем в венозной крови. Содержание глюкозы в крови регулируется гормонами. инсулин, инкретин и глюкагон.[82][84] Инсулин снижает уровень глюкозы, глюкагон повышает его.[40] Кроме того, гормоны адреналин, тироксин, глюкокортикоиды, соматотропин и адренокортикотропин приводят к повышению уровня глюкозы.[40] Также существует гормонально-независимая регуляция, которая называется ауторегуляция глюкозы.[85] После приема пищи концентрация сахара в крови увеличивается. Значения более 180 мг / дл в цельной венозной крови являются патологическими и называются гипергликемия, значения ниже 40 мг / дл называются гипогликемия.[86] При необходимости глюкоза высвобождается в кровоток глюкозо-6-фосфатазой из глюкозо-6-фосфата, происходящего из гликогена печени и почек, тем самым регулируя гомеостаз концентрации глюкозы в крови.[58][39] В жвачные животные, концентрация глюкозы в крови ниже (60 мг / дл в крупный рогатый скот и 40 мг / дл в овца ), потому что углеводы больше превращаются кишечной флорой в короткоцепочечные жирные кислоты.[87]
Некоторая глюкоза превращается в молочная кислота к астроциты, который затем используется в качестве источника энергии клетки мозга; некоторая часть глюкозы используется клетками кишечника и красные кровяные тельца, а остальное достигает печень, жировая ткань и мышца клетки, где он всасывается и хранится в виде гликогена (под действием инсулин ). Гликоген клеток печени может превращаться в глюкозу и возвращаться в кровь при низком уровне инсулина или его отсутствии; Гликоген мышечных клеток не возвращается в кровь из-за недостатка ферментов. В жировые клетки, глюкоза используется для питания реакций, которые синтезируют некоторые толстый типы и имеют другие цели. Гликоген - это механизм «хранения энергии глюкозы» в организме, потому что он гораздо более «экономит пространство» и менее реактивен, чем сама глюкоза.
В силу своей важности для здоровья человека глюкоза является аналитом в тесты на глюкозу это обычные медицинские анализы крови.[88] Прием пищи или голодание перед взятием образца крови влияет на анализ глюкозы в крови; высокий уровень глюкозы натощак содержание сахара в крови уровень может быть признаком преддиабет или же сахарный диабет.[89]
В Гликемический индекс является показателем скорости резорбции и преобразования в уровень глюкозы в крови из потребленных углеводов, измеряемой как площадь под кривой уровней глюкозы в крови после потребления по сравнению с глюкозой (глюкоза определяется как 100).[90] Клиническое значение гликемического индекса является спорным,[90][91] продукты с высоким содержанием жира замедляют всасывание углеводов и снижают гликемический индекс, например мороженое.[91] Альтернативный индикатор - инсулиновый индекс,[92] измеряется как влияние потребления углеводов на уровень инсулина в крови. В гликемическая нагрузка является показателем количества глюкозы, добавленной к уровню глюкозы в крови после потребления, на основе гликемического индекса и количества потребляемой пищи.
Предшественник
Организмы используют глюкозу в качестве прекурсора для синтеза нескольких важных веществ. Крахмал, целлюлоза, и гликоген («животный крахмал») - обычная глюкоза полимеры (полисахариды ). Некоторые из этих полимеров (крахмал или гликоген) служат накопителями энергии, а другие (целлюлоза и хитин, который сделан из производной глюкозы) играют структурную роль. Олигосахариды глюкозы в сочетании с другими сахарами служат важными запасами энергии. К ним относятся лактоза, преобладающий сахар в молоке, который является дисахаридом глюкоза-галактоза, и сахароза, другой дисахарид, который состоит из глюкозы и фруктоза. Глюкоза также добавляется к определенным белкам и липиды в процессе, называемом гликозилирование. Это часто имеет решающее значение для их функционирования. Ферменты, которые соединяют глюкозу с другими молекулами, обычно используют фосфорилированный глюкоза для формирования новой связи, связывая ее с разрывом глюкозо-фосфатной связи.
Помимо прямого использования в качестве мономера, глюкоза может быть расщеплена для синтеза большого количества других биомолекул. Это важно, поскольку глюкоза служит одновременно и основным хранилищем энергии, и источником органического углерода. Глюкозу можно расщепить и превратить в липиды. Он также является прекурсором для синтеза других важных молекул, таких как витамин С (аскорбиновая кислота ). В живых организмах глюкоза превращается в несколько других химических соединений, которые являются исходным материалом для различных метаболические пути. Среди них все остальные моносахариды[93] таких как фруктоза (через путь полиола ),[47] манноза (эпимер глюкозы в положении 2), галактоза (эпимер в положении 4), фукоза, различные уроновые кислоты и аминосахара производятся из глюкозы.[49] Помимо фосфорилирования до глюкозо-6-фосфата, которое является частью гликолиза, глюкоза может окисляться во время разложения до глюконо-1,5-лактон. Глюкоза используется некоторыми бактериями в качестве строительного материала для трегалоза или декстран биосинтез и у животных в качестве строительного блока гликогена. Глюкоза также может быть преобразована из бактериальной ксилозоизомераза к фруктозе. Кроме того, глюкоза метаболиты производить все несущественное аминокислоты, сахарные спирты Такие как маннитол и сорбитол, жирные кислоты, холестерин и нуклеиновые кислоты.[93] Наконец, глюкоза используется как строительный блок в гликозилирование белков в гликопротеины, гликолипиды, пептидогликаны, гликозиды и другие вещества (катализируемые гликозилтрансферазы ) и может быть оторван от них гликозидазы.
Патология
Сахарный диабет
Сахарный диабет нарушение обмена веществ, при котором организм не может регулировать уровень глюкозы в крови либо из-за недостатка инсулина в организме, либо из-за неспособности клеток организма должным образом реагировать на инсулин. Каждая из этих ситуаций может быть вызвана постоянно высоким повышением уровня глюкозы в крови, выгоранием поджелудочной железы и резистентность к инсулину. В поджелудочная железа это орган, ответственный за секрецию гормонов инсулина и глюкагона.[94] Инсулин - это гормон, который регулирует уровень глюкозы, позволяя клеткам организма поглощать и использовать глюкозу. Без него глюкоза не может попасть в клетку и, следовательно, не может использоваться в качестве топлива для функций организма.[95] Если поджелудочная железа подвергается постоянно высокому повышению уровня глюкозы в крови, инсулинпродуцирующие клетки в поджелудочной железе могут быть повреждены, вызывая недостаток инсулина в организме. Инсулинорезистентность возникает, когда поджелудочная железа пытается вырабатывать все больше и больше инсулина в ответ на постоянно повышенный уровень глюкозы в крови. В конце концов, остальная часть тела становится резистентной к инсулину, который вырабатывает поджелудочная железа, тем самым требуя больше инсулина для достижения того же эффекта снижения уровня глюкозы в крови и заставляя поджелудочную железу производить еще больше инсулина, чтобы конкурировать с резистентностью. Эта негативная спираль способствует выгоранию поджелудочной железы и прогрессированию диабета.
Чтобы контролировать реакцию организма на терапию, снижающую уровень глюкозы в крови, можно измерить уровень глюкозы. Мониторинг уровня глюкозы в крови может выполняться несколькими методами, например, тестом на глюкозу натощак, который измеряет уровень глюкозы в крови после 8 часов голодания. Другой тест - это 2-часовой тест на толерантность к глюкозе (GTT) - для этого теста человеку делают тест на глюкозу натощак, затем он выпивает 75-граммовый напиток с глюкозой и повторно тестируется. Этот тест измеряет способность организма человека перерабатывать глюкозу. Со временем уровень глюкозы в крови должен снизиться, поскольку инсулин позволяет ему поглощаться клетками и выходить из кровотока.
Лечение гипогликемии

Лица с сахарный диабет или другие условия, которые приводят к низкий уровень сахара в крови часто переносят небольшое количество сахара в различных формах. Одним из обычно используемых сахаров является глюкоза, часто в форме таблеток глюкозы (глюкоза спрессована в форму таблетки, иногда с одним или несколькими другими ингредиентами в качестве связующего), Леденец, или же сахарный пакет.
Источники

Большинство пищевых углеводов содержат глюкозу либо в качестве единственного строительного материала (как в полисахаридах крахмал и гликоген ) или вместе с другим моносахаридом (как в гетерополисахаридах сахароза и лактоза ).[96] Неограниченная глюкоза - один из основных ингредиентов медовый.
| Еда | Общий углевод,А включая "пищевые волокна " | Общий сахара | Свободный фруктоза | Свободный глюкоза | Сахароза | Фруктоза / глюкоза соотношение | Сахароза в процентах от общий сахар |
|---|---|---|---|---|---|---|---|
| Фрукты | |||||||
| яблоко | 13.8 | 10.4 | 5.9 | 2.4 | 2.1 | 2.0 | 19.9 |
| Абрикос | 11.1 | 9.2 | 0.9 | 2.4 | 5.9 | 0.7 | 63.5 |
| Банан | 22.8 | 12.2 | 4.9 | 5.0 | 2.4 | 1.0 | 20.0 |
| Рис сушеные | 63.9 | 47.9 | 22.9 | 24.8 | 0.9 | 0.93 | 0.15 |
| Виноград | 18.1 | 15.5 | 8.1 | 7.2 | 0.2 | 1.1 | 1 |
| Пупок оранжевый | 12.5 | 8.5 | 2.25 | 2.0 | 4.3 | 1.1 | 50.4 |
| Персик | 9.5 | 8.4 | 1.5 | 2.0 | 4.8 | 0.9 | 56.7 |
| Груша | 15.5 | 9.8 | 6.2 | 2.8 | 0.8 | 2.1 | 8.0 |
| Ананас | 13.1 | 9.9 | 2.1 | 1.7 | 6.0 | 1.1 | 60.8 |
| слива | 11.4 | 9.9 | 3.1 | 5.1 | 1.6 | 0.66 | 16.2 |
| Овощи | |||||||
| Свекла, красный | 9.6 | 6.8 | 0.1 | 0.1 | 6.5 | 1.0 | 96.2 |
| Морковь | 9.6 | 4.7 | 0.6 | 0.6 | 3.6 | 1.0 | 77 |
| красный перец, милая | 6.0 | 4.2 | 2.3 | 1.9 | 0.0 | 1.2 | 0.0 |
| Лук, милая | 7.6 | 5.0 | 2.0 | 2.3 | 0.7 | 0.9 | 14.3 |
| Сладкий картофель | 20.1 | 4.2 | 0.7 | 1.0 | 2.5 | 0.9 | 60.3 |
| сладкий картофель | 27.9 | 0.5 | следы | следы | следы | на | следы |
| Сахарный тростник | 13–18 | 0.2–1.0 | 0.2–1.0 | 11–16 | 1.0 | высоко | |
| Сахарная свекла | 17–18 | 0.1–0.5 | 0.1–0.5 | 16–17 | 1.0 | высоко | |
| Зерна | |||||||
| Кукуруза, милая | 19.0 | 6.2 | 1.9 | 3.4 | 0.9 | 0.61 | 15.0 |
^ А Ценность углеводов рассчитывается в базе данных USDA и не всегда соответствует сумме сахаров, крахмала и «пищевых волокон».
Коммерческое производство
Глюкоза производится промышленным способом из крахмала ферментативный гидролиз с помощью глюкозоамилаза или с помощью кислоты. Ферментативный гидролиз в значительной степени вытеснил гидролиз, катализируемый кислотой.[98] В результате получается сироп глюкозы (ферментативно с более чем 90% глюкозы в сухом веществе).[98] с годовым объемом производства в мире 20 миллионов тонн (по состоянию на 2011 год).[99] Отсюда и бывшее нарицательное название «крахмальный сахар». Амилазы чаще всего получают из Bacillus licheniformis[100] или же Bacillus subtilis (штамм MN-385),[100] которые более термостабильны, чем изначально используемые ферменты.[100][101] Начиная с 1982 г. пуллуланазы из Aspergillus niger были использованы в производстве сиропа глюкозы для превращения амилопектина в крахмал (амилозу), тем самым увеличивая выход глюкозы.[102] Реакцию проводят при pH = 4,6–5,2 и температуре 55–60 ° C.[8] Кукурузный сироп содержит от 20% до 95% глюкозы в сухом веществе.[103][104] Японская форма сиропа глюкозы, Мизуаме, изготовлен из сладкий картофель или же рис крахмал.[105] Мальтодекстрин содержит около 20% глюкозы.
Многие культуры можно использовать в качестве источника крахмала. Кукуруза,[98] рис,[98] пшеница,[98] маниока,[98] картофель,[98] ячмень,[98] сладкий картофель,[106] кукурузная шелуха и саго все они используются в разных частях света. в Соединенные Штаты, кукурузный крахмал (из кукурузы) используется почти исключительно. Некоторая коммерческая глюкоза встречается как компонент инвертный сахар, примерно 1: 1 смесь глюкозы и фруктоза который производится из сахарозы. В принципе, целлюлозу можно гидролизовать до глюкозы, но этот процесс еще не является коммерчески практичным.[23]
Превращение во фруктозу
В США почти исключительно кукуруза (точнее: кукурузный сироп) используется в качестве источника глюкозы для производства изоглюкоза, который представляет собой смесь глюкозы и фруктозы, поскольку фруктоза обладает более высокой подслащивающей способностью - с такой же физиологической теплотворной способностью 374 килокалорий на 100 г. Ежегодное мировое производство изоглюкозы составляет 8 миллионов тонн (по состоянию на 2011 год).[99] При приготовлении из кукурузного сиропа конечный продукт кукурузный сироп с высоким содержанием фруктозы (HFCS).
Коммерческое использование

Глюкоза в основном используется для производства фруктозы и продуктов, содержащих глюкозу. В пищевых продуктах он используется как подсластитель, увлажнитель, чтобы увеличить объем и создать более мягкий ощущение во рту.[98] Различные источники глюкозы, такие как виноградный сок (для вина) или солод (для пива), используются для ферментации до этанола во время производства Алкогольные напитки. В большинстве безалкогольных напитков в США используется HFCS-55 (с содержанием фруктозы 55% в сухой массе), тогда как в большинстве других подслащенных HFCS пищевых продуктов в США используется HFCS-42 (с содержанием фруктозы 42% в сухой массе). ).[108] В соседней стране Мексика, с другой стороны, тростниковый сахар используется в безалкогольных напитках в качестве подсластителя, который имеет более высокую подслащивающую способность.[109] Кроме того, сироп глюкозы используется, в частности, в производстве кондитерские изделия Такие как конфеты, ириска и помадка.[110] Типичные химические реакции глюкозы при нагревании в безводных условиях: карамелизация а в присутствии аминокислот реакция Майяра.
Кроме того, различные органические кислоты могут быть получены биотехнологическим путем из глюкозы, например, путем ферментации с Clostridium thermoaceticum производить уксусная кислота, с Penicilium notatum для производства арабоаскорбиновая кислота, с Ризоп делемар для производства фумаровая кислота, с Aspergillus niger для производства глюконовая кислота, с Candida brumptii производить изоцитриновая кислота, с Aspergillus terreus для производства итаконовая кислота, с Pseudomonas fluorescens для производства 2-кетоглюконовая кислота, с Gluconobacter suboxydans для производства 5-кетоглюконовая кислота, с Aspergillus oryzae для производства койевая кислота, с Lactobacillus delbrueckii для производства молочная кислота, с Lactobacillus brevis для производства яблочная кислота, с Propionibacter shermanii для производства пропионовая кислота, с Синегнойная палочка для производства пировиноградная кислота и с Gluconobacter suboxydans для производства Винная кислота.[111]
Анализ
В частности, когда молекула глюкозы должна быть обнаружена в определенном положении в более крупной молекуле, спектроскопия ядерного магнитного резонанса, Рентгеновская кристаллография анализ или лектин иммуноокрашивание выполняется с конканавалин А конъюгат репортерного фермента (связывающий только глюкозу или маннозу).
Классические качественные реакции обнаружения
Эти реакции имеют только историческое значение:
Тест Фелинга
В Тест Фелинга классический метод обнаружения альдоз.[112] Из-за мутаротации глюкоза всегда присутствует в небольшом количестве в виде альдегида с открытой цепью. При добавлении реагентов Фелинга (раствор Фелинга (I) и раствор Фелинга (II)) альдегидная группа окисляется до карбоновая кислота, а Cu2+ тартратный комплекс восстанавливается до Cu+ и образуя кирпично-красный осадок (Cu2О).
Тест Толленса
в Тест Толленса, после добавления аммиачной AgNO3 к раствору образца, Ag+ восстанавливается глюкозой до элементарного серебро.[113]
Бородатый тест
В Тест Барфеда,[114] раствор растворенных ацетат меди, ацетат натрия и уксусная кислота добавляется к исследуемому раствору сахара и затем нагревается на водяной бане в течение нескольких минут. Глюкоза и другие моносахариды быстро приобретают красноватый цвет и красновато-коричневый цвет. оксид меди (I) (Cu2О).
Тест Нюландера
Как редуцирующий сахар глюкоза реагирует в Тест Нюландера.[115]
Другие тесты
При нагревании разбавленного гидроксид калия раствор с глюкозой до 100 ° C, появляется сильное красноватое потемнение и карамельный запах.[116] Концентрированный серная кислота растворяет сухую глюкозу без почернения при комнатной температуре с образованием сахарной серной кислоты.[116] В дрожжевом растворе при спиртовой ферментации образуется углекислый газ в соотношении 2,0454 молекулы глюкозы на одну молекулу CO2.[116] Глюкоза образует черную массу с хлорид олова.[116] В аммиачном растворе серебра глюкоза (а также лактоза и декстрин) приводит к отложению серебра. В аммиачном ацетат свинца раствор, белый гликозид свинца образуется в присутствии глюкозы, которая становится менее растворимой при приготовлении пищи и становится коричневой.[116] В аммиачном растворе меди желтый оксид меди гидрат образуется с глюкозой при комнатной температуре, в то время как красный оксид меди образуется при кипячении (то же самое с декстрином, за исключением аммиачного ацетат меди решение).[116] С Реагент Хагера, формы глюкозы оксид ртути во время кипячения.[116] Щелочной висмут раствор используется для осаждения элементарного черно-коричневого висмута с глюкозой.[116] Глюкоза вареная в молибдат аммония раствор окрашивает раствор в синий цвет. Решение с индиго кармин и карбонат натрия обесцвечивается при кипячении с глюкозой.[116]
Инструментальная количественная оценка
Рефрактометрия и поляриметрия
В концентрированных растворах глюкозы с низким содержанием других углеводов ее концентрацию можно определить с помощью поляриметра. Для сахарных смесей концентрацию можно определить с помощью рефрактометр, например в Oechsle определение в процессе производства вина.
Фотометрические ферментативные методы в растворе
Фермент глюкозооксидаза (GOx) превращает глюкозу в глюконовую кислоту и перекись водорода, потребляя кислород. Другой фермент, пероксидаза, катализирует хромогенную реакцию (реакция Триндера).[117] из фенол с 4-аминоантипирин к пурпурному красителю.
Фотометрический метод тест-полосок
В методе тест-полосок используется упомянутое выше ферментативное превращение глюкозы в глюконовую кислоту с образованием перекиси водорода. Реагенты иммобилизованы на полимерной матрице, так называемой тест-полоске, которая приобретает более или менее интенсивный цвет. Это можно измерить рефлектометрическим методом на длине волны 510 нм с помощью портативного фотометра на основе светодиода. Это позволяет обычным людям определять уровень сахара в крови. В дополнение к реакции фенола с 4-аминоантипирином были разработаны новые хромогенные реакции, которые позволяют проводить фотометрию на более высоких длинах волн (550 нм, 750 нм).[118]
Амперометрический датчик глюкозы
Электроанализ глюкозы также основан на ферментативной реакции, упомянутой выше. Полученный пероксид водорода может быть количественно определен амперометрическим методом анодным окислением при потенциале 600 мВ.[119] GOx иммобилизован на поверхности электрода или в мембране, расположенной рядом с электродом. В электродах используются драгоценные металлы, такие как платина или золото, а также электроды из углеродных нанотрубок, которые, например, легированы бором.[120] Нанопроволоки Cu – CuO также используются в качестве безферментных амперометрических электродов. Таким образом был достигнут предел обнаружения 50 мкмоль / л.[121] Особенно многообещающим методом является так называемая «ферментная разводка». В этом случае электрон, текущий во время окисления, передается непосредственно от фермента через молекулярную проволоку к электроду.[122]
Другие сенсорные методы
Существует множество других химических датчиков для измерения глюкозы.[123][124] Учитывая важность анализа глюкозы в науках о жизни, были также разработаны многочисленные оптические датчики для сахаридов на основе использования бороновых кислот,[125] которые особенно полезны для внутриклеточных сенсорных приложений, где другие (оптические) методы не подходят или могут использоваться только условно. В дополнение к производным органической бороновой кислоты, которые часто очень специфично связываются с 1,2-диольными группами сахаров, существуют также другие концепции зондов, классифицированные по функциональным механизмам, которые используют селективные связывающие глюкозу белки (например, конканавалин A) в качестве рецептора. . Кроме того, были разработаны методы, которые косвенно определяют концентрацию глюкозы через концентрацию продуктов метаболизма, например по потреблению кислорода с помощью флуоресцентно-оптических сенсоров.[126] Наконец, существуют концепции, основанные на ферментах, которые используют собственное поглощение или флуоресценцию (меченных флуоресценцией) ферментов в качестве репортеров.[123]
Иодометрия меди
Глюкозу можно определить количественно с помощью йодометрии меди.[127]
Хроматографические методы
В частности, для анализа сложных смесей, содержащих глюкозу, например в меде, хроматографические методы, такие как высокоэффективная жидкостная хроматография и газовая хроматография[127] часто используются в сочетании с масс-спектрометрии.[128][129] Принимая во внимание соотношение изотопов, с помощью этих методов также можно надежно обнаружить фальсификацию меда добавлением сахара.[130] Обычно используется дериватизация с использованием силилирующих реагентов.[131] Кроме того, можно количественно определить пропорции ди- и трисахаридов.
Анализ in vivo
Поглощение глюкозы клетками организмов измеряется с помощью 2-дезокси-D-глюкоза или же фтордезоксиглюкоза.[81] (18F) фтордезоксиглюкоза используется как индикатор в позитронно-эмиссионная томография в онкологии и неврологии,[132] где это, безусловно, наиболее часто используемый диагностический агент.[133]
Рекомендации
- ^ а б Берио-Гоутс, Джулиана (1991), "Измерения теплоемкости и термодинамические функции кристаллической α-D-глюкозы при температурах от 10K до 340K", J. Chem. Термодинамика., 23 (5): 403–09, Дои:10.1016 / S0021-9614 (05) 80128-4
- ^ Пономарев, В. В .; Мигарская, Л. Б. (1960), "Теплоты сгорания некоторых аминокислот", Русь. J. Phys. Chem. (Англ. Пер.), 34: 1182–83
- ^ Domb, Abraham J .; Кост, Джозеф; Уайзман, Дэвид (1998-02-04). Справочник биоразлагаемых полимеров. п. 275. ISBN 978-1-4200-4936-7.
- ^ Кенджи Камиде: Целлюлоза и производные целлюлозы. Эльзевир, 2005 г., ISBN 978-0-080-45444-3, п. 1.
- ^ а б Всемирная организация здоровья (2019). Типовой список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г.. Женева: Всемирная организация здравоохранения. HDL:10665/325771. WHO / MVP / EMP / IAU / 2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ «Интернет-этимологический словарь». Etymonline.com. В архиве из оригинала от 26.11.2016. Получено 2016-11-25.
- ^ Тенар, Гей-Люссак, Био и Дюма (1838) "Rapport sur un mémoire de M. Péligiot, intitulé: Recherches sur la nature et les propriétés chimiques des Sucres". В архиве 2015-12-06 в Wayback Machine (Отчет о мемуарах г-на Пелиджио, озаглавленный: Исследования природы и химических свойств сахаров), Comptes rendus, 7 : 106–113. Со страницы 109. В архиве 2015-12-06 в Wayback Machine: "Il résulte des Comparison faites par M. Péligot, que le sucre de raisin, celui d'amidon, celui de diabètes et celui de miel ont parfaitement la même композиция и les mêmes propriétés, и составляющие un seul corps que nous Propriétés Глюкоза (1). … (1) γλευχος, moût, vin doux."Из сравнений, проведенных г-ном Пелиго, следует, что сахар из винограда, сахар из крахмала, сахар от диабета и сахар из меда имеют совершенно одинаковый состав и одинаковые свойства и составляют единое вещество, которое мы предлагаем назвать глюкоза (1) … (1) γλευχος, должно, сладкое вино.
- ^ а б Энциклопедия еды и здоровья. Академическая пресса. 2015. стр. 239. ISBN 9780123849533. В архиве из оригинала от 23.02.2018.
- ^ Маргграф (1747) "Опыт chimiques faites dans le dessein de tyrer un true sucre de diverses plantes, qui croissent dans nos contrées" В архиве 2016-06-24 в Wayback Machine [Химические эксперименты, проведенные с целью извлечения настоящего сахара из различных растений, произрастающих на наших землях], Histoire de l'académie royale des Sciences et belles-lettres de BerlinС. 79–90. Со страницы 90: В архиве 2014-10-27 на Wayback Machine "Les raisins secs, etant humectés d'une petite Quantité d'eau, de maniere qu'ils mollissent, peuvent alors etre pilés, & le Suc qu'on en exprime, etant depuré & épaissi, fournira une espece de Sucre". (Изюм, смоченный небольшим количеством воды до размягчения, затем может быть отжат, и выдавленный сок, [после] очистки и загустения, станет своего рода сахаром.)
- ^ Джон Ф. Робит: Основы химии углеводов. Springer Science & Business Media, 2012 г., ISBN 978-1-461-21622-3. п. 7.
- ^ Розанов, М.А. (1906). «О классификации стереоизомеров Фишера» 1.. Журнал Американского химического общества. 28: 114–121. Дои:10.1021 / ja01967a014.
- ^ Эмиль Фишер, Нобелевский фонд, в архиве из оригинала от 03.09.2009, получено 2009-09-02
- ^ Фрейзер-Рид, Берт, «Глюкоза Вант Хоффа», Chem. Англ. Новости, 77 (39): 8
- ^ "Отто Мейерхоф - Факты - NobelPrize.org" В архиве 2018-07-15 в Wayback Machine. NobelPrize.org. Проверено 5 сентября 2018.
- ^ "Ганс фон Эйлер-Челпин - Факты - NobelPrize.org" В архиве 2018-09-03 в Wayback Machine. NobelPrize.org. Проверено 5 сентября 2018.
- ^ "Артур Харден - Факты - NobelPrize.org" В архиве 2018-09-03 в Wayback Machine. NobelPrize.org. Проверено 5 сентября 2018.
- ^ "Бернардо Хусей - Факты - NobelPrize.org" В архиве 2018-07-15 в Wayback Machine. NobelPrize.org. Проверено 5 сентября 2018.
- ^ "Карл Кори - Факты - NobelPrize.org" В архиве 2018-07-15 в Wayback Machine. NobelPrize.org. Проверено 5 сентября 2018.
- ^ "Герти Кори - Факты - NobelPrize.org" В архиве 2018-07-15 в Wayback Machine. NobelPrize.org. Проверено 5 сентября 2018.
- ^ "Луис Лелуар - Факты - NobelPrize.org" В архиве 2018-07-15 в Wayback Machine. NobelPrize.org. Проверено 5 сентября 2018.
- ^ Йебра-Биуррун, M.C. (2005), «Подсластители», Энциклопедия аналитической науки, Elsevier, стр. 562–572, Дои:10.1016 / b0-12-369397-7 / 00610-5, ISBN 978-0-12-369397-6, получено 2020-09-15
- ^ «глюкоза». Колумбийская энциклопедия, 6-е изд .. 2015. Encyclopedia.com. 17 ноября 2015 г. http://www.encyclopedia.com В архиве 2009-04-26 на Wayback Machine.
- ^ а б Шенк, Фред В. (2006). «Глюкоза и глюкозосодержащие сиропы». Энциклопедия промышленной химии Ульмана. Дои:10.1002 / 14356007.a12_457.pub2. ISBN 978-3527306732.
- ^ Патрик Ф. Фокс: Advanced Dairy Chemistry Volume 3: лактоза, вода, соли и витамины, Springer, 1992. Том 3, ISBN 9780412630200. п. 316.
- ^ Бенджамин Кабальеро, Пол Финглас, Фидель Толдра: Энциклопедия еды и здоровья. Академическая пресса (2016). ISBN 9780123849533, Том 1, стр. 76.
- ^ Веню Кан и Чжицзюнь Чжан (2020): «Селективное производство уксусной кислоты путем каталитического быстрого пиролиза гексоз над солями калия», Катализаторы, том 10, страницы 502-515. Дои:10.3390 / catal10050502
- ^ Takagi, S .; Джеффри Г.А. (1979). «1,2-О-изопропилиден-D-глюкофураноза». Acta Crystallographica Раздел B. B35 (6): 1522–1525. Дои:10.1107 / S0567740879006968.
- ^ Белецкий, Миа; Эггерт, Ханне; Кристиан Норрилд, Йенс (1999). «Флуоресцентный датчик глюкозы, ковалентно связывающийся со всеми пятью гидроксигруппами α-D-глюкофуранозы. Повторное исследование». Журнал химического общества, Perkin Transactions. 2 (3): 449–456. Дои:10.1039 / A808896I.
- ^ Chandran, Sreekanth K .; Нангиа, Ашвини (2006). «Модулированная кристаллическая структура (Z '= 2) α-d-глюкофуранозо-1,2∶3,5-бис (п-толил) бороната». CrystEngComm. 8 (8): 581–585. Дои:10.1039 / B608029D.
- ^ Сообщается, что для метил-α-D-глюкуопиранозы в равновесии соотношение молекул в каждой конформации ротамера составляет 57% gg, 38% gt и 5% tg. Видеть Киршнер, Карл Н .; Вудс, Роберт Дж. (2001), «Взаимодействие с растворителями определяет конформацию углеводов», Proc. Natl. Акад. Sci. Соединенные Штаты Америки, 98 (19): 10541–45, Bibcode:2001ПНАС ... 9810541К, Дои:10.1073 / pnas.191362798, ЧВК 58501, PMID 11526221.[неосновной источник необходим ]
- ^ Макмерри, Джон Э. (1988), Органическая химия (2-е изд.), Брукс / Коул, стр. 866, г. ISBN 0534079687.
- ^ Хуаристи, Эйсебио; Куэвас, Габриэль (1995), Аномерный эффект, CRC Press, стр. 9–10, ISBN 978-0-8493-8941-2
- ^ а б Манфред Гессе, Герберт Мейер, Бернд Зее, Стефан Биенц, Лоран Биглер, Томас Фокс: Spektroskopische Methoden in der Organischen Chemie. 8-е исправленное издание. Георг Тиме, 2011 г., ISBN 978-3-13-160038-7, п. 34 (на немецком языке).
- ^ а б c d Bunn, H.F .; Хиггинс, П. Дж. (1981). «Реакция моносахаридов с белками: возможное эволюционное значение». Наука. 213 (4504): 222–24. Bibcode:1981Научный ... 213..222B. Дои:10.1126 / science.12192669. PMID 12192669.
- ^ Джереми М. Берг: Stryer Biochemie. Springer-Verlag, 2017, ISBN 978-3-662-54620-8, п. 531. (немецкий)
- ^ Реджинальд Х. Гарретт: Биохимия. Cengage Learning, 2012 г., ISBN 978-1-133-10629-6. С. 194, 199.
- ^ Дональд Воет, Джудит Г. Воет: Биохимия, 4-е издание. Джон Вили и сыновья, 2010 год, ISBN 978-0470-57095-1. п. 363.
- ^ Альберт Л. Ленингер, Биохимия, 6-е изд., Worth Publishers Inc., 1972 г., ISBN 0-87901-009-6 п. 228.
- ^ а б Питер К. Генрих: Löffler / Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014 г., ISBN 978-3-642-17972-3, п. 195. (немецкий)
- ^ а б c d е У. Сатьянараяна: Биохимия. Elsevier Health Sciences, 2014 г., ISBN 978-8-131-23713-7. п. 674.
- ^ Вассерман, Д. Х. (2009). «Четыре грамма глюкозы». Американский журнал физиологии. Эндокринология и метаболизм. 296 (1): E11–21. Дои:10.1152 / ajpendo.90563.2008. ЧВК 2636990. PMID 18840763.
- ^ «Высокий уровень глюкозы в крови и осложнения диабета: накопление молекул, известных как AGE, может быть ключевым звеном», Прогноз диабета, Американская диабетическая ассоциация, 2010 г., ISSN 0095-8301, заархивировано из оригинал на 2013-10-14, получено 2010-05-20
- ^ Основы гликобиологии. Аджит Варки (ред.) (2-е изд.). Пресса Лаборатории Колд Спринг Харбор. 2009 г. ISBN 978-0-87969-770-9. В архиве из оригинала от 06.12.2016.CS1 maint: другие (связь)
- ^ Питер К. Генрих: Löffler / Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014 г., ISBN 978-3-642-17972-3, п. 404.
- ^ Гарольд А. Харпер: Medizinische Biochemie. Springer-Verlag, 2013 г., ISBN 978-3-662-22150-1, п. 641. (немецкий)
- ^ Navale, A.M .; Паранджапе, А. Н. (2016). «Транспортеры глюкозы: физиологические и патологические роли». Биофизические обзоры. 8 (1): 5–9. Дои:10.1007 / s12551-015-0186-2. ЧВК 5425736. PMID 28510148.
- ^ а б c d е ж грамм Питер К. Генрих: Löffler / Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014 г., ISBN 978-3-642-17972-3, п. 199, 200. (немецкий)
- ^ Торенс, Б. (2015). «GLUT2, определение глюкозы и гомеостаз глюкозы». Диабетология. 58 (2): 221–32. Дои:10.1007 / s00125-014-3451-1. PMID 25421524.
- ^ а б Питер К. Генрих: Löffler / Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014 г., ISBN 978-3-642-17972-3, п. 214. (немецкий)
- ^ Huang, S .; Чех, М. П. (2007). «Транспортер глюкозы GLUT4». Клеточный метаболизм. 5 (4): 237–52. Дои:10.1016 / j.cmet.2007.03.006. PMID 17403369.
- ^ Говерс, Р. (2014). Клеточная регуляция поглощения глюкозы переносчиком глюкозы GLUT4. Достижения в клинической химии. 66. С. 173–240. Дои:10.1016 / B978-0-12-801401-1.00006-2. ISBN 9780128014011. PMID 25344989.
- ^ Ghezzi, C .; Loo DDF; Райт, Э. М. (2018). «Физиология почечной обработки глюкозы через SGLT1, SGLT2 и GLUT2». Диабетология. 61 (10): 2087–2097. Дои:10.1007 / s00125-018-4656-5. ЧВК 6133168. PMID 30132032.
- ^ Poulsen, S. B .; Fenton, R.A .; Риг, Т. (2015). «Натрий-глюкозный котранспорт». Текущее мнение в нефрологии и гипертонии. 24 (5): 463–9. Дои:10.1097 / MNH.0000000000000152. ЧВК 5364028. PMID 26125647.
- ^ «Химия для биологов: фотосинтез». www.rsc.org. В архиве из оригинала на 2016-08-04. Получено 2018-02-05.
- ^ Смит, Элисон М .; Zeeman, Samuel C .; Смит, Стивен М. (2005). «Деградация крахмала». Анну. Rev. Plant Biol. 56: 73–98. Дои:10.1146 / annurev.arplant.56.032604.144257. PMID 15862090.
- ^ Дональд Воет, Джудит Г. Воет: Биохимия, 4-е издание. Джон Вили и сыновья, 2010 год, ISBN 978-0470-57095-1. п. 359.
- ^ а б Дональд Воет, Джудит Г. Воет: Биохимия, 4-е издание. Джон Вили и сыновья, 2010 год, ISBN 978-0470-57095-1. п. 59.
- ^ а б Лешек Саблевски: Гомеостаз глюкозы и инсулинорезистентность. Издательство Bentham Science, 2011 г., ISBN 978-1-608-05189-2, п. 46.
- ^ Питер К. Генрих: Löffler / Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014 г., ISBN 978-3-642-17972-3, п. 389. (немецкий)
- ^ Adeva-Andany, M. M .; Pérez-Felpete, N .; Fernández-Fernández, C .; Donapetry-García, C .; Пасос-Гарсия, К. (2016). «Метаболизм глюкозы в печени у человека». Отчеты по бионауке. 36 (6): e00416. Дои:10.1042 / BSR20160385. ЧВК 5293555. PMID 27707936.
- ^ Х. Роберт Хортон, Лоуренс А. Моран, К. Грей Скримджер, Марк Д. Перри, Дж. Дэвид Рон: Биохимия. Pearson Studium; 4. aktualisierte Auflage 2008; ISBN 978-3-8273-7312-0; п. 490–496. (Немецкий)
- ^ а б Брайан К. Холл: Эволюция Стрикбергера. Jones & Bartlett Publishers, 2013 г., ISBN 978-1-449-61484-3, п. 164.
- ^ Реджинальд Х. Гарретт: Биохимия. Cengage Learning, 2012 г., ISBN 978-1-133-10629-6, п. 551.
- ^ Джонс, Дж. Г. (2016). «Глюкоза в печени и метаболизм липидов». Диабетология. 59 (6): 1098–103. Дои:10.1007 / s00125-016-3940-5. PMID 27048250.
- ^ Entner, N .; Дудоров, М. (1952). «Окисление глюкозы и глюконовой кислоты Pseudomonas saccharophila». J Biol Chem. 196 (2): 853–862. PMID 12981024.
- ^ Бонадонна, Риккардо С; Бонора, Энцо; Дель Прато, Стефано; Саккомани, Мария; Кобелли, Клаудио; Натали, Андреа; Фрассерра, Сильвия; Пекори, Неда; Ферраннини, Элеутерио; Бир, Деннис; ДеФронцо, Ральф А; Гули, Джованни (июль 1996 г.). «Роль транспорта глюкозы и фосфорилирования глюкозы в мышечной инсулинорезистентности NIDDM» (PDF). Сахарный диабет. 45 (7): 915–25. Дои:10.2337 / diab.45.7.915. PMID 8666143. S2CID 219249555. Получено 5 марта, 2017.
- ^ Краткий обзор медицинской биохимии @Google books, Blackwell Publishing, 2006, стр. 52, ISBN 978-1-4051-1322-9, в архиве из оригинала от 23.02.2018
- ^ Краткий обзор медицинской биохимии @Google books, Blackwell Publishing, 2006, стр. 50, ISBN 978-1-4051-1322-9, в архиве из оригинала от 23.02.2018
- ^ Аннибальди, А .; Видманн, К. (2010). «Метаболизм глюкозы в раковых клетках». Текущее мнение о клиническом питании и метаболическом лечении. 13 (4): 466–70. Дои:10.1097 / MCO.0b013e32833a5577. PMID 20473153. S2CID 205782021.
- ^ Саблевски, Л. (2013). «Экспрессия переносчиков глюкозы при раке». Biochimica et Biophysica Acta (BBA) - Обзоры на рак. 1835 (2): 164–9. Дои:10.1016 / j.bbcan.2012.12.004. PMID 23266512.
- ^ Adekola, K .; Rosen, S.T .; Шанмугам, М. (2012). «Транспортеры глюкозы в метаболизме рака». Текущее мнение в области онкологии. 24 (6): 650–4. Дои:10.1097 / CCO.0b013e328356da72. ЧВК 6392426. PMID 22913968.
- ^ «Глава 3: Расчет энергетического содержания пищевых продуктов - коэффициенты преобразования энергии», Пищевая энергия - методы анализа и коэффициенты пересчета, Документ 77 ФАО по продовольствию и питанию, Рим: Продовольственная и сельскохозяйственная организация, 2003 г., ISBN 978-92-5-105014-9, в архиве из оригинала 24.05.2010
- ^ Георг Шведт: Zuckersüße Chemie. Джон Вили и сыновья, 2012 год, ISBN 978-3-527-66001-8, п. 100 (на немецком языке).
- ^ Шмидт, Ланг: Physiologie des Menschen, 30. Auflage. Springer Verlag, 2007, стр. 907 (на немецком языке).
- ^ Dandekar, T .; Schuster, S .; Snel, B .; Huynen, M .; Борк, П. (1999). «Выравнивание пути: приложение для сравнительного анализа гликолитических ферментов». Биохимический журнал. 343 (1): 115–124. Дои:10.1042 / bj3430115. ЧВК 1220531. PMID 10493919.
- ^ Даш, Прамод. «Кровяной мозговой барьер и церебральный метаболизм (раздел 4, глава 11)». Neuroscience Online: Электронный учебник для нейронаук. Отделение нейробиологии и анатомии - Медицинская школа Техасского университета в Хьюстоне. Архивировано из оригинал на 17.11.2016.
- ^ Fairclough, Стивен Х .; Хьюстон, Ким (2004), «Метаболическая мера умственного усилия», Биол. Psychol., 66 (2): 177–190, Дои:10.1016 / j.biopsycho.2003.10.001, PMID 15041139, S2CID 44500072
- ^ Gailliot, Matthew T .; Баумейстер, Рой Ф .; Деуолл, К. Натан; Плант, Э. Эшби; Брюэр, Лорен Э .; Шмейхель, Брэндон Дж .; Тайс, Дайан М .; Манер, Джон К. (2007), «Самоконтроль полагается на глюкозу как на ограниченный источник энергии: сила воли - это больше, чем метафора» (PDF), J. Pers. Soc. Psychol., 92 (2): 325–336, CiteSeerX 10.1.1.337.3766, Дои:10.1037/0022-3514.92.2.325, PMID 17279852, в архиве (PDF) из оригинала от 18.08.2017
- ^ Gailliot, Matthew T .; Баумейстер, Рой Ф. (2007), «Физиология силы воли: связь глюкозы в крови с самоконтролем», Личное. Soc. Psychol. Ред., 11 (4): 303–327, CiteSeerX 10.1.1.475.9484, Дои:10.1177/1088868307303030, PMID 18453466, S2CID 14380313
- ^ Masicampo, E.J .; Баумейстер, Рой Ф. (2008 г.), «К физиологии двойного процесса мышления и суждения: лимонад, сила воли и дорогостоящий анализ на основе правил», Psychol. Sci., 19 (3): 255–60, Дои:10.1111 / j.1467-9280.2008.02077.x, PMID 18315798, S2CID 38596025
- ^ а б c Донард Дуайер: Метаболизм глюкозы в головном мозге. Academic Press, 2002 г., ISBN 978-0-123-66852-3, п. XIII.
- ^ а б c Koekkoek, L. L .; Mul, J.D .; Ла Флер, С. Э. (2017). «Определение уровня глюкозы в системе вознаграждения». Границы неврологии. 11: 716. Дои:10.3389 / fnins.2017.00716. ЧВК 5742113. PMID 29311793.
- ^ а б Tucker, R.M .; Тан, С. Ю. (2017). «Влияют ли непитательные подсластители на острый гомеостаз глюкозы у людей? Систематический обзор». Физиология и поведение. 182: 17–26. Дои:10.1016 / j.physbeh.2017.09.016. PMID 28939430. S2CID 38764657.
- ^ La Fleur, S.E .; Fliers, E .; Калсбек, А. (2014). Неврология гомеостаза глюкозы. Справочник по клинической неврологии. 126. С. 341–351. Дои:10.1016 / B978-0-444-53480-4.00026-6. ISBN 9780444534804. PMID 25410233..
- ^ Bisschop, P.H .; Fliers, E .; Калсбек, А. (2015). «Вегетативная регуляция выработки глюкозы в печени». Комплексная физиология. 5 (1): 147–165. Дои:10.1002 / cphy.c140009. PMID 25589267.
- ^ В. А. Шербаум, Б. М. Лобниг, В: Ганс-Петер Вольф, Томас Р. Вайхраух: Internistische Therapie 2006, 2007. 16-е издание. Эльзевир, 2006 г., ISBN 3-437-23182-0, п. 927, 985 (на немецком языке).
- ^ Гарольд А. Харпер: Medizinische Biochemie. Springer-Verlag, 2013 г., ISBN 978-3-662-22150-1, п. 294.
- ^ Clarke, S. F .; Фостер, Дж. Р. (2012). «История глюкометров и их роль в самоконтроле сахарного диабета». Британский журнал биомедицинских наук. 69 (2): 83–93. CiteSeerX 10.1.1.468.2196. Дои:10.1080/09674845.2012.12002443. PMID 22872934. S2CID 34263228.
- ^ «Диагностика диабета и изучение предиабета». Американская диабетическая ассоциация. В архиве из оригинала от 28.07.2017. Получено 2018-02-20.
- ^ а б Ричард А. Харви, Дениз Р. Ферье: Биохимия. 5-е издание, Lippincott Williams & Wilkins, 2011 г., ISBN 978-1-608-31412-6, п. 366.
- ^ а б У Сатьянараяна: Биохимия. Elsevier Health Sciences, 2014 г., ISBN 978-8-131-23713-7, п. 508.
- ^ Holt, S. H .; Miller, J.C .; Петоч, П. (1997). «Индекс инсулина пищевых продуктов: потребность в инсулине, вызванная порциями обычных пищевых продуктов по 1000 кДж». Американский журнал клинического питания. 66 (5): 1264–1276. Дои:10.1093 / ajcn / 66.5.1264. PMID 9356547.
- ^ а б Питер К. Генрих: Löffler / Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014 г., ISBN 978-3-642-17972-3, п. 27. (немецкий)
- ^ Рёдер П.В., Ву Б., Лю И, Хань В. (2016). "Панкреатическая регуляция гомеостаза глюкозы". Exp. Мол. Med. 48 (3, март): e219–. Дои:10.1038 / emm.2016.6. ЧВК 4892884. PMID 26964835.
- ^ Эстела, Карлос (2011) «Уровни глюкозы в крови», Журнал математического моделирования для студентов: One + Two: Vol. 3: Вып. 2, статья 12.
- ^ «Углеводы и сахар в крови». Источник питания. 2013-08-05. В архиве с оригинала на 30.01.2017. Получено 2017-01-30 - через Harvard T.H. Школа общественного здравоохранения Чан.
- ^ "Базы данных о составе пищевых продуктов показывают список продуктов". В архиве 2017-12-22 в Wayback Machine. ndb.nal.usda.gov.
- ^ а б c d е ж грамм час я П. Дж. Стипендиаты: Технология пищевой промышленности. Издательство Woodhead Publishing, 2016, ISBN 978-0-081-00523-1, п. 197.
- ^ а б Томас Беккер, Дитмар Брайтхаупт, Хорст Вернер Доэлле, Армин Фихтер, Гюнтер Шлегель, Сакаю Симидзу, Хидеаки Ямада: Биотехнологии, в: Энциклопедия промышленной химии Ульмана, 7-е издание, Wiley-VCH, 2011. ISBN 978-3-527-32943-4. Том 6, с. 48.
- ^ а б c Японское общество исследования амилазы: Справочник по амилазам и родственным ферментам. Эльзевир, 2014 г. ISBN 978-1-483-29939-6, п. 195.
- ^ Madsen, G.B .; Norman, B.E .; Слотт, С. (1973). «Новая термостойкая бактериальная амилаза и ее использование в высокотемпературном сжижении». Крахмал - Stärke. 25 (9): 304–308. Дои:10.1002 / звезда.19730250906.
- ^ Норман Б. Э. (1982). «Новый фермент разветвления для применения в индустрии глюкозного сиропа». Крахмал - Stärke. 34 (10): 340–346. Дои:10.1002 / звезда.19820341005.
- ^ Джеймс Н. Бемиллер, Рой Л. Уистлер (2009). Крахмал: химия и технология. Пищевая наука и технология (3-е изд.). Нью-Йорк: Academic Press. ISBN 978-0080926551.
- ^ BeMiller, Джеймс Н .; Уистлер, Рой Л., ред. (2009). Крахмал: химия и технология. Пищевая наука и технология (3-е изд.). Нью-Йорк: Academic Press. ISBN 978-0080926551. Получено 25 ноября 2016.
- ^ Алан Дэвидсон: Оксфордский компаньон к еде (1999). «Мидзуаме», стр. 510 ISBN 0-19-211579-0.
- ^ Алан Дэвидсон: Оксфордский компаньон к еде. ОУП Оксфорд, 2014 г., ISBN 978-0-191-04072-6, п. 527.
- ^ Государственный университет Орегона: Сахар, по состоянию на 28 июня 2018 г.
- ^ «Кукурузный сироп с высоким содержанием фруктозы: вопросы и ответы». Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. 2014-11-05. В архиве из оригинала на 2018-01-25. Получено 2017-12-18.
- ^ Кевин Панг: Мексиканская кока-кола стала хитом в США. В: Сиэтл Таймс, 29 октября 2004 г.
- ^ Стив Т. Беккет: Производство и использование промышленного шоколада Beckett. Джон Уайли и сыновья, 2017, ISBN 978-1-118-78014-5, п. 82.
- ^ Джеймс А. Кент: Справочник Ригеля по промышленной химии. Springer Science & Business Media, 2013 г., ISBN 978-1-475-76431-4, п. 938.
- ^ Х. Фелинг: Quantitative Bestimmung des Zuckers im Harn. В: Архив для физиологии Хайлькунде (1848), том 7, стр. 64–73 (на немецком языке).
- ^ Б. Толленс: Über Ammon-alkalische Silberlösung als Reagens auf Aldehyd. В Berichte der Deutschen Chemischen Gesellschaft (1882), том 15, стр. 1635–1639 (на немецком языке).
- ^ Барфоед, К. (1873). "Ueber die Nachweisung des Traubenzuckers neben Dextrin und verwandten Körpern". Zeitschrift für Analytische Chemie (на немецком). 12: 27–32. Дои:10.1007 / BF01462957. S2CID 95749674.
- ^ Эмиль Нюландер: Über alkalische Wismuthlösung als Reagens auf Traubenzucker im Harne, Zeitschrift für Physiologische Chemie. Том 8, выпуск 3, 1884 г., стр. 175–185 Абстрактный. В архиве 2015-09-23 на Wayback Machine (на немецком).
- ^ а б c d е ж грамм час я Георг Шведт: Zuckersüße Chemie. Джон Вили и сыновья, 2012 год, ISBN 978-3-527-66001-8, п. 102 (на немецком языке).
- ^ Триндер, П. (1969). «Определение глюкозы в крови с помощью оксидазы глюкозы с альтернативным кислородным акцептором». Анналы клинической биохимии. 6: 24–27. Дои:10.1177/000456326900600108. S2CID 58131350.
- ^ Мидзогути, Макото; Исияма, Мунетака; Шига, Масанобу (1998). «Водорастворимый хромогенный реагент для колориметрического определения перекиси водорода - альтернатива 4-аминоантипирину, работающему на длинных волнах». Аналитические коммуникации. 35 (2): 71–74. Дои:10.1039 / A709038B.
- ^ Ван, Дж. (2008). «Электрохимические биосенсоры глюкозы». Химические обзоры. 108 (2): 814–825. Дои:10.1021 / cr068123a. PMID 18154363..
- ^ Чен, X .; Chen, J .; Deng, C .; Xiao, C .; Ян, Й .; Nie, Z .; Яо, С. (2008). «Амперометрический биосенсор глюкозы на основе электрода, модифицированного углеродными нанотрубками, легированными бором». Таланта. 76 (4): 763–767. Дои:10.1016 / j.talanta.2008.04.023. PMID 18656655.
- ^ Ван, Гуанфэн; Вэй, Ян; Чжан, Вэй; Чжан, Сяоцзюнь; Клык, Бин; Ван, Лун (2010). «Безферментное амперометрическое определение глюкозы с использованием композитов нанопроволоки Cu-CuO». Microchimica Acta. 168 (1–2): 87–92. Дои:10.1007 / s00604-009-0260-1. S2CID 98567636.
- ^ Охара, Т. Дж .; Rajagopalan, R .; Хеллер, А. (1994). ""Проводные «ферментные электроды для амперометрического определения глюкозы или лактата в присутствии мешающих веществ». Аналитическая химия. 66 (15): 2451–2457. Дои:10.1021 / ac00087a008. PMID 8092486.
- ^ а б Борисов, С. М .; Вольфбайс, О. С. (2008). «Оптические биосенсоры». Химические обзоры. 108 (2): 423–461. Дои:10.1021 / cr068105t. PMID 18229952.
- ^ Ferri, S .; Кодзима, К .; Соде, К. (2011). «Обзор глюкозооксидаз и глюкозодегидрогеназ: ферменты, чувствительные к глюкозе с высоты птичьего полета». Журнал диабетической науки и технологий. 5 (5): 1068–76. Дои:10.1177/193229681100500507. ЧВК 3208862. PMID 22027299.
- ^ Mader, Heike S .; Вольфбайс, Отто С. (2008). «Зонды на основе бороновой кислоты для микроопределения сахаридов и гликозилированных биомолекул». Microchimica Acta. 162 (1–2): 1–34. Дои:10.1007 / s00604-008-0947-8. S2CID 96768832.
- ^ Wolfbeis, Otto S .; Оэме, Инес; Папковская, Наталья; Климант, Инго (2000). «Биосенсоры глюкозы на основе золь-геля, использующие оптические преобразователи кислорода, и способ компенсации переменного кислородного фона». Биосенсоры и биоэлектроника. 15 (1–2): 69–76. Дои:10.1016 / S0956-5663 (99) 00073-1. PMID 10826645.
- ^ а б Галант, А. Л .; Kaufman, R.C .; Уилсон, Дж. Д. (2015). «Глюкоза: обнаружение и анализ». Пищевая химия. 188: 149–160. Дои:10.1016 / j.foodchem.2015.04.071. PMID 26041177.
- ^ Sanz, M. L .; Sanz, J .; Мартинес-Кастро, И. (2004). «Газохромато-масс-спектрометрический метод качественного и количественного определения дисахаридов и трисахаридов в меде». Журнал хроматографии А. 1059 (1–2): 143–148. Дои:10.1016 / j.chroma.2004.09.095. PMID 15628134.
- ^ Институт молекулярной физиологии растений им. Макса Планка в базе данных Golm (19 июля 2007 г.). «Масс-спектр глюкозы». База данных метаболома Голма. В архиве из оригинала на 2018-09-09. Получено 2018-06-04.
- ^ Cabañero, A.I .; Recio, J. L .; Руперес, М. (2006). «Жидкостная хроматография в сочетании с масс-спектрометрией изотопного состава: новый взгляд на обнаружение фальсификации меда». J Agric Food Chem. 54 (26): 9719–9727. Дои:10.1021 / jf062067x. PMID 17177492.
- ^ Беккер, М .; Либнер, Ф .; Rosenau, T .; Поттхаст, А. (2013). «Подход этоксимации-силилирования для анализа моно- и дисахаридов и характеристики их идентификационных параметров с помощью ГХ / МС». Таланта. 115: 642–51. Дои:10.1016 / j.talanta.2013.05.052. PMID 24054643.
- ^ Gesellschaft Deutscher Chemiker: wayback = 20100331071121 Anlagen zum Positionspapier der Fachgruppe Nuklearchemie В архиве 2010-03-31 на Wayback Machine, Февраль 2000 г.
- ^ Maschauer, S .; Пранте, О. (2014). «Подслащивание фармацевтической радиохимии с помощью (18) f-фторгликозилирования: краткий обзор». BioMed Research International. 2014: 1–16. Дои:10.1155/2014/214748. ЧВК 4058687. PMID 24991541.
внешняя ссылка
- «Глюкоза». Портал информации о наркотиках. Национальная медицинская библиотека США.
- «Смесь декстрозы с хлоридом натрия». Портал информации о наркотиках. Национальная медицинская библиотека США.
АТФ ADP АТФ ADP + + 2 ×  2 ×  2 × 3-фосфоглицерат 2 ×  2 × 2-фосфоглицерат 2 ×  2 × Фосфоенолпируват 2 ×  ADP АТФ 2 × Пируват 2 × |