Лигнин - Lignin
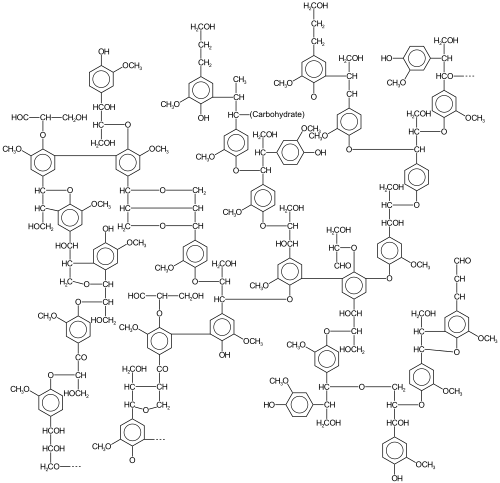
Лигнин это класс сложных органические полимеры которые образуют ключевые структурные материалы в опорных тканях сосудистые растения и немного водоросли.[1] Лигнины особенно важны в образовании клеточные стенки, особенно в дерево и лай, потому что они придают жесткость и не гниют. Химически лигнины сшиты фенольный полимеры.[2]
История
Лигнин впервые был упомянут в 1813 году швейцарским ботаником. А. П. де Кандоль, который описал его как волокнистый безвкусный материал, не растворимый в воде и спирте, но растворимый в слабых щелочных растворах, и который может быть осажденный из раствора с помощью кислоты.[3] Он назвал это вещество «лигнин», которое происходит от латинского слова lignum,[4] имея в виду дерево. Это один из самых распространенных органические полимеры на земной шар, превосходит только целлюлоза. Лигнин составляет 30% не-ископаемое органический углерод[5] и от 20 до 35% от сухой массы древесины.[6] В Каменноугольный Период (геология) был частично определен эволюция лигнина.
Состав и структура
Состав лигнина варьируется от вида к виду. Пример композиции из осина[7] образец - 63,4% углерода, 5,9% водорода, 0,7% золы (минеральные компоненты) и 30% кислорода (по разнице),[8] что приблизительно соответствует формуле (C31ЧАС34О11)п.
Как биополимер, лигнин необычен из-за неоднородность и отсутствие определенной первичной структуры. Его наиболее часто отмечаемая функция - поддержка путем укрепления древесины (в основном состоящей из ксилема клетки и лигнифицированные склеренхима волокна) в сосудистых растениях.[9][10][11]
В лигнолы это сшивка бывают трех основных типов, все производные от фенилпропана: 4-гидрокси-3-метоксифенилпропан, 3,5-диметокси-4-гидроксифенилпропан и 4-гидроксифенилпропан. Первые чаще встречаются у хвойных пород, а вторые - у лиственных пород.
Лигнин представляет собой сшитый полимер с молекулярные массы свыше 10 000 ты. Это относительно гидрофобный и богат ароматный субъединицы. В степень полимеризации измерить сложно, так как материал неоднороден. Были описаны различные типы лигнина в зависимости от способов выделения.[12]

Три монолигнол мономеры являются предшественниками, и все они метоксилированный в различной степени: п-кумариловый спирт, конифериловый спирт, и синапиловый спирт.[13] Эти лигнолы входят в состав лигнина в виде фенилпропаноиды п-гидроксифенил (H), гваяцил (G) и сирингил (S) соответственно.[5] Голосеменные имеют лигнин, который почти полностью состоит из G с небольшими количествами H. двудольные покрытосеменные чаще всего представляет собой смесь G и S (с очень небольшим количеством H), и однодольные лигнин представляет собой смесь всех трех.[5] Многие травы содержат в основном G, а в некоторых пальмах - S.[14] Все лигнины содержат небольшие количества неполных или модифицированных монолигнолов, а другие мономеры являются заметными в недревесных растениях.[15]
Биологическая функция
Лигнин заполняет пробелы в клеточная стенка между целлюлоза, гемицеллюлоза, и пектин компоненты, особенно в сосудистых и опорных тканях: ксилема трахеиды, элементы судна и склереида клетки. это ковалентно связан с гемицеллюлоза и поэтому перекрестные ссылки другое растение полисахариды, придавая механическую прочность клеточная стенка и, как следствие, завод в целом.[16] Его особенно много в сжатой древесине, но мало в растянутой древесине,[нужна цитата ] какие типы реакция дерева.
Лигнин играет решающую роль в проведении воды в растение стебли. В полисахарид компоненты растения клеточные стенки очень гидрофильный и поэтому проницаемый поливать, тогда как лигнин больше гидрофобный. Сшивание полисахаридов лигнином является препятствием для поглощения воды клеточной стенкой. Таким образом, лигнин позволяет сосудистой ткани растения эффективно проводить воду.[17] Лигнин присутствует во всех сосудистые растения, но не в мохообразные, поддерживая идею о том, что первоначальная функция лигнина была ограничена водным транспортом. Однако он присутствует в красные водоросли, что, по-видимому, предполагает, что общий предок растений и красных водорослей также синтезировал лигнин. Это предполагает, что его первоначальная функция была структурной; он играет эту роль в красных водорослях Каллиартрон, где он поддерживает стыки между кальцинированный сегменты.[1]Другая возможность заключается в том, что лигнины в красных водорослях и в растениях являются результатом конвергентной эволюции, а не общего происхождения.[1]
Экономическое значение

Мировое коммерческое производство лигнина является следствием производства бумаги. В 1988 году во всем мире было произведено более 220 миллионов тонн бумаги.[18] Большая часть этой статьи была одобрена; лигнин составляет около 1/3 массы лигноцеллюлозы, предшественника бумаги. Таким образом, можно видеть, что с лигнином обращаются в очень больших масштабах. Лигнин является препятствием для производства бумаги, поскольку он окрашен, желтеет на воздухе, а его присутствие ослабляет бумагу. После отделения от целлюлозы она сжигается как топливо. Лишь небольшая фракция используется в широком диапазоне приложений небольшого объема, где важна форма, но не качество.[19]
Механический, или высокопроизводительный мякоть, который используется для создания газетная бумага, по-прежнему содержит большую часть лигнина, изначально присутствующего в древесине. Этот лигнин вызывает пожелтение газетной бумаги с возрастом.[4] Бумага высокого качества требует удаления лигнина из целлюлозы. Эти процессы делигнификации являются основными технологиями бумажной промышленности, а также источником серьезных экологических проблем.
В сульфитная варка, лигнин удаляется из древесной массы как лигносульфонаты, для которого было предложено множество приложений.[20] Они используются как диспергенты, увлажнители, стабилизаторы эмульсии, и секвестранты (очистка воды ).[21] Лигносульфонат также был первым семейством редукторы воды или суперпластификаторы будет добавлен в 1930-х годах в качестве добавки к свежим конкретный чтобы уменьшить переход воды в цемент (Туалет) коэффициент, основной параметр, контролирующий бетон пористость, и, следовательно, его механическая сила, это диффузионность и это гидравлическая проводимость, все параметры, необходимые для его долговечности. Он применяется в составе экологически безопасных средств пылеподавления для дорог. Кроме того, его можно использовать при производстве биоразлагаемого пластика вместе с целлюлозой в качестве альтернативы пластмассам, полученным из углеводородов, если экстракция лигнина достигается с помощью более экологически безопасного процесса, чем производство обычных пластиков.
Лигнин удаляется крафт-процесс обычно сжигается из-за его топливной ценности, обеспечивая энергией мельницу. Существуют два коммерческих процесса удаления лигнина из черного щелока для более ценных видов использования: LignoBoost (Швеция) и LignoForce (Канада). Лигнин более высокого качества потенциально может стать возобновляемым источником ароматный составы для химической промышленности с доступным рынком более 130 миллиардов долларов.[22]
Учитывая, что это самый распространенный биополимер после целлюлоза, лигнин был исследован как сырье для производства биотоплива и может стать важным растительным экстрактом при разработке нового класса биотоплива.[23][24]
Биосинтез
Лигнин биосинтез начинается в цитозоль с синтезом гликозилированный монолигнолы из аминокислота фенилаланин. Эти первые реакции делятся с фенилпропаноид путь. Прикрепленный глюкоза делает их водорастворимыми и менее токсичный. После транспортировки через клеточная мембрана к апопласт, глюкоза удаляется, и начинается полимеризация.[25] Многое о его анаболизм не понимается даже после более чем столетнего изучения.[5]

В полимеризация шаг, то есть радикально-радикальное соединение, катализированный к окислительные ферменты. Обе пероксидаза и лакказа ферменты присутствуют в растение клеточные стенки, и неизвестно, участвует ли одна или обе эти группы в полимеризации. Также могут быть задействованы низкомолекулярные окислители. Окислительный фермент катализирует образование монолигнола. радикалы. Часто говорят, что эти радикалы подвергаются некаталитическому взаимодействию с образованием лигнина. полимер, но эта гипотеза недавно была оспорена.[26] Однако альтернативная теория, предполагающая неопределенный биологический контроль, не получила широкого распространения.
Биоразложение
В отличие от других биополимеров (например, белков, ДНК и даже целлюлозы) лигнин устойчив к деградации и гидролизу, катализируемому кислотами и основаниями. Однако степень, в которой лигнин разлагается или не разлагается, зависит от вида и типа растительной ткани. Например, сирингил (S) лигнол более восприимчив к разложению в результате грибкового разложения, поскольку он имеет меньше ариларильных связей и более низкий окислительно-восстановительный потенциал, чем гваяцильные звенья.[27][28] Поскольку он сшит с другими компонентами клеточной стенки, лигнин сводит к минимуму доступность целлюлозы и гемицеллюлозы для микробных ферментов, что приводит к снижению усвояемости биомассы.[17]
Некоторые лигнинолитические ферменты включают: гем пероксидазы такие как лигнин пероксидазы, пероксидазы марганца, универсальные пероксидазы, и обесцвечивающие красители пероксидазы а также на основе меди лаккейсы. Пероксидазы лигнина окисляют нефенольный лигнин, тогда как пероксидазы марганца окисляют только фенольные структуры. Обесцвечивающие краситель пероксидазы, или DyP, проявляют каталитическую активность в отношении широкого диапазона модельных соединений лигнина, но их in vivo субстрат неизвестен. В общем, лакказы окисляют фенольные субстраты, но было показано, что некоторые грибные лакказы окисляют нефенольные субстраты в присутствии синтетических окислительно-восстановительных медиаторов.[29][30]
Разложение лигнина грибами
Хорошо изученные лигнинолитические ферменты обнаружены в Phanerochaete chrysosporium[31] и другие грибы белой гнили. Некоторые грибы белой гнили, такие как С. subvermispora, может разлагать лигнин в лигноцеллюлоза, но у других такой способности нет. В большинстве случаев деградация грибкового лигнина связана с секретируемыми пероксидазы. Многие грибковые лаккейсы также секретируются, что облегчает разложение соединений, производных фенольного лигнина, хотя также описаны несколько внутриклеточных грибковых лакказ. Важным аспектом деградации грибкового лигнина является активность вспомогательных ферментов по выработке H2О2 требуется для функции лигнин пероксидаза и другие гем пероксидазы.[29]
Разложение лигнина бактериями
Бактериям не хватает большинства ферментов, используемых при расщеплении лигнина грибами, но бактериальная деградация может быть довольно обширной.[32] Лигнинолитическая активность бактерий широко не изучалась, хотя впервые она была описана в 1930 году. Были охарактеризованы многие бактериальные DyP. Бактерии не экспрессируют пероксидазы растительного типа (лигнинпероксидаза, Mn пероксидаза или универсальные пероксидазы), но три из четырех классов DyP обнаруживаются только у бактерий. В отличие от грибов, большинство бактериальных ферментов, участвующих в деградации лигнина, являются внутриклеточными, включая два класса DyP и большинство бактериальных лакказ.[30]
Бактериальное разложение лигнина особенно актуально в водных системах, таких как озера, реки и ручьи, где поступающие с суши материалы (например, опавшие листья) могут попадать в водные пути и вымываться. растворенный органический углерод богат лигнином, целлюлозой и гемицеллюлозой. В окружающей среде лигнин может разлагаться либо биотически через бактерии, либо абиотически через фотохимические изменения, и часто последнее способствует первому.[33] В дополнение к наличию или отсутствию света на биоразлагаемость лигнина влияют несколько факторов окружающей среды, включая состав бактериального сообщества, минеральные ассоциации и окислительно-восстановительное состояние.[34][35]
Пиролиз
Пиролиз лигнина во время горение из дерева или уголь Производство выпускает ряд продуктов, наиболее характерными из которых являются метокси -замещенный фенолы. Из них наиболее важными являются гваякол и сирингол и их производные. Их присутствие можно использовать для отслеживания курить источник пожара. В Готовка, лигнин в виде твердая древесина является важным источником этих двух соединений, которые придают характерный аромат и вкус копченые продукты такие как барбекю. Основные вкусовые соединения копченая ветчина находятся гваякол и его 4-, 5- и 6-метилпроизводные, а также 2,6-диметилфенол. Эти соединения образуются в результате термического разложения лигнина в древесине, используемой в коптильне.[36]
Химический анализ
Традиционным методом количественного определения лигнина в целлюлозно-бумажной промышленности является тест лигнина Класона и растворимого в кислоте лигнина, который стандартизирован в соответствии с TAPPI.[37] или NREL[38] процедура. Целлюлозу сначала декристаллизовывают и частично деполимеризуют до олигомеров, выдерживая образец в 72% -ной серной кислоте при 30 ° C в течение 1 часа. Затем кислоту разбавляют до 4%, добавляя воду, и деполимеризацию завершают кипячением (100 ° C) в течение 4 часов или варкой под давлением при 2 барах (124 ° C) в течение 1 часа. Кислоту вымывают и образец сушат. Остающийся остаток называется лигнином Класона. Часть лигнина, растворимого в кислоте лигнина (ASL) растворяется в кислоте. ASL количественно определяется интенсивностью его УФ поглощение пик при 280 нм. Этот метод подходит для древесных лигнинов, но не одинаково хорошо для различных лигнинов из разных источников. Углеводный состав также может быть проанализирован из ликеров Класона, хотя могут быть продукты распада сахара (фурфурол и 5-гидроксиметилфурфурол ).
Раствор соляной кислоты и флороглюцин используется для обнаружения лигнина (тест Виснера). Появляется ярко-красный цвет благодаря наличию кониферальдегид группы в лигнине.[39]
Тиогликолиз аналитический метод для лигнина количественное определение.[40] Структура лигнина также может быть изучена с помощью компьютерного моделирования.[41]
Термохимолиз (химическое разложение вещества в вакууме и при высокой температуре) с гидроксид тетраметиламмония (TMAH) или оксид меди[42] также использовался для характеристики химического состава лигнина. Отношение сирингиллигнола (S) к ванилиллигнолу (V) и циннамиллигнола (C) к ваниллиллигнолу (V) варьируется в зависимости от типа растения и, следовательно, может использоваться для отслеживания источников растений в водных системах (древесные или неделимые) древесные и покрытосеменные против голосеменных).[43] Отношения карбоновых кислот (Ad) к альдегидным (Al) формам лигнолов (Ad / Al) показывают диагенетическую информацию, причем более высокие отношения указывают на более сильно разложившийся материал.[44][45] Увеличение значения (Ad / Al) указывает на то, что в боковой цепи алкиллигнина произошла реакция окислительного расщепления, которая, как было показано многими, является этапом разложения древесины. белая гниль и немного мягкого грибы гнили.[44][45][46][47][48]
Твердое состояние 13C ЯМР был использован для определения концентрации лигнина, а также других основных компонентов в древесине, например целлюлоза, и как это меняется с микробным распадом.[44][45][47][48] Возможен традиционный ЯМР в растворе для лигнина. Однако многие интактные лигнины имеют сшитую очень высокую молярную массовую долю, которую трудно растворить даже для функционализации.
Более поздние разработки в этой области привели к высокопроизводительному анализу лигнина с использованием пиролизера и молекулярно-лучевого масс-спектрометра. С помощью этого метода можно анализировать сотню образцов в день и не требует влажной химии.
Смотрите также
- Клеточная стенка - Наружный слой некоторых ячеек
Рекомендации
- ^ а б c Martone, Pt; Эстевес, Jm; Лу, Ф; Руэль, К; Денни, штат Массачусетс; Somerville, C; Ральф, Дж (январь 2009 г.). «Открытие лигнина в морских водорослях показывает конвергентную эволюцию архитектуры клеточной стенки». Текущая биология. 19 (2): 169–75. Дои:10.1016 / j.cub.2008.12.031. ISSN 0960-9822. PMID 19167225. S2CID 17409200.
- ^ Лебо, Стюарт Э. мл .; Гаргулак, Джерри Д.; МакНелли, Тимоти Дж. (2001). «Лигнин». Энциклопедия химической технологии Кирка-Отмера. Энциклопедия химической технологии Кирка-Отмера. John Wiley & Sons, Inc. Дои:10.1002 / 0471238961.12090714120914.a01.pub2. ISBN 978-0-471-23896-6. Получено 2007-10-14.
- ^ де Кандоль, M.A.P. (1813 г.). Theorie Elementaire de la Botanique or Exposition des Principes de la Classification Naturelle et de l'Art de Decrire et d'Etudier les Vegetaux. Париж: Детервиль. См. Стр. 417.
- ^ а б Э. Шёстрём (1993). Химия древесины: основы и приложения. Академическая пресса. ISBN 978-0-12-647480-0.
- ^ а б c d W. Boerjan; Дж. Ральф; М. Баучер (июнь 2003 г.). «Биосинтез лигнина». Анну. Rev. Plant Biol. 54 (1): 519–549. Дои:10.1146 / annurev.arplant.54.031902.134938. PMID 14503002.
- ^ Ли Цзинцзин (2011) Выделение лигнина из дерева. САЙМСКИЙ УНИВЕРСИТЕТ ПРИКЛАДНЫХ НАУК.
- ^ В упомянутой статье не указывается порода осины, только то, что она была из Канады.
- ^ Сян-Хуэй Кинг; Питер Р. Соломон; Эйтан Авни; Роберт В. Кафлин (осень 1983 г.). «Моделирование состава смолы при пиролизе лигнина» (PDF). Симпозиум по математическому моделированию явлений пиролиза биомассы, Вашингтон, округ Колумбия, 1983 г.. п. 1.
- ^ (1995, Биология, оружие и лагерь).
- ^ Анатомия семенных растений, Исав, 1977.
- ^ Wardrop; (1969). "Эрингиум sp .; ". Aust. J. Botany. 17 (2): 229–240. Дои:10.1071 / bt9690229.
- ^ «Лигнин и его свойства: Глоссарий номенклатуры лигнина». Диалог / Информационные бюллетени Том 9, Номер 1. Институт Лигнина. Июль 2001 г. Архивировано с оригинал на 2007-10-09. Получено 2007-10-14.
- ^ К. Фройденберг и А.К. Нэш (редакторы) (1968). Конституция и биосинтез лигнина. Берлин: Springer-Verlag.CS1 maint: дополнительный текст: список авторов (ссылка на сайт)
- ^ Курода К., Одзава Т., Уэно Т. (апрель 2001 г.). «Характеристика лигнина саговой пальмы (Metroxylon sagu) с помощью аналитического пиролиза». J Agric Food Chem. 49 (4): 1840–7. Дои:10.1021 / jf001126i. PMID 11308334. S2CID 27962271.
- ^ Дж. Ральф; и другие. (2001). «Выявление новых структур лигнинов CAD- и COMT-дефицитных растений методом ЯМР». Фитохимия. 57 (6): 993–1003. Дои:10.1016 / S0031-9422 (01) 00109-1. PMID 11423146.
- ^ Chabannes, M .; и другие. (2001). "На месте анализ лигнинов в трансгенном табаке показывает различное влияние индивидуальных трансформаций на пространственные паттерны отложения лигнина на клеточном и субклеточном уровнях ». Завод J. 28 (3): 271–282. Дои:10.1046 / j.1365-313X.2001.01159.x. PMID 11722770.
- ^ а б К.В. Сарканен и К. Людвиг (ред.) (1971). Лигнины: появление, образование, структура и реакции. Нью-Йорк: Wiley Intersci.CS1 maint: дополнительный текст: список авторов (ссылка на сайт)
- ^ Рудольф Патт et аль. (2005). «Мякоть». Бумага и целлюлоза. Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. С. 1–92. Дои:10.1002 / 14356007.a18_545.pub4. ISBN 9783527306732.
- ^ Информационный бюллетень NNFCC по возобновляемым химическим веществам: лигнин
- ^ «Использование лигнина от сульфитной варки». Архивировано из оригинал на 2007-10-09. Получено 2007-09-10.
- ^ Барбара А. Токай (2000). «Биомасса химикатов». Энциклопедия промышленной химии Ульмана. Дои:10.1002 / 14356007.a04_099. ISBN 978-3527306732.
- ^ «Frost & Sullivan: полный рост рынка лигнина с перспективными возможностями уже в 2017 году».
- ^ Фолкедал, Брюс (2016), «Целлюлозный этанол: что делать с лигнином», Биомасса, получено 2016-08-10.
- ^ Абенгоа (2016-04-21), Важность лигнина для производства этанола, получено 2016-08-10.
- ^ Сэмюэлс А.Л., Ренсинг К.Х., Дуглас С.Дж., Мэнсфилд С.Д., Дхармавардхана Д.П., Эллис Б.Э. (ноябрь 2002 г.). «Клеточные машины производства древесины: дифференциация вторичной ксилемы Pinus contorta var. Latifolia». Planta. 216 (1): 72–82. Дои:10.1007 / s00425-002-0884-4. PMID 12430016. S2CID 20529001.
- ^ Davin, L.B .; Льюис, Н.Г. (2005). «Первичные структуры лигнина и дирижентные участки». Текущее мнение в области биотехнологии. 16 (4): 407–415. Дои:10.1016 / j.copbio.2005.06.011. PMID 16023847.
- ^ Vane, Christopher H .; Драге, Тревор С .; Снейп, Колин Э. (февраль 2003 г.). «Биоразложение древесины дуба во время роста гриба шиитаке: молекулярный подход». Журнал сельскохозяйственной и пищевой химии. 51 (4): 947–956. Дои:10.1021 / jf020932h. PMID 12568554.
- ^ Vane, Christopher H .; Драге, Тревор С .; Снейп, Колин Э. (январь 2006 г.). «Разложение коры грибком белой гнили Lentinula edodes: потеря полисахаридов, устойчивость к лигнину и выявление суберина». Международный биодестерирование и биоразложение. 57 (1): 14–23. Дои:10.1016 / j.ibiod.2005.10.004.
- ^ а б Успехи прикладной микробиологии. Vol. 82. Гэдд, Джеффри М., Сариаслани, Сима. Оксфорд: академический. 2013. С. 1–28. ISBN 9780124076792. OCLC 841913543.CS1 maint: другие (ссылка на сайт)
- ^ а б де Гонсало, Гонсало; Colpa, Dana I .; Habib, Mohamed H.M .; Fraaije, Марко В. (2016). «Бактериальные ферменты, участвующие в деградации лигнина». Журнал биотехнологии. 236: 110–119. Дои:10.1016 / j.jbiotec.2016.08.011. PMID 27544286.
- ^ Тьен, М. (1983). «Лигнин-деградирующий фермент из Burds Hymenomycete Phanerochaete chrysosporium». Наука. 221 (4611): 661–3. Bibcode:1983Научный ... 221..661Т. Дои:10.1126 / science.221.4611.661. PMID 17787736. S2CID 8767248.
- ^ Pellerin, Brian A .; Hernes, Peter J .; Сарасено, Джон Франко; Спенсер, Роберт Г. М .; Бергамаски, Брайан А. (май 2010 г.). «Микробное разложение сточных вод растений изменяет фенолы лигнина и предшественники тригалометана». Журнал качества окружающей среды. 39 (3): 946–954. Дои:10.2134 / jeq2009.0487. ISSN 0047-2425. PMID 20400590.
- ^ Хернес, Питер Дж. (2003). «Фотохимическая и микробная деградация растворенных фенолов лигнина: последствия для судьбы растворенных терригенных органических веществ в морской среде». Журнал геофизических исследований. 108 (C9): 3291. Bibcode:2003JGRC..108.3291H. Дои:10.1029 / 2002JC001421. Получено 2018-11-27.
- ^ «Стойкость органического вещества почвы как свойство экосистемы». ResearchGate. Получено 2018-11-27.
- ^ Диттмар, Торстен (01.01.2015). «Причины долговременной стабильности растворенных органических веществ». Биогеохимия растворенных в море органических веществ. С. 369–388. Дои:10.1016 / B978-0-12-405940-5.00007-8. ISBN 9780124059405.
- ^ Витковски, Райнер; Рутер, Иоахим; Дринда, Хайке; Рафией-Таганаки, Фороозан «Образование ароматических соединений дыма путем термического разложения лигнина» Серия симпозиумов ACS (Прекурсоры вкуса), 1992, том 490, стр 232–243. ISBN 978-0-8412-1346-3.
- ^ ТАППИ. T 222 om-02 - Кислотонерастворимый лигнин древесины и целлюлозы
- ^ Слэйтер, А., Хамес, Б., Руис, Р., Скарлата, К., Слэйтер, Дж., Темплтон, Д., Крокер, Д. Определение структурных углеводов и лигнина в биомассе. Технический отчет NREL / TP-510-42618, Министерство энергетики США, 2008 г. [1]
- ^ Производство и обнаружение лигнина в древесине. Джон М. Харкин, Записка об исследовании лесной службы США FPL-0148, ноябрь 1966 г. (статья )
- ^ Lange, B.M .; Lapierre, C .; Сандерманн-младший (1995). «Стрессовый лигнин ели, индуцированный элиситором (структурное сходство с лигнинами раннего развития)». Физиология растений. 108 (3): 1277–1287. Дои:10.1104 / pp.108.3.1277. ЧВК 157483. PMID 12228544.
- ^ Glasser, Wolfgang G .; Глассер, Хайдемари Р. (1974). «Компьютерное моделирование реакций с лигнином (Simrel). II. Модель лигнина из мягкой древесины». Holzforschung. 28 (1): 5–11, 1974. Дои:10.1515 / hfsg.1974.28.1.5. S2CID 95157574.
- ^ Хеджес, Джон I .; Эртель, Джон Р. (февраль 1982 г.). «Характеристика лигнина методом газовой капиллярной хроматографии продуктов окисления оксида меди». Аналитическая химия. 54 (2): 174–178. Дои:10.1021 / ac00239a007. ISSN 0003-2700.
- ^ Хеджес, Джон I .; Манн, Дейл К. (1979-11-01). «Характеристика тканей растений по продуктам окисления лигнина». Geochimica et Cosmochimica Acta. 43 (11): 1803–1807. Bibcode:1979GeCoA..43.1803H. Дои:10.1016/0016-7037(79)90028-0. ISSN 0016-7037.
- ^ а б c Vane, C.H .; и другие. (2003). «Биоразложение древесины дуба (Quercus alba) во время роста грибов шиитаке (Lentinula edodes): молекулярный подход». Журнал сельскохозяйственной и пищевой химии. 51 (4): 947–956. Дои:10.1021 / jf020932h. PMID 12568554.
- ^ а б c Vane, C.H .; и другие. (2006). «Разложение коры грибком белой гнили Lentinula edodes: потеря полисахаридов, устойчивость к лигнину и выявление суберина». Международный биодестерирование и биоразложение. 57 (1): 14–23. Дои:10.1016 / j.ibiod.2005.10.004.
- ^ Vane, C.H .; и другие. (2001). «Влияние грибковой гнили (Agaricus bisporus) на лигнин соломы пшеницы с использованием пиролиза-ГХ-МС в присутствии гидроксида тетраметиламмония (ТМАГ)». Журнал аналитического и прикладного пиролиза. 60 (1): 69–78. Дои:10.1016 / с0165-2370 (00) 00156-х.
- ^ а б Vane, C.H .; и другие. (2001). «Деградация лигнина в пшеничной соломе во время роста вешенки (Pleurotus ostreatus) с использованием автономного термохимолиза с гидроксидом тетраметиламмония и твердотельным ЯМР 13С». Журнал сельскохозяйственной и пищевой химии. 49 (6): 2709–2716. Дои:10.1021 / jf001409a. PMID 11409955.
- ^ а б Vane, C.H .; и другие. (2005). «Разложение культивированной древесины абрикоса (Prunus armeniaca) аскомицетом Hypocrea sulphurea с использованием твердотельного ЯМР 13С и автономного термохимолиза ТМАГ с ГХ-МС». Международный биодестерирование и биоразложение. 55 (3): 175–185. Дои:10.1016 / j.ibiod.2004.11.004.
