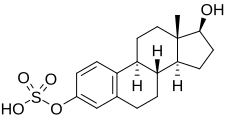
Эстрадиола сульфат - Estradiol sulfate
 | |
| Имена | |
|---|---|
| Название ИЮПАК [(8р,9S,13S,14S,17S) -17-Гидрокси-13-метил-6,7,8,9,11,12,14,15,16,17-декагидроциклопента [а] фенантрен-3-ил] гидросульфат | |
| Другие имена Эстра-1,3,5 (10) -триен-3,17β-диол 3-сульфат | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C18ЧАС24О5S | |
| Молярная масса | 352,445 г / моль |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Эстрадиола сульфат (E2S), или же 17β-эстрадиол 3-сульфат,[1] это естественный, эндогенный стероидный препарат и эфир эстрогена.[2] E2S сам по себе биологически неактивен,[3] но его можно преобразовать стероид сульфатаза (также называемая эстрогенсульфатазой) в эстрадиол, что является мощным эстроген.[2][4][5] Одновременно, эстроген сульфотрансферазы преобразовать эстрадиол в E2S, в результате чего равновесие между двумя стероидами в различных тканях.[2][5] Estrone и E2S - два непосредственных метаболические источники эстрадиола.[6] E2S также может метаболизироваться в эстрон сульфат (E1S), которые, в свою очередь, могут превращаться в эстрон и эстрадиол.[7] Циркулирующие концентрации E2S намного ниже, чем у E1S.[1] Высокие концентрации E2S присутствуют в грудь ткани, и E2S участвует в биологии рак молочной железы служа активным резервуаром эстрадиола.[2][4]
Поскольку натрий поваренная соль, сульфат эстрадиола натрия, E2S присутствует в качестве второстепенного компонента (0,9%) конъюгированные лошадиные эстрогены (ЦВЕ) или Premarin.[8] Он эффективно функционирует как пролекарство к эстрадиолу в этом препарате, аналогично E1S. E2S также формируется как метаболит эстрадиола, а также эстрона и E1S.[9][10] Помимо присутствия в ЦВЕ, E2S недоступен в качестве коммерческого фармацевтический препарат.[11]
E2S показывает примерно в 10 000 раз меньше потенция в активации рецепторы эстрогена относительно эстрадиола in vitro.[12] В 10 раз меньше мощный чем эстрон сульфат устно с точки зрения in vivo утеротрофный эффект у крыс.[13] Сульфаты эстрогена, такие как сульфат эстрадиола или сульфат эстрона, примерно в два раза больше мощный как соответствующие свободные эстрогены с точки зрения эстрогенный эффект при пероральном введении грызунам.[14] Частично это привело к появлению конъюгированные эстрогены (Premarin), которые в основном представляют собой сульфат эстрона, в 1941 году.[14]
Хотя неактивен в рецепторы стероидных гормонов, Было обнаружено, что E2S действует как мощный ингибитор из глутатион S-трансфераза,[15] ан фермент что способствует инактивации эстрадиола за счет его превращения в эстрадиол-глутатион сопрягать.[16] Таким образом, E2S может косвенно служить положительным эффектором передачи сигналов эстрогена.[15]
Уровень эстрадиола у женщин примерно в 1,5–4 раза выше, чем уровень E2S. Это контрастирует с E1S, уровень которого примерно в 10-15 раз выше, чем у эстрона.[17]
E2S при пероральной дозировке 5 мг / день у женщин приводил к ингибированию овуляция в 89% циклов (47 из 53).[18]
| Эстроген | Другие имена | РБА (%)а | REP (%)б | |||
|---|---|---|---|---|---|---|
| ER | ERα | ERβ | ||||
| Эстрадиол | E2 | 100 | 100 | 100 | ||
| Эстрадиол 3-сульфат | E2S; E2-3S | ? | 0.02 | 0.04 | ||
| Эстрадиол 3-глюкуронид | E2-3G | ? | 0.02 | 0.09 | ||
| Эстрадиол 17β-глюкуронид | E2-17G | ? | 0.002 | 0.0002 | ||
| Бензоат эстрадиола | EB; Эстрадиол 3-бензоат | 10 | 1.1 | 0.52 | ||
| Эстрадиол 17β-ацетат | E2-17A | 31–45 | 24 | ? | ||
| Эстрадиола диацетат | EDA; Эстрадиол 3,17β-диацетат | ? | 0.79 | ? | ||
| Эстрадиола пропионат | EP; Эстрадиол 17β-пропионат | 19–26 | 2.6 | ? | ||
| Эстрадиола валерат | EV; Эстрадиол 17β-валерат | 2–11 | 0.04–21 | ? | ||
| Эстрадиола ципионат | ЕС; Эстрадиол 17β-ципионат | ?c | 4.0 | ? | ||
| Эстрадиола пальмитат | Эстрадиол 17β-пальмитат | 0 | ? | ? | ||
| Стеарат эстрадиола | Эстрадиол 17β-стеарат | 0 | ? | ? | ||
| Estrone | E1; 17-кетоэстрадиол | 11 | 5.3–38 | 14 | ||
| Эстрона сульфат | E1S; Эстрон 3-сульфат | 2 | 0.004 | 0.002 | ||
| Глюкуронид эстрона | E1G; Эстрон 3-глюкуронид | ? | <0.001 | 0.0006 | ||
| Этинилэстрадиол | EE; 17α-этинилэстрадиол | 100 | 17–150 | 129 | ||
| Местранол | EE 3-метиловый эфир | 1 | 1.3–8.2 | 0.16 | ||
| Quinestrol | EE 3-циклопентиловый эфир | ? | 0.37 | ? | ||
| Сноски: а = Относительное сродство связывания (RBA) были определены через in vitro вытеснение маркированный эстрадиол из рецепторы эстрогена (ER) обычно грызун матка цитозоль. Эстрогеновые эфиры по-разному гидролизованный в эстрогены в этих системах (более короткая длина сложноэфирной цепи -> большая скорость гидролиза), и ER RBA сложных эфиров сильно уменьшаются, когда гидролиз предотвращается. б = Относительная эстрогенная активность (REP) рассчитывалась из полумаксимальные эффективные концентрации (EC50), которые были определены через in vitro β-галактозидаза (β-гал) и зеленый флуоресцентный белок (GFP) производство анализы в дрожжи выражая человека ERα и человек ERβ. Обе млекопитающее клетки а дрожжи обладают способностью гидролизовать сложные эфиры эстрогена. c = Сходство эстрадиола ципионат для ER аналогичны тем из эстрадиола валерат и эстрадиол бензоат (фигура ). Источники: См. Страницу шаблона. | ||||||
| Эстроген | Структура | Сложный эфир (ы) | Относительный мол. масса | Относительный E2 содержаниеб | logPc | ||||
|---|---|---|---|---|---|---|---|---|---|
| Должность (я) | Moiet (ы) | Тип | Длинаа | ||||||
| Эстрадиол | – | – | – | – | 1.00 | 1.00 | 4.0 | ||
| Эстрадиола ацетат | C3 | Этановая кислота | Жирная кислота с прямой цепью | 2 | 1.15 | 0.87 | 4.2 | ||
| Бензоат эстрадиола | C3 | Бензолкарбоновая кислота | Ароматическая жирная кислота | – (~4–5) | 1.38 | 0.72 | 4.7 | ||
| Дипропионат эстрадиола | C3, C17β | Пропановая кислота (×2) | Жирная кислота с прямой цепью | 3 (×2) | 1.41 | 0.71 | 4.9 | ||
| Эстрадиола валерат | C17β | Пентановая кислота | Жирная кислота с прямой цепью | 5 | 1.31 | 0.76 | 5.6–6.3 | ||
| Бутират бензоата эстрадиола | C3, C17β | Бензойная кислота, Масляная кислота | Смешанная жирная кислота | – (~6, 2) | 1.64 | 0.61 | 6.3 | ||
| Эстрадиола ципионат | C17β | Циклопентилпропановая кислота | Ароматическая жирная кислота | – (~6) | 1.46 | 0.69 | 6.9 | ||
| Эстрадиол энантат | C17β | Гептановая кислота | Жирная кислота с прямой цепью | 7 | 1.41 | 0.71 | 6.7–7.3 | ||
| Эстрадиола диенантат | C3, C17β | Гептановая кислота (×2) | Жирная кислота с прямой цепью | 7 (×2) | 1.82 | 0.55 | 8.1–10.4 | ||
| Эстрадиола ундецилат | C17β | Ундекановая кислота | Жирная кислота с прямой цепью | 11 | 1.62 | 0.62 | 9.2–9.8 | ||
| Стеарат эстрадиола | C17β | Октадекановая кислота | Жирная кислота с прямой цепью | 18 | 1.98 | 0.51 | 12.2–12.4 | ||
| Дистеарат эстрадиола | C3, C17β | Октадекановая кислота (×2) | Жирная кислота с прямой цепью | 18 (×2) | 2.96 | 0.34 | 20.2 | ||
| Эстрадиола сульфат | C3 | Серная кислота | Водорастворимый конъюгат | – | 1.29 | 0.77 | 0.3–3.8 | ||
| Эстрадиол глюкуронид | C17β | Глюкуроновая кислота | Водорастворимый конъюгат | – | 1.65 | 0.61 | 2.1–2.7 | ||
| Эстрамустин фосфатd | C3, C17β | Нормюстин, фосфорная кислота | Водорастворимый конъюгат | – | 1.91 | 0.52 | 2.9–5.0 | ||
| Полиэстрадиолфосфате | C3 – C17β | Фосфорная кислота | Водорастворимый конъюгат | – | 1.23ж | 0.81ж | 2.9грамм | ||
| Сноски: а = Длина сложный эфир в углерод атомы за жирные кислоты с прямой цепью или приблизительная длина сложного эфира в атомах углерода для ароматические жирные кислоты. б = Относительное содержание эстрадиола по весу (т. Е. Относительное эстрогенный воздействие). c = Экспериментальный или прогнозируемый коэффициент разделения октанол / вода (т.е. липофильность /гидрофобность ). Полученное из PubChem, ChemSpider, и DrugBank. d = Также известен как эстрадиол нормустин фосфат. е = Полимер из эстрадиолфосфат (~13 повторять единицы ). ж = Относительная молекулярная масса или содержание эстрадиола на повторяющуюся единицу. грамм = logP повторяющейся единицы (т. е. эстрадиолфосфата). Источники: Смотрите отдельные статьи. | |||||||||
Смотрите также
- Катехол эстроген
- Сульфат ДГЭА
- Эстрадиол глюкуронид
- Эстриола сульфат
- Конъюгат эстрогена
- Липоидальный эстрадиол
- Прегненолона сульфат
- Список эфиров эстрогена § эфиры эстрадиола
Рекомендации
- ^ а б Ф. А. Кинкл; Дж. Р. Паскуалини (22 октября 2013 г.). Гормоны и плод: Том 1: Производство, концентрация и метаболизм во время беременности. Elsevier Science. С. 39–. ISBN 978-1-4832-8538-2.
- ^ а б c d Питер Дж. О'Брайен; Уильям Роберт Брюс (2 декабря 2009 г.). Эндогенные токсины: цели для лечения и профилактики заболеваний, набор из 2 томов. Джон Вили и сыновья. С. 869–. ISBN 978-3-527-32363-0.
- ^ Ван, Ли-Цюань; Джеймс, Маргарет О. (2005). «Сульфотрансфераза 2A1 образует эстрадиол-17-сульфат, а целекоксиб переключает доминирующий продукт с эстрадиол-3-сульфата на эстрадиол-17-сульфат». Журнал стероидной биохимии и молекулярной биологии. 96 (5): 367–374. Дои:10.1016 / j.jsbmb.2005.05.002. ISSN 0960-0760. PMID 16011896.
- ^ а б Хорхе Р. Паскуалини (17 июля 2002 г.). Рак груди: прогноз, лечение и профилактика. CRC Press. С. 195–. ISBN 978-0-203-90924-9.
- ^ а б Рабочая группа МАИР по оценке канцерогенных рисков для человека; Всемирная организация здоровья; Международное агентство по изучению рака (2007 г.). Комбинированные эстроген-прогестагенные контрацептивы и комбинированная эстроген-прогестагенная терапия в период менопаузы. Всемирная организация здоровья. С. 279–. ISBN 978-92-832-1291-1.
- ^ Г. Леклерк; С. Тома; R. Paridaens; Дж. К. Хьюсон (6 декабря 2012 г.). Клинический интерес рецепторов стероидных гормонов при раке груди. Springer Science & Business Media. С. 2105–. ISBN 978-3-642-82188-2.
- ^ А. Т. Грегуар (13 марта 2013 г.). Противозачаточные стероиды: фармакология и безопасность. Springer Science & Business Media. С. 109–. ISBN 978-1-4613-2241-2.
- ^ Марк А. Фриц; Леон Сперофф (28 марта 2012 г.). Клиническая гинекологическая эндокринология и бесплодие. Липпинкотт Уильямс и Уилкинс. С. 751–. ISBN 978-1-4511-4847-3.
- ^ Кристиан Лауритцен; Джон В. В. Стадд (22 июня 2005 г.). Текущее лечение менопаузы. CRC Press. С. 364–. ISBN 978-0-203-48612-2.
- ^ Райан Дж. Хакстейбл (11 ноября 2013 г.). Биохимия серы. Springer Science & Business Media. С. 312–. ISBN 978-1-4757-9438-0.
- ^ Кинг, Роберта; Гош, Анасуя; Ву, Цзиньфан (2006). «Ингибирование человеческого фенола и эстроген сульфотрансферазы некоторыми нестероидными противовоспалительными средствами». Текущий метаболизм лекарств. 7 (7): 745–753. Дои:10.2174/138920006778520615. ISSN 1389-2002. ЧВК 2105742. PMID 17073578.
- ^ Колдхэм Н.Г., Дэйв М., Сивапатхасундарам С., Макдоннелл Д.П., Коннор С., Зауэр М.Дж. (июль 1997 г.). «Оценка скринингового анализа рекомбинантных дрожжевых клеток на эстроген». Environ. Перспектива здоровья. 105 (7): 734–42. Дои:10.1289 / ehp.97105734. ЧВК 1470103. PMID 9294720.
- ^ Бхавнани Б.Р. (ноябрь 1988 г.). «Сага о ненасыщенных конских эстрогенах кольца B». Endocr. Rev. 9 (4): 396–416. Дои:10.1210 / edrv-9-4-396. PMID 3065072.
- ^ а б Herr, F .; Revesz, C .; Мэнсон, А. Дж .; Джуэлл, Дж. Б. (1970). «Биологические свойства сульфатов эстрогенов»: 368–408. Дои:10.1007/978-3-642-95177-0_8. Цитировать журнал требует
| журнал =(Помогите) - ^ а б Рунге-Моррис MA (1997). «Регулирование экспрессии цитозольных сульфотрансфераз грызунов». FASEB J. 11 (2): 109–17. PMID 9039952.
- ^ Сингх Д., Пандей Р.С. (1996). «Глутатион-S-трансфераза в яичнике крысы: ее изменения во время эстрального цикла и повышение активности за счет эстрадиола-17 бета». Индийский J. Exp. Биол. 34 (11): 1158–60. PMID 9055636.
- ^ Коуи, Альфред Т .; Forsyth, Isabel A .; Харт, Ян К. (1980). «Рост и развитие молочной железы». 15: 58–145. Дои:10.1007/978-3-642-81389-4_3. ISSN 0077-1015. Цитировать журнал требует
| журнал =(Помогите) - ^ Гуаль С., Бесерра С., Райс-Рэй Э, Гольдзихер Дж. У. (февраль 1967 г.). «Подавление овуляции эстрогенами». Am J Obstet Gynecol. 97 (4): 443–7. Дои:10.1016/0002-9378(67)90555-8. PMID 4163201.
