Диглицерид - Diglyceride

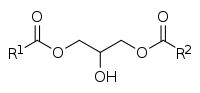
А диглицерид, или же диацилглицерин (DAG), это глицерид состоящий из двух жирная кислота цепи ковалентно связанный к глицерин молекула через сложный эфир связи.[1] Существуют две возможные формы: 1,2-диацилглицерины и 1,3-диацилглицерины. Группы DAG могут действовать как поверхностно-активные вещества и обычно используются как эмульгаторы в обработанных пищевых продуктах. Масло, обогащенное ДАГ (особенно 1,3-ДАГ) широко исследовались как заменитель жира из-за его способности подавлять накопление жировых отложений;[2][3] с общим годовым объемом продаж около 200 миллионов долларов США в Японии с момента его появления в конце 1990-х до 2009 года.[2]
Производство
Диглицериды являются второстепенным компонентом многих масла семян и обычно присутствуют в количестве ~ 1–6%; или в случае хлопковое масло целых 10%.[4] Промышленное производство в первую очередь достигается за счет глицеролиз реакция между триглицериды и глицерин. Сырьем для этого может быть овощ или же животное жиры и масла.[5]
Пищевая добавка
Диглицериды, как правило, в смеси с моноглицериды (E471 ), распространенные пищевые добавки, широко используемые в качестве эмульгаторы. Значения, указанные на этикетках пищевых продуктов для общего жира, насыщенных жиров и транс жиры не включают те, которые присутствуют в моно- и диглицеридах[нужна цитата ]. Их часто включают в хлебобулочные изделия, напитки, мороженое, арахисовое масло, жевательная резинка, сокращение, взбитые начинки, маргарин, кондитерские изделия, конфеты и Pringles картофельные чипсы.
Биологические функции
Активация протеинкиназы C

В биохимической передаче сигналов диацилглицерин действует как второй посланник сигнальный липид, и является продуктом гидролиз фосфолипида фосфатидилинозитол-4,5-бисфосфат (PIP2) посредством фермент фосфолипаза C (ПЛК) (a мембрана -связанный фермент), который в результате той же реакции производит трифосфат инозита (IP3). Хотя трифосфат инозитола проникает в цитозоль, диацилглицерин остается в плазматическая мембрана, благодаря гидрофобный характеристики. IP3 стимулирует высвобождение ионов кальция из гладкой эндоплазматический ретикулум, тогда как ДАГ является физиологическим активатором протеинкиназа C (PKC). Продукция DAG в мембране способствует перемещению PKC из цитозоля в плазматическая мембрана.
Активация Munc13
Было показано, что диацилглицерин оказывает некоторые из своих возбуждающих действий на высвобождение везикул через взаимодействия с семейством пресинаптических прайминговых белков. Munc13. Связывание DAG с доменом C1 Munc13 увеличивает способность слияния синаптических везикул, что приводит к усиленному высвобождению.
Диацилглицерин может имитироваться соединениями, способствующими развитию опухоли. сложные эфиры форбола.[6]
Другой
Помимо активации PKC, диацилглицерин выполняет ряд других функций в клетка:
- источник для простагландины
- предшественник эндоканнабиноид 2-арахидоноилглицерин
- активатор подсемейства временный рецепторный потенциал канонический (TRPC) катионные каналы, TRPC3 / 6/7.
Метаболизм
Синтез диацилглицерина начинается с глицерин-3-фосфат, который в основном получен из дигидроксиацетонфосфат, продукт гликолиз (обычно в цитоплазме клеток печени или жировой ткани). Глицерин-3-фосфат - первый ацилированный с ацил-коэнзимом А (ацил-КоА) с образованием лизофосфатидная кислота, который затем ацилируется другой молекулой ацил-КоА с образованием фосфатидная кислота. Затем фосфатидная кислота де-фосфорилируется с образованием диацилглицерина.
Пищевой жир в основном состоит из триглицериды. Поскольку триглицериды не могут абсорбироваться пищеварительной системой, триглицериды должны сначала ферментативно перевариваться в моноацилглицерин, диацилглицерин или свободные жирные кислоты (см. Пищевые источники жирных кислот, их переваривание, всасывание, перенос в крови и хранение для более подробной информации). Диацилглицерин является предшественником триацилглицерин (триглицерид), который образуется при добавлении третьей жирной кислоты к диацилглицерину при катализе диглицерид ацилтрансфераза.
Поскольку диацилглицерин синтезируется через фосфатидную кислоту, он обычно будет содержать насыщенную жирную кислоту в положении C-1 глицеринового фрагмента и ненасыщенную жирную кислоту в положении C-2.[7]
Диацилглицерин можно фосфорилировать до фосфатидной кислоты с помощью диацилглицеринкиназа.
Резистентность к инсулину
Активация PKC-θ диацилглицерином может вызвать резистентность к инсулину в мышце за счет уменьшения IRS1 -ассоциированный PI3K Мероприятия.[8] Аналогичным образом активация PKCε Диациглицерин может вызвать инсулинорезистентность в печени.[8][9]
Смотрите также
- Пищевые источники жирных кислот, их переваривание, всасывание, перенос в крови и хранение
- Липид
- Моноглицерид
- Триглицерид
Рекомендации
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "глицериды ". Дои:10.1351 / goldbook.G02647
- ^ а б Фуах, Энг-Тонг; Тан, Тек-Ким; Ли, Йи-Инь; Чунг, Томас Шин-Яу; Тан, Чин-Пинг; Лай, Ой-Мин (2015). «Обзор текущего состояния производства диацилглицерина с использованием ферментативного подхода» (PDF). Пищевые и биотехнологические технологии. 8 (6): 1169–1186. Дои:10.1007 / s11947-015-1505-0. ISSN 1935-5130. S2CID 84353775.
- ^ Ло, Сон-Кун; Тан, Чин-Пинг; Лонг, Камария; Юсофф, Мохд. Сурия Аффанди; Лай, Ой-Мин (2008). «Диацилглицериновое масло - свойства, процессы и продукты: обзор» (PDF). Пищевые и биотехнологические технологии. 1 (3): 223–233. Дои:10.1007 / s11947-007-0049-3. ISSN 1935-5130. S2CID 86604260.
- ^ Фликингер, Брент Д .; Мацуо, Нобору (февраль 2003 г.). «Пищевая ценность масла DAG». Липиды. 38 (2): 129–132. Дои:10.1007 / s11745-003-1042-8. PMID 12733744. S2CID 4061326.
- ^ Зоннтаг, Норман О. В. (1982). «Глицеролиз жиров и метиловых эфиров - Статус, обзор и критика». Журнал Американского общества химиков-нефтяников. 59 (10): 795A – 802A. Дои:10.1007 / BF02634442. ISSN 0003-021X. S2CID 84808531.
- ^ Блумберг, Питер М. (1988). «Протеинкиназа C как рецептор для промоутеров опухолей сложного эфира форбола: Шестая лекция о присуждении премии памяти Роадса». Исследования рака. 48 (1): 1–8. PMID 3275491.
- ^ Берг Дж., Тимочко Дж. Л., Страйер Л. (2006). Биохимия (6-е изд.). Сан-Франциско: В. Х. Фриман. ISBN 0-7167-8724-5.[страница нужна ]
- ^ а б Эрион Д.М., Шульман Г.И. (2010). «Опосредованная диацилглицерином инсулинорезистентность». Природа Медицина. 16 (4): 400–402. Дои:10,1038 / нм0410-400. ЧВК 3730126. PMID 20376053.
- ^ Петерсен М.С., Мадираджу А.К., Гассавей Б.М., Марсель М., Насири А.Р., Бутрико Дж., Маркучи М.Дж., Чжан Д., Абулизи А., Чжан Х.М., Филбрик В., Хаббард С.Р., Юрчак М.Дж., Самуэль В.Т., Райнхарт Дж., Шульман Г.И. . «Фосфорилирование Thr1160 рецептора инсулина опосредует индуцированную липидами резистентность к инсулину печени». Журнал клинических исследований. 126 (11): 4361–4371. Дои:10.1172 / JCI86013. ЧВК 5096902. PMID 27760050.

