Оксид трифенилфосфина - Triphenylphosphine oxide
 | |
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Трифенил-λ5-фосфанон | |
| Другие имена Оксид трифенилфосфина | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.011.217 |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| |
| |
| Характеристики | |
| C18ЧАС15OP | |
| Молярная масса | 278,29 г / моль |
| Внешность | белые кристаллы |
| Плотность | 1,212 г / см ^ 3 |
| Температура плавления | От 154 до 158 ° C (от 309 до 316 ° F, от 427 до 431 K) |
| Точка кипения | 360 ° С (680 ° F, 633 К) |
| низкий | |
| Растворимость в других растворителях | полярные органические растворители |
| Структура | |
| четырехгранный | |
| Опасности | |
| Главный опасности | слабый |
| R-фразы (устарело) | 22-36/37/38 |
| S-фразы (устарело) | 26 |
| Родственные соединения | |
Родственные соединения | ПК6ЧАС5)3S; |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Оксид трифенилфосфина (часто сокращенно TPPO) - фосфорорганическое соединение с формулой OP (C6ЧАС5)3, также пишется как Ph3PO или PPh3O (Ph = C6ЧАС5 ). Это бесцветное кристаллическое соединение является обычным, но потенциально полезным отходом в реакциях с участием трифенилфосфин. Это популярный реагент для кристаллизующийся химических соединений.
Структура и свойства
Ph3ПО представляет собой тетраэдрическую молекулу, относящуюся к POCl3.[1] Кислородный центр относительно основной. Жесткость основной цепи и основность кислородного центра делают этот вид популярным агентом для кристаллизации молекул, которые иначе трудно кристаллизовать. Этот прием применим к молекулам, имеющим кислые атомы водорода, например фенолы.[2]
На сегодняшний день существует несколько модификаций Ph3PO были обнаружены: например, моноклинная форма кристаллизуется в пространственной группе п21/c с Z = 4 и a = 15,066 (1) Å, b = 9,037 (2) Å, c = 11,296 (3) Å и β = 98,47 (1) °.[3] Орторомбическая модификация кристаллизуется в пространственной группе Pbca с Z = 4 и 29,089 (3) Å, b = 9,1347 (9), c = 11,261 (1) Å.[4]
Как побочный продукт органического синтеза
Ph3ПО является побочным продуктом многих полезных реакций в органический синтез в том числе Виттиг, Штаудингер, и Мицунобу реакции. Также он образуется при PPh3Cl2 используется для преобразования спирты в алкилхлориды:
- Ph3PCl2 + ROH → Ph3ПО + HCl + RCl
Трифенилфосфин можно регенерировать из оксида обработкой различными дезоксигенирующими агентами, такими как фосген или же трихлорсилан / триэтиламин:[5]
- Ph3ПО + SiHCl3 → PPh3 + 1 / n (OSiCl2)п + HCl
Оксид трифенилфосфина бывает трудно удалить из реакционных смесей с помощью хроматографии. Плохо растворяется в гексане и холодном диэтиловом эфире. Растирание или хроматография сырых продуктов с этими растворителями часто приводит к хорошему разделению оксида трифенилфосфина. Его удалению способствует превращение в комплекс Mg (II), который плохо растворяется в толуоле или дихлорметане и может быть отфильтрован.[6] Альтернативный метод фильтрации, где ZnCl2(TPPO)2 образуется при добавлении ZnCl2 может использоваться с более полярными растворителями, такими как этанол, этилацетат и тетрагидрофуран.[7]
Координационная химия
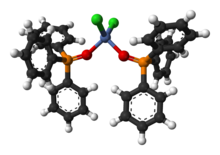
Ph3ПО является лигандом для "жесткий «металлические центры. Типичный комплекс - тетраэдрическая разновидность NiCl.2(OPPh3)2.[8]
Ph3ПО - обычная примесь в PPh3. Окисление PPh3 кислородом, в том числе воздухом, катализируется ионами многих металлов:
- 2 человека в час3 + O2 → 2 Ph3PO
Рекомендации
- ^ Д. Э. К. Корбридж "Фосфор: краткое описание его химии, биохимии и технологии", 5-е издание Elsevier: Amsterdam. ISBN 0-444-89307-5.
- ^ М. К. Эттер и П. В. Баурес (1988). «Трифенилфосфиноксид как вспомогательное средство для кристаллизации». Варенье. Chem. Soc. 110 (2): 639–640. Дои:10.1021 / ja00210a076.
- ^ Спек, Энтони Л. (1987). «Структура второго моноклинного полиморфа оксида трифенилфосфина». Acta Crystallographica. C43 (6): 1233–1235. Дои:10.1107 / S0108270187092345.
- ^ Аль-Фархан, Халид А. (1992). «Кристаллическая структура оксида трифенилфосфина». Журнал кристаллографических и спектроскопических исследований. 22 (6): 687–689. Дои:10.1007 / BF01160986. S2CID 98335827.
- ^ van Kalkeren, H.A .; van Delft, F. L .; Рутес, Ф. П. Дж. Т. (2013). «Фосфорорганический катализ в обход отходов оксида фосфина». ChemSusChem. 6 (9): 1615–24. Дои:10.1002 / cssc.201300368. PMID 24039197.CS1 maint: несколько имен: список авторов (связь)
- ^ Патент WO 1998007724. «Способ получения производных 7-алкоксиалкил-1,2,4-триазоло [1,5-a] пиримидина».
- ^ Batesky, Donald C .; Голдфогель, Мэтью Дж .; Вейкс, Дэниел Дж. (2017). «Удаление оксида трифенилфосфина осаждением хлоридом цинка в полярных растворителях». Журнал органической химии. 82 (19): 9931–9936. Дои:10.1021 / acs.joc.7b00459. ЧВК 5634519. PMID 28956444.
- ^ Д. М. Л. Гудгейм и М. Гудгейм (1965). «Спектры некоторых псевдотетраэдрических комплексов кобальта (II) и никеля (II) в ближней инфракрасной области». Неорг. Chem. 4 (2): 139–143. Дои:10.1021 / ic50024a002.
