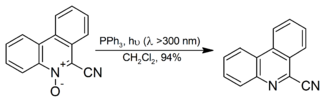Трифенилфосфин - Triphenylphosphine
 | |
 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Трифенилфосфан | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.009.124 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| |
| |
| Характеристики | |
| C18ЧАС15п | |
| Молярная масса | 262.292 г · моль−1 |
| Внешность | Белый твердый |
| Плотность | 1,1 г см−3, твердый |
| Температура плавления | 80 ° С (176 ° F, 353 К) |
| Точка кипения | 377 ° С (711 ° F, 650 К) |
| Нерастворимый | |
| Растворимость | органические растворители |
| Кислотность (пKа) | 7.64[1] (пKа конъюгированной кислоты в ацетонитриле) |
| -166.8·10−6 см3/ моль | |
| 1.59; εр, так далее. | |
| Структура | |
| Пирамидальный | |
| 1,4 - 1,44 Д [2] | |
| Опасности | |
| Паспорт безопасности | Джей Ти Бейкер |
Классификация ЕС (DSD) (устарело) | Нет в списке |
| R-фразы (устарело) | R20 R22 R40 R43 R50 R53 |
| S-фразы (устарело) | S36 S37 S45 S57 S60 |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | 180 ° С (356 ° F, 453 К) |
| Родственные соединения | |
Связанный третичные фосфины | Триметилфосфин Фосфин |
Родственные соединения | Трифениламин Трифениларсин Оксид трифенилфосфина Сульфид трифенилфосфина Трифенилфосфина дихлорид Селенид трифенилфосфина, Pd (PPh3)4 |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Трифенилфосфин (Название ИЮПАК: трифенилфосфан) является обычным фосфорорганическое соединение с формулой P (C6ЧАС5)3 - часто сокращенно пPh3 или Ph3П. Широко используется при синтезе органический и металлоорганический соединения. PPh3 существует в виде относительно устойчивых на воздухе бесцветных кристаллов при комнатной температуре. Растворяется в неполярных органических растворителях, таких как бензол и диэтиловый эфир.
Подготовка и состав
Трифенилфосфин можно получить в лаборатории путем лечения трихлорид фосфора с фенилмагний бромид или же фениллитий. Промышленный синтез включает реакцию между трихлорид фосфора, хлорбензол, и натрий .:[3]
- PCl3 + 3 PhCl + 6 Na → PPh3 + 6 NaCl
Трифенилфосфин кристаллизуется в триклинной[4] и моноклинная модификация[5] В обоих случаях молекула принимает пирамидальную структуру с пропеллероподобным расположением трех фенильных групп.
Основные реакции с халькогенами, галогенами и кислотами
Трифенилфосфин медленно окисляется воздухом с образованием оксид трифенилфосфина, Ph3ПО:
- 2 человека в час3 + O2 → 2 OPPh3
Эта примесь может быть удалена перекристаллизация PPh3 от горячего этиловый спирт или горячий изопропанол.[6] Этот метод основан на том, что OPPh3 более полярен и, следовательно, более растворим в полярных растворителях, чем PPh3.
Рефераты трифенилфосфина сера из полисульфид соединения, эписульфиды и элементарные сера. Простые сероорганические соединения, такие как тиолы и тиоэфиры однако неактивны. Фосфорсодержащий продукт сульфид трифенилфосфина, Ph3PS. Эта реакция может быть использована для анализа «лабильного» S0 содержимое образца, скажем, вулканизированной резины. Селенид трифенилфосфина, Ph3PSe, может быть легко получен путем лечения PPh3 с красным (альфа-моноклинный) Se. Соли селеноцианат, SeCN−, используются как Se0 источник. PPh3 также может образовывать аддукт с Те, хотя этот аддукт в основном существует как (Ph3П)2Te, а не PPh3Te.[7]
Арил азиды реагировать с PPh3 дать фосфанимины, аналоги OPPh3, через Реакция Штаудингера. Показательным является приготовление трифенилфосфин фенилимид:
- PPh3 + PhN3 → ПНПФ3 + N2
Фосфанимин можно гидролизовать до амина. Обычно промежуточный фосфанимин не выделяют.
- PPh3 + RN3 + H2O → OPPh3 + N2 + RNH2
Cl2 добавляет в PPh3 давать дихлорид трифенилфосфина ([PPh3Cl] Cl), который существует как влагочувствительный галогенид фосфония. Этот реагент используется для преобразования спирты к алкилхлориды в органический синтез. Бис (трифенилфосфин) иминия хлорид (PPN+Cl−, формула [(C6ЧАС5)3П)2N] Cl получают из дихлорида трифенилфосфина:[8]
- 2 Ph3PCl2 + NH2ОН · HCl + Ph3P → {[Ph3П]2N} Cl + 4HCl + Ph3PO
PPh3 это слабая база. Он образует выделяемые соли с сильными кислотами, такими как HBr. Продукт содержит катион фосфония [HPPh3]+.
PPh3 является пирамидальным с хиральным расположением трех фенильных колец в виде пропеллера. Жесткость PPh3 способствует легкости кристаллизации его производных.
Органические реакции
PPh3 широко используется в органический синтез. Свойства, которые определяют его использование, - это его нуклеофильность и его восстанавливающий характер.[9] Нуклеофильность PPh3 на это указывает его реакционная способность по отношению к электрофильным алкенам, таким как акцепторы Михаэля и алкилгалогениды. Он также используется в синтезе биарильных соединений, таких как Сузуки реакция.
Кватернизация
PPh3 сочетается с алкилгалогениды давать соли фосфония. Объект кватернизация реакция протекает по обычной схеме, при которой бензиловые и аллильные галогениды являются особенно эффективными реагентами:
- PPh3 + CH3я → [CH3PPh3]+я−
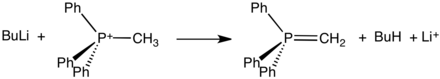
Эти соли, которые часто можно выделить в виде кристаллических твердых веществ, реагируют с сильными основаниями с образованием илиды:
Такие илиды являются ключевыми реагентами в Реакции Виттига, используется для преобразования альдегиды и кетоны в алкены.
Арилгалогениды будут кватернизовать PPh3 давать Тетрафенилфосфоний соли:
- PPh3 + PhBr → [PPh4] Br
Однако реакция требует повышенных температур и металлических катализаторов.
Мицунобу реакция
в Мицунобу реакция, смесь трифенилфосфина и диизопропилазодикарбоксилат («DIAD» или его диэтиловый аналог, DEAD) превращает спирт и карбоновую кислоту в сложный эфир. DIAD восстанавливается, поскольку он служит акцептором водорода, а PPh3 окисляется до OPPh3.
Реакция Аппеля
в Реакция Аппеля, смесь PPh3 и CX4 (X = Cl, Br) используется для превращения спиртов в алкилгалогениды. Оксид трифенилфосфина (OPPh3) является побочным продуктом.
- PPh3 + CBr4 + RCH2OH → OPPh3 + RCH2Br + HCBr3
Эта реакция начинается с нуклеофильной атаки PPh.3 на CBr4, продолжение реакции кватернизации, перечисленной выше.
Деоксигенация
Легкая оксигенация PPh3 используется для деоксигенирования органических пероксидов, что обычно происходит с сохранением конфигурации:
- PPh3 + RO2H → OPPh3 + ROH (R = алкил)
Он также используется для разложения органических озониды к кетонам и альдегидам, хотя диметилсульфид более популярен в качестве побочного продукта, диметилсульфоксид легче отделяется от реакционной смеси, чем оксид трифенилфосфина. Ароматный N-оксиды восстанавливаются до соответствующего амина с высоким выходом при комнатной температуре при облучении:[10]
Сульфирование
Сульфирование PPh3 дает трис (3-сульфофенил) фосфин, P (C6ЧАС4-3-SO3−)3 (ТППЦ ), обычно выделяемый в виде тринатриевой соли. В отличие от PPh3, TPPTS растворим в воде, как и его металлические производные. Родиевые комплексы ТППЦ используются в некоторых промышленных гидроформилирование реакции.[11]

Восстановление до дифенилфосфида
Литий в THF а также Na или K реагируют с PPh3 давать Ph2ВЕЧЕРА (M = Li, Na, K). Эти соли являются универсальными предшественниками третичных фосфинов.[12][13] Например, 1,2-дибромэтан и Ph2PM реагирует, чтобы дать Ph2PCH2CH2PPh2. Слабые кислоты, такие хлорид аммония, преобразовать Ph2PM (M = Li, Na, K) в дифенилфосфин:[13]
- (C6ЧАС5)2PM + H2O → (C6ЧАС5)2PH + MOH
Комплексы переходных металлов
Трифенилфосфин хорошо связывается с большинством переходные металлы, особенно в средних и поздних переходных металлах 7–10 групп.[14] По стерической массе PPh3 есть Толмен угол конуса 145 °,[15] который занимает промежуточное положение между P (C6ЧАС11)3 (170 °) и P (CH3)3 (115 °). В раннем приложении в гомогенный катализ, NiBr2(PPh3)2 использовался Уолтер Реппе для синтеза акрилатных эфиров из алкины, монооксид углерода, и спирты.[16] Использование PPh3 был популяризирован его использованием в гидроформилирование катализатор RhH (PPh3)3(CO).
PPh с полимерным анкерным креплением3 производные
Полимерные аналоги PPh3 известны модификации полистирола PPh2 группы в парапозиции. Такие полимеры можно использовать во многих областях применения PPh.3 с тем преимуществом, что полимер, будучи нерастворимым, может быть отделен от продуктов простой фильтрацией реакционных суспензий. Такие полимеры получают обработкой 4-литиофенилзамещенного полистирола хлордифенилфосфин (PPh2Cl).
Смотрите также
Рекомендации
- ^ Хаав, Кристьян; Сааме, Яан; Кютт, Агнес; Лейто, Иво (2012). «Основность фосфанов и дифосфанов в ацетонитриле». Европейский журнал органической химии. 2012 (11): 2167–2172. Дои:10.1002 / ejoc.201200009. ISSN 1434–193X.
- ^ Warchol, M .; Dicarlo, E.N .; Марьянов, К. А .; Мислоу, К. (1975). «Доказательства вклада неподеленной пары в молекулярный дипольный момент триарилфосфинов». Буквы Тетраэдра. 16 (11): 917–920. Дои:10.1016 / S0040-4039 (00) 72019-3.
- ^ Корбридж, Д. Е. С. (1995). Фосфор: краткое описание его химии, биохимии и технологии (5-е изд.). Амстердам: Эльзевир. ISBN 0-444-89307-5.
- ^ Kooijman, H .; Spek, A. L .; ван Боммель, К. Дж. С .; Verboom, W .; Рейнхудт, Д. Н. (1998). «Триклинная модификация трифенилфосфина» (PDF). Acta Crystallographica. C54 (11): 1695–1698. Дои:10.1107 / S0108270198009305.
- ^ Dunne, B.J .; Орпен, А. Г. (1991). «Трифенилфосфин: новое определение» (PDF). Acta Crystallographica. C47 (2): 345–347. Дои:10.1107 / S010827019000508X.
- ^ Armarego, W. L. F .; Perrin, D. D .; Перрин, Д. Р. (1980). Очистка лабораторных химикатов (2-е изд.). Нью-Йорк: Пергамон. п. 455. ISBN 9780080229614.
- ^ Jones, C.H.W .; Шарма, Р. Д. (1987). "125Те ЯМР и мессбауэровская спектроскопия комплексов теллур-фосфин и теллуроцианатов ». Металлоорганические соединения. 6 (7): 1419–1423. Дои:10.1021 / om00150a009.
- ^ Ruff, J.K .; Шленц, W.J. (1974). «Соли μ-нитридо-бис (трифенилфосфор) (1+ (« PPN ») с карбонильными анионами металлов»). Неорг. Synth. 15: 84–90. Дои:10.1002 / 9780470132463.ch19.
- ^ Cobb, J.E .; Cribbs, C.M .; Henke, B.R .; Uehling, D. E .; Hernan, A. G .; Martin, C .; Райнер, К. М. (2004). «Трифенилфосфин». В Л. Пакетте (ред.). Энциклопедия реагентов для органического синтеза. Нью-Йорк: J. Wiley & Sons. Дои:10.1002 / 047084289X.rt366.pub2. ISBN 0471936235.
- ^ Burke, S.D .; Данхайзер, Р. Л. (1999). «Трифенилфосфин». Справочник реагентов для органического синтеза, окислителей и восстановителей. Вайли. п. 495. ISBN 978-0-471-97926-5.
- ^ Herrmann, W. A .; Кольпайнтнер, К. В. (1998). «Синтезы водорастворимых фосфинов и комплексов их переходных металлов». Неорг. Синтезатор. 32: 8–25. Дои:10.1002 / 9780470132630.ch2.
- ^ Джордж У. Лютер III, Гордон Байерле (1977). «Дифенилфосфид лития и дифенил (триметилсилил) фосфин». Неорганические синтезы. Неорганические синтезы. 17. С. 186–188. Дои:10.1002 / 9780470132487.ch51. ISBN 9780470132487.CS1 maint: использует параметр авторов (связь)
- ^ а б В. Д. Бьянко С. Доронцо (1976). «Дифенилфосфин». Неорганические синтезы. Неорганические синтезы. 16. С. 161–188. Дои:10.1002 / 9780470132470.ch43. ISBN 9780470132470.CS1 maint: использует параметр авторов (связь)
- ^ Elschenbroich, C .; Зальцер, А. (1992). Металлоорганические соединения: краткое введение (2-е изд.). Вайнхайм: Wiley-VCH. ISBN 3-527-28165-7.
- ^ Иммирзи, А .; Муско, А. (1977). «Метод измерения размеров фосфорных лигандов в координационных комплексах». Неорганика Chimica Acta. 25: L41 – L42. Дои:10.1016 / S0020-1693 (00) 95635-4.
- ^ *Reppe, W .; Schweckendiek, W. J. (1948). "Cyclisierende Polymerisation von Acetylen. III Benzol, Benzolderivate und hydroaromatische Verbindungen". Юстус Либигс Аннален дер Хеми. 560 (1): 104–116. Дои:10.1002 / jlac.19485600104.