Алкин - Alkyne

В органическая химия, алкин является ненасыщенный углеводород содержащий по крайней мере один углерод - углерод тройная связь.[1] Простейшие ациклические алкины только с одной тройной связью и без других функциональные группы сформировать гомологическая серия с общей химической формулой CпЧАС2п−2. Алкины традиционно известны как ацетилены, хотя название ацетилен также относится конкретно к C2ЧАС2, официально известный как этин с помощью Номенклатура ИЮПАК. Как и другие углеводороды, алкины обычно гидрофобны.
Структура и склеивание
В ацетилене H – C≡C валентные углы равны 180 °. Благодаря этому валентному углу алкины подобны стержням. Соответственно, циклические алкины редки. Бензин крайне нестабилен. Связующее расстояние C≡C 121 пикометры намного короче, чем расстояние C = C в алкены (134 пм) или связь C – C в алканах (153 пм).
 Иллюстративные алкины: а, ацетилен, б, два изображения пропина, c, 1-бутин, d, 2-бутин, е, встречающийся в природе 1-фенилгепта-1,3,5-триин, и ж, деформированный циклогептин. Выделены тройные связи синий.
Иллюстративные алкины: а, ацетилен, б, два изображения пропина, c, 1-бутин, d, 2-бутин, е, встречающийся в природе 1-фенилгепта-1,3,5-триин, и ж, деформированный циклогептин. Выделены тройные связи синий.
В тройная связь очень силен с прочность сцепления 839 кДж / моль. Сигма-связь дает 369 кДж / моль, первая пи-связь дает 268 кДж / моль, а вторая пи-связь дает силу связи 202 кДж / моль. Связь обычно обсуждается в контексте теория молекулярных орбиталей, который распознает тройную связь как результат перекрытия s- и p-орбиталей. На языке теория валентной связи, атомы углерода в алкиновой связи являются sp гибридизированный: у каждого из них есть два негибридных p орбитали и два sp гибридные орбитали. Перекрытие sp-орбитали от каждого атома образует одну sp – sp сигма-облигация. Каждая p-орбиталь одного атома перекрывается одна на другом атоме, образуя два пи-облигации, всего три облигации. Оставшаяся sp-орбиталь на каждом атоме может образовывать сигма-связь с другим атомом, например с атомами водорода в исходном ацетилене. Две sp-орбитали проецируются с противоположных сторон от атома углерода.
Терминальные и внутренние алкины
Внутренние алкины имеют углеродные заместители на каждом ацетиленовом углероде. Симметричные примеры включают дифенилацетилен и 3-гексин.
Терминальные алкины имеют формулу RC2H. Примером является метилацетилен (пропин по номенклатуре IUPAC). Терминальные алкины, такие как ацетилен сами по себе являются умеренно кислыми, с pKа значения около 25. Они намного более кислые, чем алкены и алканы, которые имеют pKа значения около 40 и 50 соответственно. Кислый водород на концевых алкинах может быть заменен множеством групп, приводящих к гало-, силил- и алкоксоалкинам. В карбанионы образующиеся при депротонировании терминальных алкинов, называются ацетилиды.[2]
Обозначение алкинов
В систематическая химическая номенклатура, алкины названы с использованием греческой префиксной системы без дополнительных букв. Примеры включают этин или октин. В родительских цепях с четырьмя или более атомами углерода необходимо указать, где находится тройная связь. За октин, можно написать 3-октин или окт-3-ин, когда связь начинается с третьего атома углерода. Минимально возможное число присваивается тройная связь. Когда нет высших функциональных групп, родительская цепь должна включать тройную связь, даже если это не самая длинная углеродная цепь в молекуле. Этин обычно называют ацетиленом.
В химии суффикс -yne используется для обозначения наличия тройной связи. В органическая химия, суффикс часто следует за Номенклатура ИЮПАК. Тем не мение, неорганические соединения с участием ненасыщенность в форме тройных связей могут быть обозначены заместительной номенклатурой теми же методами, которые используются с алкинами (т.е. название соответствующего насыщенного соединения модифицируется путем замены "-ан "оканчивающийся на" -yne "). "-диыне" используется, когда есть две тройные связи и так далее. Положение ненасыщенности указывается числовым местный житель непосредственно перед суффиксом «-yne» или «locants» в случае множественных тройных связей. Локанты выбираются так, чтобы их количество было как можно меньше. "-yne" также используется как инфикс для обозначения групп заместителей, которые трижды связаны с исходным соединением.
Иногда число между дефисы вставляется перед ним, чтобы указать, между какими атомами находится тройная связь. Этот суффикс возник как свернутая форма окончания слова "ацетилен ". Последний" -e "исчезает, если за ним следует другой суффикс, начинающийся с гласной.[3]
Синтез
Растрескивание
В коммерческом отношении преобладающим алкином является сам ацетилен, который используется в качестве топлива и предшественника других соединений, например, акрилаты. Сотни миллионов килограммов ежегодно производятся путем частичного окисления натуральный газ:[4]
- 2 канала4 + 3/2 О2 → HC≡CH + 3 H2О
Пропин, также используемый в промышленности, также получают термическое растрескивание углеводородов.
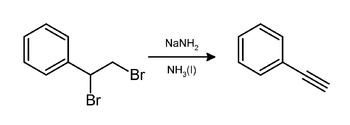
Специальные алкины получают двойным дегидрогалогенирование. Реакция обеспечивает средства для образования алкинов из алкенов, которые сначала галогенируют, а затем дегидрогалогенируют. Например, фенилацетилен может быть получен из стирола путем бромирования с последующей обработкой полученного дибромида стирола амид натрия в аммиак:[5]
Через Перегруппировка Фрича – Буттенберга – Вихелла., алкины получают из винилбромиды. Алкины можно получить из альдегиды с использованием Реакция Кори – Фукса и из альдегидов или кетоны посредством Соответствие Сейферта – Гилберта.
Реакции, в том числе приложения
С реактивным функциональная группа, алкины участвуют во многих органические реакции. Такое использование было впервые предложено Ральф Рафаэль, которые в 1955 году написали первую книгу, описывая их универсальность как промежуточные звенья в синтез.[6]
Гидрирование
Быть больше ненасыщенный чем алкены, алкины обычно подвергаются реакциям, которые показывают, что они «дважды ненасыщены». Алкины способны добавлять два эквивалента H2, тогда как алкен добавляет только один эквивалент.[7] В зависимости от катализаторов и условий к алкинам добавляют один или два эквивалента водорода. Частичное гидрирование, останавливаясь после добавления только одного эквивалента, чтобы получить алкен, обычно более желательны, поскольку алканы менее полезны:

Наиболее масштабным применением этой технологии является преобразование ацетилена в этилен на нефтеперерабатывающих заводах (паровой крекинг алканов дает несколько процентов ацетилена, который селективно гидрируется в присутствии палладий /серебро катализатор). Для более сложных алкинов Катализатор Линдлара широко рекомендуется, чтобы избежать образования алкана, например, при превращении фенилацетилен к стирол.[8] По аналогии, галогенирование алкинов дает алкендигалогениды или алкилтетрагалогениды:
- RC≡CR ′ + H2 → цис-RCH = CR′H
- RCH = CR′H + H2 → RCH2CR′H2
Добавление одного эквивалента H2 к внутренним алкинам дает цис-алкены.
Алкины, как правило, способны добавлять два эквивалента галогены и галогениды водорода.
- RC≡CR ′ + 2 Br2 → RCBr2CR′Br2
Добавление неполярных связей E – H через C≡C является общим для силанов, боранов и родственных гидридов. В гидроборирование алкинов дает виниловые бораны, которые окисляются до соответствующих альдегид или кетон. в тиолиновая реакция субстрат - тиол.
Добавление галогенидов водорода вызывает интерес. В присутствии хлорид ртути как катализатор, ацетилен и хлористый водород реагировать, чтобы дать винилхлорид. Хотя на Западе от этого метода отказались, он остается основным методом производства в Китае.[9]
Гидратация
В реакция гидратации ацетилена дает ацетальдегид. Реакция протекает с образованием винилового спирта, который подвергается таутомеризуется с образованием альдегида. Эта реакция когда-то была крупным промышленным процессом, но ее заменили Wacker процесс. Эта реакция протекает в природе, катализатор - ацетиленгидратаза.
Увлажнение фенилацетилен дает ацетофенон,[10] и (Ph3P) AuCH3-катализируемая гидратация 1,8-нонадина до 2,8-нонандиона:[11]
- PhC≡CH + H2O → PhCOCH3
- HC≡C (CH2)5C≡CH + 2H2O → CH3CO (CH2)5COCH3
Циклоприсоединения и окисление
Алкины претерпевают разнообразные циклоприсоединение реакции. В Реакция Дильса – Альдера с 1,3-диены дайте 1,4-циклогексадиены. Эта общая реакция получила широкое развитие. Электрофильные алкины особенно эффективны диенофилы. «Циклоаддукт», полученный в результате присоединения алкинов к 2-пирон устраняет углекислый газ дать ароматный сложный. Другие специализированные циклоприсоединения включают многокомпонентные реакции, такие как тримеризация алкинов давать ароматный соединения и [2 + 2 + 1] -циклоприсоединение алкина, алкен и монооксид углерода в Реакция Паусона-Ханда. Неуглеродные реагенты также подвергаются циклизации, например Азид алкин циклоприсоединение Huisgen давать триазолы. Процессы циклоприсоединения с участием алкинов часто катализируются металлами, например Enyne Metathesis и метатезис алкинов, что позволяет скремблировать центры карбина (RC):
- RC≡CR + R′C≡CR ′ ⇌ 2 RC≡CR ′
Окислительное расщепление алкинов протекает через циклоприсоединение к оксидам металлов. Самое известное, перманганат калия превращает алкины в пару карбоновые кислоты.
Реакции, характерные для концевых алкинов
Терминальные алкины легко превращаются во многие производные, например за счет реакций сочетания и конденсации. Путем конденсации формальдегида и ацетилена получают бутиндиол:[4][12]
- 2 канала2O + HC≡CH → HOCH2CCCH2ОЙ
в Соногашира реакция, концевые алкины связаны с арил- или винилгалогенидами
 Реакция Соногашира
Реакция Соногашира
Эта реакционная способность основана на том факте, что концевые алкины являются слабыми кислотами, типичные для которых пKа значения около 25 помещают их между аммиак (35) и этиловый спирт (16):
Реакции алкинов с катионами некоторых металлов, например Ag+ и Cu+ также дает ацетилиды. Таким образом, несколько капель диамминесеребра (I) гидроксид (Ag (NH3)2OH) реагирует с концевыми алкинами, о чем свидетельствует образование белого осадка ацетилида серебра. Эта реакционная способность является основой алкиновой реакции сочетания, в том числе Муфта Кадио – Ходкевича, Муфта Glaser, а Муфта Эглинтон:[13]
в Реакция Фаворского И в алкинилирование как правило, концевые алкины добавляют к карбонил соединения, чтобы дать гидроксиалкин.
Металлические комплексы
Алкины образуют комплексы с переходными металлами. Такие комплексы встречаются также в катализируемых металлами реакциях алкинов, таких как тримеризация алкинов. Конечные алкины, включая сам ацетилен, реагируют с водой с образованием альдегидов. Для преобразования обычно требуются металлические катализаторы, чтобы получить результат добавления антимарковникова.[14]
Алкины в природе и медицине
По словам Фердинанда Больмана, первое встречающееся в природе ацетиленовое соединение, эфир дегидроматрикарии, было выделено из Полынь видов в 1826 году. За прошедшие почти два столетия было открыто и зарегистрировано более тысячи встречающихся в природе ацетиленов. Полиины, подмножество этого класса натуральных продуктов, были выделены из широкого спектра видов растений, культур высших грибов, бактерий, морских губок и кораллов.[15] Некоторые кислоты, такие как дегтярная кислота содержат алкиновую группу. Diynes и triynes, виды со связью RC≡C – C≡CR ′ и RC≡C – C≡C – C≡CR ′ соответственно, встречаются у некоторых растений (Ихтиотере, Хризантема, Cicuta, Oenanthe и другие члены Сложноцветные и Apiaceae семьи). Некоторые примеры цикутоксин, энантотоксин, и фалькаринол . Эти соединения обладают высокой биологической активностью, например в качестве нематоциды.[16] 1-Фенилгепта-1,3,5-трин является иллюстрацией встречающегося в природе трина.
Алкины содержатся в некоторых фармацевтических препаратах, включая противозачаточные. норэтинодрел. Тройная связь углерод-углерод также присутствует в имеющихся на рынке лекарствах, таких как антиретровирусные препараты. Эфавиренц и противогрибковые Тербинафин. Молекулы, называемые ен-диинами, имеют кольцо, содержащее алкен («ен») между двумя алкиновыми группами («дийн»). Эти соединения, например калихеамицин, являются одними из наиболее агрессивных известных противоопухолевых препаратов, настолько, что субъединицу ен-дийн иногда называют «боеголовкой». Эне-дийны претерпевают перегруппировку через Циклизация Бергмана, генерируя высокореактивные радикальные промежуточные соединения, которые атакуют ДНК внутри опухоли.[17]
Смотрите также
Рекомендации
- ^ Алкин. Британская энциклопедия
- ^ Блох, Дэниел Р. (2012). Демистификация органической химии (2-е изд.). Макгроу-Хилл. п. 57. ISBN 978-0-07-176797-2.
- ^ Комиссия по номенклатуре органической химии (1971) [1958 (A: углеводороды и B: основные гетероциклические системы), 1965 (C: характеристические группы)]. Номенклатура органической химии (3-е изд.). Лондон: Баттервортс. ISBN 0-408-70144-7.
- ^ а б Грефье, Хайнц; Кёрниг, Вольфганг; Вайц, Ханс-Мартин; Рейс, Вольфганг; Стеффан, Гвидо; Диль, Герберт; Бош, Хорст; Шнайдер, Курт; Кечка (2000). «Бутандиолы, бутендиол и бутиндиол». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a04_455.
- ^ Кеннет Н. Кэмпбелл, Барбара К. Кэмпбелл (1950). «Фенилацетилен». Органический синтез. 30: 72. Дои:10.15227 / orgsyn.030.0072.
- ^ Рафаэль, Ральф Александр (1955). Ацетиленовые соединения в органическом синтезе. Лондон: Научные публикации Баттерворта. OCLC 3134811.
- ^ Россер и Уильямс (1977). Современная органическая химия для A-level. Великобритания: Коллинз. п. 82. ISBN 0003277402.
- ^ Х. Линдлар; Р. Дюбуи (1973). «Палладиевый катализатор частичного восстановления ацетиленов». Органический синтез.; Коллективный объем, 5, п. 880.
- ^ Дреер, Эберхард-Людвиг; Торкельсон, Теодор Р .; Бойтель, Клаус К. (2011). «Хлорэтаны и хлорэтилены». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.o06_o01.
- ^ Fukuda, Y .; Утимото, К. (1991). «Эффективное превращение неактивированных алкинов в кетоны или ацетали с катализатором золота (III)». J. Org. Chem. 56 (11): 3729. Дои:10.1021 / jo00011a058..
- ^ Mizushima, E .; Cui, D.-M .; Nath, D.C.D .; Hayashi, T .; Танака, М. (2005). "Au (I) -катализируемая гидратация алкинов: 2,8-нонандион". Органический синтез. 83: 55.
- ^ Петер Песслер; Вернер Хефнер; Клаус Бакль; Хельмут Мейнасс; Андреас Мейсвинкель; Ханс-Юрген Вернике; Гюнтер Эберсберг; Рихард Мюллер; Юрген Бесслер (2008). "Ацетилен". Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a01_097.pub3.
- ^ К. Штёкель и Ф. Сондхаймер (1974). «[18] Аннулен». Органический синтез. 54: 1. Дои:10.15227 / orgsyn.054.0001.
- ^ Хинтерманн, Лукас; Лабонн, Орели (2007). «Каталитическая гидратация алкинов и ее применение в синтезе». Синтез. 2007 (8): 1121–1150. Дои:10.1055 / с-2007-966002. S2CID 95666091.
- ^ Аннабель Л. К. Ши Шун; Рик Р. Тыквински (2006). «Синтез естественных полиинов». Энгью. Chem. Int. Эд. 45 (7): 1034–1057. Дои:10.1002 / anie.200502071. PMID 16447152.
- ^ Лам, Йорген (1988). Химия и биология природных ацетиленов и родственных соединений (NOARC): материалы конференции по химии и биологии естественных ацетиленов и родственных соединений (NOARC). Амстердам: Эльзевир. ISBN 0-444-87115-2.
- ^ С. Уокер; Р. Ландовиц; W.D. Ding; Г.А. Эллестад; Д. Канне (1992). «Расщепление калихеамицина гамма 1 и калихеамицина Т». Proc Natl Acad Sci USA. 89 (10): 4608–12. Bibcode:1992PNAS ... 89.4608W. Дои:10.1073 / pnas.89.10.4608. ЧВК 49132. PMID 1584797.



![{displaystyle {ce {2R -! {Equiv}! - H -> [{ce {Cu (OAc) 2}}] [{ce {pyridine}}] R -! {Equiv}! -! {Equiv}! - Р}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8fe5690544a4da60b118164e70291e6eae02f82e)