Фосфорорганическое соединение - Organophosphorus compound
Фосфорорганические соединения находятся органические соединения содержащий фосфор.[1] Они используются в основном в борьба с вредителями как альтернатива хлорированные углеводороды которые сохраняются в окружающей среде. Некоторые фосфорорганические соединения очень эффективны. инсектициды, хотя некоторые из них чрезвычайно токсичны для человека, в том числе зарин и VX нервно-паралитические агенты.[2]
Химия фосфорорганических соединений - это соответствующая наука о свойствах и реакционной способности фосфорорганических соединений. Фосфор, как азот, в группа 15 периодической таблицы Менделеева, и, таким образом, соединения фосфора и соединения азота обладают многими схожими свойствами.[3][4][5] Определение фосфорорганических соединений варьируется, что может привести к путанице. В промышленной химии и химии окружающей среды фосфорорганическое соединение должно содержать только органическое соединение. заместитель, но не обязательно иметь прямую связь фосфор-углерод (Р-С).[нужна цитата ] Таким образом, большая часть пестицидов (например, малатион ), часто входят в этот класс соединений.
Фосфор может принимать множество состояния окисления и обычно классифицируют фосфорорганические соединения на основе того, что они являются производными фосфора (V) по сравнению с фосфором (III), которые являются преобладающими классами соединений. В описательной, но только периодически используемой номенклатуре соединения фосфора идентифицируются по их координационный номер σ и их валентность λ. В этой системе фосфин представляет собой σ3λ3 сложный.
Фосфорорганические (V) соединения, основные категории
Фосфатные эфиры и амиды
Фосфорные эфиры имеют общую структуру P (= O) (OR)3 особенность P (V). Такие виды имеют технологическое значение, как огнестойкий агенты и пластификаторы. Не обладая связью P-C, эти соединения в техническом смысле являются не фосфорорганическими соединениями, а сложными эфирами фосфорной кислоты. Многие производные встречаются в природе, например, фосфатидилхолин. Фосфатный эфир синтезируются алкоголиз оксихлорида фосфора. Известно множество смешанных амидоалкоксопроизводных, одним из важных с медицинской точки зрения примером является противораковое лекарственное средство. циклофосфамид. Также производные, содержащие тиофосфорильную группу (P = S), включают пестицид малатион. Крупнейшие органофосфаты - это дитиофосфаты цинка, в качестве присадок к моторным маслам. Несколько миллионов килограммов этого координационный комплекс производятся ежегодно реакцией пентасульфида фосфора со спиртами.[6]
 Иллюстративные органофосфаты и родственные соединения: фосфатидилхолин, трифенилфосфат, циклофосфамид, паратион, и дитиофосфат цинка.
Иллюстративные органофосфаты и родственные соединения: фосфатидилхолин, трифенилфосфат, циклофосфамид, паратион, и дитиофосфат цинка.
В окружающей среде эти соединения распадаются через гидролиз в конечном итоге позволить фосфат и органический спирт или амин, из которого они получены.
Фосфоновая и фосфиновая кислоты и их сложные эфиры
Фосфонаты представляют собой сложные эфиры фосфоновой кислоты и имеют общую формулу RP (= O) (OR ')2. Фосфонаты находят множество технических применений, среди которых широко известен глифосат, более известный как Roundup. По формуле (HO)2P (O) CH2NHCH2CO2H, эта производная от глицин является одним из наиболее широко используемых гербицидов. Бисфосфонаты класс препаратов для лечения остеопороз. Агент нервно-паралитического действия зарин, содержащий как связи C – P, так и F – P, представляет собой фосфонат.
Особенность фосфинатов два Связи P – C с общей формулой R2P (= O) (ИЛИ '). Коммерчески значимый член - гербицид. Глюфосинат. Подобно упомянутому выше глифосату, он имеет структуру CH3P (O) (OH) CH2CH2CH (NH2) CO2ЧАС.
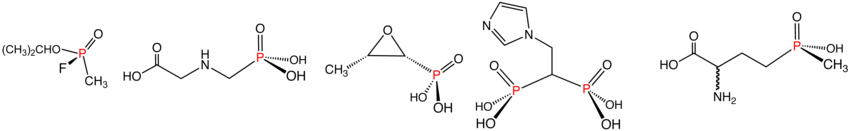 Иллюстративные примеры фосфонатов и фосфинатов в указанном порядке: зарин (фосфонат), Глифосат (фосфонат), фосфомицин (фосфонат), золедроновая кислота (фосфонат) и Глюфосинат (фосфинат). В водном растворе фосфоновые кислоты ионизируются с образованием соответствующих органофосфонатов.
Иллюстративные примеры фосфонатов и фосфинатов в указанном порядке: зарин (фосфонат), Глифосат (фосфонат), фосфомицин (фосфонат), золедроновая кислота (фосфонат) и Глюфосинат (фосфинат). В водном растворе фосфоновые кислоты ионизируются с образованием соответствующих органофосфонатов.
В Реакция Михаэлиса – Арбузова является основным методом синтеза этих соединений. Например, диметилметилфосфонат (см. Рисунок выше) возникает в результате перегруппировки триметилфосфит, который катализируется метилиодид. в Реакция Хорнера – Уодсворта – Эммонса и Соответствие Сейферта – Гилберта, фосфонаты используются в реакциях с карбонил соединения. В Реакция Кабачника – Филдса. представляет собой метод получения аминофосфонатов. Эти соединения содержат очень инертную связь между фосфором и углеродом. Следовательно, они гидролизуются с образованием производных фосфоновой и фосфиновой кислоты, но не фосфата.
Оксиды, имиды и халькогениды фосфина
Оксиды фосфина (обозначение σ4λ5) имеют общую структуру R3P = O с формальной степенью окисления V. Формируются оксиды фосфина. водородные связи и поэтому некоторые из них растворимы в воде. Связь P = O очень полярна с дипольный момент 4,51 D для оксид трифенилфосфина.
Соединения, относящиеся к оксидам фосфина, включают: фосфинимиды (Р3PNR ') и связанные халькогениды (Р3PE, где E = S, Se, Te ). Эти соединения являются одними из самых термостойких фосфорорганических соединений.
Соли фосфония и фосфораны
Соединения с формулой [PR4+]ИКС− составляют соли фосфония. Эти соединения представляют собой тетраэдрические соединения фосфора (V). С коммерческой точки зрения наиболее важным членом является тетракис (гидроксиметил) фосфоний хлорид, [P (CH2ОЙ)4] Cl, который используется в качестве антипирена в текстиль. Ежегодно производится около 2 млн кг хлорида и соответствующего сульфата.[6] Они образуются в результате реакции фосфина с формальдегид в присутствии минеральной кислоты:
- PH3 + HX + 4 CH2O → [P (CH2ОЙ)4+]ИКС−
Различные соли фосфония могут быть получены путем алкилирование и арилирование органофосфинов:
- PR3 + R'X → [PR3Р'+]ИКС−
Метилирование трифенилфосфина - это первый шаг в приготовлении реагента Виттига.
 Иллюстративные соединения фосфора (V): ион фосфония P (CH2ОЙ)4+, две резонансные структуры для Реагент Виттига Ph3PCH2и пентафенилфосфоран, редкое пентаорганофосфорное соединение.
Иллюстративные соединения фосфора (V): ион фосфония P (CH2ОЙ)4+, две резонансные структуры для Реагент Виттига Ph3PCH2и пентафенилфосфоран, редкое пентаорганофосфорное соединение.
Родитель фосфоран (σ5λ5) равно PH5, что неизвестно.[нужна цитата ] Родственные соединения, содержащие как галогенидные, так и органические заместители у фосфора, довольно распространены. С пятью органическими заместителями встречаются редко, хотя P (C6ЧАС5)5 известно, получено из ПК6ЧАС5)4+ по реакции с фениллитий.
Фосфор илиды ненасыщенные фосфораны, известные как Реагенты Виттига, например CH2ПК6ЧАС5)3. Эти соединения содержат тетраэдрический фосфор (V) и считаются родственниками оксидов фосфора. Их также получают из солей фосфония, но путем депротонирования, а не алкилирования.
Фосфорорганические (III) соединения, основные категории
Фосфиты, фосфониты и фосфиниты
Фосфиты, иногда называемые фосфитовые эфиры, имеют общую структуру P (OR)3 со степенью окисления +3. Такие виды возникают в результате алкоголиза треххлористого фосфора:
- PCl3 + 3 ROH → P (ИЛИ)3 + 3 HCl
Реакция является общей, поэтому известно огромное количество таких видов. Фосфиты используются в Реакция Перкова и Реакция Михаэлиса – Арбузова. Они также служат лигандами в металлоорганической химии.
Промежуточным звеном между фосфитами и фосфинами являются фосфониты (P (ИЛИ)2R ') и фосфинит (P (OR) R '2). Такие частицы возникают в результате реакций алкоголиза соответствующих фосфиновых и фосфонистых хлоридов ((PClR '2) и PCl2R 'соответственно).
Фосфины
Исходным соединением фосфинов является PH.3, называется фосфин в США и Британском Содружестве, но фосфан в других местах.[7] Замена одного или нескольких водородных центров на органические заместители (алкил, арил) дает PH3-хрИкс, органофосфин, обычно называемый фосфинами.
 Различные восстановленные фосфорорганические соединения: комплекс фосфорорганического лиганда, хиральный дифосфин используется в гомогенный катализ, первичный фосфин PhPH2, и соединение фосфора (I) (PPh)5.
Различные восстановленные фосфорорганические соединения: комплекс фосфорорганического лиганда, хиральный дифосфин используется в гомогенный катализ, первичный фосфин PhPH2, и соединение фосфора (I) (PPh)5.
Сравнение фосфинов и аминов
Атом фосфора в фосфинах имеет формальную степень окисления −3 (σ3λ3) и являются фосфорными аналогами амины. Как и амины, фосфины обладают треугольная пирамидальная геометрия молекул хотя часто с меньшими углами C-E-C (E = N, P), по крайней мере, при отсутствии стерических эффектов. C-P-C угол связи составляет 98,6 ° для триметилфосфина и увеличивается до 109,7 ° при замене метильных групп на терт-бутил группы. При использовании в качестве лигандов стерическая масса третичных фосфинов оценивается по их угол конуса. Барьер для пирамидальная инверсия также намного выше, чем азотная инверсия происходить, и, следовательно, фосфины с тремя различными заместители можно разложить на термически стабильные оптические изомеры. Фосфины часто менее основные, чем соответствующие амины, например, сам ион фосфония имеет пKа -14 по сравнению с 9,21 для иона аммония; триметилфосфоний имеет пKа 8,65 по сравнению с 9,76 для триметиламмоний. Однако трифенилфосфин (pKа 2.73) более простой, чем трифениламин (пKа −5), главным образом потому, что неподеленная пара азота в NPh3 частично делокализован на три фенильных кольца. В то время как неподеленная пара по азоту делокализованный в пиррол неподеленная пара на атоме фосфора в фосфорном эквиваленте пиррол (фосфол ) не является. Реакционная способность фосфинов соответствует реакционной способности аминов в отношении нуклеофильность в формировании соли фосфония с общей структурой PR4+Икс−. Это свойство используется в Реакция Аппеля для преобразования спирты к алкилгалогениды. Фосфины легко окисленный к соответствующему оксиды фосфина, тогда как оксиды аминов образуются с меньшей легкостью. Отчасти по этой причине фосфины очень редко встречаются в природе.
Синтетические маршруты
С коммерческой точки зрения наиболее важным фосфином является трифенилфосфин, ежегодно производится несколько миллионов килограммов. Его готовят по реакции хлорбензол, PCl3, и натрий.[6] Фосфины более специализированной природы обычно получают другими способами.[8] Галогениды фосфора подвергаются Нуклеофильное смещение металлоорганическими реагентами, такими как Реактивы Гриньяра. И наоборот, некоторые синтезы влекут за собой нуклеофильное замещение эквивалентов фосфид-анионов («R2п−") арил- и алкилгалогенидами. Первичный (RPH2) и вторичных фосфинов (RRPH и R2PH) добавить в алкены при наличии сильного основания (например, КОН в ДМСО ). Правила Марковникова подать заявление. Подобные реакции происходят с участием алкины.[9] Основание не требуется для электронодефицитных алкенов (например, производных акрилонитрил ) и алкины.
Под свободнорадикальные состояния связи P-H первичных и вторичных фосфинов присоединяются через алкены. Такие реакции протекают с антимарковниковской региохимией. AIBN или органический перекиси используются как инициаторы. Оксиды и сульфиды третичного фосфина могут быть уменьшенный с хлорсиланы и другие реагенты.
Реакции
Органофосфины - это нуклеофилы и лиганды. Два основных применения - это реагенты в Реакция Виттига и в качестве поддержки фосфиновые лиганды в гомогенный катализ.
Их нуклеофильность подтверждается их реакциями с алкилгалогениды давать соли фосфония. Фосфины нуклеофильные катализаторы в органический синтез, например то Реакция Раухута – Курье и Реакция Бейлиса-Хиллмана.
Фосфины восстановители, как показано на Редукция Штаудингера для превращения органических азидов в амины и в Мицунобу реакция для превращения спиртов в сложные эфиры. В этих процессах фосфин окисляется до фосфора (V). Было также обнаружено, что фосфины восстанавливают активированные карбонильные группы, например, восстановление α-кетоэфира до α-гидроксиэфира в схема 2.[10] В предлагаемом механизм реакции, первый протон заимствован из метильной группы в триметилфосфине (трифенилфосфин не реагирует).
 Восстановление активированных карбонильных групп алкилфосфинами
Восстановление активированных карбонильных групп алкилфосфинами
Первичные и вторичные фосфины
В дополнение к другим реакциям, связанным с фосфинами, те, которые содержат группы P-H, проявляют дополнительную реакционную способность, связанную со связями P-H. Они легко депротонируются с помощью сильных оснований с образованием фосфид-анионов. Первичные и вторичные фосфины обычно получают восстановлением соответствующих галогенидов или сложных эфиров фосфора, но фосфонаты также могут быть восстановлены до первичных фосфинов, например:[11]

Бинафтил-первичный фосфин, проиллюстрированный выше, демонстрирует замечательную стабильность на воздухе, которая объясняется высокой степенью спряжение в бинафтильном скелете [12]. Это же объяснение было использовано для объяснения устойчивости к воздуху первого высоко флуоресцентного первичного фосфина, BodPH2. [13].
Фосфаалкены и фосфаалкины
Соединения с кратными связями углерод-фосфор (III) называются фосфаалкены (Р2C = PR) и фосфаалкины (RC≡P). Они похожи по структуре, но не по реакционной способности, на имины (Р2C = NR) и нитрилы (RC≡N) соответственно. В комплексе фосфор, один атом углерода в бензоле заменен на фосфор. Виды этого типа относительно редки, но по этой причине представляют интерес для исследователей. Общий метод синтеза фосфаалкенов заключается в следующем: 1,2-устранение подходящих предшественников, инициированных термически или основанием, таким как DBU, DABCO, или же триэтиламин:
Термолиз меня2PH генерирует CH2= PMe, нестабильная разновидность в конденсированной фазе.
Фосфорорганические соединения (0), (I) и (II)
Соединения, в которых фосфор находится в формальной степени окисления менее III, встречаются редко, но известны примеры для каждого класса. Фосфорорганический (0) видов спорные иллюстрируются карбеновыми аддуктами, [Р (NHC)]2, где NHC - N-гетероциклический карбен.[14] С формулами (RP)п и (R2П)2соответственно, соединения фосфора (I) и (II) образуются путем восстановления соответствующих хлоридов фосфорорганических соединений (III):
Дифосфены, с формулой R2п2, формально содержат двойные связи фосфор-фосфор. Эти виды фосфора (I) редки, но стабильны при условии, что органические заместители достаточно велики, чтобы предотвратить цепочка. Много смешанная валентность соединения известны, например клетка P7(CH3)3.
Смотрите также
- Протеомика, основанная на деятельности раздел биохимии, который часто полагается на фосфорорганические зонды для исследования активности ферментов
- Органофосфаты
- Инцидент отравления в школьной еде в Бихаре
- Органотиофосфаты
Рекомендации
- ^ Мерриам-Вебстер, Полный словарь Мерриам-Вебстера, Мерриам-Вебстер.
- ^ Льюис, Роберт Алан (1998). Словарь токсикологии Льюиса. CRC Льюис. п. 763. ISBN 978-1-56670-223-2. Получено 18 июля 2013.
- ^ Диллон, К. Б .; Mathey, F .; Никсон, Дж. Ф. (1997) Фосфор. Копия; Джон Уайли и сыновья, ISBN 0-471-97360-2
- ^ Куин, Л. Д. (2000) Руководство по фосфорорганической химии; Джон Уайли и сыновья, ISBN 0-471-31824-8
- ^ Раке, К. (1992). «Разложение фосфорорганических инсектицидов в матрицах окружающей среды», стр. 47–73 в: Chambers, J.E., Levi, P.E. (ред.), Органофосфаты: химия, судьба и эффекты. Academic Press, Сан-Диего, ISBN 0121673456.
- ^ а б c Свара, Юрген; Weferling, Norbert & Hofmann, Thomas (2006). «Соединения фосфора органические». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a19_545.pub2. ISBN 978-3527306732.
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) "фосфаны ". Дои:10.1351 / goldbook.P04548
- ^ Даунинг, Дж. Х .; Смит, М. (2003). «Фосфорные лиганды». Комплексная координационная химия II. 2003: 253–296. Дои:10.1016 / B0-08-043748-6 / 01049-5. ISBN 9780080437484.
- ^ Арбузова, С. Н .; Гусарова, Н.К .; Трофимов, Б.А. (2006). «Нуклеофильные и свободнорадикальные присоединения фосфинов и халькогенидов фосфина к алкенам и алкинам». Аркивок. v (5): 12–36. Дои:10.3998 / ark.5550190.0007.503.
- ^ Zhang, W .; Ши, М. (2006). «Восстановление активированных карбонильных групп алкилфосфинами: образование α-гидроксиэфиров и кетонов». Chem. Commun. 2006 (11): 1218–1220. Дои:10.1039 / b516467b.
- ^ Hiney, Rachel M .; Higham, Lee J .; Мюллер-Бунц, Хельге; Гилхиани, Деклан Г. (2006). «Укрощение функциональной группы: создание устойчивых к воздуху хиральных первичных фосфанов». Angewandte Chemie International Edition. 45 (43): 7248–7251. Дои:10.1002 / anie.200602143. PMID 17022105.
- ^ https://pubs.acs.org/doi/full/10.1021/om200070a
- ^ https://www.onlinelibrary.wiley.com/doi/10.1002/anie.201108416
- ^ Ван, Юйчжун; Се, Яомин; Вэй, Пингронг; Кинг, Р. Брюс; Шефер, III; Schleyer, Paul v. R .; Робинсон, Грегори Х. (2008). «Карбен-стабилизированный дифосфор». Журнал Американского химического общества. 130 (45): 14970–1. Дои:10.1021 / ja807828t. PMID 18937460.
внешняя ссылка
- фосфорорганическая химия @ users.ox.ac.uk; @ www.chem.wisc.edu
- ЯМР-прогнозатор химических сдвигов фосфорорганических соединений от Алан Брисдон исследовательская группа Связь







