Органоиридиевое соединение - Organoiridium compound
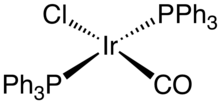





Органоиридий химия это химия из металлоорганические соединения содержащий иридий -углерод химическая связь.[2] Иридийорганические соединения имеют отношение ко многим важным процессам, включая олефиновые. гидрирование и промышленный синтез уксусной кислоты. Они также представляют большой академический интерес из-за разнообразия реакций и их отношения к синтезу тонких химикатов.[3]
Классификация на основе основных степеней окисления
Органические иридиевые соединения имеют много общих характеристик с родием, но в меньшей степени с кобальтом. Иридиум может существовать в состояния окисления от -III до + V, но иридий (I) и иридий (III) встречаются чаще. соединения иридия (I) (d8 конфигурации) обычно имеют плоскую квадратную или тригонально-бипирамидальную геометрию, тогда как соединения иридия (III) (d6 конфигурация) обычно имеют октаэдрическую геометрию.[3]
Иридий (0)
Комплексы иридия (0) представляют собой бинарные карбонилы, главным членом которых является тетраиридий додекакарбонил, Ir4(CO)12. В отличие от родственного Rh4(CO)12, все лиганды CO терминальные в Ir4(CO)12, аналогично разнице между Fe3(CO)12 и Ру3(CO)12.[4]
Иридий (I)
Хорошо известный пример: Васьковский комплекс, бис (трифенилфосфин) карбонилхлорид иридия. Хотя комплексы иридия (I) часто полезны гомогенные катализаторы, Васьки комплекса нет. Скорее, это знаковое по разнообразию своих реакций. Другие распространенные комплексы включают: Ir2Cl2(циклооктадиен)2, хлорбис (циклооктен) димер иридия, Аналог Катализатор Уилкинсона, IrCl (PPh3)3), проходит ортометалляцию:
- IrCl (PPh3)3 → HIrCl (PPh3)2(PPh2C6ЧАС4)
Эта разница между RhCl (PPh3)3 и IrCl (PPh3)3 отражает в целом большую склонность иридия к окислительная добавка. Аналогичную тенденцию демонстрирует RhCl (CO) (PPh3)2 и IrCl (CO) (PPh3)2, только последний окислительно добавляет O2 и H2.[5] Олефиновые комплексы хлорбис (циклооктен) димер иридия и циклооктадиен димер хлорида иридия часто используются в качестве источников «IrCl», используя лабильность алкеновых лигандов или их чувствительность к удалению путем гидрирования. Катализатор Крэбтри ([Ir (P (C6ЧАС11)3) (пиридин) (циклооктадиен)] PF6) является универсальным гомогенным катализатором гидрирование алкенов.[6]
(η5-Cp ) Ir (CO)2 окислительно добавляет связи C-H при фотолитической диссоциации одного лиганда CO.
Иридий (II)
Как и в случае с родием (II), иридий (II) встречается редко. Одним из примеров является иридоцен IrCp.2.[7] Как и с родоцен, димерисы иридоцена при комнатной температуре.[8]
Иридий (III)
Иридий обычно коммерчески поставляется в степени окисления Ir (III) и Ir (IV). Важные исходные реагенты гидратируются трихлорид иридия и гексахлориридат аммония. Эти соли восстанавливаются при обработке СО, водородом и алкенами. Показательным является карбонилирование трихлорида: IrCl3(ЧАС2O)Икс + 3 CO → [Ir (CO)2Cl2]− + CO2 + 2 часа+ + Cl− + (х-1) H2О
Многие органические иридиевые (III) соединения образуются из димер дихлорида пентаметилциклопентадиенил иридия. Многие из производных содержат кинетически инертные циклометаллированные лиганды.[9] Родственные полусэндвич-комплексы занимали центральное место в развитии C-H активация.[10][11]
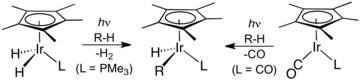 Химия органоиридия играет центральную роль в развитии C-H активация, два примера которых показаны здесь.
Химия органоиридия играет центральную роль в развитии C-H активация, два примера которых показаны здесь.
Иридий (V)
Степени окисления выше III более характерны для иридия, чем для родия. Обычно они содержат лиганды сильного поля. Одним из часто упоминаемых примеров является оксотримезитилиридий (V).[12]
Использует
Доминирующее применение органоиридиевых комплексов - это катализатор в Cativa процесс за карбонилирование из метанол производить уксусная кислота.[13]

Оптические приборы и фоторедокс
Иридий комплексы такие как циклометаллированные, полученные из 2-фенилпиридины используются как фосфоресцентные органические светодиоды.[14] Родственные комплексы фотоокислительные катализаторы.
Возможные приложения
Комплексы иридия очень активны для гидрирования как напрямую, так и через перенос гидрирования. Асимметричные варианты этих реакций широко изучаются.
Многие полусэндвич-комплексы были исследованы как возможные противораковые препараты. Родственные комплексы являются электрокатализаторами превращения диоксида углерода в формиат.[9][15] В академических лабораториях широко изучаются комплексы иридия, поскольку его комплексы способствуют C-H активация, но такие реакции не используются ни в одном коммерческом процессе.
Смотрите также
- Категория: Соединения иридия
Рекомендации
- ^ С. М. Бишофф, Р. А. Периана (2010). "Ацетилацетонато-иридиевые (III) комплексы, связанные с кислородом и углеродом". Неорганические синтезы. 35: 173. Дои:10.1002/9780470651568.CS1 maint: использует параметр авторов (связь)
- ^ Синтез металлоорганических соединений: практическое руководство. Санширо Комия Эд. С. Комия, М. Хурано 1997 г.
- ^ а б Крэбтри, Роберт Х. (2005). Металлоорганическая химия переходных металлов. (4-е изд.). США: Wiley-Interscience. ISBN 0-471-66256-9.
- ^ Greenwood, N. N .; Эрншоу, А. (1997). Химия элементов (2-е изд.). Оксфорд: Баттерворт-Хайнеманн. С. 1113–1143, 1294. ISBN 0-7506-3365-4.
- ^ Васька, Лаури; ДиЛузио, Дж. (1961). «Карбонильные и гидридокарбонильные комплексы иридия по реакции со спиртами. Гидридокомплексы по реакции с кислотой». Журнал Американского химического общества. 83 (12): 2784–2785. Дои:10.1021 / ja01473a054.
- ^ Крэбтри, Роберт Х. (1979). «Соединения иридия в катализе». Соотв. Chem. Res. 12 (9): 331–337. Дои:10.1021 / ar50141a005.
- ^ Keller, H.J .; Ваверсик, Х. (1967). "Spektroskopische Untersuchungen an Komplexverbindungen. VI. EPR-spektren von (C5ЧАС5)2Rh и (C5ЧАС5)2Ir ". J. Organomet. Chem. (на немецком). 8 (1): 185–188. Дои:10.1016 / S0022-328X (00) 84718-X.
- ^ Фишер, Э.; Ваверсик, Х. (1966). "Über Aromatenkomplexe von Metallen. LXXXVIII. Über Monomeres und Dimeres Dicyclopentadienylrhodium und Dicyclopentadienyliridium und Über Ein Neues Verfahren Zur Darstellung Ungeladener Metall-Aromaten-Komplexe". J. Organomet. Chem. (на немецком). 5 (6): 559–567. Дои:10.1016 / S0022-328X (00) 85160-8.
- ^ а б Лю, Чжэ; Сэдлер, Питер Дж. (2014). «Органоиридиевые комплексы: противораковые агенты и катализаторы». Отчеты о химических исследованиях. 47: 1174–1185. Дои:10.1021 / ar400266c. ЧВК 3994614. PMID 24555658.CS1 maint: использует параметр авторов (связь)
- ^ Эндрю Х. Янович, Роберт Г. Бергман (1982). «Углеродно-водородная активация в насыщенных углеводородах: прямое наблюдение M + R − H → M (R) (H)». Варенье. Chem. Soc. 104: 352–354. Дои:10.1021 / ja00365a091.CS1 maint: использует параметр авторов (связь)
- ^ Грэм, Уильям А.Г. (1982). «Окислительное присоединение углерод-водородных связей неопентана и циклогексана к фотохимически генерированному комплексу иридия (I)». Журнал Американского химического общества. 104: 3723–3725. Дои:10.1021 / ja00377a032.
- ^ Hay-Мазервелл, Р. С .; Wilkinson, G .; Hussain-Bates, B .; Херстхаус, М. Б. (1993). «Синтез и рентгеновская кристаллическая структура оксотримезитил-иридия (V)». Многогранник. 12 (16): 2009–2012. Дои:10.1016 / S0277-5387 (00) 81474-6.
- ^ Чунг, Осия; Танке, Робин С .; Торренс, Дж. Пол (2000). "Уксусная кислота". Энциклопедия промышленной химии Ульмана. Вайли. Дои:10.1002 / 14356007.a01_045.
- ^ Джесанг Ли, Сяо-Фань Чен, Тилини Батагода, Калеб Кобурн, Петр И. Джурович, Марк Э. Томпсон, Стивен Р. Форрест (2016). «Темно-синие фосфоресцентные органические светодиоды с очень высокой яркостью и эффективностью». Материалы Природы. 15 (1–2): 92–98. Дои:10.1038 / nmat4446. PMID 26480228.CS1 maint: использует параметр авторов (связь)
- ^ Маенака, Юта; Суэнобу, Томоёси; Фукузуми, Шуничи (2012). «Каталитическое взаимное превращение водорода в муравьиную кислоту при температуре и давлении окружающей среды». Энергетика и экология. 5: 7360–7367. Дои:10.1039 / c2ee03315a.CS1 maint: использует параметр авторов (связь)

