Острый диссеминированный энцефаломиелит - Acute disseminated encephalomyelitis
| Острый диссеминированный энцефаломиелит | |
|---|---|
| Другие имена | Острый демиелинизирующий энцефаломиелит |
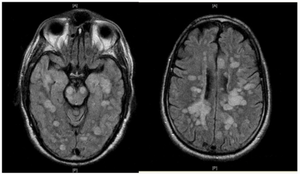 | |
| Вспышка ADEM с множеством поражений. Пациент выжил, но остался в стойкое вегетативное состояние | |
| Специальность | Неврология |
Острый диссеминированный энцефаломиелит (ADEM), или же острый демиелинизирующий энцефаломиелит, это редкий аутоиммунный заболевание, отмеченное внезапным распространенным приступом воспаления в мозг и спинной мозг. ADEM не только вызывает воспаление головного и спинного мозга, но и поражает нервы центральной нервной системы и повреждает их миелиновую изоляцию, что, в результате, разрушает белое вещество. Это часто вызывается популярный инфекционное заболевание или (очень редко) специфические нестандартные прививки.[1][2][3][4][5][6]
Симптомы ADEM напоминают симптомы рассеянный склероз (MS), поэтому само заболевание попадает в классификацию пограничный рассеянный склероз болезни. Однако у ADEM есть несколько особенностей, которые отличают его от MS.[7] В отличие от рассеянного склероза, ADEM обычно возникает у детей и характеризуется быстрым повышением температуры тела, хотя подростки и взрослые также могут заболеть этим заболеванием. ADEM состоит из одного обострения, тогда как MS отмечен несколькими обострениями (или рецидивами) в течение длительного периода времени. О рецидивах после ADEM сообщается до четверти пациентов, но большинство этих «многофазных» проявлений после ADEM, вероятно, представляют собой рассеянный склероз.[8] ADEM также отличается потерей сознания, комой и смертью, что очень редко при РС, за исключением тяжелых случаев.
От него страдают около 8 на 1 000 000 человек в год.[9] Хотя это происходит в любом возрасте, чаще всего регистрируются случаи у детей и подростки, средний возраст от 5 до 8 лет.[10][11][12][13] Заболевание почти одинаково поражает мужчин и женщин.[14] ADEM показывает сезонные колебания с более высокой заболеваемостью в зимние и весенние месяцы, что может совпадать с более высокими вирусными инфекциями в эти месяцы.[13] Уровень смертности может достигать 5%; однако полное выздоровление наблюдается в 50–75% случаев с увеличением выживаемости до 70–90% с цифрами, включающими также незначительную остаточную нетрудоспособность.[15] Среднее время восстановления после обострения ADEM составляет от одного до шести месяцев.
ADEM производит несколько воспалительный поражения в мозгу и спинной мозг, особенно в белое вещество. Обычно они обнаруживаются в подкорковом и центральном белом веществе и корковом серо-белом соединении обоих. полушария головного мозга, мозжечок, мозговой ствол и спинной мозг,[16] но перивентрикулярное белое вещество и серое вещество кора, талами и базальный ганглий также могут быть задействованы.
Когда у человека более одного демиелинизирующего эпизода ADEM, болезнь называется рецидивирующий диссеминированный энцефаломиелит[17] или же многофазный диссеминированный энцефаломиелит[18] (MDEM). Также молниеносный конечно у взрослых не было описано.[19]
Признаки и симптомы
ADEM имеет резкое начало и монофазное течение. Симптомы обычно появляются через 1–3 недели после заражения. Основные симптомы включают: высокая температура, Головная боль, тошнота и рвота, путаница, нарушение зрения, сонливость, припадки и кома. Хотя изначально симптомы обычно легкие, они быстро ухудшаются в течение нескольких часов или дней, при этом среднее время до достижения максимальной степени тяжести составляет около четырех с половиной дней.[20] Дополнительные симптомы включают гемипарез, парапарез и паралич черепных нервов.[21]
Причины
С момента открытия анти-МОГ специфичность в отношении диагностики рассеянного склероза[22] считается, что ADEM является одной из возможных клинических причин энцефаломиелит, связанный с анти-MOG[23]
О том, как антитела против MOG появляются в сыворотке крови пациентов, существует несколько теорий:
- Предыдущая антигенная проблема может быть идентифицирована примерно у двух третей людей.[14] Некоторые вирусные инфекции, которые, как считается, вызывают ADEM, включают: вирус гриппа, денге,[24] энтеровирус, корь,[25] свинка, краснуха, ветряная оспа, Вирус Эпштейна-Барра, цитомегаловирус, Вирус простого герпеса, гепатит А, вирус Коксаки и COVID-19.[26] Бактериальные инфекции включают: Mycoplasma pneumoniae, Borrelia burgdorferi, Лептоспира, и бета-гемолитические стрептококки.[27]
- Воздействие вакцин: единственная подтвержденная вакцина, связанная с ADEM, - это форма Semple. бешенство вакцина, но гепатит Б, коклюш, дифтерия, корь, эпидемический паротит, краснуха, пневмококк, ветряная оспа, грипп, японский энцефалит, и полиомиелит все вакцины были замешаны. В большинстве исследований, которые связывают вакцинацию с началом ADEM, используются небольшие выборки или тематические исследования.[нужна цитата ] Крупномасштабные эпидемиологические исследования (например, вакцины MMR или противооспенной вакцины) не показывают повышенного риска ADEM после вакцинации.[9][28][29][30][20][31][32][33][34][35][36] Верхняя граница риска ADEM от вакцинация против кори, если он существует, можно оценить как 10 на миллион,[37] что намного ниже, чем риск развития ADEM от фактической инфекции кори, который составляет примерно 1 на 1000 случаев. Риск заражения краснухой составляет 1 на 5000 случаев.[31][38] Некоторые ранние вакцины, которые, как позже выяснилось, были заражены животными-хозяевами ЦНС ткани, частота случаев ADEM составляла 1 из 600.[28]
- В редких случаях кажется, что ADEM следует из трансплантация органов.[20]
Диагностика
Термин ADEM в разное время использовался непоследовательно[39] В настоящее время общепринятым международным стандартом для определение клинического случая это тот, который опубликован Международная педиатрическая исследовательская группа РС, редакция 2007 г.[40]
Учитывая, что определение является клиническим, в настоящее время неизвестно, все ли случаи с ADEM положительны на анти-МОГ аутоантитела, но в любом случае это, по-видимому, сильно связано с диагностикой ADEM.[23]
Дифференциальная диагностика
Рассеянный склероз
Хотя ADEM и MS включают аутоиммунную демиелинизацию, они различаются по многим клиническим, генетическим, визуальным и гистопатологическим аспектам.[14][41] Некоторые авторы считают РС и его пограничные формы составить спектр, различающийся только хроничностью, тяжестью и клиническим течением,[42][43] в то время как другие считают их отдельными заболеваниями.[6]
Обычно ADEM появляется у детей после введения антигена и остается монофазным. Тем не менее, ADEM действительно встречается у взрослых,[8][12] а также может быть клинически многофазным.[44]
Проблемы дифференциальной диагностики увеличиваются из-за отсутствия согласия в отношении определения рассеянного склероза.[45] Если бы РС определяли просто разделением во времени и пространстве демиелинизирующих поражений как Макдональдс сделал,[46] этого было бы недостаточно, так как некоторые случаи ADEM удовлетворяют этим условиям. Поэтому некоторые авторы предлагают установить разделительную линию в форме очагов поражения вокруг вен, которые, следовательно, являются «перивенозной или сливной демиелинизацией».[45][47]
Патология ADEM очень похожа на патологию MS с некоторыми отличиями. Патологический признак ADEM - перивенулярное воспаление с ограниченными «рукавами демиелинизации».[48][14] Тем не менее, могут появиться бляшки, подобные РС (сливная демиелинизация).[49]
Бляшки в белом веществе при РС резко очерчены, в то время как глиальный шрам в ADEM гладко. Аксоны лучше сохраняются при поражениях ADEM. Воспаление при ADEM широко распространено и плохо определено, и, наконец, поражения строго перивенальны, тогда как при MS они располагаются вокруг вен, но не так резко.[50]
Тем не менее, совпадение перивенозной и сливной демиелинизации у некоторых людей предполагает патогенетическое совпадение между острым диссеминированным энцефаломиелитом и рассеянным склерозом и ошибочную классификацию даже при биопсии.[47] или даже посмертно[51] ADEM у взрослых может прогрессировать до MS[52]
Многофазный диссеминированный энцефаломиелит
Если у человека имеется более одного демиелинизирующего эпизода ADEM, заболевание называется рецидивирующим диссеминированным энцефаломиелитом или многофазным диссеминированным энцефаломиелитом.[18] (MDEM).
Было обнаружено, что анти-МОГ аутоантитела относятся к этому виду ADEM[53]
Описан другой вариант ADEM у взрослых, также связанный с аутоантителами против MOG, был назван молниеносным диссеминированным энцефаломиелитом, и, как сообщается, клинически он является ADEM, но при вскрытии показывает MS-подобные поражения.[19] Он был классифицирован внутри воспалительные демиелинизирующие заболевания, ассоциированные с анти-MOG.[54]
Острый геморрагический лейкоэнцефалит
Острый геморрагический лейкоэнцефалит (AHL или AHLE), острый геморрагический энцефаломиелит (AHEM), острый некротический геморрагический лейкоэнцефалит (ANHLE), синдром Вестона-Херста или болезнь Херста являются острой и часто фатальной формой ADEM. АГЛ встречается относительно редко (по состоянию на 2006 г. в медицинской литературе было зарегистрировано менее 100 случаев.[Обновить]),[55] это наблюдается примерно в 2% случаев ADEM,[20] и характеризуется некротический васкулит из венулы и кровоизлияние, и отек.[56] Смерть обычна в первую неделю[57] и общая смертность составляет около 70%,[55] но все больше данных указывает на благоприятные результаты после агрессивного лечения кортикостероидами, иммуноглобулинами, циклофосфамидом и плазмообменом.[27] Около 70% выживших демонстрируют остаточный неврологический дефицит.[56] но некоторые выжившие показали удивительно небольшой дефицит, учитывая величину пораженного белого вещества.[57]
Это заболевание иногда связывают с язвенный колит и болезнь Крона, малярия,[58] сепсис связано с отложением иммунных комплексов, метанол отравление и другие сопутствующие заболевания. Также сообщалось об анекдотической связи с РС.[59]
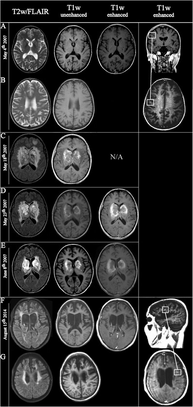
Лабораторные исследования, подтверждающие диагноз АГЛ, включают: периферический лейкоцитоз, плеоцитоз спинномозговой жидкости (ЦСЖ), связанный с нормальным уровнем глюкозы и повышенным содержанием белка. На магнитно-резонансной томографии (МРТ) поражения AHL обычно демонстрируют обширную Т2-взвешенную и ослабленную инверсией восстановления (FLAIR) гиперинтенсивность белого вещества с областями кровоизлияний, значительным отеком и масс-эффектом.[60]
Уход
Контролируемых клинических испытаний лечения ADEM не проводилось, но стандартным является агрессивное лечение, направленное на быстрое уменьшение воспаления ЦНС. Широко признанный лечение первой линии высокие дозы внутривенного кортикостероиды,[61] Такие как метилпреднизолон или же дексаметазон с последующими 3–6 неделями постепенного снижения пероральных доз преднизолон. Пациенты, получавшие метилпреднизолон, показали лучшие результаты, чем пациенты, получавшие дексаметазон.[20] Пероральные приемы длительностью менее трех недель показывают более высокую вероятность рецидива.[11][18] и, как правило, показывают худшие результаты.[нужна цитата ] Сообщалось, что другие противовоспалительные и иммунодепрессивные методы лечения показывают положительный эффект, например: плазмаферез, высокие дозы внутривенного иммуноглобулин (IVIg),[61][62] митоксантрон и циклофосфамид. Это считается альтернативным лечением, используемым, когда кортикостероиды не могут быть использованы или не дают эффекта.[нужна цитата ]
Есть некоторые свидетельства того, что пациенты могут реагировать на комбинацию метилпреднизолона и иммуноглобулинов, если они не реагируют на любой из них по отдельности.[63]В исследовании с участием 16 детей с ADEM, 10 полностью выздоровели после приема высоких доз метилпреднизолона, в одном тяжелом случае, не ответившем на стероиды, полностью выздоровел после внутривенного введения Ig; пять самых тяжелых случаев - с ADAM и тяжелым периферическая невропатия - лечились комбинированными высокими дозами метилпреднизолона и иммуноглобулина, двое остались парализованными, у одного были двигательные и когнитивные нарушения, а двое выздоровели.[61] Недавний обзор лечения ADEM внутривенным иммуноглобулином (из которых предыдущее исследование сформировал большую часть случаев) показал, что 70% детей показали полное выздоровление после лечения внутривенным иммуноглобулином или внутривенным иммуноглобулином плюс кортикостероиды.[64] Исследование лечения ВВИГ у взрослых с ADEM показало, что ВВИГ более эффективны при лечении сенсорных и моторных нарушений, в то время как стероиды кажутся более эффективными при лечении нарушений познания, сознания и окоченения.[62] В этом же исследовании был обнаружен один субъект, 71-летний мужчина, который не реагировал на стероиды, который ответил на лечение ИГВВ через 58 дней после начала заболевания.[нужна цитата ]
Прогноз
Полное выздоровление наблюдается в 50-70% случаев, в пределах от 70 до 90% выздоровления с некоторой незначительной остаточной инвалидностью (обычно оценивается с помощью таких мер, как Г-жа или же EDSS ), среднее время восстановления составляет от одного до шести месяцев.[15] Уровень смертности может достигать 5-10%.[65][66] Более плохие результаты связаны с невосприимчивостью к стероидной терапии, необычно тяжелыми неврологическими симптомами или внезапным началом. У детей, как правило, более благоприятные исходы, чем у взрослых, а у больных без лихорадки исходы обычно хуже.[67] Последний эффект может быть связан либо с защитным действием лихорадки, либо с тем, что диагноз и лечение начинают искать быстрее при наличии лихорадки.[нужна цитата ]
ADEM может перейти к MS. Считается РС, если некоторые поражения появляются в разное время и в разное время.[68]
Двигательный дефицит
По оценкам, остаточная двигательная недостаточность сохраняется примерно в 8-30% случаев, степень тяжести варьируется от легкой неуклюжести до атаксия и гемипарез.[27]
Нейрокогнитивный
У пациентов с демиелинизирующими заболеваниями, такими как рассеянный склероз, наблюдаются когнитивные нарушения даже при минимальной физической инвалидности.[69] Исследования показывают, что аналогичные эффекты наблюдаются после ADEM, но дефицит менее серьезен, чем при РС. В исследовании с участием шести детей с ADEM (средний возраст на момент обращения 7,7 года) были протестированы ряд нейрокогнитивных тестов после в среднем 3,5 лет восстановления.[70] Все шестеро детей показали нормальные результаты по большинству тестов, включая: вербальный IQ и производительность IQ, но выполнил хотя бы один стандартное отклонение ниже возрастных норм хотя бы в одной когнитивной сфере, например, комплексное внимание (один ребенок), краткосрочная память (один ребенок) и интернализирующее поведение /оказывать воздействие (двое детей). Групповые средние для каждой когнитивной области были в пределах одного стандартного отклонения от возрастных норм, демонстрируя, что как группа, они были нормальными. Эти нарушения были менее серьезными, чем те, которые наблюдались у детей того же возраста с диагнозом РС.[71]
Другое исследование сравнивало девятнадцать детей с историей ADEM, из которых 10 были в возрасте пяти лет или младше в то время (средний возраст 3,8 года, среднее тестирование прошло 3,9 года спустя) и девять детей были старше (средний возраст 7,7 года на тот момент). ADEM, протестировано в среднем 2,2 года спустя) к девятнадцати подобранным элементам контроля.[72] Результаты тестов на IQ и образовательные достижения были ниже для группы ADEM с ранним началом (средний IQ 90) по сравнению с группой с поздним началом (средний IQ 100) и контрольной группой (средний IQ 106), в то время как дети с ADEM с поздним началом получили более низкие баллы по вербальной обработке. скорость. Опять же, средние значения всех групп были в пределах одного стандартного отклонения от контроля, что означает, что, хотя эффекты были статистически надежными, дети в целом все еще были в пределах нормы. Также было больше проблем с поведением в группе с ранним началом, хотя есть некоторые предположения, что это может быть связано, по крайней мере частично, со стрессом госпитализации в молодом возрасте.[73][74]
Исследование
Отношения между ADEM и энцефаломиелит, связанный с анти-MOG в настоящее время исследуется. Была предложена новая организация под названием MOGDEM.[75]
О животных моделях, основной животной модели для РС, экспериментальный аутоиммунный энцефаломиелит (EAE) также является животной моделью для ADEM.[76] Будучи острым монофазным заболеванием, EAE гораздо больше похож на ADEM, чем на MS.[77]
Смотрите также
Рекомендации
- ^ Дейл RC (апрель 2003 г.). «Острый диссеминированный энцефаломиелит». Семин Педиатр Инфекция Дис. 14 (2): 90–5. Дои:10.1053 / spid.2003.127225. PMID 12881796.
- ^ Гарг РК (январь 2003 г.). «Острый диссеминированный энцефаломиелит». Postgrad Med J. 79 (927): 11–7. Дои:10.1136 / pmj.79.927.11. ЧВК 1742586. PMID 12566545.
- ^ Джонс CT (ноябрь 2003 г.). «Детские аутоиммунные неврологические заболевания центральной нервной системы». Neurol Clin. 21 (4): 745–64. Дои:10.1016 / S0733-8619 (03) 00007-0. PMID 14743647.
- ^ Huynh W, Cordato DJ, Kehdi E, Masters LT, Dedousis C (декабрь 2008 г.). «Поствакцинальный энцефаломиелит: обзор литературы и наглядный пример». J Clin Neurosci. 15 (12): 1315–1322. Дои:10.1016 / j.jocn.2008.05.002. ЧВК 7125578. PMID 18976924.
- ^ Rust RS (июнь 2000 г.). «Рассеянный склероз, острый диссеминированный энцефаломиелит и родственные состояния». Семин Педиатр Нейрол. 7 (2): 66–90. Дои:10.1053 / пб.2000.6693. PMID 10914409.
- ^ а б Позер CM, Бринар В.В. (октябрь 2007 г.). «Диссеминированный энцефаломиелит и рассеянный склероз: два разных заболевания - критический обзор». Acta Neurol. Сканд. 116 (4): 201–6. Дои:10.1111 / j.1600-0404.2007.00902.x. PMID 17824894.
- ^ Лорен Б. Крупп и др. Консенсусные определения, предложенные для детского рассеянного склероза и родственных заболеваний, 2007 г., AAN Enterprises, Inc. [1] В архиве 9 февраля 2015 г. Wayback Machine
- ^ а б Koelman, Diederik L.H .; Чахин, Салим; Mar, Soe S .; Венкатесан, Арун; Хогансон, Джордж М .; Йешокумар, Ануша К .; Баррерас, Паула; Маджмудар, Битту; Кляйн, Джошуа П. (31 мая 2016 г.). «Острый диссеминированный энцефаломиелит у 228 пациентов. Ретроспективное многоцентровое исследование в США». Неврология. 86 (22): 2085–2093. Дои:10.1212 / WNL.0000000000002723. ISSN 0028-3878. PMID 27164698.
- ^ а б Лик Дж. А., Албани С., Као А. С. и др. (Август 2004 г.). «Острый диссеминированный энцефаломиелит в детском возрасте: эпидемиологические, клинико-лабораторные особенности». Педиатр. Заразить. Dis. J. 23 (8): 756–64. Дои:10.1097 / 01.inf.0000133048.75452.dd. PMID 15295226.
- ^ Хайсон Дж. Л., Корнберг А. Дж., Коулман Л. Т., Шилд Л., Харви А. С., Кин М. Дж. (Май 2001 г.). «Клинико-нейрорадиологические особенности острого диссеминированного энцефаломиелита у детей». Неврология. 56 (10): 1308–12. Дои:10.1212 / WNL.56.10.1308. PMID 11376179.
- ^ а б Анлар Б., Басаран С., Козе Г. и др. (Август 2003 г.). «Острый диссеминированный энцефаломиелит у детей: исходы и прогноз». Нейропедиатрия. 34 (4): 194–9. Дои:10.1055 / с-2003-42208. PMID 12973660.
- ^ а б Schwarz S, Mohr A, Knauth M, Wildemann B, Storch-Hagenlocher B (май 2001 г.). «Острый диссеминированный энцефаломиелит: наблюдение с участием 40 взрослых пациентов». Неврология. 56 (10): 1313–8. Дои:10.1212 / WNL.56.10.1313. PMID 11376180.
- ^ а б Bhatt, P; Брей, L; Раджу, S; Чаудхари, Р. Bhatt, NS; Донда, К. (2019). «Временные тенденции педиатрических госпитализаций с острым распространенным энцефаломиелитом в Соединенных Штатах: анализ с 2006 по 2014 год с использованием национальной стационарной выборки». Журнал педиатрии. 206: 26–32.e1. Дои:10.1016 / j.jpeds.2018.10.044. PMID 30528761.
- ^ а б c d Koelman, Diederik L.H .; Матин, Фарра Дж. (13 марта 2015 г.). «Острый диссеминированный энцефаломиелит: современные противоречия в диагностике и исходе». Журнал неврологии. 262 (9): 2013–2024. Дои:10.1007 / s00415-015-7694-7. ISSN 0340-5354. PMID 25761377.
- ^ а б Менге Т., Кизейер БК, Несслер С., Хеммер Б., Хартунг ХП, Стюве О (июнь 2007 г.). «Острый диссеминированный энцефаломиелит: острое поражение головного мозга» (PDF). Curr. Мнение. Neurol. 20 (3): 247–54. Дои:10.1097 / WCO.0b013e3280f31b45. PMID 17495616.[постоянная мертвая ссылка ]
- ^ Вингерчук Д.М. (май 2003 г.). «Постинфекционный энцефаломиелит». Curr Neurol Neurosci Rep. 3 (3): 256–64. Дои:10.1007 / s11910-003-0086-х. PMID 12691631.
- ^ Poser CM (май 2008 г.). «Рассеянный склероз и рецидивирующий диссеминированный энцефаломиелит - это разные заболевания». Arch. Neurol. 65 (5): 674, ответ автора 674–5. Дои:10.1001 / archneur.65.5.674-а. PMID 18474749.
- ^ а б c Дейл Р.К., де Соуза С., Чонг В.К., Кокс Т.С., Хардинг Б., Невилл Б.Г. (декабрь 2000 г.). «Острый диссеминированный энцефаломиелит, многофазный диссеминированный энцефаломиелит и рассеянный склероз у детей». Мозг. 123 (12): 2407–22. Дои:10.1093 / мозг / 123.12.2407. PMID 11099444.
- ^ а б Ди Паули Франциска; и другие. (2015). «Фульминантный демиелинизирующий энцефаломиелит». Neurol Neuroimmunol Neuroinflamm. 2 (6): e175. Дои:10.1212 / NXI.0000000000000175. ЧВК 4635550. PMID 26587556.
- ^ а б c d е Тенембаум С., Чамолес Н., Фейерман Н. (октябрь 2002 г.). «Острый диссеминированный энцефаломиелит: долгосрочное исследование с участием 84 педиатрических пациентов». Неврология. 59 (8): 1224–31. Дои:10.1212 / WNL.59.8.1224. PMID 12391351.
- ^ Аллмендингер А., Краутхамер А., Спектор В. (2009). «Дело месяца». Диагностическая визуализация. 31 (12): 10.
- ^ Рейндл, М; Ди Паули, Ф; Rostásy, K; Бергер, Т. (август 2013 г.). «Спектр демиелинизирующих заболеваний, связанных с аутоантителами MOG». Нат Рев Нейрол. 9 (8): 455–61. Дои:10.1038 / nrneurol.2013.118. PMID 23797245.
- ^ а б Вебер М.С., Дерфус Т., Брюк В. (2018). «Демиелинизация центральной нервной системы, ассоциированная с антителами к миелиновым олигодендроцитам и гликопротеинам - новое заболевание?». JAMA Neurol. 75 (8): 909–910. Дои:10.1001 / jamaneurol.2018.1055. PMID 29913011.CS1 maint: несколько имен: список авторов (связь)
- ^ Камель М.Г., Нам Н.Т., Хан Н.Х., Эль-Шабуни А.Э., Макрам А.М., Абд-Эльхай Ф.А., Данг Т.Н., Хиеу Н.Л., Хыонг В.Т., Тунг Т.Х., Хираяма К., Хай (2017). «Острый диссеминированный энцефаломиелит после денге: отчет о болезни и метаанализ». PLOS Negl Trop Dis. 11 (6): e0005715. Дои:10.1371 / journal.pntd.0005715. PMID 28665957.CS1 maint: несколько имен: список авторов (связь)
- ^ Фишер, Д.Л .; Defres, S; Соломон, Т (2015). «Корневой энцефалит». QJM. 108 (3): 177–182. Дои:10.1093 / qjmed / hcu113. PMID 24865261.
- ^ редактор, Ian Sample Science (8 июля 2020 г.). «Предупреждение о серьезных нарушениях мозга у людей с легкими симптомами коронавируса». Хранитель. ISSN 0261-3077. Получено 8 июля 2020.CS1 maint: дополнительный текст: список авторов (связь)
- ^ а б c Тенембаум С., Читнис Т., Несс Дж., Хан Дж. С. (апрель 2007 г.). Международная педиатрическая исследовательская группа РС. «Острый диссеминированный энцефаломиелит». Неврология. 68 (16 Дополнение 2): S23–36. Дои:10.1212 / 01.wnl.0000259404.51352.7f. PMID 17438235. S2CID 19893165.
- ^ а б Hemachudha T, Griffin DE, Giffels JJ, Johnson RT, Moser AB, Phanuphak P (февраль 1987 г.). «Основной белок миелина как энцефалитоген при энцефаломиелите и полиневрите после вакцинации против бешенства». N. Engl. J. Med. 316 (7): 369–74. Дои:10.1056 / NEJM198702123160703. PMID 2433582.
- ^ Hemachudha T, Griffin DE, Johnson RT, Giffels JJ (январь 1988 г.). «Иммунологические исследования пациентов с хроническим энцефалитом, вызванным постконтактной вакциной от бешенства Семпл». Неврология. 38 (1): 42–4. Дои:10.1212 / WNL.38.1.42. PMID 2447520.
- ^ Мурти Дж. М. (сентябрь 2002 г.). «Острый диссеминированный энцефаломиелит». Neurol Индия. 50 (3): 238–43. PMID 12391446.
- ^ а б Фенихель GM (август 1982 г.). «Неврологические осложнения иммунизации». Анна. Neurol. 12 (2): 119–28. Дои:10.1002 / ana.410120202. PMID 6751212.
- ^ Takahashi H, Pool V, Tsai TF, Chen RT (июль 2000 г.). «Неблагоприятные события после вакцинации против японского энцефалита: обзор данных постмаркетингового наблюдения из Японии и США. Рабочая группа VAERS». Вакцина. 18 (26): 2963–9. Дои:10.1016 / S0264-410X (00) 00111-0. PMID 10825597.
- ^ Tourbah A, Gout O, Liblau R и др. (Июль 1999 г.). «Энцефалит после вакцинации против гепатита В: рецидивирующий диссеминированный энцефалит или РС?». Неврология. 53 (2): 396–401. Дои:10.1212 / WNL.53.2.396. PMID 10430433.
- ^ Караали-Саврун Ф., Алтынташ А., Сайп С., Шива А. (ноябрь 2001 г.). «Миелит, связанный с вакциной против гепатита В?». Евро. J. Neurol. 8 (6): 711–5. Дои:10.1046 / j.1468-1331.2001.00290.x. PMID 11784358.
- ^ Сейвар Дж. Дж., Лабутта Р. Дж., Чепмен Л. Е., Грабенштейн Дж. Д., Искандер Дж., Лейн Дж. М. (декабрь 2005 г.). «Неблагоприятные неврологические явления, связанные с вакцинацией против оспы в США, 2002-2004 гг.». JAMA. 294 (21): 2744–50. Дои:10.1001 / jama.294.21.2744. PMID 16333010.
- ^ Одзава Х., Нома С., Йошида Й., Секин Х., Хашимото Т. (август 2000 г.). «Острый диссеминированный энцефаломиелит, связанный с вакциной против полиомиелита». Педиатр. Neurol. 23 (2): 177–9. Дои:10.1016 / S0887-8994 (00) 00167-3. PMID 11020647.
- ^ Страттон, Кэтлин Р .; Хау, Синтия Дж .; Джонстон-младший, Ричард Б., ред. (1994). Неблагоприятные события, связанные с вакцинами для детей: доказательства причинно-следственной связи. Издательство национальных академий. С. 125–126. ISBN 978-0-309-07496-4. Получено 6 декабря 2015.
- ^ Миллер Х. Г., Стэнтон Дж. Б., Гиббонс Дж. Л. (1956). «Параинфекционный энцефаломиелит и родственные синдромы». Ежеквартальный медицинский журнал. 25 (100): 427–505. PMID 13379602.
- ^ JordanCole et al., Острый диссеминированный энцефаломиелит у детей: обновленный обзор, основанный на текущих диагностических критериях, Детская неврология, 3 июля 2019 г., https://doi.org/10.1016/j.pediatrneurol.2019.06.017
- ^ Тенембаум С., Читнис Т., Несс Дж., Хан Дж. С. (2007). «Острый диссеминированный энцефаломиелит». Неврология. 68 (16 добавление 2): S23 – S36. Дои:10.1212 / 01.wnl.0000259404.51352.7f. PMID 17438235. S2CID 19893165.
- ^ Вингерчук Д.М., Лучинетти С.Ф. (июнь 2007 г.). «Сравнительный иммунопатогенез острого диссеминированного энцефаломиелита, оптического нейромиелита и рассеянного склероза». Curr. Мнение. Neurol. 20 (3): 343–50. Дои:10.1097 / WCO.0b013e3280be58d8. PMID 17495631.
- ^ Вайншенкер Б., Миллер Д. (1999). Рассеянный склероз: одно заболевание или много? В: Siva A, Kesselring J, Thompson A, eds. Границы рассеянного склероза. Лондон: Дуниц, стр. 37-46.
- ^ Хартунг ХП, Гроссман Р.И. (май 2001 г.). «ADEM: отдельное заболевание или часть спектра рассеянного склероза?». Неврология. 56 (10): 1257–60. Дои:10.1212 / WNL.56.10.1257. PMID 11376169.
- ^ Krupp LB, Banwell B, Tenembaum S, Международная педиатрическая исследовательская группа MS (2007). «Консенсусные определения, предложенные для детского рассеянного склероза и родственных заболеваний». Неврология. 68 (Приложение 2): S7 – S12. Дои:10.1212 / 01.wnl.0000259422.44235.a8. PMID 17438241. S2CID 26001350.
- ^ а б Лассманн Х (февраль 2010 г.). «Острый диссеминированный энцефаломиелит и рассеянный склероз». Мозг. 133 (Pt 2): 317–319. Дои:10.1093 / мозг / awp342. PMID 20129937.
- ^ McDonald WI, Compston A, Эдан Г. и др. (2001). «Рекомендуемые диагностические критерии рассеянного склероза: рекомендации Международной группы по диагностике рассеянного склероза». Анна. Neurol. 50 (1): 121–7. CiteSeerX 10.1.1.466.5368. Дои:10.1002 / ana.1032. PMID 11456302.
- ^ а б Янг Н. П. и др. (2010). «Перивенозная демиелинизация: связь с клинически определенным острым диссеминированным энцефаломиелитом и сравнение с патологически подтвержденным рассеянным склерозом». Мозг. 133 (2): 333–48. Дои:10.1093 / мозг / awp321. ЧВК 2822631. PMID 20129932.
- ^ Молодой НП (февраль 2008 г.). «Острый диссеминированный энцефаломиелит: современное понимание и противоречия. Издательство Thieme Medical» (PDF). Семин Нейрол. 28 (1): 84–94. Дои:10.1055 / с-2007-1019130. PMID 18256989.
- ^ Гюнтер А.Д., Муньос Д.Г. (2013). «Бляшечная демиелинизация при остром диссеминированном энцефаломиелите (ADEM) - отчет о вскрытии». Клиническая невропатология. 32 (6): 486–491. Дои:10.5414 / NP300634. PMID 23863345.
- ^ Лу З., Чжан Б., Цю В., Кан З., Шен Л. и др. (2011). «Сравнительные поражения ствола головного мозга на МРТ острого рассеянного энцефаломиелита, оптического нейромиелита и рассеянного склероза». PLOS One. 6 (8): e22766. Bibcode:2011PLoSO ... 622766L. Дои:10.1371 / journal.pone.0022766. ЧВК 3154259. PMID 21853047.
- ^ Гюнтер А.Д., Муньос Д.Г. (2013). «Бляшечная демиелинизация при остром диссеминированном энцефаломиелите (ADEM) - отчет о вскрытии». Клиническая невропатология. 32 (6): 486–491. Дои:10.5414 / NP300634. PMID 23863345.
- ^ Schwarz S, Mohr A, Knauth M, Wildemann B, Storch-Hagenlocher B (2001). «Острый диссеминированный энцефаломиелит: последующее исследование 40 взрослых пациентов». Неврология. 56 (10): 1313–1318. Дои:10.1212 / WNL.56.10.1313. PMID 11376180.
- ^ М. Бауманн, Э.М. Хеннес, К. Шанда, М. Каренфорт, Б. Байер-Корнек, К. Дипольд, Б. Фидлер, И. Марквардт, Й. Страутманис, С. Викер, М. Рейндл, К. Ростаси. «Клиническая характеристика и нейрорадиологические данные у детей с многофазным демиелинизирующим энцефаломиелитом и антителами к MOG. Европейский журнал детской неврологии, Том 19, Приложение 1, май 2015 г., страницы S21, Тезисы 11-го Конгресса EPNS. 22 мая 2015. Дои:10.1016 / S1090-3798 (15) 30066-0
- ^ Baumann M; и другие. (2016). «Дети с многофазным диссеминированным энцефаломиелитом и антителами к гликопротеину миелинолигодендроцитов (MOG): расширение спектра заболеваний, вызывающих положительные антитела к MOG». Мульт Склер. 22 (14): 1821–1829. Дои:10.1177/1352458516631038. PMID 26869530.
- ^ а б Дэвис Н.В., Шариф МК, Ховард Р.С. (июль 2006 г.).«Инфекционно-ассоциированные энцефалопатии: их исследование, диагностика и лечение». J. Neurol. 253 (7): 833–45. Дои:10.1007 / s00415-006-0092-4. PMID 16715200.
- ^ а б Стоун MJ, Хокинс CP (2007). «Медицинский обзор энцефалита». Neuropsychol Rehabil. 17 (4–5): 429–49. Дои:10.1080/09602010601069430. PMID 17676529.
- ^ а б Арчер H, Wall R (февраль 2003 г.). «Острая геморрагическая лейкоэнцефалопатия: два клинических случая и обзор литературы». J. Infect. 46 (2): 133–7. Дои:10.1053 / jinf.2002.1096. PMID 12634076.
- ^ Венугопал В, Хайдер М (2013). «Отчет о первом случае острого геморрагического лейкоэнцефалита после Плазмодий вивакс инфекционное заболевание". Индийский J Med Microbiol. 31 (1): 79–81. Дои:10.4103/0255-0857.108736. PMID 23508437.
- ^ Йылдыз О .; и другие. (Сентябрь 2015 г.). «Острый геморрагический лейкоэнцефалит (синдром Вестона-Херста) у пациента с ремиттирующим рассеянным склерозом». J нейровоспаление. 12 (1): 175. Дои:10.1186 / s12974-015-0398-1. ЧВК 4574135. PMID 26376717.
- ^ Марк Вилли Мондиа и др., Острый геморрагический лейкоэнцефалит Вестона Херста, вторичный по отношению к герпетическому энцефалиту, проявляющийся как эпилептический статус: отчет о клиническом случае и обзор литературы, Журнал клинической неврологии, том 67, сентябрь 2019 г., страницы 265-270, https://doi.org/10.1016/j.jocn.2019.06.020
- ^ а б c Шахар Э., Андраус Дж., Савицки Д., Пилар Г., Зельник Н. (ноябрь 2002 г.). «Исход тяжелого энцефаломиелита у детей: действие высоких доз метилпреднизолона и иммуноглобулинов». J. Child Neurol. 17 (11): 810–4. Дои:10.1177/08830738020170111001. PMID 12585719.
- ^ а б Ravaglia S, Piccolo G, Ceroni M и др. (Ноябрь 2007 г.). «Тяжелый стероидрезистентный постинфекционный энцефаломиелит: общие характеристики и эффекты IVIg». J. Neurol. 254 (11): 1518–23. Дои:10.1007 / s00415-007-0561-4. PMID 17965959.
- ^ Штраусберг Р., Шонфельд Т., Вайц Р., Кармазин Б., Харель Л. (февраль 2001 г.). «Лечение атипичного острого диссеминированного энцефаломиелита стероидами и внутривенными иммуноглобулинами». Педиатр. Neurol. 24 (2): 139–43. Дои:10.1016 / S0887-8994 (00) 00229-0. PMID 11275464.
- ^ Фисби Т., Бэнвелл Б., Бенстед Т. и др. (Апрель 2007 г.). «Рекомендации по применению внутривенного иммуноглобулина при неврологических состояниях». Трансфус Мед Рев. 21 (2 Дополнение 1): S57–107. Дои:10.1016 / j.tmrv.2007.01.002. PMID 17397768.
- ^ «Менге и др. 2007»
- ^ Камель М.Г., Нам Н.Т., Хан Н.Х., Эль-Шабуни А.Э., Макрам А.М., Абд-Эльхай Ф.А., Данг Т.Н., Хиеу Н.Л., Хыонг В.Т., Тунг Т.Х., Хираяма К., Хай Н.Т. (2017). «Острый диссеминированный энцефаломиелит после денге: отчет о болезни и метаанализ». PLOS Negl Trop Dis. 11 (6): e0005715. Дои:10.1371 / journal.pntd.0005715. ЧВК 5509372. PMID 28665957.CS1 maint: несколько имен: список авторов (связь)
- ^ Лин Ч., Дженг Дж. С., Се СТ, Ип П. К., Ву Р. М. (февраль 2007 г.). «Острый диссеминированный энцефаломиелит: последующее исследование на Тайване». J. Neurol. Нейрохирургия. Психиатрия. 78 (2): 162–7. Дои:10.1136 / jnnp.2005.084194. ЧВК 2077670. PMID 17028121.
- ^ Мало-Пион, Кэролайн; Ламберт, Раймонд; Декари, Жан-Клод; Терпин, Софи (2018). «Визуализация приобретенного демиелинизирующего синдрома с 18F-FDG ПЭТ / КТ». Клиническая ядерная медицина. 43 (2): 103–105. Дои:10.1097 / RLU.0000000000001916. PMID 29215409.
- ^ Фунг Дж., Розевич Л., Квагебер Г. и др. (Январь 1997 г.). «Исполнительная функция при рассеянном склерозе. Роль патологии лобной доли». Мозг. 120 (1): 15–26. Дои:10.1093 / мозг / 120.1.15. PMID 9055794.
- ^ Hahn CD, Miles BS, MacGregor DL, Blaser SI, Banwell BL, Hetherington CR (август 2003 г.). «Нейрокогнитивные исходы после острого диссеминированного энцефаломиелита». Педиатр. Neurol. 29 (2): 117–23. Дои:10.1016 / S0887-8994 (03) 00143-7. PMID 14580654.
- ^ Банвелл Б.Л., Андерсон ЧП (март 2005 г.). «Познавательная нагрузка рассеянного склероза у детей». Неврология. 64 (5): 891–4. Дои:10.1212 / 01.WNL.0000152896.35341.51. PMID 15753431.
- ^ Джейкобс Р.К., Андерсон В.А., Нил Дж.Л., Шилд Л.К., Корнберг А.Дж. (сентябрь 2004 г.). «Нейропсихологический результат после острого рассеянного энцефаломиелита: влияние возраста на начало болезни». Педиатр. Neurol. 31 (3): 191–7. Дои:10.1016 / j.pediatrneurol.2004.03.008. PMID 15351018.
- ^ Дуглас Дж. В. (август 1975 г.). «Ранняя госпитализация и последующие нарушения поведения и обучения». Дев Мед Детский Нейрол. 17 (4): 456–80. Дои:10.1111 / j.1469-8749.1975.tb03497.x. PMID 1158052.
- ^ Дэвисс В.Б., Ракузин Р., Флейшер А., Муни Д., Форд Д.Д., МакХьюго Г.Дж. (май 2000 г.). «Симптоматика острого стрессового расстройства при госпитализации по поводу детской травмы». J Am Acad Детская подростковая психиатрия. 39 (5): 569–75. Дои:10.1097/00004583-200005000-00010. PMID 10802974.
- ^ Тацуро Мису, Кадзуо Фуджихара, Спектр нейромиелита зрительного нерва и диссеминированный энцефаломиелит, связанный с гликопротеином миелиновых олигодендроцитов, Cli. и эксп. нейроиммунология, Том 10, Выпуск 1, февраль 2019, страницы 9-17, https://doi.org/10.1111/cen3.12491
- ^ Реки TM, Швенткер Ф.Ф. (1935). «Энцефаломиелит с разрушением миелина, экспериментально полученный на обезьянах». J. Exp. Med. 61 (5): 689–701. Дои:10.1084 / jem.61.5.689. ЧВК 2133246. PMID 19870385.
- ^ Шрирам С., Штайнер I (декабрь 2005 г.). «Экспериментальный аллергический энцефаломиелит: вводящая в заблуждение модель рассеянного склероза». Анна. Neurol. 58 (6): 939–45. Дои:10.1002 / ana.20743. PMID 16315280.
внешняя ссылка
- Острый диссеминированный энцефаломиелит в Национальные институты здравоохранения США Офис Редкие заболевания
- Информационная страница об остром диссеминированном энцефаломиелите в NINDS
- Информация для родителей об остром диссеминированном энцефаломиелите
| Классификация | |
|---|---|
| Внешние ресурсы |
