Митохондриальная болезнь - Mitochondrial disease
эта статья нужны дополнительные цитаты для проверка. (Февраль 2014 года) (Узнайте, как и когда удалить этот шаблон сообщения) |
| Митохондриальная болезнь | |
|---|---|
 | |
| Микрофотография показывает рваные красные волокна, обнаружение, которое наблюдается при различных типах митохондриальных заболеваний. Биопсия мышц. Пятно трихрома Гомори. | |
| Специальность | Медицинская генетика |
Митохондриальные заболевания группа нарушений, вызванных дисфункциональными митохондрии, то органеллы которые генерируют энергию для клетки. Митохондрии находятся в каждой клетке человеческого тела, кроме красные кровяные клетки, и преобразовать энергию молекул пищи в АТФ это обеспечивает большинство функций клеток.
Митохондриальные заболевания приобретают уникальные характеристики как из-за того, что заболевания часто передаются по наследству, так и из-за того, что митохондрии так важны для функционирования клеток. Подкласс этих болезней, у которых есть нервно-мышечные симптомы иногда называют митохондриальные миопатии.
Признаки и симптомы
Симптомы включают:
- плохой рост
- потеря мышечной координации
- мышечная слабость
- проблемы со зрением
- проблемы со слухом
- неспособность к обучению
- сердечное заболевание
- заболевание печени
- болезнь почек
- желудочно-кишечные расстройства
- респираторные расстройства
- неврологические проблемы
- вегетативная дисфункция
- слабоумие[1]
Приобретенные состояния, в которые вовлечена митохондриальная дисфункция, включают:
- сахарный диабет
- болезнь Хантингтона
- рак
- Болезнь Альцгеймера
- болезнь Паркинсона
- биполярное расстройство,[2][3][4] шизофрения, старение и старение, тревожные расстройства[5]
- сердечно-сосудистые заболевания
- саркопения
- Синдром хронической усталости[3]
Тело и каждая мутация модулируется другими вариантами генома; мутация, которая у одного человека может вызвать заболевание печени, может у другого человека вызвать расстройство мозга. Степень тяжести конкретного дефекта также может быть большой или небольшой. Некоторые дефекты включают непереносимость упражнений. Дефекты часто более серьезно влияют на работу митохондрий и нескольких тканей, что приводит к мультисистемным заболеваниям.[6]
Как правило, митохондриальные заболевания усугубляются, когда дефектные митохондрии присутствуют в мышцы, головной мозг, или нервы,[7] потому что эти клетки используют больше энергии, чем большинство других клеток тела.
Хотя митохондриальные заболевания сильно различаются по проявлениям от человека к человеку, были определены несколько основных клинических категорий этих состояний, основанных на наиболее общих фенотипических особенностях, симптомах и признаках, связанных с конкретными мутациями, которые, как правило, вызывают их.[нужна цитата ]
Остается нерешенным вопрос и область исследований: действительно ли истощение АТФ или активные формы кислорода ответственны за наблюдаемые фенотипические последствия.[нужна цитата ]
Атрофия мозжечка или гипоплазия иногда сообщалось, что они связаны.[8]
Причины
Митохондриальные нарушения могут быть вызваны: мутации (приобретенная или унаследованная), в митохондриальной ДНК (мтДНК ) или в ядерные гены этот код для митохондриальных компонентов. Они также могут быть результатом приобретенной митохондриальной дисфункции из-за неблагоприятного воздействия наркотики, инфекции или другие экологические причины.[9]
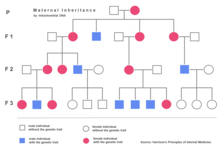
Ядерная ДНК имеет две копии на клетку (кроме сперматозоидов и яйцеклеток), одна копия унаследована от отца, а другая - от матери. Однако митохондриальная ДНК наследуется только от матери (с некоторые исключения ) и каждой митохондриальной органелла обычно содержит от 2 до 10 мтДНК копии. В течение деление клеток митохондрии случайным образом разделяются между двумя новыми клетками. Эти митохондрии делают больше копий, обычно достигая 500 митохондрий на клетку. Поскольку мтДНК копируется при пролиферации митохондрий, они могут накапливать случайные мутации, явление, называемое гетероплазмия. Если только несколько копий мтДНК, унаследованных от матери, являются дефектными, деление митохондрий может привести к тому, что большая часть дефектных копий окажется в одной из новых митохондрий (более подробные схемы наследования см. митохондриальная генетика человека ). Митохондриальное заболевание может стать клинически очевидным, когда количество пораженных митохондрий достигнет определенного уровня; это явление называется "пороговое выражение ".
Митохондрии обладают многими из тех же путей репарации ДНК, что и ядра, но не всеми;[10] следовательно, мутации чаще встречаются в митохондриальной ДНК, чем в ядерной ДНК (см. Скорость мутации ). Это означает, что нарушения митохондриальной ДНК могут возникать спонтанно и относительно часто. Дефекты ферментов, контролирующих митохондрии. Репликация ДНК (все они кодируются генами ядерной ДНК) также могут вызывать мутации митохондриальной ДНК.
Большая часть митохондриальной функции и биогенеза контролируется ядерная ДНК. Митохондриальная ДНК человека кодирует 13 белков группы дыхательная цепь, в то время как большинство из примерно 1500 белков и компонентов, нацеленных на митохондрии, кодируются ядром. Дефекты в ядерно-кодируемых митохондриальных генах связаны с сотнями клинических фенотипов заболеваний, включая анемия, слабоумие, гипертония, лимфома, ретинопатия, припадки, и расстройства нервного развития.[11]
Исследование исследователей Йельского университета (опубликовано 12 февраля 2004 г., выпуск журнала Медицинский журнал Новой Англии ) исследовали роль митохондрий в инсулинорезистентности у потомков пациентов с диабетом 2 типа.[12]Другие исследования показали, что этот механизм может включать прерывание митохондриального сигнального процесса в клетках организма (внутримиоцеллюлярные липиды ). Исследование, проведенное в Центре биомедицинских исследований Пеннингтона в Батон-Руж, штат Луизиана.[13] показали, что это, в свою очередь, частично отключает гены, производящие митохондрии.
Примеры
Примеры митохондриальных заболеваний:
- Митохондриальная миопатия
- Сахарный диабет и глухота (ПАПА)
- эта комбинация в раннем возрасте может быть связана с митохондриальным заболеванием
- Сахарный диабет и глухота можно найти вместе по другим причинам
- Наследственная оптическая нейропатия Лебера (LHON)
- потеря зрения, начинающаяся в молодом возрасте
- заболевание глаз, характеризующееся прогрессирующей потерей центрального зрения из-за дегенерации зрительных нервов и сетчатки
- затрагивает 1 из 50 000 жителей Финляндии
- Синдром Ли, подострая склерозирующая энцефалопатия
- после нормального развития заболевание обычно начинается в конце первого года жизни, хотя начало может наступить в зрелом возрасте.
- происходит быстрое снижение функции, которое сопровождается судорогами, измененным состоянием сознания, деменцией, недостаточностью дыхания
- Невропатия, атаксия, пигментный ретинит и птоз (НАРП)
- прогрессирующие симптомы, как описано в аббревиатуре
- слабоумие
- Мионеврогенная желудочно-кишечная энцефалопатия (MNGIE)
- желудочно-кишечная псевдообструкция
- невропатия
- Миоклоническая эпилепсия с рваными красными волокнами (MERRF)
- прогрессирующая миоклоническая эпилепсия
- «Рваные красные волокна» - это скопления пораженных митохондрий, которые накапливаются в субстрате.сарколеммаль области мышечного волокна и появляются, когда мышца окрашивается модифицированным Пятно трихрома Гемёри
- невысокий рост
- потеря слуха
- лактоацидоз
- непереносимость упражнений
- Синдром MELAS
- Синдром истощения митохондриальной ДНК
Такие условия как Атаксия Фридрейха может повлиять на митохондрии но не связаны с митохондриальными белками.
Механизмы
Общая эффективная единица энергии для доступной энергии тела называется дневной гликоген генерирующая мощность,[14][15][16] и используется для сравнения митохондриального выхода здоровых людей с митохондриями, страдающими или хронически истощенными гликогеном. Это значение медленно изменяется у конкретного человека, так как для завершения полного цикла требуется от 18 до 24 месяцев.[15]
Способность генерировать гликоген полностью зависит от рабочих уровней организма и определяется ими. митохондрии во всех клетки из человеческое тело;[17] однако связь между энергия генерируется митохондриями, а емкость гликогена очень слаба и опосредуется многими биохимические пути.[14] Энергетический выход полноценной здоровой митохондриальной функции можно точно предсказать с помощью сложного теоретического аргумента, но этот аргумент непрост, поскольку большая часть энергии потребляется мозгом и ее нелегко измерить.
Диагностика
Митохондриальные заболевания обычно обнаруживают путем анализа образцов мышц, в которых присутствие этих органелл выше. Наиболее распространенными тестами для выявления этих заболеваний являются:
- Саузерн-блот для обнаружения больших удалений или дубликатов
- Полимеразной цепной реакции и конкретные мутации
- Последовательность действий
Лечение
Хотя исследования продолжаются, варианты лечения в настоящее время ограничены; витамины часто назначаются, хотя доказательства их эффективности ограничены.[18] Пируват был предложен в 2007 году как вариант лечения.[19] N-ацетил цистеин обращает вспять многие модели митохондриальной дисфункции.[20] В случае расстройств настроения, особенно биполярное расстройство предполагается, что N-ацетилцистеин (NAC), ацетил-L-карнитин (ALCAR), S-аденозилметионин (SAMe), кофермент Q10 (CoQ10), альфа-липоевая кислота (ALA), моногидрат креатина (CM), и мелатонин могут быть потенциальными вариантами лечения.[21]
Генная терапия до зачатия
Передача шпинделя, где ядерная ДНК переносится в другую здоровую яйцеклетку, оставляя дефектную митохондриальная ДНК позади - потенциальная лечебная процедура, успешно проведенная на обезьянах.[22][23] Используя аналогичный пронуклеарный перенос техники, исследователи Ньюкаслский университет во главе с Дуглас Тернбулл успешно трансплантировали здоровую ДНК из человеческих яйцеклеток от женщин с митохондриальными заболеваниями в яйцеклетки женщин-доноров, которые не были затронуты.[24][25] В таких случаях возникают этические вопросы относительно биологического материнства, поскольку ребенок получает гены и генные регуляторные молекулы. от двух разных женщин. Использование генной инженерии в попытках произвести на свет детей, свободных от митохондриальных заболеваний, вызывает споры в некоторых кругах и поднимает важные вопросы. этические вопросы.[26][27] Ребенок мужского пола родился в Мексике в 2016 году от матери с синдромом Ли с использованием переноса веретена.[28]
В сентябре 2012 года в Великобритании были начаты общественные консультации для изучения связанных с этим этических проблем.[29] Генная инженерия человека использовалась в небольших масштабах, чтобы позволить бесплодным женщинам с генетическими дефектами в их митохондрии иметь детей.[30] В июне 2013 г. объединенное Королевство правительство согласилось разработать закон, который узаконит ЭКО 'процедура как лечение для исправления или устранения митохондриальных заболеваний, которые передаются от матери к ребенку. Процедура может быть предложена с 29 октября 2015 года после того, как будут установлены правила.[31][32][33]Эмбриональный митохондриальный трансплантат и защита были предложены в качестве возможного лечения наследственных митохондриальных заболеваний, и аллотопическое выражение митохондриальных белков как радикальное лечение нагрузки мутаций мтДНК.
В июне 2018 года Комитет по делам сообщества Сената Австралии рекомендовал предпринять шаги по легализации Заместительная митохондриальная терапия (MRT). Исследования и клиническое применение MRT контролировались законами, принятыми федеральным правительством и правительствами штатов. Законы штатов по большей части соответствовали федеральному закону. Во всех штатах законодательство запрещает использование методов МРТ в клинике, и, за исключением Западной Австралии, исследования ограниченного диапазона МРТ были разрешены до 14 дня развития эмбриона при условии предоставления лицензии. В 2010 году Hon. Член парламента Марк Батлер, тогдашний федеральный министр психического здоровья и старения, назначил независимый комитет для рассмотрения двух соответствующих актов: Закон о запрещении клонирования человека в целях воспроизводства 2002 г. и Закон об исследованиях, связанных с человеческими эмбрионами, 2002 г.. В отчете комитета, выпущенном в июле 2011 года, было рекомендовано оставить действующее законодательство без изменений.
В настоящее время проводятся клинические испытания на людях в GenSight Biologics (ClinicalTrials.gov # NCT02064569) и Университете Майами (ClinicalTrials.gov # NCT02161380) для изучения безопасности и эффективности митохондриальной генной терапии при наследственной оптической невропатии Лебера.
Эпидемиология
Примерно у 1 из 4000 детей в Соединенных Штатах к 10 годам разовьются митохондриальные заболевания. До 4000 детей в год в США рождаются с типом митохондриального заболевания.[34] Поскольку митохондриальные нарушения содержат множество вариаций и подмножеств, некоторые конкретные митохондриальные нарушения очень редки.
Среднее число рождений в год среди женщин с риском передачи мтДНК оценивается примерно в 150 в объединенное Королевство и 800 в Соединенные Штаты.[35]
История
Первая патогенная мутация в митохондриальной ДНК была обнаружена в 1988 г .; с того времени до 2016 года было выявлено около 275 других болезнетворных мутаций.[36]:37
Известные случаи
Известные люди, страдающие митохондриальными заболеваниями, включают:
- Мэтти Степанек, поэт, защитник мира и мотивирующий оратор, страдавший от дисвегетативной митохондриальной миопатии и умерший в 13 лет.
- Рокко Бальделли, тренер и бывший центральный игрок в Высшая лига бейсбола который был вынужден уйти из активной игры в возрасте 29 лет из-за митохондриальной каннелопатии.
- Чарли Гард, британский мальчик, страдавший от синдром истощения митохондриальной ДНК; решения о его опеке были переданы в различные суды.
использованная литература
- ^ Ненад Блау; Маринус Дюран; K Майкл Гибсон; Карло Диониси Вичи (2014-07-08). Руководство для врача по диагностике, лечению и наблюдению за наследственными метаболическими заболеваниями. Springer. стр. 339–. ISBN 978-3-642-40337-8.
- ^ Аист, Ц; Реншоу, П. Ф. (2005). «Дисфункция митохондрий при биполярном расстройстве: данные исследований магнитно-резонансной спектроскопии». Молекулярная психиатрия. 10 (10): 900–19. Дои:10.1038 / sj.mp.4001711. PMID 16027739.
- ^ а б Печеник, Стив Р.; Нойштадт, Джон (2007). «Митохондриальная дисфункция и молекулярные пути заболевания». Экспериментальная и молекулярная патология. 83 (1): 84–92. Дои:10.1016 / j.yexmp.2006.09.008. PMID 17239370.
- ^ Ниренберг, Эндрю А; Канский, Кристина; Бреннан, Брайан П.; Шелтон, Ричард С; Перлис, Рой; Иосифеску, Дэн V (2012). «Модуляторы митохондрий для биполярного расстройства: патофизиологически обоснованная парадигма для разработки новых лекарств». Австралийский и новозеландский журнал психиатрии. 47 (1): 26–42. Дои:10.1177/0004867412449303. PMID 22711881.
- ^ Мисевич, Зузанна; Юрато, Стелла; Кулеская Наталья; Салминен, Лаура; Родригес, Луис; Маккарроне, Джузеппина; Мартинс, Джейд; Чамара, Дарина; Laine, Mikaela A .; Соколовская, Ева; Тронтти, Калеви; Ревертс, Кристиана; Новак, Божидар; Волк, Наама; Парк, Донг Ик; Йокитало, Эйджа; Паулин, Ларс; Аувинен, Петри; Войкар, Воотеле; Чен, Алон; Эрхардт, Анжелика; Терк, Кристоф В .; Ховатта, Иирис (26 сентября 2019 г.). «Многокомпонентный анализ определяет митохондриальные пути, связанные с поведением, связанным с тревогой». PLOS Genetics. 15 (9): e1008358. Дои:10.1371 / journal.pgen.1008358. ISSN 1553-7404. ЧВК 6762065. PMID 31557158.
- ^ Нуннари Дж, Суомалайнен А (2012). «Митохондрии: в болезни и в здоровье». Ячейка. 148 (6): 1145–59. Дои:10.1016 / j.cell.2012.02.035. ЧВК 5381524. PMID 22424226.
- ^ Финстерер, Йозеф (2007). «Гематологические проявления первичных митохондриальных заболеваний». Acta Haematologica. 118 (2): 88–98. Дои:10.1159/000105676. PMID 17637511.
- ^ Лакс, Николай Зои; Хепплуайт, Филиппа Денис; Рив, Эми Кэтрин; Несбитт, Виктория; Макфарланд, Роберт; Ярос, Эвелин; Тейлор, Роберт Уильям; Тернбулл, Дуглас Мэтью (2012). «Мозжечковая атаксия у пациентов с заболеванием митохондриальной ДНК». Журнал невропатологии и экспериментальной неврологии. 71 (2): 148–61. Дои:10.1097 / NEN.0b013e318244477d. ЧВК 3272439. PMID 22249460.
- ^ «Митохондриальные болезни». MeSH. Получено 2 августа 2019.
- ^ Алексеев М., Шоколенко И., Уилсон Г., Леду С. (май 2013 г.). «Поддержание целостности митохондриальной ДНК - критический анализ и обновление». Перспективы Колд-Спринг-Харбор в биологии. 5 (5): a012641. Дои:10.1101 / cshperspect.a012641. ЧВК 3632056. PMID 23637283.
- ^ Шарфе К., Лу Х. Х., Нойенбург Дж. К., Аллен Э. А., Ли Г. К., Клопсток Т., Коуэн Т. М., Эннс Г. М., Дэвис Р. В. (2009). Ржецкий А (ред.). «Картирование ассоциаций генов в митохондриях человека с использованием клинических фенотипов болезни». PLOS Comput Biol. 5 (4): e1000374. Bibcode:2009PLSCB ... 5E0374S. Дои:10.1371 / journal.pcbi.1000374. ЧВК 2668170. PMID 19390613.
- ^ Петерсен, Китт Фальк; Дюфур, Сильви; Бефрой, Дуглас; Гарсия, Рина; Шульман, Джеральд И. (2004). «Нарушение митохондриальной активности у инсулинорезистентных потомков пациентов с диабетом 2 типа». Медицинский журнал Новой Англии. 350 (7): 664–671. Дои:10.1056 / NEJMoa031314. ISSN 0028-4793. ЧВК 2995502. PMID 14960743.
- ^ Сахарный диабет 54, 2005 1926-33
- ^ а б Митчелл, Питер. «Концепция дыхательной цепи Дэвида Кейлина и ее хемиосмотические последствия» (PDF). Нобелевский институт.
- ^ а б Микелакис, Евангелос (январь 2007 г.). «Ось Mitochondria-K + Channel подавлена при раке, и ее нормализация способствует апоптозу и подавляет рост рака». Университет Альберты. Университет Альберты, 2007. 11 (1): 37–51. Дои:10.1016 / j.ccr.2006.10.020. PMID 17222789.
- ^ Лорини и Чиман, M, & M (1962). «Гипогликемическое действие солей диизопропиламмония при экспериментальном диабете». Институт биохимии Падуанского университета, сентябрь 1962 г.. Биохимическая фармакология. 11 (9): 823–827. Дои:10.1016/0006-2952(62)90177-6. PMID 14466716.
- ^ Стакпул П.В., Хендерсон Г.Н., Ян З., Джеймс МО (1998). «Клиническая фармакология и токсикология дихлорацетата». Environ. Перспектива здоровья. 106 Дополнение 4: 989–94. Дои:10.1289 / ehp.98106s4989. ЧВК 1533324. PMID 9703483.
- ^ Брак B, Clandinin MT, Glerum DM (2003). «Лечение питательными кофакторами при митохондриальных нарушениях». J Am Diet Assoc. 103 (8): 1029–38. Дои:10.1016 / S0002-8223 (03) 00476-0. PMID 12891154.
- ^ Танака М., Нишигаки Ю., Фуку Н., Иби Т., Сахаши К., Кога Ю. (2007). «Лечебный потенциал терапии пируватом при митохондриальных заболеваниях». Митохондрия. 7 (6): 399–401. Дои:10.1016 / j.mito.2007.07.002. PMID 17881297.
- ^ Франц М.С., Випф П. (июнь 2010 г.). «Митохондрии как мишень в лечении». Энвирон Мол Мутаген. 51 (5): 462–75. Дои:10.1002 / em.20554. ЧВК 2920596. PMID 20175113.
- ^ Ниренберг, Эндрю А., Кански, Кристин, Бреннан, Брайан П., Шелтон, Ричард С., Перлис, Рой, Иосифеску, Дэн В. (2012). «Модуляторы митохондрий для биполярного расстройства: патофизиологически обоснованная парадигма для разработки новых лекарств». Австралийский и новозеландский журнал психиатрии. 47 (1): 26–42. Дои:10.1177/0004867412449303. PMID 22711881.
- ^ Прогресс в генетике вселяет надежды на ЭКО Автор Паллаб Гош. BBC News, научный корреспондент. Последнее обновление страницы: 17:04 GMT, среда, 26 августа 2009 г., 18:04 UK
- ^ Тачибана М., Спарман М., Шританаудомчай Х., Ма Х., Клеппер Л., Вудворд Дж., Ли И, Рэмси К., Колотушкина О., Миталипов С (Сентябрь 2009 г.). «Замена митохондриальных генов в потомстве приматов и эмбриональных стволовых клетках». Природа. 461 (7262): 367–372. Bibcode:2009Натура.461..367Т. Дои:10.1038 / природа08368. ЧВК 2774772. PMID 19710649.
- ^ Бозли, Сара (14 апреля 2010 г.). «Ученые раскрывают технику обмена генами, чтобы предотвратить наследственные заболевания». Хранитель. Лондон.
- ^ Крейвен, Линдси; Tuppen, Helen A .; Greggains, Gareth D .; Harbottle, Стивен Дж .; Мерфи, Джули Л .; Кри, Линси М .; Мердок, Элисон П .; Чиннери, Патрик Ф .; Тейлор, Роберт В .; Lightowlers, Роберт Н .; Герберт, Мэри; Тернбулл, Дуглас М. (2010). «Перенуклеарный перенос в человеческих эмбрионах для предотвращения передачи болезни митохондриальной ДНК». Природа. 465 (7294): 82–85. Bibcode:2010 Натур.465 ... 82C. Дои:10.1038 / природа08958. ЧВК 2875160. PMID 20393463.

- ^ «Великобритания призвала разрешить процедуру ЭКО для предотвращения смертельных генетических заболеваний». Хранитель. Лондон. 2015-04-30.
- ^ «Закон о трех родителях -« безответственный », - заявила Англиканская церковь перед голосованием». Телеграф. Лондон. 2015-04-30.
- ^ Хамзелоу, Джессика (27.09.2016). «Эксклюзив: первый в мире ребенок, родившийся с использованием новой техники« трех родителей »». Новый ученый. Получено 2016-11-26.
- ^ Образец, Ян (2012-09-17). «Регулирующий орган должен проконсультироваться с общественностью по поводу планов новых методов лечения бесплодия». Хранитель. Лондон. Получено 8 октября 2012.
- ^ «Родились генетически измененные младенцы». Новости BBC. 2001-05-04. Получено 2008-04-26.
- ^ Постановление об оплодотворении человека и эмбриологии (донорстве митохондрий) 2015 г. № 572
- ^ «Правительство Великобритании поддерживает ЭКО для трех человек». Новости BBC. 27 июня 2013 г.
- ^ Knapton, Сара (1 марта 2014 г.) В следующем году в Великобритании могут родиться «троие дети» The Daily Telegraph Science News, по состоянию на 1 марта 2014 г.
- ^ Центр митохондриальных и метаболических заболеваний
- ^ Gorman, Gráinne S .; Грейди, Джон П .; Нг, Йи; Шефер, Эндрю М .; МакНелли, Ричард Дж .; Чинери, Патрик Ф .; Ю-Вай-Ман, Патрик; Герберт, Мэри; Тейлор, Роберт В .; Макфарланд, Роберт; Тернбулл, Дуг М. (2015). «Донорство митохондрий - сколько женщин могут получить выгоду?». Медицинский журнал Новой Англии. 372 (9): 885–887. Дои:10.1056 / NEJMc1500960. ISSN 0028-4793. ЧВК 4481295. PMID 25629662.
- ^ Комитет по этической и социальной политике в отношении новых методов профилактики материнской передачи заболеваний митохондриальной ДНК; Совет по политике в области медицинских наук; Институт медицины (2016). Клэйборн, Энн; Англичанин, Ребекка; Кан, Джеффри (ред.). Методы замены митохондрий: этические, социальные и политические соображения. Национальная академия прессы. ISBN 978-0-309-38870-2. Индексная страница со ссылками на резюме, включая листовка с кратким изложением.
внешние ссылки
| Классификация | |
|---|---|
| Внешние ресурсы |
