Воспаление - Inflammation
| Воспаление | |
|---|---|
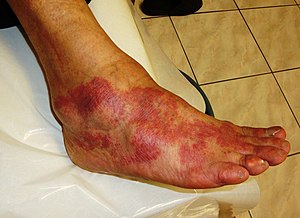 | |
| Основными признаками воспаления являются: боль, жар, покраснение, отек и потеря функции. Некоторые из этих показателей можно увидеть здесь из-за аллергической реакции. | |
| Специальность | Иммунология Ревматология |
| Симптомы | Жар, боль, покраснение, отек |
| Осложнения | Астма, пневмония, аутоиммунные заболевания |
| Продолжительность | острый Несколько дней хронический До многих месяцев или лет |
| Причины | Бактерии, вирус |
Воспаление (из латинский: воспаление ) является частью сложной биологической реакции тканей организма на вредные раздражители, такие как патогены, поврежденные клетки или раздражители,[1] и является защитным ответом, включающим иммунные клетки, кровеносный сосуд, и молекулярные медиаторы. Функция воспаления состоит в том, чтобы устранить первоначальную причину повреждения клеток, очистить некротические клетки и ткани, поврежденные в результате первоначального поражения и воспалительного процесса, и инициировать восстановление тканей.
Пятерка классические признаки воспаления жар, боль, покраснение, отек и Потеря функции (Латинский калорийность, dolor, рубин, опухоль, и functio laesa).[1] Воспаление - это общий ответ, поэтому его рассматривают как механизм врожденный иммунитет, по сравнению с адаптивный иммунитет, специфичную для каждого возбудителя.[2] Слишком слабое воспаление может привести к прогрессирующему разрушению тканей вредным стимулом (например, бактериями) и поставить под угрозу выживание организма. Напротив, хроническое воспаление связано с различными заболеваниями, такими как Сенная лихорадка, парадантоз, атеросклероз, и остеоартроз.
Воспаление можно классифицировать как острый или же хронический. Острое воспаление - это первая реакция организма на вредные раздражители, которая достигается за счет увеличения движения плазма и лейкоциты (особенно гранулоциты ) из крови в поврежденные ткани. Серия биохимических событий способствует развитию воспалительной реакции, включая локальные сосудистая система, то иммунная система, и различные клетки в поврежденной ткани. Длительное воспаление, известное как хроническое воспаление, приводит к прогрессивному изменению типа клеток, присутствующих в очаге воспаления, таких как мононуклеарные клетки, и характеризуется одновременным разрушением и выздоровление ткани от воспалительного процесса.
Воспаление не является синонимом инфекционное заболевание. Инфекция описывает взаимодействие между действием микробной инвазии и реакцией воспалительного ответа организма - эти два компонента рассматриваются вместе при обсуждении инфекции, и это слово используется для обозначения микробной инвазивной причины наблюдаемой воспалительной реакции. Воспаление же, с другой стороны, описывает чисто иммуно-сосудистую реакцию организма, какой бы ни была причина. Но из-за того, как часто эти двое коррелированный, слова, оканчивающиеся на суффикс -это (который относится к воспалению) иногда неформально описывается как относящийся к инфекции. Например, слово уретрит строго означает только «воспаление уретры», но клиническое представители здравоохранения Обычно уретрит обсуждают как инфекцию уретры, потому что микробная инвазия уретры является наиболее частой причиной уретрита.
Полезно различать воспаление и инфекцию, потому что есть типичные ситуации в патология и медицинский диагноз где воспаление не вызвано микробной инвазией - например, атеросклероз, травма, ишемия, и аутоиммунные заболевания включая гиперчувствительность III типа.
Причины
Эта секция нужны дополнительные цитаты для проверка. (Декабрь 2015 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
- Ожоги[3]
- Обморожение
- Физическая травма, тупой или проникающий[4]
- Инородные тела, в том числе занозы, грязь и мусор
- Травма[3]
- Ионизирующего излучения
Биологические:
- Инфекционное заболевание к патогены[3]
- Иммунные реакции из-за гиперчувствительность
- Стресс
Химическая:[3]
- Химическая раздражители
- Токсины
- Алкоголь
Психологические:
- Возбуждение[5]
Типы
|
| Острый | Хронический | |
|---|---|---|
| Возбудитель | Бактериальные возбудители, поврежденные ткани | Стойкое острое воспаление из-за неразлагаемых патогенов, вирусной инфекции, стойких инородных тел или аутоиммунных реакций |
| Основные задействованные клетки | нейтрофилы (в первую очередь), базофилы (воспалительная реакция) и эозинофилы (реакция на гельминтов и паразитов), мононуклеарные клетки (моноциты, макрофаги) | Мононуклеарные клетки (моноциты, макрофаги, лимфоциты, плазматические клетки), фибробласты |
| Первичные посредники | Вазоактивные амины, эйкозаноиды | IFN-γ и другие цитокины, факторы роста, активные формы кислорода, гидролитические ферменты |
| Начало | Немедленный | Отложенный |
| Продолжительность | Несколько дней | До многих месяцев или лет |
| Результаты | Разрешение, образование абсцесса, хроническое воспаление | Разрушение тканей, фиброз, некроз |
Кардинальные знаки
| английский | латинский | |
|---|---|---|
| Покраснение | Рубор * | |
| Припухлость | Опухоль * | |
| Высокая температура | Калорийность * | |
| Боль | Долор * | |
| Потеря функции | Functio laesa ** | |
| Все вышеперечисленные признаки могут наблюдаться в определенных случаях, но, разумеется, не должно быть единого знака.[6] Это изначальные, или «кардинальные признаки» воспаления.[6]* Functio laesa - устаревшее понятие, поскольку оно характерно не только для воспаления и является характеристикой многих болезненных состояний.[7]** | ||

Острое воспаление - это кратковременный процесс, обычно проявляющийся в течение нескольких минут или часов и прекращающийся после устранения повреждающего раздражителя.[8] Он включает в себя скоординированный и системный ответ на локальную мобилизацию различных иммунных, эндокринных и неврологических медиаторов острого воспаления. При нормальном здоровом ответе он активируется, удаляет патоген и начинает процесс восстановления, а затем прекращается.[9] Для него характерно пять основных знаков:[10]
Акроним, который можно использовать для запоминания основных симптомов, - «ПРИШ», обозначающий боль, покраснение, неподвижность (потеря функции), отек и жар.
Традиционные названия признаков воспаления происходят от латинского:
- Долор (боль )
- Калор (высокая температура )
- Рубор (покраснение)
- Опухоль (припухлость )
- Functio laesa (Потеря функции)[11]
Первые четыре (классические признаки) были описаны Цельс (ок. 30 г. до н.э. - 38 г. н.э.),[12] пока Потеря функции вероятно был добавлен позже Гален.[13] Однако добавление этого пятого знака также приписывается Томас Сиденхэм[14] и Вирхов.[8][10]
Покраснение и жар возникают из-за повышенного притока крови к воспаленному участку при внутренней температуре тела; отек вызван скоплением жидкости; боль происходит из-за выделения таких химических веществ, как брадикинин и гистамин, которые стимулируют нервные окончания. Нарушение функции имеет несколько причин.[10]
Острое воспаление легких (обычно возникает в результате пневмония ) не вызывает боли, если воспаление не связано с париетальная плевра, который имеет чувствительные к боли нервные окончания.[10]
Процесс острого воспаления

Процесс острого воспаления инициируется резидентными иммунными клетками, уже присутствующими в пораженной ткани, в основном резидентными. макрофаги, дендритные клетки, гистиоциты, Клетки Купфера и тучные клетки. Эти клетки обладают поверхностными рецепторами, известными как рецепторы распознавания образов (PRR), которые распознают (т. Е. Связывают) два подкласса молекул: патоген-ассоциированные молекулярные паттерны (PAMP) и молекулярные паттерны, связанные с повреждениями (ВЛАЖНОСТЬ). PAMP - это соединения, которые связаны с различными патогены, но которые можно отличить от молекул хозяина. DAMPs представляют собой соединения, которые связаны с повреждением, связанным с хозяином, и повреждением клеток.
В начале инфекции, ожога или других повреждений эти клетки подвергаются активации (одна из PRR распознает PAMP или DAMP) и высвобождают медиаторы воспаления, ответственные за клинические признаки воспаления. Расширение сосудов и, как следствие, усиление кровотока вызывает покраснение (рубин) и повышенный жар (калорийность). Повышенная проницаемость кровеносных сосудов приводит к экссудации (утечке) плазма белки и жидкость в ткани (отек ), что проявляется в виде отека (опухоль). Некоторые из выпущенных посредников, такие как брадикинин повышают чувствительность к боли (гипералгезия, dolor). Молекулы медиатора также изменяют кровеносные сосуды, позволяя миграцию лейкоцитов, в основном нейтрофилы и макрофаги, вне кровеносных сосудов (экстравазация) в ткани. Нейтрофилы мигрируют по хемотаксический градиент, создаваемый местными клетками, чтобы достичь места повреждения.[8] Потеря функции (functio laesa), вероятно, является результатом неврологического рефлекса в ответ на боль.
Помимо медиаторов клеточного происхождения, несколько бесклеточных биохимических каскадных систем, состоящих из предварительно сформированных белков плазмы, действуют параллельно, инициируя и распространяя воспалительный ответ. К ним относятся система комплемента активируется бактериями и коагуляция и системы фибринолиза активирован некроз, например ожог или травма.[8]
Острое воспаление можно рассматривать как первую линию защиты от травм. Острая воспалительная реакция требует постоянной стимуляции. Медиаторы воспаления недолговечны и быстро разрушаются в тканях. Следовательно, острое воспаление начинает прекращаться после устранения раздражителя.[8]
Сосудистый компонент
Расширение сосудов и повышение проницаемости
Согласно определению, острое воспаление представляет собой иммунно-сосудистый ответ на воспалительный стимул. Это означает, что острое воспаление можно в общих чертах разделить на сосудистую фазу, которая возникает первой, за которой следует клеточная фаза с участием иммунных клеток (точнее, миелоидных клеток). гранулоциты в острой постановке). Сосудистый компонент острого воспаления включает движение плазменная жидкость, содержащий важные белки Такие как фибрин и иммуноглобулины (антитела ), в воспаленную ткань.
При контакте с PAMP, ткани макрофаги и мастоциты высвобождают вазоактивные амины, такие как гистамин и серотонин, а также эйкозаноиды Такие как простагландин E2 и лейкотриен B4 реконструировать местную сосудистую сеть. Высвобождение макрофагов и эндотелиальных клеток оксид азота. Эти медиаторы расширяют сосуды и проницаемость кровеносный сосуд, что приводит к чистому распределению плазма крови из сосуда в тканевое пространство. Увеличенное скопление жидкости в ткани вызывает ее набухание (отек ). Эта выделяемая тканевая жидкость содержит различные антимикробные медиаторы из плазмы, такие как дополнять, лизоцим, антитела, который может немедленно нанести вред микробам и опсонизировать микробы при подготовке к клеточной фазе. Если воспалительный раздражитель представляет собой рваную рану, выделяющуюся тромбоциты, коагулянты, плазмин и кинины может сгусток раненый участок и предоставить гемостаз в первую очередь. Эти медиаторы свертывания также обеспечивают структурную основу для определения стадии в участке воспалительной ткани в виде фибрин решетка - как и конструкция строительные леса на строительной площадке - с целью облегчения очистки фагоцитов и заживление ран позже. Некоторая часть выделяемой тканевой жидкости также выводится через лимфатические сосуды в регионарные лимфатические узлы, вымывая бактерии, чтобы начать фазу распознавания и атаки адаптивная иммунная система.
Острое воспаление характеризуется выраженными изменениями сосудов, в том числе: расширение сосудов, повышенная проницаемость и усиление кровотока, которые вызваны действием различных медиаторов воспаления. Вазодилатация возникает сначала в артериола уровень, переходя на капилляр уровень и вызывает чистое увеличение количества крови, вызывая покраснение и жар воспаления. Повышенная проницаемость сосудов приводит к движению плазма в ткани, в результате чего застой из-за увеличения концентрации клеток в крови - состояние, характеризующееся увеличенными сосудами, заполненными клетками. Стазис позволяет лейкоциты выделить (переместить) вдоль эндотелий, процесс, критически важный для их набора в ткани. Нормальное течение крови препятствует этому, так как сила сдвига по периферии сосудов перемещает клетки крови в середину сосуда.
Плазменные каскадные системы
- В система комплемента при активации создает каскад химических реакций, который способствует опсонизация, хемотаксис, и агглютинация, и производит MAC.
- В кининовая система вырабатывает белки, способные поддерживать расширение сосудов и другие физические воспалительные эффекты.
- В система коагуляции или же каскад свертывания, который образует защитную протеиновую сетку над участками травм
- В система фибринолиза, который действует в противовес система коагуляции, чтобы уравновесить свертывание крови и выработать несколько других медиаторов воспаления.
Медиаторы, полученные из плазмы
* неполный список
| Имя | Произведено | Описание |
|---|---|---|
| Брадикинин | Кининовая система | Вазоактивный белок, способный вызывать вазодилатацию, увеличивать проницаемость сосудов, вызывать сокращение гладких мышц и вызывать боль. |
| C3 | Система комплемента | Раскалывает производить C3a и C3b. C3a стимулирует высвобождение гистамина тучными клетками, тем самым вызывая расширение сосудов. C3b способен связываться со стенками бактериальных клеток и действовать как опсонин, который отмечает захватчика как цель для фагоцитоз. |
| C5a | Система комплемента | Стимулирует высвобождение гистамина тучными клетками, вызывая расширение сосудов. Он также может действовать как хемоаттрактант направлять клетки через хемотаксис к месту воспаления. |
| Фактор XII (Фактор Хагемана) | Печень | Белок, который неактивно циркулирует, пока не будет активирован коллагеном, тромбоцитами или подвергнутся воздействию подвальные мембраны через конформационное изменение. При активации он, в свою очередь, способен активировать три плазменные системы, участвующие в воспалении: систему кининов, систему фибринолиза и систему свертывания крови. |
| Комплекс мембранной атаки | Система комплемента | Комплекс белков комплемента C5b, C6, C7, C8, и несколько единиц C9. Комбинация и активация этого диапазона белков комплемента формируют комплекс мембранной атаки, который способен внедряться в стенки бактериальных клеток и вызывать лизис клеток с последующей гибелью бактерий. |
| Плазмин | Система фибринолиза | Способен разрушать фибриновые сгустки, расщеплять белок комплемента C3 и активировать фактор XII. |
| Тромбин | Система коагуляции | Расщепляет растворимый белок плазмы фибриноген производить нерастворимый фибрин, который объединяется с образованием тромб. Тромбин также может связываться с клетками через PAR1 рецептора, чтобы вызвать несколько других воспалительных реакций, таких как производство хемокины и оксид азота. |
Сотовый компонент
В клеточный компонент вовлекает лейкоциты, которые обычно находятся в крови и должны попасть в воспаленные ткани через экстравазация чтобы помочь при воспалении. Некоторые действуют как фагоциты, глотание бактерии, вирусы и клеточный мусор. Другие выделяют ферментативные гранулы которые повреждают патогенных захватчиков. Лейкоциты также выделяют медиаторы воспаления, которые развивают и поддерживают воспалительный ответ. Как правило, острое воспаление опосредуется: гранулоциты, тогда как хроническое воспаление опосредуется мононуклеарными клетками, такими как моноциты и лимфоциты.
Лейкоцитарная экстравазация

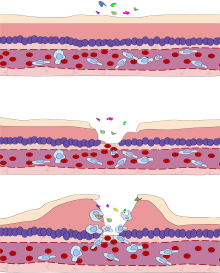
Разные лейкоциты, особенно нейтрофилы, критически вовлечены в инициирование и поддержание воспаления. Эти клетки должны иметь возможность перемещаться к месту повреждения из своего обычного местоположения в крови, поэтому существуют механизмы для набора и направления лейкоцитов в соответствующее место. Процесс перемещения лейкоцитов из крови в ткани по кровеносным сосудам известен как экстравазация, и в общих чертах его можно разделить на несколько этапов:
- Маргинализация лейкоцитов и адгезия эндотелия: Лейкоциты внутри сосудов, которые обычно расположены в центре, перемещаются по периферии к стенкам сосудов.[15] Активированные макрофаги в ткани высвобождают цитокины Такие как Ил-1 и TNFα, что, в свою очередь, приводит к производству хемокины это привязано к протеогликаны образуя градиент в воспаленной ткани и вдоль эндотелиальный стена. Воспалительные цитокины вызывают немедленную экспрессию Р-селектин на поверхности эндотелиальных клеток и Р-селектин слабо связывается с углеводными лигандами на поверхности лейкоцитов и заставляет их «катиться» по эндотелиальной поверхности по мере образования и разрыва связей. Цитокины, высвобождаемые из поврежденных клеток, вызывают экспрессию E-selectin на эндотелиальных клетках, который действует аналогично Р-селектину. Цитокины также вызывают экспрессию интегрин лиганды, такие как ICAM-1 и VCAM-1 на эндотелиальных клетках, которые опосредуют адгезию и еще больше замедляют лейкоциты. Эти слабо связанные лейкоциты могут отделяться, если не активируются хемокинами, продуцируемыми в поврежденной ткани после преобразование сигнала через соответствующие G-белковые рецепторы который активирует интегрины на поверхности лейкоцитов для прочной адгезии. Такая активация увеличивает сродство связанных рецепторов интегрина к ICAM-1 и VCAM-1 на поверхности эндотелиальных клеток, прочно связывая лейкоциты с эндотелием.
- Миграция через эндотелий, известная как переселение через процесс диапедез: Градиенты хемокинов стимулируют прилипшие лейкоциты перемещаться между соседними эндотелиальными клетками. Эндотелиальные клетки втягиваются, и лейкоциты проходят через базальную мембрану в окружающие ткани с помощью молекул адгезии, таких как ICAM-1.[15]
- Перемещение лейкоцитов в ткани через хемотаксис: Лейкоциты, достигающие интерстиция ткани, связываются с внеклеточный матрикс белки через экспрессируемые интегрины и CD44 чтобы они не покинули сайт. Различные молекулы ведут себя как хемоаттрактанты, например, C3a или C5, и заставляют лейкоциты двигаться по хемотаксическому градиенту к источнику воспаления.
Фагоцитоз
Экстравазированные нейтрофилы в клеточной фазе вступают в контакт с микробами в воспаленной ткани. Фагоциты экспрессировать эндоцитоз клеточной поверхности рецепторы распознавания образов (PRR), которые обладают сродством и эффективностью против неспецифических молекулярные структуры, связанные с микробами (PAMP). Большинство PAMP, которые связываются с PRR эндоцитов и инициируют фагоцитоз являются компонентами клеточной стенки, включая сложные углеводы, такие как маннаны и β-глюканы, липополисахариды (LPS), пептидогликаны, и поверхностные белки. Эндоцитарные PRR на фагоцитах отражают эти молекулярные паттерны с Лектин С-типа рецепторы, связывающиеся с маннанами и β-глюканами, и рецепторы мусорщика привязка к LPS.
После связывания эндоцитарной PRR, актин -миозин цитоскелет перестройка рядом с плазматической мембраной происходит таким образом, что эндоцитозирует плазматическую мембрану, содержащую комплекс PRR-PAMP, и микроб. Фосфатидилинозитол и Vps34 -Vps15 -Beclin1 сигнальные пути участвуют в перемещении эндоцитированной фагосомы во внутриклеточные лизосомы, где слияние фагосомы и лизосомы дает фаголизосому. В активные формы кислорода, супероксиды и гипохлорит отбеливатель внутри фаголизосом убивает микробы внутри фагоцита.
Фагоцитарную эффективность можно повысить за счет опсонизация. Комплемент, полученный из плазмы C3b и антитела, которые выделяются в воспаленную ткань во время сосудистой фазы, связываются с микробными антигенами и покрывают их. Помимо эндоцитарных PRR, фагоциты также экспрессируют опсонин рецепторы Рецептор Fc и рецептор комплемента 1 (CR1), которые связываются с антителами и C3b соответственно. Костимуляция эндоцитарного PRR и рецептора опсонина увеличивает эффективность фагоцитарного процесса, усиливая лизосомный устранение возбудителя инфекции.
Медиаторы клеточного происхождения
* неполный список
| Имя | Тип | Источник | Описание |
|---|---|---|---|
| Гранулы лизосом | Ферменты | Гранулоциты | Эти клетки содержат большое количество разнообразных ферментов, которые выполняют ряд функций. Гранулы можно разделить на специфический или же азурофильный в зависимости от содержимого и способны расщеплять ряд веществ, некоторые из которых могут быть белками плазмы, которые позволяют этим ферментам действовать как медиаторы воспаления. |
| Гистамин | Моноамин | Тучные клетки и базофилы | Хранящийся в предварительно сформированных гранулах, гистамин высвобождается в ответ на ряд стимулов. Это вызывает артериола расширение, увеличенное венозный проницаемость и широкий спектр органо-специфических эффектов. |
| IFN-γ | Цитокин | Т-клетки, NK-клетки | Противовирусные, иммунорегуляторные и противоопухолевые свойства. Этот интерферон первоначально назывался фактором, активирующим макрофаги, и особенно важен для поддержания хронического воспаления. |
| Ил-8 | Хемокин | В первую очередь макрофаги | Активация и хемоаттракция нейтрофилов со слабым действием на моноциты и эозинофилы. |
| Лейкотриен B4 | Эйкозаноид | Лейкоциты, раковые клетки | Способен опосредовать адгезию и активацию лейкоцитов, позволяя им связываться с эндотелием и перемещаться по нему. В нейтрофилах он также является мощным хемоаттрактантом и способен индуцировать образование активных форм кислорода и высвобождение лизосомальных ферментов этими клетками. |
| LTC4, LTD4 | Эйкозаноид | эозинофилы, тучные клетки, макрофаги | Эти три Цистеин -содержащие лейкотриены сокращают дыхательные пути легких, увеличивают проницаемость микрососудов, стимулируют секрецию слизи и способствуют воспалению на основе эозинофилов в легких, коже, носу, глазах и других тканях. |
| 5-оксо-эйкозатетраеновая кислота | Эйкозаноид | лейкоциты, раковые клетки | Мощный стимулятор хемотаксиса нейтрофилов, высвобождения лизосомных ферментов и образования активных форм кислорода; хемотаксис моноцитов; и с еще большей эффективностью хемотаксиса эозинофилов, высвобождения лизосомных ферментов и образования активных форм кислорода. |
| 5-HETE | Эйкозаноид | Лейкоциты | Метаболический предшественник 5-оксо-эйкозатетраеновой кислоты, он является менее мощным стимулятором хемотаксиса нейтрофилов, высвобождения лизосомных ферментов и образования активных форм кислорода; хемотаксис моноцитов; и хемотаксис эозинофилов, высвобождение лизосомных ферментов и образование активных форм кислорода. |
| Простагландины | Эйкозаноид | Тучные клетки | Группа липидов, вызывающих вазодилатацию, жар и боль. |
| Оксид азота | Растворимый газ | Макрофаги, эндотелиальные клетки, некоторые нейроны | Сильное вазодилататорное средство, расслабляет гладкие мышцы, снижает агрегацию тромбоцитов, способствует привлечению лейкоцитов, прямое противомикробное действие в высоких концентрациях. |
| TNF-α и Ил-1 | Цитокины | В первую очередь макрофаги | Оба влияют на широкий спектр клеток, вызывая множество схожих воспалительных реакций: лихорадку, выработку цитокинов, регуляцию эндотелиальных генов, хемотаксис, прикрепление лейкоцитов, активацию фибробласты. Отвечает за системные эффекты воспаления, такие как потеря аппетита и учащение пульса. TNF-α подавляет дифференцировку остеобластов. |
| Триптаза | Ферменты | Тучные клетки | Считается, что эта сериновая протеаза накапливается исключительно в тучных клетках и секретируется вместе с гистамином во время активации тучных клеток.[16][17][18] |
Морфологические закономерности
Конкретные модели острого и хронического воспаления наблюдаются в определенных ситуациях, возникающих в организме, например, когда воспаление возникает на эпителиальный поверхность, или пиогенный участвуют бактерии.
- Гранулематозное воспаление: Характеризуется образованием гранулемы, они являются результатом ограниченного, но разнообразного числа заболеваний, в том числе туберкулез, проказа, саркоидоз, и сифилис.
- Фибринозное воспаление: Воспаление, приводящее к значительному увеличению проницаемости сосудов, позволяет фибрин проходить по кровеносным сосудам. Если соответствующий прокоагуляционный стимул присутствует, например, раковые клетки,[8] откладывается фибринозный экссудат. Это обычно наблюдается в серозные полости, где между серозными оболочками может происходить превращение фибринозного экссудата в рубец, ограничивая их функцию. Отложение иногда образует псевдомембранный лист. При воспалении кишечника (Псевдомембранозный колит ) могут образовываться псевдомембранозные трубки.
- Гнойное воспаление: Воспаление, приводящее к большому количеству гной, который состоит из нейтрофилов, мертвых клеток и жидкости. Заражение гноеродными бактериями, такими как стафилококки характерно для этого вида воспаления. Большие локализованные скопления гноя в окружающих тканях называются абсцессы.
- Серозное воспаление: Характеризуется обильным излитием невязкой серозной жидкости, обычно производимой мезотелиальный ячейки серозные оболочки, но может происходить из плазмы крови. Кожа волдыри иллюстрируют этот образец воспаления.
- Язвенное воспаление: Воспаление, возникающее возле эпителия, может привести к некротический выпадение ткани с поверхности, обнажая нижние слои. Последующие выемки в эпителии известны как язва.
Воспалительные расстройства


Воспалительные аномалии - это большая группа расстройств, лежащих в основе множества заболеваний человека. Иммунная система часто связана с воспалительными заболеваниями, что проявляется как в аллергические реакции и немного миопатии, со многими нарушения иммунной системы что приводит к аномальному воспалению. Неиммунные заболевания, причиной которых являются воспалительные процессы, включают рак, атеросклероз, и ишемическая болезнь сердца.[8]
Примеры заболеваний, связанных с воспалением, включают:
- Юношеские угри
- Астма
- Аутоиммунные заболевания
- Аутовоспалительные заболевания
- Глютеновая болезнь
- Хронический простатит
- Колит
- Дивертикулит
- Семейная средиземноморская лихорадка
- Гломерулонефрит
- Гнойный гидраденит
- Гиперчувствительность
- Воспалительные заболевания кишечника
- Интерстициальный цистит
- Красный плоский лишай
- Синдром активации тучных клеток
- Мастоцитоз
- Отит
- Воспалительные заболевания органов малого таза
- пневмония
- Реперфузионная травма
- Ревматическая лихорадка
- Ревматоидный артрит
- Ринит
- Саркоидоз
- Отторжение трансплантата
- Васкулит
Атеросклероз
Атеросклероз, ранее считавшийся легкой болезнью накопления липидов, на самом деле связан с продолжающейся воспалительной реакцией. Недавние достижения фундаментальной науки установили фундаментальную роль воспаления в опосредовании всех стадий этого заболевания от начала до прогрессирования и, в конечном итоге, тромботических осложнений атеросклероза. Эти новые данные обеспечивают важную связь между факторами риска и механизмами атерогенеза. Клинические исследования показали, что эта новая биология воспаления при атеросклерозе применима непосредственно к пациентам-людям. Повышение маркеров воспаления позволяет прогнозировать исходы пациентов с острыми коронарными синдромами, независимо от повреждения миокарда. Кроме того, хроническое воспаление слабой степени, на что указывает уровень воспалительного маркера. С-реактивный белок, проспективно определяет риск атеросклеротических осложнений, тем самым дополняя прогностическую информацию, предоставляемую традиционными факторами риска. Более того, некоторые виды лечения, снижающие риск коронарных заболеваний, также ограничивают воспаление. В случае снижения уровня липидов статинами этот противовоспалительный эффект, по-видимому, не коррелирует со снижением уровня липопротеинов низкой плотности. Эти новые взгляды на воспаление при атеросклерозе не только расширяют наши представления об этом заболевании, но также имеют практическое клиническое применение для стратификации риска и выбора терапии этого бедствия, значение которого растет во всем мире.[19]
Аллергия
Аллергическая реакция, официально известная как гиперчувствительность 1 типа, является результатом несоответствующего иммунного ответа, вызывающего воспаление, расширение сосудов и раздражение нервов. Типичный пример: Сенная лихорадка, что вызвано гиперчувствительной реакцией на тучные клетки к аллергены. Предварительно сенсибилизированные тучные клетки отвечают дегранулирующий, выпуская вазоактивный химические вещества, такие как гистамин. Эти химические вещества вызывают чрезмерную воспалительную реакцию, характеризующуюся расширением кровеносных сосудов, образованием провоспалительных молекул, высвобождением цитокинов и привлечением лейкоцитов.[8] Тяжелая воспалительная реакция может перерасти в системную реакцию, известную как анафилаксия.
Миопатии
Воспалительные миопатии вызваны тем, что иммунная система неправильно атакует компоненты мышц, что приводит к появлению признаков воспаления мышц. Они могут возникать в сочетании с другими иммунными нарушениями, такими как системный склероз, и включать дерматомиозит, полимиозит, и миозит с тельцами включения.[8]
Дефекты лейкоцитов
Из-за центральной роли лейкоцитов в развитии и распространении воспаления дефекты функциональности лейкоцитов часто приводят к снижению способности к воспалительной защите с последующей уязвимостью к инфекции.[8] Дисфункциональные лейкоциты могут быть неспособны правильно связываться с кровеносными сосудами из-за мутаций поверхностных рецепторов, переваривать бактерии (Синдром Чедиака – Хигаши ) или произвести микробициды (хроническая гранулематозная болезнь ). Кроме того, заболевания, влияющие на Костный мозг может привести к аномальному образованию лейкоцитов или их небольшому количеству.
Фармакологический
Известно, что некоторые лекарства или экзогенные химические соединения влияют на воспаление. Витамин А дефицит вызывает усиление воспалительных реакций,[20] и противовоспалительное средство лекарства работают специально, ингибируя ферменты, которые производят воспалительные эйкозаноиды. Некоторые запрещенные наркотики, такие как кокаин и экстази, могут оказывать некоторые пагубные эффекты, активируя факторы транскрипции, непосредственно связанные с воспалением (например, NF-κB ).[21][22]
Рак
Воспаление управляет микросредой вокруг опухолей, способствуя их распространению, выживанию и миграции.[23] Раковые клетки используют селектины, хемокины и их рецепторы для инвазии, миграции и метастазирования.[24] С другой стороны, многие клетки иммунной системы способствуют иммунология рака, подавляя рак.[25]Молекулярное пересечение рецепторов стероидных гормонов, которые оказывают важное влияние на развитие клеток, и факторов транскрипции, которые играют ключевую роль в воспалении, таких как NF-κB, может опосредовать некоторые из наиболее важных эффектов воспалительных стимулов на раковые клетки.[26] Эта способность медиатора воспаления влиять на действие стероидных гормонов в клетках с большой вероятностью влияет на канцерогенез, с одной стороны; с другой стороны, из-за модульной природы многих рецепторов стероидных гормонов это взаимодействие может предлагать способы препятствовать прогрессированию рака путем нацеливания на определенный белковый домен в конкретном типе клеток. Такой подход может ограничить побочные эффекты, не связанные с интересующей опухолью, и может помочь сохранить жизненно важные гомеостатические функции и процессы развития в организме.
Согласно обзору 2009 года, последние данные показывают, что воспаление, связанное с раком (CRI), может приводить к накоплению случайных генетических изменений в раковых клетках.[27]
Роль в раке
В 1863 году Рудольф Вирхов выдвинул гипотезу о том, что рак берет начало в местах хронического воспаления.[28][29] В настоящее время, по оценкам, хроническое воспаление является причиной примерно от 15% до 25% случаев рака у человека.[29][30]
Медиаторы и повреждение ДНК при раке
Медиатор воспаления - это посредник, который действует на кровеносные сосуды и / или клетки, способствуя воспалительной реакции.[31] Медиаторы воспаления, которые способствуют неоплазии, включают: простагландины, воспалительный цитокины Такие как ИЛ-1β, TNF-α, Ил-6 и Ил-15 и хемокины Такие как Ил-8 и GRO-альфа.[32][29] Эти медиаторы воспаления и другие организуют среду, которая способствует распространению и выживанию.[28][32]
Воспаление также вызывает повреждение ДНК из-за индукции активные формы кислорода (ROS) различными внутриклеточными медиаторами воспаления.[28][32][29] Кроме того, лейкоциты и другие фагоцитарные клетки привлеченные к месту воспаления, вызывают повреждения ДНК в пролиферирующих клетках за счет генерации ими АФК и активные формы азота (RNS). Эти клетки обычно вырабатывают АФК и РНС для борьбы с инфекцией.[28] Только АФК вызывают более 20 типов повреждений ДНК.[33] Окислительные повреждения ДНК вызывают оба мутации[34] и эпигенетические изменения.[35][29][36] РНС также вызывают мутагенные повреждения ДНК.[37]
Нормальная клетка может подвергнуться канцерогенез стать раковой клеткой, если она часто подвергается повреждению ДНК в течение длительных периодов хронического воспаления. Повреждения ДНК могут вызывать генетические мутации из-за неаккуратный ремонт. Кроме того, ошибки в процессе восстановления ДНК могут вызвать эпигенетический переделки.[29][32][36] Мутации и эпигенетические изменения, которые реплицируются и обеспечивают селективное преимущество во время пролиферации соматических клеток, могут быть канцерогенными.
Полногеномный анализ раковых тканей человека показывает, что одна типичная раковая клетка может обладать примерно 100 мутациями в кодирующие области, 10-20 из которых "Драйверные мутации" которые способствуют развитию рака.[29] Однако хроническое воспаление также вызывает эпигенетические изменения, такие как: Метилирование ДНК, которые часто встречаются чаще, чем мутации. Обычно в раковой клетке метилируются от нескольких сотен до тысяч генов (см. Метилирование ДНК при раке ). Сайты окислительного повреждения в хроматин может набирать комплексы, содержащие ДНК-метилтрансферазы (DNMT), гистондеацетилаза (SIRT1 ), а гистон-метилтрансфераза (EZH2), и, таким образом, вызывают метилирование ДНК.[29][38][39] Метилирование ДНК Остров CpG в промоутер регион может вызвать молчание его нижнего гена (см. CpG сайт и регуляция транскрипции при раке ). В частности, гены репарации ДНК часто инактивируются метилированием при различных формах рака (см. гиперметилирование генов репарации ДНК при раке ). Отчет за 2018 год[40] оценили относительную важность мутаций и эпигенетических изменений в прогрессировании двух различных типов рака. Этот отчет показал, что эпигенетические изменения были гораздо важнее мутаций в возникновении рака желудка (связанного с воспалением).[41] Однако мутации и эпигенетические изменения имели примерно равное значение в возникновении плоскоклеточного рака пищевода (связанного с табачные химикаты и ацетальдегид, продукт метаболизма алкоголя).
ВИЧ и СПИД
Давно признано, что инфекция ВИЧ характеризуется не только развитием глубокого иммунодефицита, но также стойким воспалением и активацией иммунной системы.[42][43][44] Значительный объем доказательств указывает на то, что хроническое воспаление является важным фактором иммунной дисфункции, преждевременного появления заболеваний, связанных со старением, и иммунной недостаточности.[42][45] Многие теперь рассматривают ВИЧ-инфекцию не только как развивающийся вирусный иммунодефицит, но и как хроническое воспалительное заболевание.[46] Даже после введения эффективная антиретровирусная терапия (АРТ) и эффективное подавление вирусемии у ВИЧ-инфицированных, хроническое воспаление сохраняется. Исследования на животных также подтверждают связь между активацией иммунной системы и прогрессирующим клеточным иммунодефицитом: SIV sm заражение его естественных нечеловеческих приматов-хозяев, закопченный мангабей, вызывает репликацию вируса на высоком уровне, но с ограниченными признаками заболевания.[47][48] Это отсутствие патогенности сопровождается отсутствием воспаления, иммунной активации и клеточной пролиферации. В резком контрасте экспериментальные SIV sm инфекция макака резус вызывает активацию иммунной системы и заболевание, подобное СПИДу, во многих отношениях с ВИЧ-инфекцией человека.[49]
Определение того, как истощаются Т-лимфоциты CD4 и как индуцируются хроническое воспаление и активация иммунной системы, лежит в основе понимания патогенеза ВИЧ - одного из главных приоритетов исследований в области ВИЧ, проводимых Управлением исследований СПИДа, Национальные институты здоровья. Недавние исследования показали, что каспаза-1 -опосредованный пироптоз, высоко воспалительная форма запрограммированной гибели клеток, вызывает истощение CD4-лимфоцитов и воспаление, вызванное ВИЧ.[50][51][52] Это два характерных события, которые способствуют прогрессированию ВИЧ-инфекции. СПИД. Пироптоз, по-видимому, создает патогенный порочный круг, в котором умирающие CD4 T-клетки и другие иммунные клетки (включая макрофаги и нейтрофилы) испускают воспалительные сигналы, которые привлекают больше клеток в инфицированные лимфоидные ткани, чтобы умереть. Прямой характер этого воспалительного ответа вызывает хроническое воспаление и повреждение тканей.[53] Выявление пироптоза как преобладающего механизма, вызывающего истощение CD4 Т-клеток и хроническое воспаление, открывает новые терапевтические возможности, а именно каспазу-1, которая контролирует путь пироптоза. В связи с этим наблюдается пироптоз CD4 Т-клеток и секреция провоспалительных цитокинов, таких как ИЛ-1β и Ил-18 может блокироваться в лимфоидных тканях ВИЧ-инфицированного человека добавлением ингибитора каспазы-1 VX-765,[50] который уже доказал свою безопасность и хорошую переносимость в клинических испытаниях фазы II на людях.[54] Эти открытия могут способствовать разработке совершенно нового класса «противоспидных» методов лечения, которые воздействуют на хозяина, а не на вирус. Такие агенты почти наверняка будут использоваться в сочетании с АРТ. Способствуя «толерантности» к вирусу вместо подавления его репликации, VX-765 или родственные ему препараты могут имитировать эволюционные решения, возникающие у нескольких обезьян-хозяев (например, сажистый мангабей), инфицированных видоспецифичными лентивирусами, которые привели к отсутствию заболевания. , нет снижения количества CD4 Т-лимфоцитов и хронического воспаления.
Разрешение воспаления
Воспалительный ответ должен быть активно прекращен, когда он больше не нужен, чтобы предотвратить ненужное повреждение тканей "сторонним наблюдателем".[8] Несоблюдение этого правила приводит к хроническому воспалению и разрушению клеток. Разрешение воспаления происходит с помощью различных механизмов в разных тканях. Механизмы, которые служат для прекращения воспаления, включают:[8][55]
- короткий период полураспада из медиаторы воспаления in vivo.
- Производство и выпуск трансформирующий фактор роста (TGF) бета из макрофаги[56][57][58]
- Производство и выпуск интерлейкин 10 (Ил-10)[59]
- Производство противовоспалительных специализированные прорешающие посредники, т.е. липоксины, резолвины, марезины, и нейропротектины[60][61]
- Подавление провоспалительных молекул, таких как лейкотриены.
- Повышение активности противовоспалительных молекул, таких как антагонист рецептора интерлейкина 1 или растворимый рецептор фактора некроза опухоли (TNFR)
- Апоптоз провоспалительных клеток[62]
- Десенсибилизация рецепторов.
- Повышенная выживаемость клеток в очагах воспаления за счет их взаимодействия с внеклеточный матрикс (ECM)[63][64]
- Подавление активности рецепторов высокими концентрациями лиганды
- Расщепление хемокины к матричные металлопротеиназы (MMP) могут приводить к выработке противовоспалительных факторов.[65]
Острое воспаление обычно проходит с помощью механизмов, которые до сих пор остаются неуловимыми. Новые данные свидетельствуют о том, что активная скоординированная программа выздоровления начинается в первые несколько часов после начала воспалительной реакции. После попадания в ткани, гранулоциты способствовать переключению арахидоновая кислота -полученный простагландины и лейкотриены к липоксинам, которые инициируют последовательность терминации. Нейтрофил вербовка, таким образом, прекращается, и смерть программируется апоптоз задействован. Эти события совпадают с биосинтезом, от омега-3 полиненасыщенные жирные кислоты, из резолвины и протектины, которые существенно сокращают период инфильтрации нейтрофилов, инициируя апоптоз. Как следствие, апоптотические нейтрофилы подвергаются фагоцитоз к макрофаги, что приводит к клиренсу нейтрофилов и высвобождению противовоспалительных и репаративных цитокины такие как трансформирующий фактор роста-β1. Противовоспалительная программа заканчивается уходом макрофагов через лимфатические сосуды.[66]
— Чарльз Серхан
Связь с депрессией
Есть доказательства связи между воспалением и депрессия.[67] Воспалительные процессы могут быть вызваны негативными познаниями или их последствиями, такими как стресс, насилие или депривация. Таким образом, негативные когниции могут вызвать воспаление, которое, в свою очередь, может привести к депрессии.[68][69][сомнительный ]Кроме того, появляется все больше доказательств того, что воспаление может вызывать депрессию из-за увеличения цитокинов, переводя мозг в «режим болезни».[70] Классические симптомы физического недомогания, такие как летаргия, во многом совпадают с поведением, характеризующим депрессию. Уровни цитокинов имеют тенденцию резко повышаться во время депрессивных эпизодов у людей с биполярным расстройством и падают во время ремиссии.[71] Кроме того, в клинических испытаниях было показано, что противовоспалительные препараты, принимаемые в дополнение к антидепрессантам, не только значительно улучшают симптомы, но и увеличивают долю субъектов, положительно реагирующих на лечение.[72]Воспаления, приводящие к серьезной депрессии, могут быть вызваны обычными инфекциями, например, вирусами, бактериями или даже паразитами.[73]
Системные эффекты
An инфекционный организм может выйти за пределы непосредственной ткани через сердечно-сосудистая система или же лимфатическая система, где он может распространиться на другие части тела. Если организм не сдерживается действием острого воспаления, он может получить доступ к лимфатической системе через близлежащие лимфатические сосуды. Инфекция лимфатических сосудов известна как лимфангит, а инфекция лимфатического узла известна как лимфаденит. Когда лимфатические узлы не могут уничтожить все патогены, инфекция распространяется дальше. Патоген может получить доступ к кровотоку через лимфатический дренаж в систему кровообращения.
Когда воспаление охватывает хозяина, синдром системной воспалительной реакции поставлен диагноз. Когда это связано с инфекционное заболевание, период, термин сепсис применяется, с условиями бактериемия применяется специально для бактериального сепсиса и виремия конкретно на вирусный сепсис. Расширение сосудов и дисфункция органов - серьезные проблемы, связанные с широко распространенной инфекцией, которая может привести к септический шок и смерть.
Белки острой фазы
Воспаление также вызывает высокие системные уровни белки острой фазы. Эти белки полезны при остром воспалении; однако при хроническом воспалении они могут способствовать амилоидоз.[8] Эти белки включают С-реактивный белок, сывороточный амилоид А, и амилоид P сыворотки, которые вызывают ряд системных эффектов, включая:[8]
Число лейкоцитов
Воспаление часто влияет на количество лейкоцитов, присутствующих в организме:
- Лейкоцитоз часто наблюдается при воспалении, вызванном инфекцией, что приводит к значительному увеличению количества лейкоцитов в крови, особенно незрелых клеток. Количество лейкоцитов обычно увеличивается до 15 000–20 000 клеток на микролитр, но в крайних случаях может достигать 100 000 клеток на микролитр.[8] Бактериальная инфекция обычно приводит к увеличению нейтрофилы, создавая нейтрофилия, тогда как такие болезни, как астма, Сенная лихорадка, а заражение паразитами приводит к увеличению эозинофилы, создавая эозинофилия.[8]
- Лейкопения могут быть вызваны определенными инфекциями и заболеваниями, включая вирусную инфекцию, Риккетсия инфекция, некоторые простейшие, туберкулез, и немного раки.[8]
Системное воспаление и ожирение
С открытием интерлейкины (IL), концепция системное воспаление развитый. Хотя вовлеченные процессы идентичны воспалению ткани, системное воспаление не ограничивается конкретной тканью, а включает эндотелий и другие системы органов.
Хроническое воспаление широко наблюдается в ожирение.[74][75] У людей с ожирением обычно наблюдается повышенный уровень маркеров воспаления, в том числе:[76][77]
Хроническое воспаление слабой степени характеризуется двух-трехкратным увеличением системных концентраций цитокинов, таких как TNF-α, IL-6 и CRP.[80] Окружность талии значительно коррелирует с системной воспалительной реакцией.[81]
Утрата белая жировая ткань снижает уровень маркеров воспаления.[74] Связь системного воспаления с резистентность к инсулину и диабет 2 типа, и с атеросклероз находится в стадии предварительного исследования, хотя клинические испытания не проводилось, чтобы подтвердить такие отношения.[82]
С-реактивный белок (CRP) вырабатывается на более высоком уровне у людей с ожирением и может увеличить риск сердечно-сосудистые заболевания.[83]
Результаты
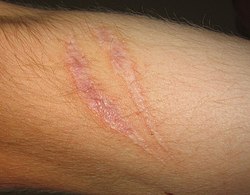
Результат в конкретных обстоятельствах будет определяться тканью, в которой произошло повреждение, и повреждающим агентом, который его вызывает. Вот возможные последствия воспаления:[8]
- Разрешение
Полное восстановление воспаленных тканей до нормального состояния. Воспалительные меры, такие как расширение сосудов, химическое производство и инфильтрация лейкоцитов, прекращаются и повреждаются паренхиматозный клетки регенерируют. В ситуациях, когда возникло ограниченное или непродолжительное воспаление, это обычно является результатом. - Фиброз
Разрушение тканей в больших количествах или повреждение тканей, неспособных к регенерации, не может быть полностью восстановлено организмом. Волокнистый рубцевание возникает в этих областях повреждения, образуя рубец, состоящий в основном из коллаген. Шрам не будет содержать никаких специализированных структур, таких как паренхиматозный клетки, следовательно, могут возникнуть функциональные нарушения. - Образование абсцесса
Образуется полость, содержащая гной, непрозрачную жидкость, содержащую мертвые белые кровяные тельца и бактерии, а также остатки разрушенных клеток. - Хроническое воспаление
При остром воспалении, если повреждающий агент сохраняется, возникает хроническое воспаление. Этот процесс, характеризующийся воспалением, продолжающимся много дней, месяцев или даже лет, может привести к образованию хроническая рана. Хроническое воспаление характеризуется преобладающим присутствием макрофагов в поврежденной ткани. Эти клетки являются мощными защитными агентами организма, но токсины они выпускают (в том числе активные формы кислорода ) вредны как для собственных тканей организма, так и для агентов-вторжений. Как следствие, хроническое воспаление почти всегда сопровождается разрушением тканей.
Примеры
Воспаление обычно обозначается добавлением суффикса "это ", как показано ниже. Однако некоторые условия, такие как астма и пневмония не следуйте этому соглашению. Дополнительные примеры доступны на сайте список видов воспаления.

Острый аппендицит

Острый дерматит

Острый заразный менингит
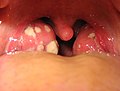
Острый тонзиллит
Смотрите также
Рекомендации
- ^ Ферреро-Милиани Л., Нильсен Огайо, Андерсен П.С., Жирардин С.Е.; Нильсен; Андерсен; Жирарден (февраль 2007 г.). «Хроническое воспаление: важность NOD2 и NALP3 в генерации интерлейкина-1бета». Clin. Exp. Иммунол. 147 (2): 227–35. Дои:10.1111 / j.1365-2249.2006.03261.x. ЧВК 1810472. PMID 17223962.CS1 maint: несколько имен: список авторов (связь)
- ^ Аббас А.Б .; Лихтман А.Х. (2009). «Глава 2 Врожденный иммунитет». В Сондерсе (Elsevier) (ред.). Основы иммунологии. Функции и нарушения иммунной системы (3-е изд.). ISBN 978-1-4160-4688-2.
- ^ а б c d Холл, Джон (2011). Гайтон и Холл учебник медицинской физиологии (12-е изд.). Филадельфия, Пенсильвания: Saunders / Elsevier. п. 428. ISBN 978-1-4160-4574-8.
- ^ Грейнджер, Д. Нил; Сенченкова, Елена (2010). «Адгезия лейкоцитов к эндотелиальным клеткам». Воспаление и микроциркуляция. Физиология интегрированных систем - от клетки к функции. Морган и Клейпул Науки о жизни.
- ^ Пиира, Олли-Пекка; Miettinen, Johanna A .; Хаутала, Арто Дж .; Huikuri, Heikki V .; Тулппо, Микко П. (2013). «Физиологические реакции на эмоциональное возбуждение у здоровых людей и пациентов с ишемической болезнью сердца». Автономная неврология. 177 (2): 280–5. Дои:10.1016 / j.autneu.2013.06.001. PMID 23916871. S2CID 19823098.
- ^ а б Медицинский словарь Стедмана (Двадцать пятое изд.). Уильямс и Уилкинс. 1990 г.
- ^ Скорее, L.J. (1971). «Нарушение функции (functio laesa): легендарный пятый кардинальный признак воспаления, добавленный Галеном к четырем кардинальным знакам Цельсия». Bull N Y Acad Med. 47 (3): 303–322. ЧВК 1749862. PMID 5276838.
- ^ а б c d е ж грамм час я j k л м п о п q р Котран; Кумар, Коллинз (1998). Патологическая основа болезни Роббинса. Филадельфия: Компания У. Б. Сондерса. ISBN 978-0-7216-7335-6.
- ^ Кумар, Рукмини; Клермон, Жиль; Водовоц, Йорам; Чоу, Карсон С. (21 сентября 2004 г.). «Динамика острого воспаления». Журнал теоретической биологии. 230 (2): 145–155. arXiv:q-bio / 0404034. Bibcode:2004ФДТ ....... 405К. Дои:10.1016 / j.jtbi.2004.04.044. PMID 15321710. S2CID 16992741.
- ^ а б c d Паракрама Чандрасома; Клайв Р. Тейлор (2005). «Часть A.« Общая патология », раздел II.« Реакция хозяина на травму », глава 3.« Острая воспалительная реакция », подраздел« Основные клинические признаки »"". Краткая патология (3-е изд.). Макгроу-Хилл. ISBN 978-0-8385-1499-3. OCLC 150148447. Получено 5 ноября 2008.
- ^ Вернер, Рут (2009). Руководство по патологии для массажиста (4-е изд.). Wolters Kluwer. ISBN 978-0781769198.
- ^ Vogel, Wolfgang H .; Берке, Андреас (2009). Краткая история зрения и глазной медицины. Публикации Куглера. п. 97. ISBN 978-90-6299-220-1.
- ^ Порт, Кэрол (2007). Основы пахтофизиологии: концепции измененных состояний здоровья. Хагерстаун, Мэриленд: Липпинкотт Уильямс и Уилкинс. п. 270. ISBN 978-0-7817-7087-3.
- ^ Дорманди, Томас (2006). Худшее из зол: борьба человека с болью. Нью-Хейвен, Коннектикут: Издательство Йельского университета. стр.22. ISBN 978-0-300-11322-8.
- ^ а б Херрингтон, Саймон (2014). Учебник патологии Мюира (15-е изд.). CRC Press. п. 59. ISBN 978-1444184990.
- ^ Чевикбас, Ферда; Кемпкес, Кордула; Буль, Тимо; Беспорядок, Кристиан; Будденкотте, Йорг; Стейнхофф, Мартин (2014). Carstens, E .; Акияма, Тасуку (ред.). Зуд: механизмы и лечение. Границы неврологии. Бока-Ратон (Флорида): CRC Press / Taylor & Francis. ISBN 9781466505438. PMID 24830021.
- ^ Коуги, Джордж Х. (1 июня 2007 г.). «Триптазы и химазы тучных клеток при воспалении и защите хозяина». Иммунологические обзоры. 217 (1): 141–154. Дои:10.1111 / j.1600-065x.2007.00509.x. ЧВК 2275918. PMID 17498057.
- ^ Коуги, Джордж Х. (5 мая 2016 г.). «Протеазы тучных клеток как фармакологические мишени». Европейский журнал фармакологии. Фармакологическая модуляция тучных клеток и базофилов. 778: 44–55. Дои:10.1016 / j.ejphar.2015.04.045. ЧВК 4636979. PMID 25958181.
- ^ Либби, П. (19–26 декабря 2002 г.). «Воспаление при атеросклерозе». Природа. 420 (6917): 868–74. Bibcode:2002Натурал.420..868Л. Дои:10.1038 / природа01323. PMID 12490960. S2CID 407449.
- ^ Wiedermann U, et al. (1996). «Дефицит витамина А усиливает воспалительные реакции». Сканд Дж Иммунол. 44 (6): 578–584. Дои:10.1046 / j.1365-3083.1996.d01-351.x. PMID 8972739. S2CID 3079540.
- ^ Hargrave, B. Y .; Tiangco, D.A .; Латтанцио, Ф. А .; Биби, С. Дж. (2003). «Кокаин, а не морфин, вызывает образование активных форм кислорода и активацию NF-κB в временно котрансфицированных клетках сердца». Кардиоваск токсикол. 3 (2): 141–151. Дои:10.1385 / CT: 3: 2: 141. PMID 14501032. S2CID 35240781.
- ^ Montiel-Duarte, C .; Ansorena, E .; López-Zabalza, M.J .; Cenarruzabeitia, E .; Ирабуру, М. Дж. (2004). «Роль активных форм кислорода, глутатиона и NF-κB в апоптозе, вызванном 3,4-метилендиоксиметамфетамином (« экстази ») на звездчатых клетках печени». Биохим Фармакол. 67 (6): 1025–33. Дои:10.1016 / j.bcp.2003.10.020. PMID 15006539.
- ^ Хендрик Унгефрорен; Сюзанна Себенс; Даниэль Зайдл; Хендрик Ленерт; Ральф Хаас (2011). «Взаимодействие опухолевых клеток с микросредой». Сотовая связь и сигнализация. 9 (18). Дои:10.1186 / 1478-811X-9-18. ЧВК 3180438. PMID 21914164.
- ^ Coussens, L.M .; Верб, З. (2002). «Воспаление и рак». Природа. 420 (6917): 860–7. Bibcode:2002Натурал. 420..860С. Дои:10.1038 / природа01322. ЧВК 2803035. PMID 12490959.
- ^ Ганн, L; Дин, С; Лю, М; Май; Ци, С; Cai, Y; Hu, X; Aggarwal, D; Zhang, HG; Ян, Дж (15 сентября 2012 г.). «Противоположные роли компонента комплемента C5a в прогрессировании опухоли и микроокружении опухоли». Журнал иммунологии. 189 (6): 2985–94. Дои:10.4049 / jimmunol.1200846. ЧВК 3436956. PMID 22914051.
- ^ Copland, JA; Шеффилд-Мур, М; Колдзич-Живанович, Н; Джентри, S; Lamprou, G; Цорцату-Статопулу, Ф; Zoumpourlis, V; Городской, RJ; Влахопулос, С.А. (июнь 2009 г.). «Рецепторы половых стероидов в дифференцировке скелета и эпителиальной неоплазии: возможно ли тканеспецифическое вмешательство?». BioEssays. 31 (6): 629–41. Дои:10.1002 / bies.200800138. PMID 19382224. S2CID 205469320.
- ^ Колотта Ф, Аллавена П., Сика А, Гарланда С., Мантовани А; Аллавена; Sica; Гарланда; Мантовани (июль 2009 г.). «Воспаление, связанное с раком, седьмой признак рака: связь с генетической нестабильностью». Канцерогенез (рассмотрение). 30 (7): 1073–81. Дои:10.1093 / carcin / bgp127. PMID 19468060.CS1 maint: несколько имен: список авторов (связь)
- ^ а б c d Куссенс Л.М., Верб З. (2002). «Воспаление и рак». Природа. 420 (6917): 860–7. Bibcode:2002Натурал. 420..860С. Дои:10.1038 / природа01322. ЧВК 2803035. PMID 12490959.
- ^ а б c d е ж грамм час Тиба Т, Марусава Х, Ушидзима Т (2012). «Развитие рака в органах пищеварения, связанное с воспалением: механизмы и роль в генетической и эпигенетической модуляции» (PDF). Гастроэнтерология. 143 (3): 550–563. Дои:10.1053 / j.gastro.2012.07.009. HDL:2433/160134. PMID 22796521.
- ^ Мантовани А, Аллавена П., Сика А, Балквилл Ф (2008). «Воспаление, связанное с раком» (PDF). Природа. 454 (7203): 436–44. Bibcode:2008Натура.454..436М. Дои:10.1038 / природа07205. HDL:2434/145688. PMID 18650914. S2CID 4429118.
- ^ Ларсен ГЛ, Хенсон ПМ (1983). «Медиаторы воспаления». Анну. Преп. Иммунол. 1: 335–59. Дои:10.1146 / annurev.iy.01.040183.002003. PMID 6399978.
- ^ а б c d Шактер Э, Вайцман С.А. (2002). «Хроническое воспаление и рак». Онкология (Уиллистон-Парк, Нью-Йорк). 16 (2): 217–26, 229, обсуждение 230–2. PMID 11866137.
- ^ Ю Й, Цуй Й, Нидернхофер Л. Дж., Ван И (2016). «Возникновение, биологические последствия и значимость для здоровья человека повреждения ДНК, вызванного окислительным стрессом». Chem. Res. Токсикол. 29 (12): 2008–2039. Дои:10.1021 / acs.chemrestox.6b00265. ЧВК 5614522. PMID 27989142.
- ^ Диздароглу М (2012). «Окислительное повреждение ДНК: механизмы, восстановление и болезнь». Рак Lett. 327 (1–2): 26–47. Дои:10.1016 / j.canlet.2012.01.016. PMID 22293091.
- ^ Нисида Н, Кудо М (2013). «Окислительный стресс и эпигенетическая нестабильность в гепатоканцерогенезе человека». Dig Dis. 31 (5–6): 447–53. Дои:10.1159/000355243. PMID 24281019.
- ^ а б Дин Н., Майури А. Р., О'Хаган Х. М. (2017). «Возникающая роль эпигенетических модификаторов в восстановлении повреждений ДНК, связанных с хроническими воспалительными заболеваниями». Мутационные исследования. 780: 69–81. Дои:10.1016 / j.mrrev.2017.09.005. ЧВК 6690501. PMID 31395351.CS1 maint: несколько имен: список авторов (связь)
- ^ Каваниши С., Охниши С., Ма Н., Хираку Ю., Оикава С., Мурата М. (2016). «Нитативное и окислительное повреждение ДНК в канцерогенезе, связанном с инфекцией, в отношении раковых стволовых клеток». Гены окружающей среды. 38: 26. Дои:10.1186 / s41021-016-0055-7. ЧВК 5203929. PMID 28050219.
- ^ О'Хаган Х.М., Ван В., Сен С., Дестефано Шилдс С., Ли С.С., Чжан Ю.В., Клементс Э.Г., Кай Й., Ван Несте Л., Ишваран Х., Касеро Р.А., Сирс С.Л., Бейлин С.Б. (2011). «Окислительное повреждение нацелено на комплексы, содержащие ДНК-метилтрансферазы, SIRT1 и члены polycomb, на промоторные острова CpG». Раковая клетка. 20 (5): 606–19. Дои:10.1016 / j.ccr.2011.09.012. ЧВК 3220885. PMID 22094255.
- ^ Maiuri AR, Peng M, Sriramkumar S, Kamplain CM, DeStefano Shields CE, Sears CL, O'Hagan HM (2017). «Белки восстановления несоответствия инициируют эпигенетические изменения во время опухолевого процесса, вызванного воспалением». Рак Res. 77 (13): 3467–3478. Дои:10.1158 / 0008-5472.CAN-17-0056. ЧВК 5516887. PMID 28522752.
- ^ Ямасита С., Кишино Т., Такахаши Т., Симадзу Т., Чарват Х, Какугава Ю., Накадзима Т., Ли Ю.С., Иида Н., Маеда М., Хаттори Н., Такешима Н., Нагано Р., Ода I, Цуганэ С., Ву М.С., Ушидзима Т. (2018). «Генетические и эпигенетические изменения в нормальных тканях по-разному влияют на риск рака среди тканей». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 115 (6): 1328–1333. Дои:10.1073 / pnas.1717340115. ЧВК 5819434. PMID 29358395.
- ^ Раза Й, Хан А., Фаруки А., Мубарак М., Фасиста А., Ахтар С. С., Хан С., Кази Дж. И., Бернштейн С., Казми С.У. (2014). «Окислительное повреждение ДНК как потенциальный ранний биомаркер канцерогенеза, связанного с Helicobacter pylori». Патол. Онкол. Res. 20 (4): 839–46. Дои:10.1007 / s12253-014-9762-1. PMID 24664859. S2CID 18727504.
- ^ а б Дикс, Стивен Г. (1 января 2011 г.). «ВИЧ-инфекция, воспаление, иммунное старение и старение». Ежегодный обзор медицины. 62: 141–155. Дои:10.1146 / annurev-med-042909-093756. ЧВК 3759035. PMID 21090961.
- ^ Klatt, Nichole R .; Хомонт, Николас; Douek, Daniel C .; Дикс, Стивен Г. (1 июля 2013 г.). «Активация иммунитета и сохранение ВИЧ: значение для лечебных подходов к ВИЧ-инфекции». Иммунологические обзоры. 254 (1): 326–342. Дои:10.1111 / imr.12065. ЧВК 3694608. PMID 23772629.
- ^ Salazar-Gonzalez, J. F .; Мартинес-Маза, О .; Нишанян, П .; Азиз, Н .; Shen, L.P .; Grosser, S .; Taylor, J .; Detels, R .; Фэи, Дж. Л. (1 августа 1998 г.). «Повышенная иммунная активация предшествует точке перегиба Т-лимфоцитов CD4 и увеличению вирусной нагрузки в сыворотке крови при инфицировании вирусом иммунодефицита человека». Журнал инфекционных болезней. 178 (2): 423–430. Дои:10.1086/515629. PMID 9697722.
- ^ Ипп, Хейли; Землин, Аннализ (1 февраля 2013 г.). «Парадокс иммунного ответа при ВИЧ-инфекции: когда воспаление становится опасным». Clinica Chimica Acta; Международный журнал клинической химии. 416: 96–99. Дои:10.1016 / j.cca.2012.11.025. PMID 23228847.
- ^ Наси, Милена; Пинти, Марчелло; Муссини, Кристина; Коссарицца, Андреа (1 октября 2014 г.). «Стойкое воспаление при ВИЧ-инфекции: устоявшиеся концепции, новые перспективы». Письма иммунологии. 161 (2): 184–8. Дои:10.1016 / j.imlet.2014.01.008. PMID 24487059.
- ^ Милуш, Джеффри М .; Mir, Kiran D .; Сундараварадан, Васудха; Гордон, Шари Н .; Энграмма, Джессика; Кано, Кристофер А .; Ривз, Жаклин Д.; Антон, Елизавета; О'Нил, Эдуардо (1 марта 2011 г.). «Отсутствие клинических проявлений СПИДа у SIV-инфицированных сажистых плодов манга со значительной потерей CD4 + Т-клеток связано с дважды отрицательными Т-клетками». Журнал клинических исследований. 121 (3): 1102–10. Дои:10.1172 / JCI44876. ЧВК 3049370. PMID 21317533.
- ^ Rey-Cuillé, M.A .; Berthier, J. L .; Bomsel-Demontoy, M.C .; Chaduc, Y .; Montagnier, L .; Ованесян, А.Г .; Чакрабарти, Л. А. (1 мая 1998 г.). «Вирус обезьяньего иммунодефицита реплицируется до высоких уровней в покрытых сажей мангабеях, не вызывая болезни». Журнал вирусологии. 72 (5): 3872–86. Дои:10.1128 / JVI.72.5.3872-3886.1998. ЧВК 109612. PMID 9557672.
- ^ Chahroudi, Ann; Босинджер, Стивен Э .; Vanderford, Thomas H .; Пайардини, Мирко; Сильвестри, Гвидо (9 марта 2012 г.). «Естественные хозяева SIV: открывая дверь СПИДу». Наука. 335 (6073): 1188–93. Bibcode:2012Sci ... 335.1188C. Дои:10.1126 / наука.1217550. ЧВК 3822437. PMID 22403383.
- ^ а б Дойш, Гилад; Галлоуэй, Николь Л. К .; Гэн, Синь; Ян, Чжиюань; Монро, Кэтрин М .; Зепеда, Орландо; Хант, Питер В .; Хатано, Хирою; Совински, Стефани (23 января 2014 г.). «Гибель клеток в результате пироптоза приводит к истощению Т-лимфоцитов CD4 при инфекции ВИЧ-1». Природа. 505 (7484): 509–514. Bibcode:2014Натура.505..509D. Дои:10.1038 / природа12940. ЧВК 4047036. PMID 24356306.
- ^ Монро, Кэтрин М .; Ян, Чжиюань; Джонсон, Джеффри Р .; Гэн, Синь; Дойш, Гилад; Krogan, Nevan J .; Грин, Уорнер С. (24 января 2014 г.). «Датчик ДНК IFI16 необходим для гибели лимфоидных CD4 T-клеток, абортивно инфицированных ВИЧ». Наука. 343 (6169): 428–432. Bibcode:2014Наука ... 343..428М. Дои:10.1126 / science.1243640. ЧВК 3976200. PMID 24356113.
- ^ Галлоуэй, Николь Л. К .; Дойш, Гилад; Монро, Кэтрин М .; Ян, Чжиюань; Муньос-Ариас, Иса; Леви, Дэвид Н .; Грин, Уорнер К. (8 сентября 2015 г.). «Передача ВИЧ-1 от клетки к клетке необходима для запуска пироптотической гибели лимфоидных Т-лимфоцитов CD4». Отчеты по ячейкам. 12 (10): 1555–63. Дои:10.1016 / j.celrep.2015.08.011. ЧВК 4565731. PMID 26321639.
- ^ Дойш, Гилад; Грин, Уорнер С. (9 марта 2016 г.). «Анализ того, как теряются CD4 Т-клетки во время ВИЧ-инфекции». Клеточный хозяин и микроб. 19 (3): 280–291. Дои:10.1016 / j.chom.2016.02.012. ЧВК 4835240. PMID 26962940.
- ^ «Исследование VX-765 у субъектов с резистентной к лечению частичной эпилепсией - полный текст - ClinicalTrials.gov». Clinicaltrials.gov. Получено 21 мая 2016.
- ^ Eming, S.A .; Krieg, T .; Дэвидсон, Дж. М. (2007). «Воспаление при заживлении ран: молекулярные и клеточные механизмы». Журнал следственной дерматологии. 127 (3): 514–525. Дои:10.1038 / sj.jid.5700701. PMID 17299434.
- ^ Ashcroft, G.S .; Ян, Х; Glick, A.B .; Вайнштейн, М; Letterio, J. L .; Mizel, D.E .; Анзано, М; Гринвелл-Уайлд, Т; Wahl, S.M .; Дэн, С; Робертс, А. Б. (1999). «Мыши, у которых отсутствует Smad3, демонстрируют ускоренное заживление ран и нарушение местной воспалительной реакции». Nat Cell Biol. 1 (5): 260–6. Дои:10.1038/12971. PMID 10559937. S2CID 37216623.
- ^ Эшкрофт, Г. С. (1999). «Двунаправленная регуляция функции макрофагов с помощью TGF-β». Микробы заражают. 1 (15): 1275–82. Дои:10.1016 / S1286-4579 (99) 00257-9. PMID 10611755.
- ^ Вернер, Ф; Jain, M. K .; Файнберг, М. В .; Sibinga, N.E .; Пеллакани, А; Wiesel, P; Чин, М. Т .; Topper, J. N .; Perrella, M.A .; Ли, М. Э. (2000). «Ингибирование активации макрофагов трансформирующим фактором роста-β1 опосредуется через Smad3». J Biol Chem. 275 (47): 36653–8. Дои:10.1074 / jbc.M004536200. PMID 10973958.
- ^ Sato, Y .; Ohshima, T .; Кондо, Т. (1999). «Регуляторная роль эндогенного интерлейкина-10 в кожном воспалительном ответе заживления ран у мышей». Biochem Biophys Res Commun. 265 (1): 194–9. Дои:10.1006 / bbrc.1999.1455. PMID 10548513.
- ^ Серхан, К. Н. (2008). «Контроль разрешения острого воспаления: новый род двойных противовоспалительных и прореагирующих медиаторов». J Periodontol. 79 (8 Suppl): 1520–6. Дои:10.1902 / jop.2008.080231. PMID 18673006.
- ^ Headland SE, Норлинг LV (2015). «Разрешение воспаления: принципы и проблемы». Семинары по иммунологии. 27 (3): 149–60. Дои:10.1016 / j.smim.2015.03.014. PMID 25911383.
- ^ Гринхалг, Д. Г. (1998). «Роль апоптоза в заживлении ран». Int J Biochem Cell Biol. 30 (9): 1019–30. Дои:10.1016 / S1357-2725 (98) 00058-2. PMID 9785465.
- ^ Цзян, Д. Лян, Дж; Fan, J; Ю, С; Чен, S; Луо, Y; Прествич, Г. Д .; Mascarenhas, M. M .; Garg, H.G .; Куинн, Д. А .; Гомер, Р. Дж .; Goldstein, D. R .; Bucala, R; Ли, П. Дж .; Меджитов, Р; Благородный, П. В. (2005). «Регулирование повреждения легких и восстановления с помощью Toll-подобных рецепторов и гиалуронана». Нат Мед. 11 (11): 1173–9. Дои:10,1038 / нм 1315. PMID 16244651. S2CID 11765495.
- ^ Тедер, П. (2002). «Разрешение воспаления легких по CD44». Наука. 296 (5565): 155–8. Bibcode:2002Наука ... 296..155Т. Дои:10.1126 / science.1069659. PMID 11935029. S2CID 7905603.
- ^ McQuibban, G.A .; Gong, J. H .; Tam, E.M .; McCulloch, C.A .; Кларк-Льюис, я; В целом, С. М. (2000). «Воспаление, подавленное желатиназой А, расщеплением моноцитов хемоаттрактантного белка-3». Наука. 289 (5482): 1202–6. Bibcode:2000Sci ... 289.1202M. Дои:10.1126 / science.289.5482.1202. PMID 10947989.
- ^ Серхан К.Н., Сэвилл Дж. Сэвилл (2005). «Разрешение воспаления: начало программирует конец». Nat. Иммунол. 6 (12): 1191–7. Дои:10.1038 / ni1276. PMID 16369558. S2CID 22379843.
- ^ Берк, М; Уильямс, Л. Дж .; Jacka, F. N .; О'Нил, А; Pasco, J. A .; Мойлан, S; Allen, N.B .; Стюарт, А. Л .; Hayley, A.C .; Byrne, M. L .; Маес, М (2013). «Итак, депрессия - это воспалительное заболевание, но откуда взялось воспаление?». BMC Медицина. 11: 200. Дои:10.1186/1741-7015-11-200. ЧВК 3846682. PMID 24228900.
- ^ Cox, William T. L .; Abramson, Lyn Y .; Дивайн, Патрисия Дж .; Холлон, Стивен Д. (2012). «Стереотипы, предубеждения и депрессия: комплексная перспектива». Перспективы психологической науки. 7 (5): 427–449. Дои:10.1177/1745691612455204. PMID 26168502. S2CID 1512121.
- ^ Kiecolt-Glaser, Janice K .; Дерри, Хизер М .; Фагундес, Кристофер П. (ноябрь 2015 г.). «Воспаление: Депрессия разжигает пламя и празднует жару». Американский журнал психиатрии. 172 (11): 1075–91. Дои:10.1176 / appi.ajp.2015.15020152. ЧВК 6511978. PMID 26357876.
- ^ Уильямс, Кэролайн (4 января 2015 г.). «Является ли депрессия разновидностью аллергической реакции?». хранитель.
- ^ Бретцке, Элиза; Стертц, Лаура; Фернандес, Бриса Симоэнс; Кауэр-Сант'Анна, Марсия; Маскареньяс, Марчелло; Эскостеги Варгас, Андрея; Чиес, Хосе Артур; Капчинский, Флавио (2009). «Сравнение уровней цитокинов у депрессивных, маниакальных и эутимических пациентов с биполярным расстройством». Журнал аффективных расстройств. 116 (3): 214–7. Дои:10.1016 / j.jad.2008.12.001. PMID 19251324.
- ^ Müller, N; Шварц, М. Дж .; Денинг, S; Douhe, A; Cerovecki, A; Гольдштейн-Мюллер, Б; Spellmann, I; Hetzel, G; Майно, К; Kleindienst, N; Мёллер, HJ; Арольт, В; Ридель, М (2006). «Ингибитор циклооксигеназы-2 целекоксиб оказывает терапевтическое действие при большой депрессии: результаты двойного слепого рандомизированного плацебо-контролируемого дополнительного пилотного исследования к ребоксетину». Молекулярная психиатрия. 11 (7): 680–4. Дои:10.1038 / sj.mp.4001805. PMID 16491133.
- ^ Канли, Турхан (2014). «Переосмысление большого депрессивного расстройства как инфекционного заболевания». Биология расстройств настроения и тревожности. 4: 10. Дои:10.1186/2045-5380-4-10. ЧВК 4215336. PMID 25364500.
- ^ а б Parimisetty A, Dorsemans AC, Awada R, Ravanan P, Diotel N, Lefebvre d'Hellencourt C (24 марта 2016 г.). «Секретный разговор между жировой тканью и центральной нервной системой через секретируемые факторы - новый рубеж в исследованиях нейродегенерации». J нейровоспаление (Рассмотрение). 13 (1): 67. Дои:10.1186 / s12974-016-0530-х. ЧВК 4806498. PMID 27012931.
- ^ Kershaw, E. E .; Флиер, Дж. С. (2004). «Жировая ткань как эндокринный орган». J Clin Endocrinol Metab. 89 (6): 2548–56. Дои:10.1210 / jc.2004-0395. PMID 15181022.
- ^ Бастард Дж. И др. (2000). «Повышенные уровни интерлейкина 6 снижаются в сыворотке и подкожной жировой ткани у женщин с ожирением после похудания». J Clin Endocrinol Metab. 85 (9): 3338–42. Дои:10.1210 / jc.85.9.3338. PMID 10999830.
- ^ Мохамед-Али V и др. (2001). «Бета-адренергическая регуляция высвобождения ИЛ-6 из жировой ткани: in vivo и in vitro исследования ». J Clin Endocrinol Metab. 86 (12): 5864–9. Дои:10.1210 / jc.86.12.5864. PMID 11739453.
- ^ а б c d е ж грамм Лоффреда, S; Yang, S. Q .; Lin, H. Z .; Karp, C.L .; Brengman, M. L .; Wang, D. J .; Klein, A. S .; Балкли, Г. Б .; Бао, С; Благородный, П. У .; Lane, M.D .; Диль, А. М. (1998). «Лептин регулирует провоспалительные иммунные реакции». FASEB J. 12 (1): 57–65. Дои:10.1096 / fasebj.12.1.57. PMID 9438411.
- ^ а б c d е ж грамм Эспозито, К; Наппо, Франция; Marfella, R; Джульяно, G; Джульяно, F; Ciotola, M; Quagliaro, L; Ceriello, A; Джульяно, Д. (2002). «Концентрации воспалительных цитокинов резко увеличиваются при гипергликемии у людей: роль окислительного стресса». Тираж. 106 (16): 2067–72. Дои:10.1161 / 01.CIR.0000034509.14906.AE. PMID 12379575.
- ^ Петерсен, А. М .; Педерсен, Б. К. (2005). «Противовоспалительный эффект физических упражнений». J Appl Physiol. 98 (4): 1154–62. Дои:10.1152 / japplphysiol.00164.2004. PMID 15772055. S2CID 4776835.
- ^ Роговский, О; Шапира, я; Bassat, O.K .; Чундадзе, Т; Финн, Т; Берлинер, S; Стейнвиль, А (2010). «Окружность талии как основной фактор микровоспалительного ответа при метаболическом синдроме: перекрестное исследование». Журнал воспаления. 7: 35. Дои:10.1186/1476-9255-7-35. ЧВК 2919526. PMID 20659330.
- ^ Goldfine, Allison B .; Шулсон, Стивен Э. (3 января 2017 г.). «Терапевтические подходы к лечению воспаления при диабете и связанном с ним сердечно-сосудистом риске». Журнал клинических исследований. 127 (1): 83–93. Дои:10.1172 / jci88884. ISSN 0021-9738. ЧВК 5199685. PMID 28045401.
- ^ Choi, J .; Joseph, L .; Пилот, Л. (2013). «Ожирение и С-реактивный белок в различных популяциях: систематический обзор и метаанализ». Обзоры ожирения. 14 (3): 232–244. Дои:10.1111 / obr.12003. ISSN 1467-7881. PMID 23171381. S2CID 206227739.
внешняя ссылка
- Воспаление в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)



