Вирус - Virus
| Вирус | |
|---|---|
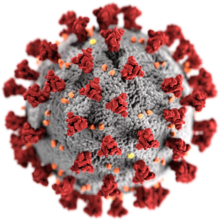 | |
| SARS-CoV-2, член подсемейства Coronavirinae | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Царства | |
А вирус это субмикроскопический инфекционный агент который копирует только внутри живого клетки из организм.[1] Вирусы заражают все типы формы жизни, от животных и растений до микроорганизмы, включая бактерии и археи.[2]С Дмитрий Ивановский статья 1892 г., описывающая небактериальный возбудитель заражение табачных растений и открытие вирус табачной мозаики к Мартинус Бейеринк в 1898 г.,[3] более 6000 виды вирусов были подробно описаны[4] из миллионов типов вирусов в окружающей среде.[5] Вирусы встречаются почти во всех экосистема на Земле и являются наиболее многочисленным типом биологических существ.[6][7] Изучение вирусов известно как вирусология, узкая специализация микробиология.
При заражении клетка-хозяин вынуждена быстро производить тысячи идентичных копий исходного вируса. Находясь вне инфицированной клетки или в процессе заражения клетки, вирусы существуют в форме независимых частиц или вирионы, состоящий из: (i) генетический материал, т. е. длинный молекулы из ДНК или же РНК которые кодируют структуру белков, с помощью которых действует вирус; (ii) а белок пальто, капсид, который окружает и защищает генетический материал; и в некоторых случаях (iii) внешний конверт из липиды. Формы этих вирусных частиц варьируются от простых спиральный и икосаэдр формы в более сложные структуры. У большинства видов вирусов вирионы слишком малы, чтобы их можно было увидеть оптический микроскоп, поскольку они составляют одну сотую размера большинства бактерий.
Происхождение вирусов в эволюционная история жизни неясны: некоторые могут иметь развился из плазмиды - фрагменты ДНК, которые могут перемещаться между клетками - в то время как другие могли развиться из бактерий. В эволюции вирусы являются важным средством горизонтальный перенос генов, что увеличивает генетическое разнообразие способом, аналогичным половое размножение.[8] Вирусы считаются некоторыми биологи быть формой жизни, потому что они несут генетический материал, воспроизводятся и развиваются естественный отбор, хотя им не хватает ключевых характеристик, таких как структура ячеек, которые обычно считаются необходимыми критериями для жизнь. Поскольку они обладают некоторыми, но не всеми такими качествами, вирусы были описаны как «организмы на краю жизни»,[9] и, как саморепликаторы.[10]
Вирусы распространяются разными способами. Один путь передачи - через болезнетворные организмы, известные как векторов: например, вирусы часто передаются с растения на растение насекомыми, которые питаются сок растений, Такие как тля; и вирусы у животных могут переноситься кровосос насекомые. Вирусы гриппа распространяются при кашле и чихании. Норовирус и ротавирус, частые причины вирусных гастроэнтерит, передаются фекально-оральный путь, передаваемые из рук в рот, с едой или водой. В инфекционная доза норовируса, необходимого для заражения человека, составляет менее 100 частиц.[11] ВИЧ один из нескольких вирусов, передающихся через половой контакт и контактом с инфицированной кровью. Разнообразие хозяйских клеток, которые вирус может заразить, называется его "диапазон хостов ". Оно может быть узким, что означает, что вирус способен заразить несколько видов, или широким, что означает, что он способен заразить многие.[12]
Вирусные инфекции у животных вызывают иммунная реакция это обычно устраняет заражающий вирус. Иммунные ответы также могут быть вызваны вакцина, что дает искусственно приобретенный иммунитет к конкретной вирусной инфекции. Некоторые вирусы, в том числе вызывающие СПИД, Инфекция ВПЧ, и вирусный гепатит уклоняются от этих иммунных реакций и приводят к хронический инфекции. Несколько противовирусные препараты были разработаны.
Этимология
Слово происходит от латинского среднего рода вирус ссылаясь на яд и другие ядовитые жидкости из той же Индоевропейская база в качестве санскрит via, Авестийский Виша, и древнегреческий ἰός (все означает «яд»), сначала засвидетельствован на английском языке в 1398 г. Джона Тревизы перевод Варфоломея Англиканского De Proprietatibus Rerum.[13][14] Вирулентный, от латинского вирулентус (ядовитый), датируется с. 1400.[15][16] Значение «агент, вызывающий инфекционное заболевание» впервые упоминается в 1728 году.[14] задолго до открытия вирусов Дмитрий Ивановский в 1892 году. множественное число является вирусы (иногда также вира),[17] тогда как латинское слово массовое существительное, который не имеет классически засвидетельствовано множественное число (вира используется в Неолатынь[18]). Прилагательное популярный датируется 1948 годом.[19] Период, термин вирион (множественное число вирионы), которая датируется 1959 г.,[20] также используется для обозначения одной вирусной частицы, которая высвобождается из клетки и способна инфицировать другие клетки того же типа.[21]
История

Луи Пастер не удалось найти возбудителя бешенство и размышляли о патогенах, которые слишком малы, чтобы их можно было обнаружить под микроскопом.[22] В 1884 году французы микробиолог Чарльз Чемберленд изобрел Фильтр Чемберленда (или фильтр Пастера-Чемберленда) с порами достаточно маленькими, чтобы удалить все бактерии из раствора, прошедшего через него.[23] В 1892 году русский биолог Дмитрий Ивановский использовал этот фильтр для изучения того, что сейчас известно как вирус табачной мозаики: экстракты измельченных листьев инфицированных растений табака оставались заразными даже после фильтрации для удаления бактерий. Ивановский предположил, что инфекция может быть вызвана токсин производятся бактериями, но он не преследовал эту идею.[24] В то время считалось, что все инфекционные агенты могут задерживаться фильтрами и выращиваться на питательной среде - это было частью микробная теория болезни.[3] В 1898 году голландский микробиолог Мартинус Бейеринк повторил эксперименты и убедился, что отфильтрованный раствор содержит новую форму инфекционного агента.[25] Он заметил, что этот агент размножается только в делящихся клетках, но, поскольку его эксперименты не показали, что он состоит из частиц, он назвал его contagium vivum fluidum (растворимый живой микроб) и вновь ввел слово вирус. Бейеринк утверждал, что вирусы имеют жидкую природу, и эту теорию позже дискредитировал Венделл Стэнли, которые доказали, что они были твердыми частицами.[24] В том же году, Фридрих Лёффлер и Пол Фрош передал первый вирус животных, афтовирус (агент ящур ) через аналогичный фильтр.[26]
В начале 20 века английский бактериолог Фредерик Творт обнаружил группу вирусов, поражающих бактерии, которые теперь называются бактериофаги[27] (или обычно «фаги») и французско-канадский микробиолог Феликс д'Эрель описал вирусы, которые при добавлении к бактериям на пластина с агаром, будет производить участки мертвых бактерий. Он точно разбавил суспензию этих вирусов и обнаружил, что самые высокие разведения (самые низкие концентрации вируса), а не уничтожение всех бактерий, образуют отдельные области мертвых организмов. Подсчет этих площадей и умножение на коэффициент разведения позволили ему рассчитать количество вирусов в исходной суспензии.[28] Фаги были объявлены потенциальным средством лечения таких заболеваний, как брюшной тиф и холера, но их обещание было забыто с развитием пенициллин. Развитие устойчивость бактерий к антибиотикам возобновил интерес к терапевтическому использованию бактериофагов.[29]
К концу XIX века вирусы были определены с точки зрения их заразительность, их способность проходить фильтры и их требования к живым хозяевам. Вирусы выращивали только на растениях и животных. В 1906 г. Росс Грэнвилл Харрисон изобрел метод для растущая ткань в лимфа, а в 1913 г. Э. Стейнхардт, К. Израэли и Р.А. Ламберт использовал этот метод для выращивания вакцина вирус во фрагментах ткани роговицы морской свинки.[30] В 1928 году Х. Б. Мейтленд и М. К. Мейтленд вырастили вирус коровьей оспы в суспензиях из измельченных почек кур. Их метод не получил широкого распространения до 1950-х годов, когда полиовирус был выращен в больших масштабах для производства вакцины.[31]
Еще один прорыв произошел в 1931 году, когда американский патологоанатом Эрнест Уильям Гудпастур и Элис Майлз Вудрафф вырастил грипп и несколько других вирусов в оплодотворенных куриных яйцах.[32] В 1949 г. Джон Франклин Эндерс, Томас Веллер, и Фредерик Роббинс выращивал полиовирус в культивируемых клетках из абортированной эмбриональной ткани человека,[33] первый вирус, выращиваемый без использования твердых тканей животных или яиц. Эта работа позволила Хилари Копровски, а потом Йонас Солк, чтобы сделать эффективный вакцина от полиомиелита.[34]
Первые изображения вирусов были получены после изобретения электронная микроскопия в 1931 году немецкими инженерами Эрнст Руска и Макс Нолл.[35] В 1935 году американский биохимик и вирусолог Венделл Мередит Стэнли исследовали вирус табачной мозаики и обнаружили, что он в основном состоит из белка.[36] Спустя некоторое время этот вирус был разделен на белковые и РНК-части.[37]Вирус табачной мозаики был первым, кто кристаллизованный и поэтому его структура могла быть выяснена подробно. Первый дифракция рентгеновских лучей снимки кристаллизованного вируса были получены Берналом и Фанкухен в 1941 году. На основе ее рентгеновских кристаллографических снимков, Розалинд Франклин открыл полную структуру вируса в 1955 году.[38] В том же году, Хайнц Френкель-Конрат и Робли Уильямс показали, что очищенная РНК вируса табачной мозаики и его белковая оболочка могут собираться сами по себе с образованием функциональных вирусов, предполагая, что этот простой механизм, вероятно, был средством, с помощью которого вирусы были созданы в их клетках-хозяевах.[39]
Вторая половина 20-го века была золотым веком открытия вирусов, и большинство задокументированных видов животных, растений и бактериальных вирусов были обнаружены именно в эти годы.[40] В 1957 г. конский артеривирус и причина Диарея, вызванная вирусом крупного рогатого скота (а пестивирус ) были обнаружены. В 1963 г. вирус гепатита В был обнаружен Барух Блумберг,[41] и в 1965 г. Говард Темин описал первый ретровирус. Обратная транскриптаза, то фермент что ретровирусы используют для создания ДНК-копий своей РНК, было впервые описано в 1970 году Темином и Дэвид Балтимор независимо.[42] В 1983 г. Люк Монтанье команда в Институт Пастера во Франции был впервые выделен ретровирус, который теперь называется ВИЧ.[43] В 1989 г. Майкл Хоутон команда в Корпорация Chiron обнаруженный Гепатит С.[44][45]
Происхождение
Вирусы можно найти везде, где есть жизнь, и, вероятно, они существовали с момента появления живых клеток.[46] Происхождение вирусов неясно, потому что они не образуют окаменелостей, поэтому молекулярные методы используются для исследования того, как они возникли.[47] Кроме того, вирусный генетический материал иногда интегрируется в зародышевый организмов-хозяев, через которые они могут передаваться вертикально потомству хозяина на протяжении многих поколений. Это бесценный источник информации для палеовирологи для отслеживания древних вирусов, которые существовали миллионы лет назад. Есть три основные гипотезы, которые призваны объяснить происхождение вирусов:[48][49]
- Регрессивная гипотеза
- Вирусы, возможно, когда-то были маленькими клетками, которые паразитированный клетки большего размера. Со временем гены, не необходимые для их паразитизма, были потеряны. Бактерии риккетсия и хламидиоз являются живыми клетками, которые, как и вирусы, могут воспроизводиться только внутри клеток-хозяев. Они подтверждают эту гипотезу, поскольку их зависимость от паразитизма, вероятно, вызвала потерю генов, которые позволили им выжить вне клетки. Это также называется «гипотезой вырождения».[50][51] или «гипотеза редукции».[52]
- Гипотеза клеточного происхождения
- Некоторые вирусы могли развиться из фрагментов ДНК или РНК, которые «ускользнули» от генов более крупного организма. Ускользнувшая ДНК могла произойти из плазмиды (фрагменты голой ДНК, которые могут перемещаться между клетками) или транспозоны (молекулы ДНК, которые реплицируются и перемещаются в разные положения в генах клетки).[53] Когда-то названные «прыгающими генами», транспозоны являются примерами мобильные генетические элементы и может быть источником некоторых вирусов. Они были обнаружены в кукурузе Барбара МакКлинток в 1950 г.[54] Иногда это называют «гипотезой бродяжничества».[50][55] или «гипотеза побега».[52]
- Гипотеза коэволюции
- Это также называется «гипотеза первого вируса».[52] и предполагает, что вирусы могли развиться из сложных молекул белка и нуклеиновая кислота в то же время эти клетки впервые появились на Земле и зависели от клеточной жизни в течение миллиардов лет. Вироиды представляют собой молекулы РНК, которые не классифицируются как вирусы, поскольку у них отсутствует белковая оболочка. Они имеют характеристики, общие для нескольких вирусов, и их часто называют субвирусными агентами.[56] Вироиды - важные возбудители болезней растений.[57] Они не кодируют белки, но взаимодействуют с клеткой-хозяином и используют аппарат хозяина для своей репликации.[58] В вирус гепатита дельта человека имеет РНК геном похож на вироиды, но имеет белковую оболочку, полученную из вируса гепатита B, и не может производить свой собственный. Следовательно, это дефектный вирус. Хотя геном вируса гепатита дельта может независимо реплицироваться внутри клетки-хозяина, он требует помощи вируса гепатита В для создания белковой оболочки, чтобы он мог передаваться в новые клетки.[59] Аналогичным образом вирофаг спутника зависит от мимивирус, который заражает простейшие Акантамеба Castellanii.[60] Эти вирусы, которые зависят от присутствия других видов вирусов в клетке-хозяине, называются «спутники 'и может представлять собой промежуточные звенья эволюции вироидов и вирусов.[61][62]
В прошлом со всеми этими гипотезами были проблемы: регрессивная гипотеза не объясняла, почему даже самые маленькие клеточные паразиты никоим образом не похожи на вирусы. Гипотеза побега не объясняет сложные капсиды и другие структуры на вирусных частицах. Гипотеза о первом вирусе противоречит определению вирусов в том смысле, что они нуждаются в клетках-хозяевах.[52] Вирусы теперь признаны древними, и их происхождение предшествовало расхождению жизни в три домена.[63] Это открытие заставило современных вирусологов пересмотреть и переоценить эти три классические гипотезы.[63]
Доказательства родовой мир РНК клетки[64] а компьютерный анализ последовательностей ДНК вируса и хозяина дает лучшее понимание эволюционных взаимоотношений между различными вирусами и может помочь идентифицировать предков современных вирусов. На сегодняшний день такой анализ не доказал, какая из этих гипотез верна.[64] Кажется маловероятным, что все известные в настоящее время вирусы имеют общего предка, и вирусы, вероятно, возникали много раз в прошлом с помощью одного или нескольких механизмов.[65]
Микробиология
Свойства жизни
Научные мнения расходятся относительно того, являются ли вирусы формой жизни или органическими структурами, взаимодействующими с живыми организмами.[10] Их описывают как «организмы на грани жизни»,[9] поскольку они напоминают организмы тем, что обладают гены, развиваться естественный отбор,[66] и воспроизводить, создавая несколько своих копий путем самосборки. Хотя у них есть гены, у них нет клеточной структуры, которую часто считают основной единицей жизни. У вирусов нет своих метаболизм и требуется клетка-хозяин для производства новых продуктов. Следовательно, они не могут естественным образом воспроизводиться вне клетки-хозяина.[67]—Хотя виды бактерий, такие как риккетсия и хламидиоз считаются живыми организмами, несмотря на то же ограничение.[68][69] Принятые формы использования жизни деление клеток размножаться, тогда как вирусы спонтанно собираются внутри клеток. Они отличаются от автономный рост из кристаллы поскольку они наследуют генетические мутации, подвергаясь естественному отбору. Самосборка вируса в клетках-хозяевах имеет значение для изучения происхождение жизни, поскольку это придает дополнительную достоверность гипотезе о том, что жизнь могла начаться как самосборные органические молекулы.[2]
Структура

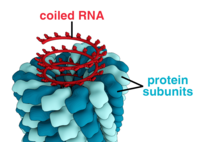


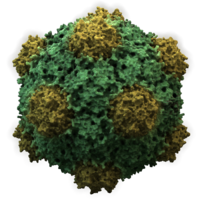
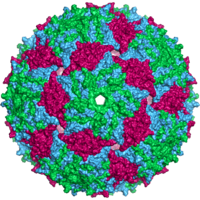
Вирусы имеют самые разные формы и размеры, называемые «морфологии '. В общем, вирусы намного меньше бактерий. Большинство изученных вирусов имеют диаметр от 20 до 300 мм. нанометры. Немного филовирусы иметь общую длину до 1400 нм; их диаметр составляет всего около 80 нм.[70] Большинство вирусов нельзя увидеть с оптический микроскоп, поэтому сканирование и передача электронные микроскопы используются для их визуализации.[71] Для увеличения контраста между вирусами и фоном используются электронно-плотные «пятна». Это решения соли тяжелых металлов, таких как вольфрам, которые рассеивают электроны из областей, покрытых пятном. Когда вирионы покрыты пятном (положительное окрашивание), мелкие детали не видны. Отрицательное окрашивание решает эту проблему, окрашивая только фон.[72]
Полная вирусная частица, известная как вирион, состоит из нуклеиновой кислоты, окруженной защитной белковой оболочкой, называемой капсид. Они образованы из идентичных белковых субъединиц, называемых капсомеры.[73] Вирусы могут иметь липид "конверт" происходит от хоста клеточная мембрана. Капсид состоит из белков, кодируемых вирусным геном а его форма служит основой для морфологического различия.[74][75] Белковые субъединицы, кодируемые вирусом, будут самоорганизовываться с образованием капсида, что обычно требует наличия вирусного генома. Сложные вирусы кодируют белки, которые помогают в построении их капсида. Белки, связанные с нуклеиновой кислотой, известны как нуклеопротеины, а ассоциация белков вирусного капсида с вирусной нуклеиновой кислотой называется нуклеокапсидом. Капсид и всю структуру вируса можно механически (физически) исследовать через атомно-силовая микроскопия.[76][77] В целом, существует четыре основных морфологических типа вирусов:
- Спиральный
- Эти вирусы состоят из одного типа капсомеров, уложенных вокруг центральной оси и образующих спиральный структура, которая может иметь центральную полость или трубку. Такое расположение приводит к образованию палочковидных или нитевидных вирионов, которые могут быть короткими и очень жесткими или длинными и очень гибкими. Генетический материал (обычно одноцепочечная РНК, но в некоторых случаях оцДНК) связывается в белковой спирали за счет взаимодействий между отрицательно заряженной нуклеиновой кислотой и положительными зарядами белка. В целом длина спирального капсида связана с длиной нуклеиновой кислоты, содержащейся в нем, а диаметр зависит от размера и расположения капсомеров. Хорошо изученный вирус табачной мозаики является примером спиралевидного вируса.[78]
- Икосаэдр
- Большинство вирусов животных являются икосаэдрическими или почти сферическими с хиральными икосаэдрическая симметрия. А правильный икосаэдр - это оптимальный способ формирования закрытой оболочки из идентичных узлов. Минимальное количество идентичных капсомеров, необходимых для каждой треугольной грани, составляет 3, что дает 60 для икосаэдра. Многие вирусы, такие как ротавирус, имеют более 60 капсомеров и имеют сферическую форму, но сохраняют эту симметрию. Для этого капсомеры на вершинах окружены пятью другими капсомерами и называются пентонами. Капсомеры на треугольных гранях окружены шестью другими и называются гексоны.[79] Гексоны в основном плоские, а пентоны, образующие 12 вершин, изогнуты. Один и тот же белок может действовать как субъединица как пентамеров, так и гексамеров, или они могут состоять из разных белков.[80]
- Пролонгировать
- Это вытянутый вдоль оси пятого порядка икосаэдр, являющийся обычным расположением головок бактериофагов. Эта конструкция состоит из цилиндра с крышками на обоих концах.[81]
- Окутанный
- Некоторые виды вирусов окутывать себя в модифицированном виде одного из клеточные мембраны, либо внешняя мембрана, окружающая инфицированную клетку-хозяин, либо внутренние мембраны, такие как ядерная мембрана или эндоплазматический ретикулум, таким образом получая внешний липидный бислой, известный как вирусный конверт. Эта мембрана усеяна белками, кодируемыми вирусным геномом и геномом хозяина; сама липидная мембрана и любые присутствующие углеводы происходят полностью от хозяина. Вирус гриппа, ВИЧ (что приводит к СПИД ), и тяжелый острый респираторный синдром коронавирус 2 (что приводит к COVID-19 )[82] используйте эту стратегию. Инфекционность большинства вирусов в оболочке зависит от оболочки.[83]
- Сложный
- Эти вирусы обладают капсидом, который не является ни чисто спиральным, ни чисто икосаэдрическим, и может иметь дополнительные структуры, такие как белковые хвосты или сложную внешнюю стенку. Некоторые бактериофаги, такие как Энтеробактерии фаг Т4, имеют сложную структуру, состоящую из головки икосаэдра, связанной со спиральным хвостом, который может иметь шестиугольник опорная пластина с выступающими белковыми волокнами хвоста. Эта структура хвоста действует как молекулярный шприц, прикрепляясь к бактериальному хозяину, а затем вводя вирусный геном в клетку.[84]
В поксвирусы представляют собой крупные сложные вирусы необычной морфологии. Вирусный геном связан с белками в центральной структуре диска, известной как нуклеоид. Нуклеоид окружен мембраной и двумя боковыми телами неизвестной функции. У вируса есть внешняя оболочка с толстым слоем белка, покрывающего ее поверхность. Весь вирион слегка плеоморфный от яйцевидной до кирпичной.[85]
Гигантские вирусы
Мимивирус является одним из самых крупных охарактеризованных вирусов с диаметром капсида 400 нм. Белковые нити размером 100 нм выступают от поверхности. Под электронным микроскопом капсид выглядит гексагональным, следовательно, капсид, вероятно, икосаэдрический.[86] В 2011 году исследователи обнаружили самый крупный на тот момент известный вирус в образцах воды, собранных со дна океана у побережья Лас-Крусес, Чили. Временно назван Мегавирус chilensis, это можно увидеть с помощью обычного оптического микроскопа.[87] В 2013 г. Пандоровирус род был обнаружен в Чили и Австралии, и его геномы примерно в два раза больше, чем у мегавирусов и мимивирусов.[88] Все гигантские вирусы имеют геномы дцДНК и подразделяются на несколько семейств: Mimiviridae, Pithoviridae, Pandoraviridae, Phycodnaviridae, и Молливирус род.[89]
Некоторые вирусы, которые заражают Археи имеют сложные структуры, не связанные с какой-либо другой формой вирусов, с широким разнообразием необычных форм, от веретенообразных структур до вирусов, напоминающих крючковидные стержни, слезинки или даже бутылки. Другие вирусы архей напоминают хвостатые бактериофаги и могут иметь несколько хвостовых структур.[90]
Геном
| Свойство | Параметры |
|---|---|
| Нуклеиновая кислота |
|
| Форма |
|
| Беспризорность |
|
| Смысл |
|
Огромное разнообразие геномных структур можно увидеть среди вирусные виды; как группа, они содержат больше структурного геномного разнообразия, чем растения, животные, археи или бактерии. Существуют миллионы различных типов вирусов,[5] хотя подробно описано менее 7000 типов.[91] По состоянию на сентябрь 2015 г. NCBI База данных вирусного генома содержит более 75000 полных последовательностей генома,[92] но, несомненно, предстоит открыть гораздо больше.[93][94]
Вирус имеет либо ДНК или РНК геном и называется ДНК-вирус или РНК-вирус, соответственно. Подавляющее большинство вирусов имеют геномы РНК. Вирусы растений обычно имеют геномы одноцепочечной РНК, а бактериофаги имеют геномы двухцепочечной ДНК.[95]
Вирусные геномы имеют круглую форму, как у полиомавирусы, или линейный, как в аденовирусы. Тип нуклеиновой кислоты не имеет отношения к форме генома. Среди РНК-вирусов и некоторых ДНК-вирусов геном часто делится на отдельные части, и в этом случае он называется сегментированным. Для РНК-вирусов каждый сегмент часто кодирует только один белок, и они обычно находятся вместе в одном капсиде. Чтобы вирус был заразным, не обязательно, чтобы все сегменты принадлежали одному и тому же вириону, как показано вирус мозаики брома и несколько других вирусов растений.[70]
Вирусный геном, независимо от типа нуклеиновой кислоты, почти всегда одноцепочечный или двухцепочечный. Одноцепочечные геномы состоят из неспаренной нуклеиновой кислоты, аналогично половине лестницы, разделенной посередине. Двухцепочечные геномы состоят из двух комплементарных парных нуклеиновых кислот, аналогично лестнице. Вирусные частицы некоторых семейств вирусов, например принадлежащих к Hepadnaviridae, содержат геном, который является частично двухцепочечным и частично одноцепочечным.[95]
Для большинства вирусов с геномами РНК и некоторых вирусов с геномами одноцепочечной ДНК одноцепочечные цепи считаются либо положительный смысл (так называемая плюсовая нить) или отрицательный смысл (называемые «минус-цепочкой»), в зависимости от того, являются ли они комплементарными вирусному информационная РНК (мРНК). Положительно-смысловая вирусная РНК имеет тот же смысл, что и вирусная мРНК, и поэтому по крайней мере часть ее может быть немедленно переведено клеткой-хозяином. Вирусная РНК с отрицательным смыслом комплементарна мРНК и, следовательно, должна быть преобразована в РНК с положительным смыслом посредством РНК-зависимая РНК-полимераза перед переводом.Номенклатура ДНК для вирусов с односмысловой геномной оцДНК аналогична номенклатуре РНК, поскольку вирусная оцДНК с положительной цепью идентична по последовательности вирусной мРНК и, таким образом, является кодирующей цепью, в то время как вирусная оцДНК с отрицательной цепью комплементарна вирусной мРНК. и, таким образом, является шаблоном.[95] Некоторые типы вирусов оцДНК и оцРНК имеют геномы, которые амбисенс в том, что транскрипция может происходить с обеих цепей в двухцепочечном репликативном промежуточном соединении. Примеры включают геминивирусы, которые представляют собой вирусы растений ssDNA и аренавирусы, которые представляют собой ssRNA вирусы животных.[96]
Размер генома
Размер генома сильно варьируется между видами. Самые маленькие - цирковирусы оцДНК, семейство Circoviridae - кодируют только два белка и имеют размер генома всего два килобаз;[97] самый большой - самый пандоровирусы - имеют размер генома около двух мегабаз, кодирующих около 2500 белков.[88] Гены вирусов редко имеют интроны и часто расположены в геноме так, что они перекрывать.[98]
В целом, РНК-вирусы имеют меньший размер генома, чем ДНК-вирусы, из-за более высокой частоты ошибок при репликации и имеют максимальный верхний предел размера.[47] Кроме того, ошибки при репликации делают вирус бесполезным или неконкурентоспособным. Чтобы компенсировать это, РНК-вирусы часто имеют сегментированные геномы - геном разделен на более мелкие молекулы, что снижает вероятность того, что ошибка в однокомпонентном геноме выведет из строя весь геном. Напротив, ДНК-вирусы обычно имеют более крупные геномы из-за высокой точности их ферментов репликации.[99] Вирусы с одноцепочечной ДНК являются исключением из этого правила, так как частота мутаций для этих геномов может приближаться к крайним значениям в случае вируса оцРНК.[100]
Генетическая мутация

Вирусы претерпевают генетические изменения по нескольким механизмам. К ним относятся процесс, называемый антигенный дрейф где отдельные основания в ДНК или РНК мутировать на другие базы. Большинство из них точечные мутации "молчаливы" - они не изменяют белок, кодируемый геном, - но другие могут давать эволюционные преимущества, такие как устойчивость к противовирусные препараты.[101][102] Антигенный сдвиг возникает, когда в геноме вируса происходят серьезные изменения. Это может быть результатом рекомбинация или же перегруппировка. Когда это происходит с вирусами гриппа, пандемии может привести.[103] РНК-вирусы часто существуют как квазивиды или скопления вирусов одного и того же вида, но с несколько разными нуклеозидными последовательностями генома. Такие квазивиды - главная цель естественного отбора.[104]
Сегментированные геномы дают эволюционные преимущества; различные штаммы вируса с сегментированным геномом могут перетасовывать и комбинировать гены и производить потомство вирусов (или потомков), которые имеют уникальные характеристики. Это называется реассортацией или «вирусным полом».[105]
Генетическая рекомбинация это процесс, при котором цепь ДНК разрывается, а затем присоединяется к концу другой молекулы ДНК. Это может произойти, когда вирусы заражают клетки одновременно и исследования вирусная эволюция показали, что рекомбинация широко распространена среди изученных видов.[106] Рекомбинация характерна как для РНК, так и для ДНК-вирусов.[107][108]
Цикл репликации
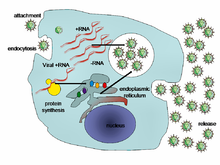
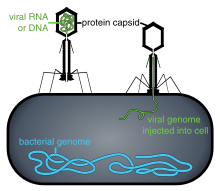
Популяции вирусов не растут путем деления клеток, потому что они бесклеточные. Вместо этого они используют механизмы и метаболизм клетки-хозяина для создания множества своих копий и собираются в клетке.[109] При заражении клетка-хозяин вынуждена быстро производить тысячи идентичных копий исходного вируса.[110]
Их жизненный цикл сильно различается между видами, но существует шесть основных этапов их жизненного цикла:[111]
Вложение представляет собой специфическое связывание между белками вирусного капсида и специфическими рецепторами на клеточной поверхности хозяина. Эта специфичность определяет круг хозяев и тип клетки-хозяина вируса. Например, ВИЧ заражает ограниченный круг людей. лейкоциты. Это потому, что его поверхностный белок, gp120, конкретно взаимодействует с CD4 молекула - а хемокиновый рецептор —Который чаще всего встречается на поверхности CD4 + Т-клетки. Этот механизм эволюционировал в пользу тех вирусов, которые инфицируют только те клетки, в которых они способны к репликации. Присоединение к рецептору может побудить белок оболочки вируса претерпеть изменения, которые приводят к слияние вирусных и клеточных мембран или изменения поверхностных белков вируса без оболочки, которые позволяют вирусу проникать.[112]
Проникновение или же вирусное проникновение следует за прикреплением: вирионы проникают в клетку-хозяина через рецептор-опосредованный эндоцитоз или же мембранный сплав. Инфекция клеток растений и грибов отличается от инфицирования клеток животных. Растения имеют жесткую клеточную стенку из целлюлоза, а грибы - один из хитина, поэтому большинство вирусов могут попасть внутрь этих клеток только после травмы клеточной стенки.[113] Почти все вирусы растений (например, вирус табачной мозаики) также могут перемещаться непосредственно от клетки к клетке в форме одноцепочечных нуклеопротеидных комплексов через поры, называемые плазмодесматы.[114] Бактерии, как и растения, имеют прочные клеточные стенки, которые вирус должен разрушить, чтобы заразить клетку. Учитывая, что стенки бактериальных клеток намного тоньше, чем стенки растительных клеток из-за их гораздо меньшего размера, некоторые вирусы развили механизмы, которые вводят свой геном в бактериальную клетку через клеточную стенку, в то время как вирусный капсид остается снаружи.[115]
Без покрытия представляет собой процесс, при котором вирусный капсид удаляется: это может происходить путем разложения вирусными ферментами или ферментами хозяина или простой диссоциацией; Конечным результатом является высвобождение вирусной геномной нуклеиновой кислоты.[116]
Репликация вирусов включает в себя прежде всего размножение генома. Репликация включает синтез вирусной информационной РНК (мРНК) из «ранних» генов (за исключением вирусов с положительной смысловой РНК), вирусной синтез белка возможна сборка вирусных белков, затем репликация вирусного генома, опосредованная ранней или регуляторной экспрессией белка. Для сложных вирусов с более крупными геномами это может сопровождаться одним или несколькими дополнительными циклами синтеза мРНК: «поздняя» экспрессия генов, как правило, связана с структурными белками или белками вириона.[117]
сборка - После структурно-опосредованной самосборки вирусных частиц часто происходит некоторая модификация белков. В вирусах, таких как ВИЧ, эта модификация (иногда называемая созреванием) происходит после того, как вирус высвобождается из клетки-хозяина.[118]
Релиз - Вирусы могут быть вышел из клетки-хозяина лизис, процесс, который убивает клетку, разрывая ее мембрану и клеточную стенку, если она присутствует: это особенность многих бактериальных вирусов и некоторых вирусов животных. Некоторые вирусы подвергаются лизогенный цикл где вирусный геном включен генетическая рекомбинация в определенное место в хромосоме хозяина. Вирусный геном тогда известен как "провирус "или, в случае бактериофагов а"профаг ".[119] Когда хозяин делится, вирусный геном также реплицируется. Вирусный геном в основном молчит внутри хозяина. В какой-то момент провирус или профаг может дать начало активному вирусу, который может лизировать клетки-хозяева.[120] Оболочечные вирусы (например, ВИЧ) обычно высвобождаются из клетки-хозяина подающий надежды. Во время этого процесса вирус приобретает свою оболочку, которая представляет собой модифицированный кусок плазмы хозяина или другой внутренней мембраны.[121]
Репликация генома
Генетический материал внутри вирусных частиц и метод репликации этого материала значительно различаются для разных типов вирусов.
- ДНК-вирусы
- Репликация генома большинства ДНК-вирусы происходит в камере ядро. Если клетка имеет соответствующий рецептор на своей поверхности, эти вирусы проникают в клетку либо путем прямого слияния с клеточной мембраной (например, герпесвирусы), либо - чаще - посредством рецептор-опосредованного эндоцитоза. Большинство ДНК-вирусов полностью зависят от оборудования клетки-хозяина, синтезирующего ДНК и РНК, и оборудования для обработки РНК. Вирусы с более крупными геномами могут сами кодировать большую часть этого механизма. У эукариот вирусный геном должен пересечь ядерную мембрану клетки, чтобы получить доступ к этому механизму, тогда как у бактерий ему нужно только проникнуть в клетку.[122]
- РНК-вирусы
- Репликация РНК-вирусы обычно происходит в цитоплазма. РНК-вирусы можно разделить на четыре разные группы в зависимости от способа их репликации. В полярность (может ли он использоваться непосредственно рибосомами для производства белков) одноцепочечных РНК-вирусов в значительной степени определяет репликативный механизм; другим важным критерием является то, является ли генетический материал одноцепочечным или двухцепочечным. Все РНК-вирусы используют свои собственные РНК-репликаза ферменты для создания копий своих геномов.[123]
- Обратная транскрипция вирусов
- Обратная транскрипция вирусов имеют оцРНК (Retroviridae, Metaviridae, Псевдовирусы ) или дцДНК (Caulimoviridae, и Hepadnaviridae ) в своих частицах. Обратная транскрипция вирусов с геномами РНК (ретровирусы ) используют промежуточный ДНК для репликации, тогда как те, у кого есть ДНК-геномы (параретровирусы ) использовать промежуточную РНК во время репликации генома. Оба типа используют обратная транскриптаза или фермент РНК-зависимая ДНК-полимераза, чтобы осуществить превращение нуклеиновой кислоты. Ретровирусы интегрируют ДНК, продуцируемую обратная транскрипция в геном хозяина в виде провируса в процессе репликации; параретровирусы этого не делают, хотя интегрированные копии генома, особенно параретровирусов растений, могут давать начало инфекционному вирусу.[124] Они восприимчивы к противовирусные препараты которые ингибируют фермент обратной транскриптазы, например зидовудин и ламивудин. Примером первого типа является ВИЧ, который является ретровирусом. Примеры второго типа: Hepadnaviridae, который включает вирус гепатита В.[125]
Цитопатические эффекты на клетку-хозяина
Диапазон структурных и биохимических эффектов, которые вирусы оказывают на клетку-хозяина, обширен.[126] Они называются 'цитопатические эффекты '.[127] Большинство вирусных инфекций в конечном итоге приводит к гибели клетки-хозяина. Причины смерти включают лизис клеток, изменения поверхностной мембраны клетки и апоптоз.[128] Часто смерть клетки вызывается прекращением ее нормальной деятельности из-за подавления вирус-специфическими белками, не все из которых являются компонентами вирусной частицы.[129] Различие между цитопатическим и безвредным проводится постепенно. Некоторые вирусы, например Вирус Эпштейна-Барра, может вызывать размножение клеток, не вызывая злокачественных новообразований,[130] в то время как другие, такие как папилломавирусы, являются установленными причинами рака.[131]
Спящие и латентные инфекции
Некоторые вирусы не вызывают видимых изменений в инфицированной клетке. Клетки, в которых находится вирус скрытый и неактивные проявляют мало признаков инфекции и часто функционируют нормально.[132] Это вызывает стойкие инфекции, и вирус часто бездействует в течение многих месяцев или лет. Это часто бывает с вирусы герпеса.[133][134]
Диапазон хостов
Вирусы на сегодняшний день являются самыми многочисленными биологическими объектами на Земле, и они превосходят по численности все остальные вместе взятые.[135] Они заражают все виды клеточной жизни, включая животных, растения, бактерии и грибы.[91] Различные типы вирусов могут инфицировать только ограниченный круг хозяев, и многие из них видоспецифичны. Некоторые, например вирус оспы например, может заразить только один вид - в данном случае людей,[136] и, как говорят, имеют узкую диапазон хостов. Другие вирусы, такие как вирус бешенства, могут инфицировать различные виды млекопитающих и, как говорят, имеют широкий спектр.[137] Вирусы, поражающие растения, безвредны для животных, а большинство вирусов, поражающих других животных, безвредны для человека.[138] Диапазон хозяев некоторых бактериофагов ограничен одним напряжение бактерий, и их можно использовать для отслеживания источника вспышек инфекций методом, называемым фаговое типирование.[139] Полный набор вирусов в организме или среде обитания называется виром; например, все человеческие вирусы составляют человеческий виром.[140]
Классификация
Классификация направлена на описание разнообразия вирусов путем присвоения им имен и группировки на основе сходства. В 1962 г. Андре Львофф, Роберт Хорн и Поль Турнье первыми разработали средства классификации вирусов на основе Линнеевский иерархическая система.[141] Эта система основана на классификации филюм, учебный класс, порядок, семья, род, и разновидность. Вирусы были сгруппированы согласно их общим свойствам (не свойствам их хозяев) и типу нуклеиновой кислоты, образующей их геномы.[142] В 1966 г. Международный комитет по таксономии вирусов (ICTV) была создана. Система, предложенная Lwoff, Horne и Tournier, изначально не была принята ICTV, потому что небольшой размер генома вирусов и их высокая скорость мутации затрудняли определение их предков вне порядка. Таким образом, Балтиморская классификация Система стала использоваться для дополнения более традиционной иерархии.[143] Начиная с 2018 года, ICTV начал признавать более глубокие эволюционные связи между вирусами, которые были обнаружены с течением времени, и принял 15-ранговую систему классификации, варьирующуюся от области к виду.[144]
Классификация ICTV
ICTV разработала текущую систему классификации и написала руководящие принципы, в которых большее значение придается определенным свойствам вируса для сохранения однородности семейства. Создана единая таксономия (универсальная система классификации вирусов). Из всего разнообразия вирусов изучена лишь небольшая часть.[145] По состоянию на 2019 год, 4 царства, 9 царств, 16 типов, 2 подтипа, 36 классов, 55 порядков, 8 подотрядов, 168 семей, 103 подсемейства, 1421 род, 68 подродов, и 6589 видов вирусов были определены ICTV.[4]
Общая таксономическая структура ареалов таксонов и суффиксы, используемые в таксономических названиях, показаны ниже. По состоянию на 2019 год ранги субрегиона, субцарства и подкласса не используются, тогда как все остальные ранги используются.
- Область (-вирия)
- Подобласть (-вира)
- Королевство (-виры)
- Подцарство (-вириты)
- Тип (-viricota)
- Подтип (-вирикотина)
- Учебный класс (-viricetes)
- Подтип (-вирикотина)
- Тип (-viricota)
- Подцарство (-вириты)
- Королевство (-виры)
- Подобласть (-вира)
Балтиморская классификация

Биолог, лауреат Нобелевской премии Дэвид Балтимор разработал Балтиморская классификация система.[42][146] Система классификации ICTV используется вместе с системой классификации Балтимора в современной классификации вирусов.[147][148][149]
Балтиморская классификация вирусов основана на механизме мРНК производство. Вирусы должны генерировать мРНК из своих геномов, чтобы производить белки и воспроизводить себя, но в каждом семействе вирусов для этого используются разные механизмы. Вирусные геномы могут быть одноцепочечными (ss) или двухцепочечными (ds), РНК или ДНК и могут использовать или не использовать обратная транскриптаза (RT). Кроме того, вирусы ssRNA могут быть либо смысл (+) или антисмысловой (-). Эта классификация делит вирусы на семь групп:
- Я: вирусы дцДНК (например. Аденовирусы, Герпесвирусы, Поксвирусы )
- II: ssDNA вирусы (+ цепь или "смысл") ДНК (например, Парвовирусы )
- III: дцРНК вирусы (например. Реовирусы )
- IV: (+) ssRNA вирусы (+ цепь или смысловая) РНК (например, Коронавирусы, Пикорнавирусы, Тогавирусы )
- V: (-) ssRNA вирусы (- цепь или антисмысловая) РНК (например, Ортомиксовирусы, Рабдовирусы )
- VI: ssRNA-RT вирусы (+ цепь или смысловая) РНК с промежуточной ДНК в жизненном цикле (например, Ретровирусы )
- VII: dsDNA-RT вирусы ДНК с промежуточной РНК в жизненном цикле (например, Гепаднавирусы )
Роль в заболевании человека

Примеры распространенных заболеваний человека, вызываемых вирусами, включают: простуда, грипп, ветряная оспа, и герпес. Многие серьезные заболевания, такие как бешенство, Болезнь, вызванная вирусом Эбола, СПИД (ВИЧ), птичий грипп, и ОРВИ вызваны вирусами. Относительная способность вирусов вызывать болезнь описывается с точки зрения вирулентность. Другие заболевания исследуются, чтобы определить, есть ли у них вирус в качестве возбудителя, например, возможная связь между вирус герпеса человека 6 (HHV6) и неврологические заболевания, такие как рассеянный склероз и Синдром хронической усталости.[151] Есть споры о том, борнавирус, ранее считалось причиной неврологический заболевания лошадей, могут быть ответственны за психиатрический болезни у человека.[152]
У вирусов есть разные механизмы, с помощью которых они вызывают заболевание в организме, что в значительной степени зависит от вида вируса. Механизмы на клеточном уровне в первую очередь включают лизис клеток, вскрытие и последующую гибель клетки. В многоклеточные организмы, если погибнет достаточно клеток, весь организм начнет страдать от последствий. Хотя вирусы вызывают нарушение здорового гомеостаз приводя к заболеванию, они могут относительно безвредно существовать в организме. Примером может быть способность Вирус простого герпеса, который вызывает герпес, остается в организме человека в спящем состоянии. Это называется задержкой[153] и является характеристикой вирусов герпеса, в том числе вируса Эпштейна-Барра, вызывающего железистую лихорадку, и вирус ветряной оспы, вызывающий ветряную оспу и опоясывающий лишай. Большинство людей были инфицированы хотя бы одним из этих типов вируса герпеса.[154] Эти латентные вирусы иногда могут быть полезными, поскольку присутствие вируса может повысить иммунитет против бактериальных патогенов, таких как Yersinia pestis.[155]
Некоторые вирусы могут вызывать пожизненное или хронический инфекции, при которых вирусы продолжают размножаться в организме, несмотря на защитные механизмы хозяина.[156] Это обычное явление при вирусных инфекциях гепатита В и гепатита С. Хронически инфицированные люди известны как носители, поскольку они служат резервуарами инфекционного вируса.[157] В популяциях с высокой долей носителей заболевание считается эндемичный.[158]
Эпидемиология
Популярный эпидемиология это отрасль медицинской науки, которая занимается передачей вирусных инфекций среди людей и борьбой с ними. Передача вирусов может быть вертикальной, что означает от матери к ребенку, или горизонтальной, что означает от человека к человеку. Примеры вертикальная передача включают вирус гепатита В и ВИЧ, когда ребенок рождается уже инфицированным этим вирусом.[159] Другой, более редкий пример - вирус ветряной оспы, который, хотя и вызывает относительно легкие инфекции у детей и взрослых, может быть фатальным для плода и новорожденного.[160]
Горизонтальная передача является наиболее частым механизмом распространения вирусов в популяциях.[161] Горизонтальная передача может происходить при обмене жидкостями организма во время сексуальной активности, при обмене слюной или при проглатывании зараженной пищи или воды. Это также может произойти, когда аэрозоли содержащие вирусы вдыхаются или насекомыми векторов например, когда инфицированные комары проникают через кожу хозяина.[161] Большинство типов вирусов ограничены одним или двумя из этих механизмов, и их называют «респираторными вирусами» или «кишечными вирусами» и так далее. Скорость или скорость передачи вирусных инфекций зависит от факторов, которые включают плотность населения, количество восприимчивых людей (т.е. тех, кто не имеет иммунитета),[162] качество здравоохранения и погода.[163]
Эпидемиология используется для разрыва цепи заражения населения во время вспышек вирусные заболевания.[164] Используются меры контроля, основанные на знании того, как передается вирус. Важно найти источник или источники вспышки и идентифицировать вирус. После идентификации вируса цепь передачи иногда может быть прервана вакцинами. Когда вакцины недоступны, санитария и дезинфекция могут быть эффективными. Часто инфицированные люди изолированы от остальной части сообщества, а те, кто подвергся воздействию вируса, помещаются в карантин.[165] Чтобы контролировать вспышка из ящур в Великобритании в 2001 году были забиты тысячи голов крупного рогатого скота.[166] Большинство вирусных инфекций человека и других животных имеют инкубационные периоды во время которого инфекция не вызывает никаких признаков или симптомов.[167] Инкубационные периоды вирусных заболеваний составляют от нескольких дней до недель, но известны для большинства инфекций.[168] В некоторой степени частично совпадающий, но в основном следующий за инкубационным периодом, существует период передачи информации - время, когда инфицированный человек или животное заразны и могут заразить другого человека или животное.[168] Это также известно для многих вирусных инфекций, и знание продолжительности обоих периодов важно для борьбы со вспышками.[169] Когда вспышки вызывают необычно высокую долю случаев в популяции, сообществе или регионе, они называются эпидемиями. Если вспышки распространяются по всему миру, их называют пандемии.[170]
Эпидемии и пандемии
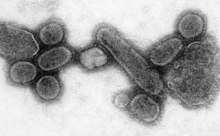
А пандемия всемирный эпидемия. В Пандемия гриппа 1918 года, которая просуществовала до 1919 г., была категория 5 пандемия гриппа, вызванная необычно тяжелым и смертельным вирусом гриппа А. Жертвами часто становились здоровые молодые люди, в отличие от большинства вспышек гриппа, от которых в основном страдают подростки, пожилые или ослабленные иным образом пациенты.[171] По старым оценкам, в результате этого погибло 40–50 миллионов человек,[172] в то время как более поздние исследования показывают, что в 1918 году он мог убить до 100 миллионов человек, или 5% населения мира.[173]
Хотя вирусные пандемии - явление редкое, ВИЧ, который произошел от вирусов, обнаруженных у обезьян и шимпанзе, является пандемией по крайней мере с 1980-х годов.[174] В течение 20 века было четыре пандемии, вызванных вирусом гриппа, и те, что произошли в 1918, 1957 и 1968 годах, были серьезными.[175] Большинство исследователей считают, что ВИЧ возник в К югу от Сахары в течение 20 века;[176] сейчас это пандемия, и, по оценкам, 37,9 миллиона человек во всем мире живут с этим заболеванием.[177] В 2018 году от СПИДа умерло около 770 тысяч человек.[178] В Объединенная программа Организации Объединенных Наций по ВИЧ / СПИДу (ЮНЭЙДС) и Всемирная организация здоровья По оценкам ВОЗ, СПИД унес жизни более 25 миллионов человек с момента его первого обнаружения 5 июня 1981 года, что делает его одной из самых разрушительных эпидемий в истории человечества.[179] В 2007 году было зарегистрировано 2,7 миллиона новых случаев инфицирования ВИЧ и 2 миллиона случаев смерти, связанных с ВИЧ.[180]


Несколько высоколетальных вирусных патогенов являются членами Filoviridae. Филовирусы - это филаментные вирусы, вызывающие вирусная геморрагическая лихорадка, и включать эболавирусы и марбургвирусы. Марбургский вирус, впервые обнаруженный в 1967 г., привлек внимание широкой прессы в апреле 2005 г. из-за вспышки в Ангола.[181] Болезнь, вызванная вирусом Эбола также вызвал периодические вспышки с высоким уровнем смертности с 1976 г., когда он был впервые обнаружен. Самый худший и последний - 2013–2016 гг. Эпидемия в Западной Африке.[182]
За исключением оспы, большинство пандемий вызывается недавно появившимися вирусами. Эти "возникающий" вирусы обычно являются мутантами менее вредных вирусов, которые ранее циркулировали либо у людей, либо у других животных.[183]
Острое респираторное заболевание (ОРВИ ) и Ближневосточный респираторный синдром (MERS) вызваны новыми типами коронавирусы. Известно, что другие коронавирусы вызывают легкие инфекции у людей,[184] поэтому вирулентность и быстрое распространение инфекций SARS, которые к июлю 2003 года вызвали около 8000 случаев заболевания и 800 смертей, были неожиданными, и большинство стран не были готовы к этому.[185]
Связанный с этим коронавирус появился в Ухань, Китай в ноябре 2019 года и стремительно распространился по миру. Считается, что произошел от летучих мышей и впоследствии назван тяжелый острый респираторный синдром коронавирус 2, заражение вирусом вызвало пандемия в 2020 году.[186][187][188] В мирное время были введены беспрецедентные ограничения на международные поездки,[189] и комендантский час наложен в нескольких крупных городах мира.[190]
Рак
Вирусы являются признанной причиной рака у людей и других видов. Вирусный рак встречается только у меньшинства инфицированных людей (или животных). Раковые вирусы происходят из ряда семейств вирусов, включая РНК- и ДНК-вирусы, поэтому не существует единого типа вирусов "онковирус "(устаревший термин, первоначально использовавшийся для острой трансформации ретровирусов). Развитие рака определяется множеством факторов, например иммунитетом хозяина.[191] и мутации в хозяине.[192] Вирусы, признанные причиной рака человека, включают некоторые генотипы вирус папилломы человека, вирус гепатита В, вирус гепатита С, Вирус Эпштейна-Барра, Вирус герпеса, связанный с саркомой Капоши и человеческий Т-лимфотропный вирус. Самым недавно обнаруженным вирусом рака человека является полиомавирус (Полиомавирус клеток Меркеля ), который вызывает большинство случаев редкой формы рака кожи, называемой Карцинома из клеток Меркеля.[193]Вирусы гепатита могут перерасти в хроническую вирусную инфекцию, которая приводит к рак печени.[194][195] Заражение Т-лимфотропным вирусом человека может привести к тропический спастический парапарез и Т-клеточный лейкоз взрослых.[196] Вирусы папилломы человека являются признанной причиной рака шейка матки, кожа, анус, и пенис.[197] В рамках Herpesviridae, Вирус герпеса, связанный с саркомой Капоши причины Саркома Капоши и лимфома полости тела, и вирус Эпштейна-Барра вызывает Лимфома Беркитта, Лимфома Ходжкина, B лимфопролиферативное заболевание, и карцинома носоглотки.[198] Полиомавирус клеток Меркеля, тесно связанный с SV40 и мышиные полиомавирусы, которые использовались в качестве животных моделей для онкологических вирусов более 50 лет.[199]
Защитные механизмы хозяина
Первая линия защиты организма от вирусов - это врожденная иммунная система. Сюда входят клетки и другие механизмы, которые неспецифическим образом защищают хозяина от инфекции. Это означает, что клетки врожденной системы распознают патогены и реагируют на них обычным образом, но, в отличие от адаптивная иммунная система, он не наделяет хозяина длительным или защитным иммунитетом.[200]
РНК-интерференция является важной врожденной защитой от вирусов.[201] Многие вирусы имеют стратегию репликации, которая включает двухцепочечную РНК (дцРНК). Когда такой вирус заражает клетку, он высвобождает ее молекулу или молекулы РНК, которые немедленно связываются с белковым комплексом, называемым белком. dicer который разрезает РНК на более мелкие части. Биохимический путь - RISC комплекс - активируется, что обеспечивает выживание клеток за счет разрушения вирусной мРНК. Ротавирусы эволюционировали, чтобы избежать этого защитного механизма, поскольку они не полностью покрываются оболочкой внутри клетки и высвобождают вновь продуцируемую мРНК через поры внутреннего капсида частицы. Их геномная дцРНК остается защищенной внутри ядра вириона.[202][203]
Когда адаптивная иммунная система из позвоночное животное встречает вирус, он производит специфические антитела которые связываются с вирусом и часто делают его неинфекционным. Это называется гуморальный иммунитет. Важны два типа антител. Первый, названный IgM, очень эффективно нейтрализует вирусы, но вырабатывается клетками иммунной системы только в течение нескольких недель. Второй, названный IgG, производится на неопределенный срок. Присутствие IgM в крови хозяина используется для проверки на острую инфекцию, тогда как IgG указывает на инфекцию когда-то в прошлом.[204] Антитела IgG измеряются при тестировании на иммунитет осуществляются.[205]
Антитела могут оставаться эффективным механизмом защиты даже после того, как вирусам удалось проникнуть в клетку-хозяин. Белок, который находится в клетках, называется TRIM21, могут прикрепляться к антителам на поверхности вирусной частицы. Это способствует последующему уничтожению вируса ферментами клетки. протеосома система.[206]
Вторая защита позвоночных от вирусов называется клеточный иммунитет и включает в себя иммунные клетки, известные как Т-клетки. Клетки организма постоянно демонстрируют короткие фрагменты своих белков на поверхности клетки, и, если Т-клетка распознает там подозрительный вирусный фрагмент, клетка-хозяин разрушается «Т-киллерами», и вирус-специфические Т-клетки размножаются. Ячейки, такие как макрофаг специалисты в этом презентация антигена.[207] Производство интерферон является важным механизмом защиты хозяина. Это гормон, вырабатываемый организмом при наличии вирусов. Его роль в иммунитете сложна; в конечном итоге он останавливает размножение вирусов, убивая инфицированную клетку и ее ближайших соседей.[208]
Не все вирусные инфекции вызывают таким образом защитный иммунный ответ. ВИЧ ускользает от иммунной системы, постоянно меняя аминокислотную последовательность белков на поверхности вириона. Это известно как «ускользающая мутация», поскольку вирусные эпитопы ускользают от распознавания иммунным ответом хозяина. Эти стойкие вирусы ускользают от иммунного контроля путем секвестрации, блокады презентация антигена, цитокин сопротивление, уклонение от естественная клетка-убийца деятельность, побег из апоптоз, и антигенный сдвиг.[209] Другие вирусы, называемые 'нейротропные вирусы ', распространяются посредством нейронального распространения, где иммунная система может быть не в состоянии до них добраться.
Профилактика и лечение
Поскольку вирусы используют жизненно важные метаболические пути в клетках-хозяевах для репликации, их трудно устранить без использования лекарств, которые оказывают токсическое действие на клетки-хозяева в целом. Наиболее эффективные медицинские подходы к вирусным заболеваниям: прививки обеспечить иммунитет к инфекции, и противовирусные препараты которые избирательно препятствуют репликации вируса.
Вакцина
Вакцинация - дешевый и эффективный способ предотвращения заражения вирусами. Вакцины использовались для предотвращения вирусных инфекций задолго до открытия настоящих вирусов. Их использование привело к резкому снижению заболеваемости (заболеваемости) и смертности (смерти), связанных с вирусными инфекциями, такими как полиомиелит, корь, свинка и краснуха.[210] Оспа инфекции были искоренены.[211] Доступны вакцины для предотвращения более тринадцати вирусных инфекций человека,[212] и многое другое используются для предотвращения вирусных инфекций животных.[213] Вакцины могут состоять из живых аттенуированных или убитых вирусов или вирусных белков (антигены ).[214] Живые вакцины содержат ослабленные формы вируса, которые не вызывают заболевания, но, тем не менее, придают иммунитет. Такие вирусы называют аттенуированными. Живые вакцины могут быть опасны, если их вводить людям со слабым иммунитетом (которые описаны как с ослабленным иммунитетом ), потому что у этих людей ослабленный вирус может вызвать первоначальное заболевание.[215] Для производства субъединичных вакцин используются методы биотехнологии и генной инженерии. В этих вакцинах используются только капсидные белки вируса. Вакцина против гепатита B является примером вакцины этого типа.[216] Субъединичные вакцины безопасны для с ослабленным иммунитетом пациенты, потому что они не могут вызвать болезнь.[217] В вакцина против вируса желтой лихорадки живой аттенуированный штамм 17D, вероятно, является самой безопасной и эффективной вакциной из когда-либо созданных.[218]
Противовирусные препараты
Противовирусные препараты часто аналоги нуклеозидов (поддельные строительные блоки ДНК), которые вирусы по ошибке включают в свои геномы во время репликации. Затем жизненный цикл вируса останавливается, поскольку вновь синтезированная ДНК неактивна. Это потому, что у этих аналогов отсутствует гидроксил группы, которые вместе с фосфор атомы соединяются вместе, образуя прочный «каркас» молекулы ДНК. Это называется ДНК обрыв цепи.[219] Примеры аналогов нуклеозидов: ацикловир при инфекциях, вызванных вирусом простого герпеса, и ламивудин на инфекции, вызванные вирусом ВИЧ и гепатита В. Ацикловир - один из старейших и наиболее часто назначаемых противовирусных препаратов.[220]Другие применяемые противовирусные препараты нацелены на разные стадии жизненного цикла вируса. ВИЧ зависит от протеолитического фермента, называемого Протеаза ВИЧ-1 чтобы он стал полностью заразным. Существует большой класс препаратов, называемых ингибиторы протеазы которые инактивируют этот фермент.[221]
Гепатит С вызывается РНК-вирусом. У 80% инфицированных людей болезнь носит хронический характер, и без лечения они зараженный до конца своей жизни. В настоящее время существует эффективное лечение, в котором используется лекарственный аналог нуклеозидов. рибавирин в сочетании с интерферон.[222] Лечение хронических перевозчики вируса гепатита B с использованием аналогичной стратегии с использованием ламивудина.[223]
Заражение другими видами
Вирусы заражают всю клеточную жизнь, и, хотя вирусы встречаются повсеместно, у каждого вида клеток есть свой специфический диапазон, который часто заражает только этот вид.[224] Некоторые вирусы, называемые спутники, могут реплицироваться только внутри клеток, которые уже были инфицированы другим вирусом.[60]
Вирусы животных
Вирусы - важные патогенные микроорганизмы домашнего скота. Заболевания, такие как ящур и блютанга вызваны вирусами.[225] Животные-компаньоны, такие как кошки, собаки и лошади, если не вакцинированы, восприимчивы к серьезным вирусным инфекциям. Парвовирус собак вызывается небольшим вирусом ДНК, и инфекции у щенков часто заканчиваются смертельным исходом.[226] Как все беспозвоночные медоносная пчела восприимчива ко многим вирусным инфекциям.[227] Большинство вирусов безвредно сосуществуют в своем хозяине и не вызывают признаков или симптомов болезни.[3]
Вирусы растений

Есть много типов вирусов растений, но часто они вызывают только потерю урожай, и пытаться их контролировать экономически нецелесообразно. Вирусы растений часто передаются с растения на растение организмами, известными как векторов. Обычно это насекомые, но некоторые грибы, нематоды черви, и одноклеточные организмы было показано, что это векторы. Когда борьба с вирусными инфекциями растений считается экономичной, например, для многолетних плодов, усилия концентрируются на уничтожении переносчиков и удалении альтернативных хозяев, таких как сорняки.[228] Вирусы растений не могут инфицировать людей и других животных, потому что они могут воспроизводиться только в живых клетках растений.[229]
Родом из Перу, картофель стал основной культурой во всем мире.[230] В картофельный вирус Y вызывает болезни у картофеля и родственных ему видов, включая помидоры и перец. В 1980-х годах этот вирус приобрел экономическое значение, когда оказалось, что с ним трудно бороться с посевами семенного картофеля. Передано тля, этот вирус может снизить урожайность сельскохозяйственных культур на 80 процентов, что приведет к значительным потерям урожая картофеля.[231]
У растений есть продуманные и эффективные механизмы защиты от вирусов. Одним из наиболее эффективных является наличие так называемых генов устойчивости (R). Каждый ген R придает устойчивость к определенному вирусу, вызывая локальные области гибели клеток вокруг инфицированной клетки, которые часто можно увидеть невооруженным глазом в виде больших пятен. Это останавливает распространение инфекции.[232] РНК-интерференция также является эффективной защитой растений.[233] Когда они заражены, растения часто производят натуральные дезинфицирующие средства, убивающие вирусы, например салициловая кислота, оксид азота, и реактивные молекулы кислорода.[234]
Частицы вирусов растений или вирусоподобные частицы (VLP) могут применяться как в биотехнология и нанотехнологии. Капсиды большинства вирусов растений представляют собой простые и надежные структуры и могут продуцироваться в больших количествах либо путем инфицирования растений, либо путем экспрессии в различных гетерологичных системах. Частицы вируса растений могут быть модифицированы генетически и химически, чтобы инкапсулировать чужеродный материал, и могут быть включены в супрамолекулярные структуры для использования в биотехнологии.[235]
Бактериальные вирусы

Бактериофаги представляют собой обычную и разнообразную группу вирусов и являются наиболее распространенным биологическим организмом в водной среде - этих вирусов в океанах в десять раз больше, чем бактерий,[236] достигая уровня 250 000 000 бактериофагов на миллилитр морской воды.[237] Эти вирусы заражают определенные бактерии, связываясь с молекулы поверхностных рецепторов а затем вход в камеру. За короткий промежуток времени, в некоторых случаях всего за несколько минут, бактериальный полимераза начинает транслировать вирусную мРНК в белок. Эти белки становятся либо новыми вирионами внутри клетки, либо вспомогательными белками, которые помогают сборке новых вирионов, либо белками, участвующими в лизисе клетки. Вирусные ферменты способствуют разрушению клеточной мембраны, а в случае Фаг Т4, всего за двадцать минут после инъекции может высвободиться более трехсот фагов.[238]
Основной способ защиты бактерий от бактериофагов - выработка ферментов, разрушающих чужеродную ДНК. Эти ферменты, называемые эндонуклеазы рестрикции, разрезать вирусную ДНК, которую бактериофаги вводят в бактериальные клетки.[239] Бактерии также содержат систему, которая использует CRISPR последовательности для сохранения фрагментов геномов вирусов, с которыми бактерии контактировали в прошлом, что позволяет им блокировать репликацию вируса с помощью формы РНК-интерференция.[240][241] Эта генетическая система обеспечивает бактерии приобретенный иммунитет к инфекции.[242]
Вирусы архей
Некоторые вирусы размножаются внутри археи: это двухцепочечные ДНК-вирусы необычной, а иногда и уникальной формы.[6][90] Эти вирусы наиболее подробно изучены в теплолюбивый архей, особенно отряды Sulfolobales и Thermoproteales.[243] Защита от этих вирусов включает вмешательство РНК со стороны повторяющаяся ДНК последовательности в геномах архей, которые связаны с генами вирусов.[244][245] Большинство архей имеют системы CRISPR – Cas в качестве адаптивной защиты от вирусов. Это позволяет архее сохранять участки вирусной ДНК, которые затем используются для нацеливания и устранения последующих заражений вирусом с использованием процесса, аналогичного вмешательству РНК.[246]
Роль в водных экосистемах
Вирусы являются наиболее распространенным биологическим объектом в водной среде.[2] Их около десяти миллионов в чайной ложке морской воды.[247] Большинство этих вирусов бактериофаги заражение гетеротрофных бактерий и цианофаги заражают цианобактерии, и они необходимы для регулирования морских и пресноводных экосистем.[248]Бактериофаги безвредны для растений и животных и необходимы для регулирования морских и пресноводных экосистем.[249] являются важными факторами смертности фитопланктон, основа пищевая цепочка в водных средах.[250] Они заражают и уничтожают бактерии в водных микробных сообществах и являются одним из важнейших механизмов переработка углерода круговорот питательных веществ в морской среде. Органические молекулы, высвобождаемые из мертвых бактериальных клеток, стимулируют рост свежих бактерий и водорослей в процессе, известном как вирусный шунт.[251] В частности, было показано, что лизис бактерий вирусами усиливает круговорот азота и стимулирует рост фитопланктона.[252] Вирусная активность также может влиять на биологический насос, процесс, посредством которого углерод является изолирован в глубоком океане.[253]
Микроорганизмы составляют более 90% биомассы моря. Подсчитано, что вирусы убивают приблизительно 20% этой биомассы каждый день и что в океанах в 10-15 раз больше вирусов, чем бактерий и архей.[254] Вирусы также являются основными агентами, ответственными за разрушение фитопланктон включая вредоносное цветение водорослей,[255]Количество вирусов в океанах уменьшается дальше от берега и глубже в воду, где меньше организмов-хозяев.[253]
В январе 2018 года ученые сообщили, что 800 миллионов вирусов, в основном морского происхождения, ежедневно депонируются из земной шарс атмосфера на каждый квадратный метр поверхности планеты в результате глобального атмосферного потока вирусов, циркулирующих над погодной системой, но ниже высоты обычных авиаперелетов, распространяющих вирусы по планете.[256][257]
Как любой организм, морские млекопитающие подвержены вирусным инфекциям. В 1988 и 2002 годах тысячи портовые тюлени были убиты в Европе вирус чумки фосин.[258] Многие другие вирусы, в том числе калицивирусы, герпесвирусы, аденовирусы и парвовирусы, циркулируют в популяциях морских млекопитающих.[253]
Роль в эволюции
Вирусы являются важным естественным средством передачи генов между разными видами, что увеличивает генетическое разнообразие и движет эволюцией.[8] Считается, что вирусы играли центральную роль в ранней эволюции, до того, как произошла диверсификация последний универсальный общий предок в бактерии, археи и эукариоты.[259] Вирусы по-прежнему являются одним из крупнейших резервуаров неизведанного генетического разнообразия на Земле.[253]
Приложения
Науки о жизни и медицина

Вирусы важны для изучения молекулярный и клеточная биология поскольку они предоставляют простые системы, которые можно использовать для манипулирования и исследования функций клеток.[260] Изучение и использование вирусов дало ценную информацию об аспектах клеточной биологии.[261] Например, вирусы были полезны при изучении генетика и помогли нам понять основные механизмы молекулярная генетика, Такие как Репликация ДНК, транскрипция, Обработка РНК, перевод, белок транспорт и иммунология.
Генетики часто используют вирусы как векторов ввести гены в клетки, которые они изучают. Это полезно для того, чтобы заставить клетку производить чужеродное вещество или для изучения эффекта от введения нового гена в геном. Аналогичным образом виротерапия использует вирусы в качестве векторов для лечения различных заболеваний, поскольку они могут специфически нацеливаться на клетки и ДНК. Он показывает многообещающее использование при лечении рака и генная терапия. Ученые из Восточной Европы использовали фаговая терапия в качестве альтернативы антибиотикам в течение некоторого времени, и интерес к этому подходу растет из-за высокого уровня устойчивость к антибиотикам теперь обнаружен у некоторых болезнетворных бактерий.[262]Экспрессия гетерологичных белков вирусами является основой нескольких производственных процессов, которые в настоящее время используются для производства различных белков, таких как вакцины. антигены и антитела. Недавно были разработаны промышленные процессы с использованием вирусных векторов, и ряд фармацевтических белков в настоящее время проходят доклинические и клинические испытания.[263]
Виротерапия
Виротерапия предполагает использование генетически модифицированных вирусов для лечения заболеваний.[264] Ученые модифицировали вирусы, чтобы они воспроизводились в раковых клетках и уничтожали их, но не заражали здоровые клетки. Талимоген лахерпарепвец (T-VEC), например, является модифицированным Вирус простого герпеса который имеет ген, необходимый для репликации вирусов в здоровых клетках, удален и заменен человеческим геном (GM-CSF ), что стимулирует иммунитет. Когда этот вирус заражает раковые клетки, он их уничтожает, и при этом присутствие гена GM-CSF привлекает дендритные клетки из окружающих тканей тела. Дендритные клетки обрабатывают мертвые раковые клетки и представляют их компоненты другим клеткам иммунная система.[265] Завершив успешно клинические испытания, вирус получил одобрение для лечения меланома в конце 2015 года.[266] Вирусы, которые были перепрограммированы так, чтобы убивать раковые клетки, называются онколитические вирусы.[267]
Материаловедение и нанотехнологии
Современные тенденции в нанотехнологиях обещают сделать использование вирусов более универсальным. С точки зрения материаловеда, вирусы можно рассматривать как органические наночастицы, на поверхности которых есть особые инструменты, которые позволяют им преодолевать барьеры своих клеток-хозяев. Размер и форма вирусов, а также количество и природа функциональных групп на их поверхности точно определены. Таким образом, вирусы обычно используются в материаловедении в качестве каркаса для ковалентно связанных модификаций поверхности. Особое качество вирусов состоит в том, что они могут быть адаптированы путем направленной эволюции. Мощные методы, разработанные науками о жизни, становятся основой инженерных подходов к наноматериалам, открывая широкий спектр приложений, выходящих далеко за рамки биологии и медицины.[268]
Из-за своего размера, формы и четко определенной химической структуры вирусы использовались в качестве шаблонов для организации материалов в наномасштабе. Недавние примеры включают работу в Лаборатория военно-морских исследований в Вашингтоне, округ Колумбия, используя Вирус мозаики коровьего гороха (CPMV) частицы для усиления сигналов в Микрочип ДНК на базе датчиков. В этом приложении вирусные частицы отделяют флуоресцентный красители используется для передачи сигналов, чтобы предотвратить образование нефлуоресцентных димеры которые действуют как тушители.[269] Другой пример - использование CPMV в качестве наноразмерного макета для молекулярной электроники.[270]
Синтетические вирусы
Многие вирусы можно синтезировать de novo («с нуля»), и первый синтетический вирус был создан в 2002 году.[271] Хотя это в некоторой степени заблуждение, синтезируется не сам вирус, а его ДНК-геном (в случае ДНК-вируса) или кДНК копия его генома (в случае РНК-вирусов). Для многих семейств вирусов голая синтетическая ДНК или РНК (после ферментативного преобразования обратно из синтетической кДНК) при введении в клетку заразны. То есть они содержат всю необходимую информацию для создания новых вирусов. Эта технология сейчас используется для исследования новых вакцин.[272] Способность синтезировать вирусы имеет далеко идущие последствия, поскольку вирусы больше не могут считаться вымершими, пока информация об их геномной последовательности известна и снисходительный ячейки доступны. По состоянию на ноябрь 2017 г.[Обновить], полноразмерные последовательности генома 7454 различных вирусов, включая натуральную оспу, находятся в открытом доступе в онлайн-базе данных, поддерживаемой Национальные институты здоровья.[273]
Оружие
Способность вирусов вызывать разрушительные эпидемии в человеческом обществе вызывает опасения, что вирусы могут быть использованы в качестве оружия для биологическая война. Дальнейшее беспокойство вызвало успешное воссоздание печально известного 1918 грипп вирус в лаборатории.[274]Вирус оспы опустошал множество обществ на протяжении всей истории до его искоренения. В мире есть только два центра, уполномоченных ВОЗ хранить запасы вируса оспы: Государственный научный центр вирусологии и биотехнологии ВЕКТОР в России и Центры по контролю и профилактике заболеваний В Соединенных Штатах.[275] Может использоваться как оружие,[275] поскольку вакцина от оспы иногда имела серьезные побочные эффекты, она больше не используется в повседневной практике ни в одной стране. Таким образом, большая часть современного человеческого населения почти не имеет устойчивой устойчивости к оспе и будет уязвима для вируса.[275]
Смотрите также
Рекомендации
Примечания
- ^ Ву, Кэтрин Дж. (15 апреля 2020 г.). «Во Вселенной больше вирусов, чем звезд. Почему только некоторые заражают нас? - На Земле существует более квадриллиона квадриллионов отдельных вирусов, но большинство из них не готовы проникнуть в людей. Можем ли мы найти те, которые есть?». Национальное географическое общество. Получено 18 мая 2020.
- ^ а б c Кунин Э.В., Сенкевич Т.Г., Доля В.В. (сентябрь 2006 г.). «Древний вирусный мир и эволюция клеток». Биология Директ. 1 (1): 29. Дои:10.1186/1745-6150-1-29. ЧВК 1594570. PMID 16984643.
- ^ а б c Диммок стр. 4
- ^ а б «Таксономия вирусов: выпуск 2019 г.». talk.ictvonline.org. Международный комитет по таксономии вирусов. Получено 25 апреля 2020.
- ^ а б Breitbart M, Rohwer F (июнь 2005 г.). «Здесь вирус, там вирус, везде один и тот же вирус?». Тенденции в микробиологии. 13 (6): 278–84. Дои:10.1016 / j.tim.2005.04.003. PMID 15936660.
- ^ а б Лоуренс С.М., Менон С., Эйлерс Б.Дж., Ботнер Б., Хаят Р., Дуглас Т., Янг М.Дж. (май 2009 г.). «Структурно-функциональные исследования вирусов архей». Журнал биологической химии. 284 (19): 12599–603. Дои:10.1074 / jbc.R800078200. ЧВК 2675988. PMID 19158076.
- ^ Эдвардс Р.А., Ровер Ф. (июнь 2005 г.). «Вирусная метагеномика». Обзоры природы. Микробиология. 3 (6): 504–10. Дои:10.1038 / nrmicro1163. PMID 15886693. S2CID 8059643.
- ^ а б Canchaya C, Fournous G, Chibani-Chennoufi S, Dillmann ML, Brüssow H (август 2003 г.). «Фаг как агенты латерального переноса генов». Текущее мнение в микробиологии. 6 (4): 417–24. Дои:10.1016 / S1369-5274 (03) 00086-9. PMID 12941415.
- ^ а б Рыбицкий Е.П. (1990). «Классификация организмов на пороге жизни, или проблемы с вирусной систематикой». Южноафриканский научный журнал. 86: 182–86.
- ^ а б Кунин Э.В., Старокадомский П (октябрь 2016). «Живы ли вирусы? Парадигма репликатора проливает решающий свет на старый, но ошибочный вопрос». Исследования по истории и философии биологических и биомедицинских наук. 59: 125–34. Дои:10.1016 / j.shpsc.2016.02.016. ЧВК 5406846. PMID 26965225.
- ^ Робилотти Э., Дересинский С., Пинский Б.А. (январь 2015 г.). «Норовирус». Обзоры клинической микробиологии. 28 (1): 134–64. Дои:10.1128 / CMR.00075-14. ЧВК 4284304. PMID 25567225.
- ^ Шорс с. 123–124.
- ^ «Вирус, п.». OED Online. Издательство Оксфордского университета. Март 2015 г.
- ^ а б Харпер Д. (2011). "вирус". Интернет-словарь этимологии. Получено 19 декабря 2014.
- ^ "Virulent, прилаг.". OED Online. Издательство Оксфордского университета. Март 2015 г.
- ^ Харпер Д. (2011). "опасный". Интернет-словарь этимологии. Получено 19 декабря 2014.
- ^ Бушард К., Тон Р. (2003). «Модели животных с диабетом». В Hau J, Van Hoosier Jr GL (ред.). Справочник по лабораторным зоотехникам. Модели животных. II (Второе изд.). CRC Press. С. 163, 166.
- ^ Уильям Т. Стерн: Ботаническая латынь. История, грамматика, синтаксис, терминология и словарный запас. Дэвид и Чарльз, третье издание, 1983. Цитата: «Вирус: вирус (s.n. II), ген. петь. вири ном. пл. вира ген. пл. vīrorum (отличать от virorum, мужчин) ".
- ^ Харпер Д. (2011). "популярный". Интернет-словарь этимологии. Получено 19 декабря 2014.
- ^ Харпер Д. (2011). "вирион". Интернет-словарь этимологии. Получено 19 декабря 2014.
- ^ Casjens S (2010). Mahy BW, Van Regenmortel MH (ред.). Настольная энциклопедия общей вирусологии. Бостон: Academic Press. п. 167. ISBN 978-0-12-375146-1.
- ^ Борденаве G (май 2003 г.). «Луи Пастер (1822-1895)». Микробы и инфекции. 5 (6): 553–60. Дои:10.1016 / S1286-4579 (03) 00075-3. PMID 12758285.
- ^ Шорс с. 74, 827
- ^ а б Кольер П. 3
- ^ Диммок стр. 4–5
- ^ Феннер Ф (2009). Mahy BW, Van Regenmortal MH (ред.). Настольная энциклопедия общей вирусологии (1-е изд.). Оксфорд: Academic Press. п. 15. ISBN 978-0-12-375146-1.
- ^ Шорс р. 827
- ^ D'Herelle F (сентябрь 2007 г.). «О невидимом микробе, антагонистическом дизентерийным бациллам: краткая записка г-на Ф. Д'Эрелля, представленная г-ном Ру. 1917». Исследования в области микробиологии. 158 (7): 553–54. Дои:10.1016 / j.resmic.2007.07.005. PMID 17855060.
- ^ Доминго-Калап П., Георгель П., Бахрам С. (март 2016 г.). «Назад в будущее: бактериофаги как перспективные терапевтические средства». HLA. 87 (3): 133–40. Дои:10.1111 / тан.12742. PMID 26891965. S2CID 29223662.
- ^ Стейнхардт Э., Израильский Ц., Ламберт Р.А. (1913). «Исследования по выращиванию вируса коровьей оспы». Журнал инфекционных болезней. 13 (2): 294–300. Дои:10.1093 / infdis / 13.2.294.
- ^ Кольер П. 4
- ^ Goodpasture EW, Woodruff AM, Buddingh GJ (октябрь 1931 г.). «Выращивание вакцины и других вирусов в хориоаллантоисной мембране куриных эмбрионов». Наука. 74 (1919): 371–72. Bibcode:1931Научный .... 74..371Г. Дои:10.1126 / science.74.1919.371. PMID 17810781.
- ^ Томас Хакл Веллер (2004). Выращивание патогенов в тканевых культурах: пятьдесят лет в академической тропической медицине, педиатрии и вирусологии. Бостонская медицинская библиотека. п. 57. ISBN 978-0-88135-380-8.
- ^ Розен Ф.С. (октябрь 2004 г.). «Изоляция полиовируса - Джон Эндерс и Нобелевская премия». Медицинский журнал Новой Англии. 351 (15): 1481–83. Дои:10.1056 / NEJMp048202. PMID 15470207.
- ^ Frängsmyr T, Ekspång G, ред. (1993). Нобелевские лекции по физике 1981–1990 гг.. Сингапур: World Scientific Publishing Co. Bibcode:1993nlp..book ..... F.
- В 1887 году Буист визуализировал один из крупнейших вирусов осповакцины с помощью оптической микроскопии после его окрашивания. В то время не было известно, что вирус осповакцины является вирусом. (Буист Дж. Б. Вакциния и оспа: изучение истории их жизни Черчилль, Лондон)
- ^ Стэнли WM, Лоринг HS (январь 1936 г.). «Выделение кристаллического белка вируса табачной мозаики из больных растений томатов». Наука. 83 (2143): 85. Bibcode:1936Научный .... 83 ... 85С. Дои:10.1126 / science.83.2143.85. PMID 17756690.
- ^ Стэнли WM, Lauffer MA (апрель 1939 г.). «Распад вируса табачной мозаики в растворах мочевины». Наука. 89 (2311): 345–47. Bibcode:1939Sci .... 89..345S. Дои:10.1126 / наука.89.2311.345. PMID 17788438.
- ^ Creager AN, Morgan GJ (июнь 2008 г.). "После двойной спирали: исследование Розалинды Франклин вируса табачной мозаики". Исида; Международный обзор, посвященный истории науки и ее культурному влиянию. 99 (2): 239–72. Дои:10.1086/588626. PMID 18702397. S2CID 25741967.
- ^ Диммок стр. 12
- ^ Норрби Э. (2008). «Нобелевские премии и новая концепция вирусов». Архив вирусологии. 153 (6): 1109–23. Дои:10.1007 / s00705-008-0088-8. PMID 18446425. S2CID 10595263.
- ^ Кольер П. 745
- ^ а б Темин HM, Балтимор Д. (1972). «РНК-направленный синтез ДНК и РНК опухолевых вирусов». Достижения в вирусных исследованиях. 17: 129–86. Дои:10.1016 / S0065-3527 (08) 60749-6. ISBN 9780120398171. PMID 4348509.
- ^ Barré-Sinoussi F, Chermann JC, Rey F, Nugeyre MT, Chamaret S, Gruest J, et al. (Май 1983 г.). «Выделение Т-лимфотропного ретровируса от пациента с риском синдрома приобретенного иммунодефицита (СПИД)». Наука. 220 (4599): 868–71. Bibcode:1983Научный ... 220..868B. Дои:10.1126 / science.6189183. PMID 6189183.
- ^ Choo QL, Kuo G, Weiner AJ, Overby LR, Bradley DW, Houghton M (апрель 1989 г.). «Выделение клона кДНК, полученного из передающегося с кровью генома вирусного гепатита не-A, не-B». Наука. 244 (4902): 359–62. Bibcode:1989Научный ... 244..359C. CiteSeerX 10.1.1.469.3592. Дои:10.1126 / science.2523562. PMID 2523562.
- ^ Houghton M (ноябрь 2009 г.). «Долгая и извилистая дорога, ведущая к выявлению вируса гепатита С». Журнал гепатологии. 51 (5): 939–48. Дои:10.1016 / j.jhep.2009.08.004. PMID 19781804.
- ^ Айер Л.М., Баладжи С., Кунин Е.В., Аравинд Л. (апрель 2006 г.). «Эволюционная геномика нуклео-цитоплазматических больших ДНК-вирусов». Вирусные исследования. 117 (1): 156–84. Дои:10.1016 / j.virusres.2006.01.009. PMID 16494962.
- ^ а б Санхуан Р., Небот М. Р., Кирико Н., Мански Л. М., Белшоу Р. (октябрь 2010 г.). «Частота вирусных мутаций». Журнал вирусологии. 84 (19): 9733–48. Дои:10.1128 / JVI.00694-10. ЧВК 2937809. PMID 20660197.
- ^ Шорс с. 14–16.
- ^ Кольер стр. 11–21
- ^ а б Диммок стр. 16
- ^ Кольер П. 11
- ^ а б c d Mahy WJ, Regenmortel MH, ред. (2009). Настольная энциклопедия общей вирусологии. Оксфорд: Academic Press. п. 24. ISBN 978-0-12-375146-1.
- ^ Шорс р. 810
- ^ Макклинток Б. (июнь 1950 г.). «Происхождение и поведение изменчивых локусов кукурузы». Труды Национальной академии наук Соединенных Штатов Америки. 36 (6): 344–55. Bibcode:1950ПНАС ... 36..344М. Дои:10.1073 / pnas.36.6.344. ЧВК 1063197. PMID 15430309.
- ^ Кольер стр. 11–12
- ^ Диммок стр. 55
- ^ Шорты стр.791.
- ^ Цагрис Э.М., Мартинес де Альба А.Э., Гозманова М., Калантидис К. (ноябрь 2008 г.). «Вироиды». Клеточная микробиология. 10 (11): 2168–79. Дои:10.1111 / j.1462-5822.2008.01231.x. PMID 18764915. S2CID 221581424.
- ^ Шорты стр.460
- ^ а б La Scola B, Desnues C, Pagnier I, Robert C, Barrassi L, Fournous G и др. (Сентябрь 2008 г.). «Вирофаг как уникальный паразит гигантского мимивируса». Природа. 455 (7209): 100–04. Bibcode:2008Натура.455..100л. Дои:10.1038 / природа07218. PMID 18690211. S2CID 4422249.
- ^ Кольер П. 777
- ^ Диммок стр. 55–57.
- ^ а б Mahy WJ, Van Regenmortel MH, ред. (2009). Настольная энциклопедия общей вирусологии. Оксфорд: Academic Press. п. 28. ISBN 978-0-12-375146-1.
- ^ а б Mahy WJ, Regenmortel MH, ред. (2009). Настольная энциклопедия общей вирусологии. Оксфорд: Academic Press. п. 26. ISBN 978-0-12-375146-1.
- ^ Диммок стр. 15–16
- ^ Холмс ЕС (октябрь 2007 г.). «Вирусная эволюция в эпоху генома». PLOS Биология. 5 (10): e278. Дои:10.1371 / journal.pbio.0050278. ЧВК 1994994. PMID 17914905.
- ^ Виммер Э., Мюллер С., Тампи TM, Таубенбергер Дж. К. (декабрь 2009 г.). «Синтетические вирусы: новая возможность понять и предотвратить вирусные заболевания». Природа Биотехнологии. 27 (12): 1163–72. Дои:10.1038 / nbt.1593. ЧВК 2819212. PMID 20010599.
- ^ Рог M (2008). «Хламидии как симбионты у эукариот». Ежегодный обзор микробиологии. 62: 113–31. Дои:10.1146 / annurev.micro.62.081307.162818. PMID 18473699.
- ^ Аммерман NC, Байер-Секстон М., Азад А.Ф. (ноябрь 2008 г.). «Лабораторное обеспечение риккетсии риккетсии». Текущие протоколы в микробиологии. 11 (1): 3A.5.1–3A.5.21. Дои:10.1002 / 9780471729259.mc03a05s11. ISBN 978-0471729259. ЧВК 2725428. PMID 19016440.
- ^ а б Кольер стр. 33–55
- ^ Кольер стр. 33–37
- ^ Киселев Н.А., Шерман М.Б., Цупрун В.Л. (1990). «Отрицательное окрашивание белков». Обзоры электронной микроскопии. 3 (1): 43–72. Дои:10.1016 / 0892-0354 (90) 90013-И. PMID 1715774.
- ^ Кольер П. 40
- ^ Каспар Д.Л., Клуг А. (1962). «Физические принципы построения обычных вирусов». Симпозиумы Колд-Спринг-Харбор по количественной биологии. 27: 1–24. Дои:10.1101 / sqb.1962.027.001.005. PMID 14019094.
- ^ Крик Ф. Х., Уотсон Дж. Д. (март 1956 г.). «Строение малых вирусов». Природа. 177 (4506): 473–75. Bibcode:1956 г., природа 177..473 ° C. Дои:10.1038 / 177473a0. PMID 13309339. S2CID 5740221.
- ^ Falvo MR, Washburn S, Superfine R, Finch M, Brooks FP, Chi V, Taylor RM (март 1997 г.). «Манипуляции с отдельными вирусами: трение и механические свойства». Биофизический журнал. 72 (3): 1396–403. Bibcode:1997BpJ .... 72.1396F. Дои:10.1016 / S0006-3495 (97) 78786-1. ЧВК 1184522. PMID 9138585.
- ^ Кузнецов Ю.Г., Малкин А.Дж., Лукас Р.В., Пломп М., Макферсон А. (сентябрь 2001 г.). «Визуализация вирусов с помощью атомно-силовой микроскопии». Журнал общей вирусологии. 82 (Pt 9): 2025–34. Дои:10.1099/0022-1317-82-9-2025. PMID 11514711.
- ^ Кольер П. 37
- ^ Кольер стр.40, 42
- ^ Уилсон Д.П. (2016). «Выступающие элементы вирусных капсидов сгруппированы на больших кругах икосаэдра». PLOS ONE. 11 (4): e0152319. Bibcode:2016PLoSO..1152319W. Дои:10.1371 / journal.pone.0152319. ЧВК 4821576. PMID 27045511.
- ^ Casens S (2009). Настольная энциклопедия общей вирусологии. Бостон: Academic Press. С. 167–74. ISBN 978-0-12-375146-1.
- ^ Дхама К., Хан С., Тивари Р., Сиркар С., Бхат С., Малик Ю.С., Сингх К.П., Чайкумпа В., Бонилья-Алдана Д.К., Родригес-Моралес А.Дж. (сентябрь 2020 г.). «Коронавирусная болезнь 2019-COVID-19». Обзоры клинической микробиологии. 33 (4). Дои:10.1128 / CMR.00028-20. ЧВК 7405836. PMID 32580969.
- ^ Кольер стр. 42–43
- ^ Россманн М.Г., Месянжинов В.В., Арисака Ф., Лейман П.Г. (апрель 2004 г.). «Аппарат для инъекции ДНК бактериофага Т4». Текущее мнение в структурной биологии. 14 (2): 171–80. Дои:10.1016 / j.sbi.2004.02.001. PMID 15093831.
- ^ Long GW, Nobel J, Murphy FA, Herrmann KL, Lourie B (сентябрь 1970 г.). «Опыт использования электронной микроскопии в дифференциальной диагностике оспы». Прикладная микробиология. 20 (3): 497–504. Дои:10.1128 / AEM.20.3.497-504.1970. ЧВК 376966. PMID 4322005.
- ^ Suzan-Monti M, La Scola B, Raoult D (апрель 2006 г.). «Геномные и эволюционные аспекты мимивируса». Вирусные исследования. 117 (1): 145–55. Дои:10.1016 / j.virusres.2005.07.011. PMID 16181700.
- ^ Арслан Д., Лежандр М., Зельцер В., Абергель С., Клавери Дж. М. (октябрь 2011 г.). «Дальний родственник мимивируса с более крупным геномом подчеркивает фундаментальные особенности Megaviridae». Труды Национальной академии наук Соединенных Штатов Америки. 108 (42): 17486–91. Bibcode:2011PNAS..10817486A. Дои:10.1073 / pnas.1110889108. ЧВК 3198346. PMID 21987820.
- ^ а б Филипп Н., Лежандр М., Дутре Дж., Коуте И, Пуаро О., Леско М. и др. (Июль 2013). «Пандоровирусы: вирусы амеб с геномом до 2,5 Мб, достигающие генома паразитических эукариот» (PDF). Наука. 341 (6143): 281–86. Bibcode:2013Научный ... 341..281П. Дои:10.1126 / science.1239181. PMID 23869018. S2CID 16877147.
- ^ Брандес Н, Линиал М (апрель 2019 г.). «Гигантские вирусы - большие сюрпризы». Вирусы. 11 (5): 404. Дои:10.3390 / v11050404. ЧВК 6563228. PMID 31052218.
- ^ а б Прангишвили Д., Фортер П, Гаррет Р. А. (ноябрь 2006 г.). «Вирусы архей: объединяющая точка зрения». Обзоры природы. Микробиология. 4 (11): 837–48. Дои:10.1038 / nrmicro1527. PMID 17041631. S2CID 9915859.
- ^ а б Диммок стр. 49
- ^ «База данных вирусного генома NCBI». ncbi.nlm.nih.gov. Получено 15 января 2017.
- ^ Pennisi E (март 2011 г.). «Микробиология. Вирусный рост: изучение роли вирусов в нашем организме». Наука. 331 (6024): 1513. Bibcode:2011Научный ... 331.1513P. Дои:10.1126 / science.331.6024.1513. PMID 21436418.
- ^ Ши М., Линь XD, Тиан Дж.Х., Чен Л.Дж., Чен Х, Ли СХ и др. (Декабрь 2016 г.). «Новое определение виросферы РНК беспозвоночных». Природа. 540 (7634): 539–43. Bibcode:2016Натура.540..539S. Дои:10.1038 / природа20167. PMID 27880757. S2CID 1198891.
- ^ а б c Кольер стр. 96–99
- ^ Сондерс В.А., Картер Дж. (2007). Вирусология: принципы и применение. Чичестер: Джон Уайли и сыновья. п. 72. ISBN 978-0-470-02387-7.
- ^ Белый В.А., Левин А.Ю., Скалка А.М. (декабрь 2010 г.). «Последовательности предковых одноцепочечных ДНК-вирусов в геномах позвоночных: parvoviridae и circoviridae имеют возраст более 40-50 миллионов лет». Журнал вирусологии. 84 (23): 12458–62. Дои:10.1128 / JVI.01789-10. ЧВК 2976387. PMID 20861255.
- ^ Брандес Н., Линиал М. (май 2016 г.). «Перекрытие генов и ограничения размера в вирусном мире». Биология Директ. 11 (1): 26. Дои:10.1186 / s13062-016-0128-3. ЧВК 4875738. PMID 27209091.
- ^ Нажатие J, Реанни, округ Колумбия (1984). «Разделенные геномы и внутренний шум». Журнал молекулярной эволюции. 20 (2): 135–46. Bibcode:1984JMolE..20..135P. Дои:10.1007 / BF02257374. ЧВК 7087551. PMID 6433032.
- ^ Даффи С., Холмс ЕС (июнь 2009 г.). «Подтверждение высоких показателей нуклеотидных замен в геминивирусах: филогенетические данные из вирусов мозаики маниока из Восточной Африки». Журнал общей вирусологии. 90 (Pt 6): 1539–47. Дои:10.1099 / vir.0.009266-0. ЧВК 4091138. PMID 19264617.
- ^ Sandbulte MR, Westgeest KB, Gao J, Xu X, Klimov AI, Russell CA и др. (Декабрь 2011 г.). «Дискордантный антигенный дрейф нейраминидазы и гемагглютинина в вирусах гриппа H1N1 и H3N2». Труды Национальной академии наук Соединенных Штатов Америки. 108 (51): 20748–53. Bibcode:2011ПНАС..10820748С. Дои:10.1073 / pnas.1113801108. ЧВК 3251064. PMID 22143798.
- ^ Мосс РБ, Дэви РТ, Стейгбигель РТ, Фанг Ф (июнь 2010 г.). «Ориентация на пандемический грипп: учебник по противовирусным препаратам гриппа и лекарственной устойчивости». Журнал антимикробной химиотерапии. 65 (6): 1086–93. Дои:10.1093 / jac / dkq100. PMID 20375034.
- ^ Хэмпсон А. В., Маккензи Дж. С. (ноябрь 2006 г.). «Вирусы гриппа». Медицинский журнал Австралии. 185 (S10): S39–43. Дои:10.5694 / j.1326-5377.2006.tb00705.x. PMID 17115950. S2CID 17069567.
- ^ Мецнер К.Дж. (декабрь 2006 г.). «Выявление и значение квазивидов меньшинств лекарственно-устойчивого ВИЧ-1». Журнал терапии ВИЧ. 11 (4): 74–81. PMID 17578210.
- ^ Гоудсмит, Яап. Вирусный секс. Oxford Univ Press, 1998. ISBN 978-0-19-512496-5, 0-19-512496-0
- ^ Воробей М., Холмс ЕС (октябрь 1999 г.). «Эволюционные аспекты рекомбинации в РНК-вирусах». Журнал общей вирусологии. 80 (10): 2535–43. Дои:10.1099/0022-1317-80-10-2535. PMID 10573145.
- ^ Лукашев АН (2005). «Роль рекомбинации в эволюции энтеровирусов». Обзоры в медицинской вирусологии. 15 (3): 157–67. Дои:10.1002 / rmv.457. PMID 15578739. S2CID 26000112.
- ^ Умене К. (июль 1999 г.). «Механизм и применение генетической рекомбинации в герпесвирусах». Обзоры в медицинской вирусологии. 9 (3): 171–82. Дои:10.1002 / (SICI) 1099-1654 (199907/09) 9: 3 <171 :: AID-RMV243> 3.0.CO; 2-A. PMID 10479778.
- ^ Freed EO (август 2015 г.). «Сборка, высвобождение и созревание ВИЧ-1». Обзоры природы. Микробиология. 13 (8): 484–96. Дои:10.1038 / nrmicro3490. ЧВК 6936268. PMID 26119571.
- ^ Инь Дж., Редович Дж. (Июнь 2018 г.). «Кинетическое моделирование роста вирусов в клетках». Обзоры микробиологии и молекулярной биологии. 82 (2). Дои:10.1128 / MMBR.00066-17. ЧВК 5968458. PMID 29592895.
- ^ Кольер стр. 75–91
- ^ Más V, Melero JA (2013). «Поступление оболочечных вирусов в клетки-хозяева: слияние мембран». Структура и физика вирусов. Субклеточная биохимия. 68. С. 467–87. Дои:10.1007/978-94-007-6552-8_16. ISBN 978-94-007-6551-1. ЧВК 7121288. PMID 23737062.
- ^ Диммок стр. 70
- ^ Боевинк П., Опарка К.Дж. (август 2005 г.). «Взаимодействие вируса с хостом в процессе перемещения». Физиология растений. 138 (4): 1815–21. Дои:10.1104 / стр.105.066761. ЧВК 1183373. PMID 16172094.
- ^ Диммок стр. 71
- ^ Блаас Д. (май 2016 г.). «Пути проникновения вирусов: на примере вирусов простуды». Wiener Medizinische Wochenschrift. 166 (7–8): 211–26. Дои:10.1007 / s10354-016-0461-2. ЧВК 4871925. PMID 27174165.
- ^ Исомура Х., Стински М.Ф. (февраль 2013 г.). «Согласование поздней транскрипции генов цитомегаловируса человека с синтезом вирусной ДНК: рекомбинантные вирусы как потенциальные терапевтические вакцины-кандидаты». Мнение экспертов о терапевтических целях. 17 (2): 157–66. Дои:10.1517/14728222.2013.740460. PMID 23231449. S2CID 11448687.
- ^ Бармен С., Али А., Хуэй Е.К., Адхикари Л., Наяк Д.П. (сентябрь 2001 г.). «Транспорт вирусных белков к апикальным мембранам и взаимодействие матричного белка с гликопротеинами в сборке вирусов гриппа». Вирусные исследования. 77 (1): 61–69. Дои:10.1016 / S0168-1702 (01) 00266-0. PMID 11451488.
- ^ Шорс с. 836
- ^ Диммок, Глава 15, Механизмы латентности вируса, стр. 243–59
- ^ Диммок 185–87
- ^ Шорс р. 118; Кольер П. 78
- ^ Кольер П. 79
- ^ Стагиннус С., Рихерт-Пёггелер К.Р. (октябрь 2006 г.). «Эндогенные параретровирусы: двуличные путешественники в геноме растений». Тенденции в растениеводстве. 11 (10): 485–91. Дои:10.1016 / j.tplants.2006.08.008. PMID 16949329.
- ^ Кольер стр. 88–89
- ^ Кольер стр. 115–46
- ^ Кольер П. 115
- ^ Рулстон А., Марселлус Р.К., Брантон П.Е. (1999). «Вирусы и апоптоз». Ежегодный обзор микробиологии. 53: 577–628. Дои:10.1146 / annurev.micro.53.1.577. PMID 10547702.
- ^ Алвин Дж. К. (2008). «Модуляция стрессовых ответов клетки-хозяина цитомегаловирусом человека». Актуальные темы микробиологии и иммунологии. 325: 263–79. Дои:10.1007/978-3-540-77349-8_15. ISBN 978-3-540-77348-1. PMID 18637511.
- ^ Бароцци П., Потенца Л., Рива Дж., Валлерини Д., Квадрелли С., Боско Р. и др. (Декабрь 2007 г.). «В-клетки и герпесвирусы: модель лимфопролиферации». Отзывы об аутоиммунности. 7 (2): 132–36. Дои:10.1016 / j.autrev.2007.02.018. PMID 18035323.
- ^ Субраманья Д., Гривас П.Д. (ноябрь 2008 г.). «ВПЧ и рак шейки матки: обновленная информация об установившихся отношениях». Последипломная медицина. 120 (4): 7–13. Дои:10.3810 / PGM.2008.11.1928. PMID 19020360. S2CID 1399003.
- ^ Синклер Дж (март 2008 г.). «Человеческий цитомегаловирус: латентность и реактивация в миелоидной линии». Журнал клинической вирусологии. 41 (3): 180–85. Дои:10.1016 / j.jcv.2007.11.014. PMID 18164651.
- ^ Джордан М.С., Джордан Г.В., Стивенс Дж. Г., Миллер Г. (июнь 1984 г.). «Скрытые герпесвирусы человека». Анналы внутренней медицины. 100 (6): 866–80. Дои:10.7326/0003-4819-100-6-866. PMID 6326635.
- ^ Sissons JG, Bain M, Wills MR (февраль 2002 г.). «Латентность и реактивация цитомегаловируса человека». Журнал инфекции. 44 (2): 73–77. Дои:10.1053 / jinf.2001.0948. PMID 12076064.
- ^ Кроуфорд Д.Х. (2011). Вирусы: очень краткое введение. Oxford University Press, США. стр.16. ISBN 978-0-19-957485-8.
- ^ Шорс р. 643
- ^ Шорс р. 631
- ^ Диммок стр. 272
- ^ Баггесен Д.Л., Соренсен Г., Нильсен Е.М., Вегенер Х.С. (январь 2010 г.). «Фаготипирование Salmonella Typhimurium - по-прежнему ли это полезный инструмент для надзора и расследования вспышек?». Европейское наблюдение. 15 (4): 19471. PMID 20122382. Получено 19 декабря 2014.
- ^ Parker MT (сентябрь 2016 г.). «Экологическая основа человеческого вирома обеспечивает классификацию текущих знаний и определяет области предстоящих открытий». Йельский журнал биологии и медицины. 89 (3): 339–51. ЧВК 5045143. PMID 27698618.
- ^ Львофф А., Хорн Р. В., Турнье П. (июнь 1962 г.). «[Вирусная система]». Comptes Rendus Hebdomadaires des Séances de l'Académie des Sciences (На французском). 254: 4225–27. PMID 14467544.
- ^ Львофф А., Хорн Р., Турнье П. (1962). «Система вирусов». Симпозиумы Колд-Спринг-Харбор по количественной биологии. 27: 51–55. Дои:10.1101 / sqb.1962.027.001.008. PMID 13931895.
- ^ Fauquet CM, Fargette D (август 2005 г.). «Международный комитет по таксономии вирусов и 3 142 неназначенных видов». Журнал вирусологии. 2: 64. Дои:10.1186 / 1743-422X-2-64. ЧВК 1208960. PMID 16105179.
- ^ Исполнительный комитет Международного комитета по таксономии вирусов (май 2020 г.). «Новый объем таксономии вирусов: разделение виросферы на 15 иерархических рангов». Нат Микробиол. 5 (5): 668–674. Дои:10.1038 / с41564-020-0709-х. ЧВК 7186216. PMID 32341570.
- ^ Делварт Э.Л. (2007). «Вирусная метагеномика». Обзоры в медицинской вирусологии. 17 (2): 115–31. Дои:10.1002 / RMV.532. ЧВК 7169062. PMID 17295196.
- ^ Балтимор Д. (1974). «Стратегия РНК-вирусов». Харви Лекции. 70 серии. 70 Series: 57–74. PMID 4377923.
- ^ van Regenmortel MH, Mahy BW (январь 2004 г.). «Новые проблемы в таксономии вирусов». Возникающие инфекционные заболевания. 10 (1): 8–13. Дои:10.3201 / eid1001.030279. ЧВК 3322749. PMID 15078590.
- ^ Майо М.А. (1999). «Изменения в таксономии растительных вирусов после публикации 6-го отчета ICTV. Международный комитет по таксономии вирусов». Архив вирусологии. 144 (8): 1659–66. Дои:10.1007 / s007050050620. PMID 10486120. S2CID 33422303.
- ^ де Вильерс Э.М., Фоке С., Брокер Т.Р., Бернар Х.Ю., цур Хаузен Х. (июнь 2004 г.). «Классификация папилломавирусов». Вирусология. 324 (1): 17–27. Дои:10.1016 / j.virol.2004.03.033. PMID 15183049.
- ^ В основном Глава 33 (Краткие сведения о болезнях), стр. 367–92 в:Фишер Б., Харви Р.П., Champe PC (2007). Иллюстрированные обзоры Липпинкотта: микробиология. Серия иллюстрированных обзоров Липпинкотта. Хагерствон, доктор медицины: Липпинкотт Уильямс и Уилкинс. С. 367–92. ISBN 978-0-7817-8215-9.
- ^ Комаров А.Л. (декабрь 2006 г.). «Является ли вирус герпеса-6 спусковым крючком для синдрома хронической усталости?». Журнал клинической вирусологии. 37 (Дополнение 1): S39–46. Дои:10.1016 / S1386-6532 (06) 70010-5. PMID 17276367.
- ^ Chen CH, Chiu YL, Wei FC, Koong FJ, Liu HC, Shaw CK и др. (Январь 1999 г.). «Высокая распространенность инфекции вирусом Борна среди больных шизофренией, членов их семей и психиатров на Тайване». Молекулярная психиатрия. 4 (1): 33–38. Дои:10.1038 / sj.mp.4000484. PMID 10089006. S2CID 19830976.
- ^ Марголис Т.П., Эльфман Флорида, Лейб Д., Пакпур Н., Апакупакул К., Имаи Ю., Войтек С. (октябрь 2007 г.). «Спонтанная реактивация вируса простого герпеса типа 1 в латентно инфицированных сенсорных ганглиях мыши». Журнал вирусологии. 81 (20): 11069–74. Дои:10.1128 / JVI.00243-07. ЧВК 2045564. PMID 17686862.
- ^ Уитли Р.Дж., Ройзман Б. (май 2001 г.). «Инфекции, вызванные вирусом простого герпеса». Ланцет. 357 (9267): 1513–18. Дои:10.1016 / S0140-6736 (00) 04638-9. PMID 11377626. S2CID 9854903.
- ^ Barton ES, White DW, Cathelyn JS, Brett-McClellan KA, Engle M, Diamond MS и др. (Май 2007 г.). «Латентный период вируса герпеса обеспечивает симбиотическую защиту от бактериальной инфекции». Природа. 447 (7142): 326–29. Bibcode:2007Натура.447..326Б. Дои:10.1038 / природа05762. PMID 17507983. S2CID 4425405.
- ^ Бертолетти А., Геринг А. (октябрь 2007 г.). «Иммунный ответ и толерантность при хронической инфекции вируса гепатита В». Гепатологические исследования. 37 (Приложение 3): S331–38. Дои:10.1111 / j.1872-034X.2007.00221.x. PMID 17931183. S2CID 13386004.
- ^ Родригес С., Дешмук М., Джейкоб Т., Нукала Р., Менон С., Мехта А. (2001). «Значение ДНК HBV с помощью ПЦР над серологическими маркерами HBV у пациентов с острыми и хроническими заболеваниями». Индийский журнал медицинской микробиологии. 19 (3): 141–44. PMID 17664817.
- ^ Нгуен В.Т., Маклоус М.Л., Дор Г.Дж. (декабрь 2007 г.). «Высокоэндемичная инфекция гепатита В в сельских районах Вьетнама». Журнал гастроэнтерологии и гепатологии. 22 (12): 2093–100. Дои:10.1111 / j.1440-1746.2007.05010.x. PMID 17645465. S2CID 29885790.
- ^ Фаулер М.Г., Лампе М.А., Джеймисон Д.Д., Куртис А.П., Роджерс М.Ф. (сентябрь 2007 г.). «Снижение риска передачи вируса иммунодефицита человека от матери ребенку: прошлые успехи, текущий прогресс и проблемы, а также направления на будущее». Американский журнал акушерства и гинекологии. 197 (3 Suppl): S3–9. Дои:10.1016 / j.ajog.2007.06.048. PMID 17825648.
- ^ Зауэрбрей А., Вутцлер П. (декабрь 2000 г.). «Синдром врожденной ветряной оспы». Журнал перинатологии. 20 (8, Pt 1): 548–54. Дои:10.1038 / sj.jp.7200457. PMID 11190597. S2CID 7973561.
- ^ а б Антоновикс Дж., Уилсон А.Дж., Forbes MR, Hauffe HC, Kallio ER, Leggett HC, Longdon B, Okamura B, Sait SM, Webster JP (май 2017 г.). «Эволюция режима трансмиссии». Философские труды Лондонского королевского общества. Серия B, Биологические науки. 372 (1719). Дои:10.1098 / rstb.2016.0083. ЧВК 5352810. PMID 28289251.
- ^ Гарнетт GP (февраль 2005 г.). «Роль коллективного иммунитета в определении эффекта вакцин против болезней, передающихся половым путем». Журнал инфекционных болезней. 191 (Приложение 1): S97–106. Дои:10.1086/425271. PMID 15627236.
- ^ Платонов А.Е. (2006). «[Влияние погодных условий на эпидемиологию трансмиссивных болезней на примере лихорадки Западного Нила в России]». Вестник Российской Академии медицинских наук. (2): 25–29. PMID 16544901.
- ^ Шорс р. 264
- ^ Шорс с. 894
- ^ Джуэлл С.П., Килинг MJ, Робертс GO (декабрь 2009 г.). «Прогнозирование невыявленных инфекций во время вспышки ящура 2007 г.». Журнал Королевского общества, Интерфейс. 6 (41): 1145–51. Дои:10.1098 / rsif.2008.0433. ЧВК 2817150. PMID 19091686.
- ^ Шорс р. 170
- ^ а б Шорс с. 170–72.
- ^ Шорс р. 272
- ^ Шорс с. 891
- ^ Кольер стр. 409–15
- ^ Паттерсон К.Д., Пайл Г.Ф. (1991). «География и смертность от пандемии гриппа 1918 года». Вестник истории медицины. 65 (1): 4–21. PMID 2021692.
- ^ Джонсон Н.П., Мюллер Дж. (2002). "Обновление счетов: глобальная смертность от" испанской "пандемии гриппа 1918-1920 годов". Вестник истории медицины. 76 (1): 105–15. Дои:10.1353 / bhm.2002.0022. PMID 11875246. S2CID 22974230.
- ^ Эйзингер Р.В., Фаучи А.С. (март 2018 г.). "1". Возникающие инфекционные заболевания. 24 (3): 413–16. Дои:10.3201 / eid2403.171797. ЧВК 5823353. PMID 29460740.
- ^ Цинь И, Чжао MJ, Тан YY, Ли XQ, Чжэн Дж.Д., Пэн Ц. Б., Фэн Л.З. (август 2018 г.). «[История пандемий гриппа в Китае за последний век]». Чжунхуа Лю Син Бин Сюэ За Чжи = Чжунхуа Люсинбинсюэ Цзы (на китайском языке). 39 (8): 1028–31. Дои:10.3760 / cma.j.issn.0254-6450.2018.08.003. PMID 30180422.
- ^ Гао Ф, Бейлс Э., Робертсон Д.Л., Чен Ю., Роденбург С.М., Майкл С.Ф. и др. (Февраль 1999 г.). «Происхождение ВИЧ-1 у шимпанзе Pan troglodytes troglodytes». Природа. 397 (6718): 436–41. Bibcode:1999Натура.397..436Г. Дои:10.1038/17130. PMID 9989410. S2CID 4432185.
- ^ "Информационный бюллетень" (PDF). UNAIDS.org. 2018. Получено 12 декабря 2019.
- ^ "ДАННЫЕ ООН ПО СПИДУ2019". UNAIDS.org. 2019. Получено 5 декабря 2019.
- ^ Мавар Н., Саха С., Пандит А., Махаджан У (декабрь 2005 г.). «Третья фаза пандемии ВИЧ: социальные последствия стигмы и дискриминации в связи с ВИЧ / СПИДом и будущие потребности» (PDF). Индийский журнал медицинских исследований. 122 (6): 471–84. PMID 16517997. Архивировано из оригинал (PDF) 4 марта 2016 г.. Получено 19 декабря 2014.
- ^ «Состояние глобальной эпидемии ВИЧ» (PDF). ЮНЭЙДС. 2008. Архивировано с оригинал (PDF) 22 ноября 2015 г.. Получено 19 декабря 2014.
- ^ Towner JS, Christova ML, Sealy T.K., Vincent MJ, Erickson BR, Bawiec DA, et al. (Июль 2006 г.). «Геномика марбургвируса и связь с крупной вспышкой геморрагической лихорадки в Анголе». Журнал вирусологии. 80 (13): 6497–516. Дои:10.1128 / JVI.00069-06. ЧВК 1488971. PMID 16775337.
- ^ «Отчет Всемирной организации здравоохранения, 24 сентября 2014 г.» (PDF).
- ^ «Журнал вирусологии». Журнал вирусологии.
- ^ Weiss SR, Leibowitz JL (2011). Патогенез коронавируса. Достижения в вирусных исследованиях. 81. С. 85–164. Дои:10.1016 / B978-0-12-385885-6.00009-2. ISBN 978-0-12-385885-6. ЧВК 7149603. PMID 22094080.
- ^ Wong AT, Chen H, Liu SH, Hsu EK, Luk KS, Lai CK и др. (Май 2017). «От атипичной пневмонии к готовности к птичьему гриппу в Гонконге». Клинические инфекционные болезни. 64 (Suppl_2): S98 – S104. Дои:10.1093 / cid / cix123. PMID 28475794.
- ^ Ашур Х.М., Эльхатиб В.Ф., Рахман М.М., Эльшабрави Х.А. (март 2020 г.). «Анализ недавнего нового коронавируса 2019 г. (SARS-CoV-2) в свете прошлых вспышек коронавируса человека». Патогены. 9 (3): 186. Дои:10.3390 / pathogens9030186. ЧВК 7157630. PMID 32143502.
- ^ Дэн С.К., Пэн Х.Д. (февраль 2020 г.). «Характеристики вспышки коронавирусной болезни в Китае в 2019 году и ответные меры общественного здравоохранения». Журнал клинической медицины. 9 (2): 575. Дои:10.3390 / см 9020575. ЧВК 7074453. PMID 32093211.
- ^ Хан Q, Lin Q, Jin S, You L (апрель 2020 г.). «Коронавирус 2019-nCoV: краткий обзор с передовой». Журнал инфекции. 80 (4): 373–77. Дои:10.1016 / j.jinf.2020.02.010. ЧВК 7102581. PMID 32109444.
- ^ Лондоньо Э., Ортис А (16 марта 2020 г.). «Ограничения на поездки из-за коронавируса по всему миру» - через NYTimes.com.
- ^ «США предпринимают более масштабные меры по реагированию на пандемию; в Европе растет число случаев COVID-19». CIDRAP.
- ^ Эйнштейн М.Х., Шиллер Д.Т., Вискиди Р.П., Стриклер HD, Курзаге П., Тан Т. и др. (Июнь 2009 г.). «Руководство клинициста по иммунологии вируса папилломы человека: известные и неизвестные». Ланцет. Инфекционные заболевания. 9 (6): 347–56. Дои:10.1016 / S1473-3099 (09) 70108-2. PMID 19467474.
- ^ Шуда М., Фэн Х., Квун Х.Д., Розен С.Т., Джоэруп О., Мур П.С., Чанг Й. (октябрь 2008 г.). «Мутации Т-антигена представляют собой опухоль-специфическую сигнатуру полиомавируса клеток Меркеля». Труды Национальной академии наук Соединенных Штатов Америки. 105 (42): 16272–77. Bibcode:2008ПНАС..10516272С. Дои:10.1073 / pnas.0806526105. ЧВК 2551627. PMID 18812503.
- ^ Пулитцер М.П., Амин Б.Д., Бусам К.Дж. (май 2009 г.). «Карцинома из клеток Меркеля: обзор». Достижения в анатомической патологии. 16 (3): 135–44. Дои:10.1097 / PAP.0b013e3181a12f5a. PMID 19395876. S2CID 36110778.
- ^ Койке К. (июнь 2007 г.). «Вирус гепатита С вносит свой вклад в гепатоканцерогенез, модулируя метаболические и внутриклеточные сигнальные пути». Журнал гастроэнтерологии и гепатологии. 22 (Приложение 1): S108–11. Дои:10.1111 / j.1440-1746.2006.04669.x. PMID 17567457. S2CID 25399220.
- ^ Ху Дж., Ладгейт Л. (2007). «Коинфекция ВИЧ-ВГВ и ВИЧ-ВГС и развитие рака печени». Лечение рака и исследования. 133: 241–52. Дои:10.1007/978-0-387-46816-7_9. ISBN 978-0-387-46804-4. PMID 17672044.
- ^ Беллон М., Никот С. (2007). «Теломераза: решающий игрок в индуцированном HTLV-I лейкемии Т-клеток человека». Геномика и протеомика рака. 4 (1): 21–25. PMID 17726237.
- ^ Шиффман М., Кастл П.Е., Херонимо Дж., Родригес А.С., Вахолдер С. (сентябрь 2007 г.). «Вирус папилломы человека и рак шейки матки». Ланцет. 370 (9590): 890–907. Дои:10.1016 / S0140-6736 (07) 61416-0. PMID 17826171. S2CID 20196938.
- ^ Klein E, Kis LL, Klein G (февраль 2007 г.). «Инфекция вируса Эпштейна-Барра у людей: от безвредного к опасному для жизни взаимодействию вируса с лимфоцитами». Онкоген. 26 (9): 1297–305. Дои:10.1038 / sj.onc.1210240. PMID 17322915.
- ^ Цур Хаузен Х (июль 2008 г.). «Новые полиомавирусы человека - возрождение хорошо известного семейства вирусов как возможных канцерогенов человека». Международный журнал рака. 123 (2): 247–50. Дои:10.1002 / ijc.23620. PMID 18449881. S2CID 9482506.
- ^ Альберта Б., Джонсон А., Льюис Дж, Рафф М., Робертс К., Уолтерс П. (2002). Молекулярная биология клетки (Четвертое изд.). Нью-Йорк и Лондон: Наука о гирляндах. ISBN 0-8153-3218-1.
- ^ Ding SW, Voinnet O (август 2007 г.). «Противовирусный иммунитет, управляемый малыми РНК». Клетка. 130 (3): 413–26. Дои:10.1016 / j.cell.2007.07.039. ЧВК 2703654. PMID 17693253.
- ^ Паттон Дж. Т., Васкес-Дель Карпио Р., Спенсер Э (2004). «Репликация и транскрипция генома ротавируса». Текущий фармацевтический дизайн. 10 (30): 3769–77. Дои:10.2174/1381612043382620. PMID 15579070.
- ^ Джаярам Х., Эстес М.К., Прасад Б.В. (апрель 2004 г.). «Новые темы в проникновении ротавирусных клеток, организации генома, транскрипции и репликации». Вирусные исследования. 101 (1): 67–81. Дои:10.1016 / j.virusres.2003.12.007. PMID 15010218.
- ^ Грир С., Александр Г.Дж. (декабрь 1995 г.). «Вирусная серология и обнаружение». Клиническая гастроэнтерология Байера. 9 (4): 689–721. Дои:10.1016/0950-3528(95)90057-8. PMID 8903801.
- ^ Matter L, Kogelschatz K, Germann D (апрель 1997 г.). «Уровни сывороточных антител к вирусу краснухи, указывающие на иммунитет: ответ на вакцинацию субъектов с низкими или неопределяемыми концентрациями антител». Журнал инфекционных болезней. 175 (4): 749–55. Дои:10.1086/513967. PMID 9086126.
- ^ Маллери Д.Л., Макьюэн В.А., Бидгуд С.Р., Тауэрс Г.Дж., Джонсон С.М., Джеймс Л.К. (ноябрь 2010 г.). «Антитела опосредуют внутриклеточный иммунитет через тройной мотив 21 (TRIM21)». Труды Национальной академии наук Соединенных Штатов Америки. 107 (46): 19985–90. Bibcode:2010ПНАС..10719985М. Дои:10.1073 / pnas.1014074107. ЧВК 2993423. PMID 21045130.
- ^ Каскальо М., Платт Дж. Л. (2007). «Новые функции В-клеток». Критические обзоры в иммунологии. 27 (2): 141–51. Дои:10.1615 / critrevimmunol.v27.i2.20. PMID 17725500.
- ^ Ле Паж С, Женин П., Бейн М.Г., Хискотт Дж. (2000). «Активация интерферона и врожденный иммунитет». Обзоры в Иммуногенетике. 2 (3): 374–86. PMID 11256746.
- ^ Хиллеман MR (октябрь 2004 г.). «Стратегии и механизмы выживания хозяина и патогена при острых и хронических вирусных инфекциях». Труды Национальной академии наук Соединенных Штатов Америки. 101 (Приложение 2): 14560–66. Bibcode:2004ПНАС..10114560Н. Дои:10.1073 / pnas.0404758101. ЧВК 521982. PMID 15297608.
- ^ Asaria P, MacMahon E (октябрь 2006 г.). «Корь в Соединенном Королевстве: можем ли мы искоренить ее к 2010 году?». BMJ. 333 (7574): 890–95. Дои:10.1136 / bmj.38989.445845.7C. ЧВК 1626346. PMID 17068034.
- ^ Лейн JM (2006). «Массовая вакцинация и эпиднадзор / сдерживание борьбы с оспой». Актуальные темы микробиологии и иммунологии. 304: 17–29. Дои:10.1007/3-540-36583-4_2. ISBN 978-3-540-29382-8. ЧВК 7120753. PMID 16989262.
- ^ Арвин AM, Гринберг HB (январь 2006 г.). «Новые вирусные вакцины». Вирусология. 344 (1): 240–49. Дои:10.1016 / j.virol.2005.09.057. PMID 16364754.
- ^ Пасторе П.П., Шудель А.А., Ломбард М. (август 2007 г.). «Выводы - будущие тенденции ветеринарной вакцинологии». Revue Scientifique et Technique. 26 (2): 489–94, 495–501, 503–09. Дои:10.20506 / rst.26.2.1759. PMID 17892169.
- ^ Палезе П (Январь 2006 г.). "Создание лучших вакцин против вируса гриппа?". Возникающие инфекционные заболевания. 12 (1): 61–65. Дои:10.3201 / eid1201.051043. ЧВК 3291403. PMID 16494719.
- ^ Томссен Р. (1975). «Живые аттенуированные вакцины против убитых вирусных вакцин». Монографии по аллергии. 9: 155–76. PMID 1090805.
- ^ Маклин А.А. (1986). «Разработка вакцин против гепатита А и гепатита В». Отзывы об инфекционных заболеваниях. 8 (4): 591–98. Дои:10.1093 / Clinids / 8.4.591. PMID 3018891.
- ^ Casswall TH, Fischler B (октябрь 2005 г.). «Вакцинация ребенка с ослабленным иммунитетом». Экспертный обзор вакцин. 4 (5): 725–38. Дои:10.1586/14760584.4.5.725. PMID 16221073. S2CID 40821818.
- ^ Barnett ED, Wilder-Smith A, Wilson ME (июль 2008 г.). «Вакцины против желтой лихорадки и международные путешественники». Экспертный обзор вакцин. 7 (5): 579–87. Дои:10.1586/14760584.7.5.579. PMID 18564013. S2CID 19352868.
- ^ Магден Дж., Кяэрияйнен Л., Ахола Т. (март 2005 г.). «Ингибиторы репликации вирусов: последние события и перспективы». Прикладная микробиология и биотехнология. 66 (6): 612–21. Дои:10.1007 / s00253-004-1783-3. ЧВК 7082807. PMID 15592828.
- ^ Миндел А., Сазерленд С. (сентябрь 1983 г.). «Генитальный герпес - заболевание и его лечение, в том числе ацикловир внутривенно». Журнал антимикробной химиотерапии. 12 (Дополнение B): 51–59. Дои:10.1093 / jac / 12.suppl_b.51. PMID 6355051.
- ^ Пальмизано Л., Велла С. (2011). «Краткая история антиретровирусной терапии ВИЧ-инфекции: успехи и проблемы». Annali dell'Istituto Superiore di Sanità. 47 (1): 44–48. Дои:10.4415 / ANN_11_01_10. PMID 21430338.
- ^ Witthöft T, Möller B, Wiedmann KH, Mauss S, Link R, Lohmeyer J и др. (Ноябрь 2007 г.). «Безопасность, переносимость и эффективность пегинтерферона альфа-2а и рибавирина при хроническом гепатите С в клинической практике: открытое испытание безопасности в Германии». Журнал вирусных гепатитов. 14 (11): 788–96. Дои:10.1111 / j.1365-2893.2007.00871.x. ЧВК 2156112. PMID 17927615.
- ^ Рудин Д., Шах С.М., Поцелуй А., Ветц Р.В., Соттиле В.М. (ноябрь 2007 г.). «Интерферон и ламивудин в сравнении с интерфероном при лечении гепатита В и антиген-положительного гепатита В: метаанализ рандомизированных контролируемых исследований». Liver International. 27 (9): 1185–93. Дои:10.1111 / j.1478-3231.2007.01580.x. ЧВК 2156150. PMID 17919229.
- ^ Диммок стр. 3
- ^ Горис Н., Ванденбуш Ф., Де Клерк К. (апрель 2008 г.). «Возможности противовирусной терапии и профилактики для борьбы с вирусными РНК-инфекциями домашнего скота». Противовирусные исследования. 78 (1): 170–78. Дои:10.1016 / j.antiviral.2007.10.003. PMID 18035428.
- ^ Кармайкл Л. Е. (2005). «Аннотированный исторический отчет о парвовирусе собак». Журнал ветеринарной медицины. B, Инфекционные болезни и ветеринарное здравоохранение. 52 (7–8): 303–11. Дои:10.1111 / j.1439-0450.2005.00868.x. PMID 16316389.
- ^ Чен Ю., Чжао Ю., Хаммонд Дж., Хсу Х. Т., Эванс Дж., Фельдлауфер М. (октябрь – ноябрь 2004 г.). «Множественные вирусные инфекции у медоносных пчел и расхождение генома вирусов медоносных пчел». Журнал патологии беспозвоночных. 87 (2–3): 84–93. Дои:10.1016 / j.jip.2004.07.005. PMID 15579317.
- ^ Шорс р. 802
- ^ Шорс с. 799–807.
- ^ Захир К., Ахтар М.Х. (2016). «Производство, использование и питание картофеля - обзор». Критические обзоры в области пищевой науки и питания. 56 (5): 711–21. Дои:10.1080/10408398.2012.724479. PMID 24925679. S2CID 33074838.
- ^ Фуэнтес С., Джонс Р.А., Мацуока Х., Охшима К., Кройце Дж., Гиббс А.Дж. (июль 2019 г.). «Картофельный вирус Y; связь с Анд». Эволюция вирусов. 5 (2): vez037. Дои:10.1093 / ve / vez037. ЧВК 6755682. PMID 31559020.
- ^ Динеш-Кумар SP, Tham WH, Baker BJ (декабрь 2000 г.). «Структурно-функциональный анализ гена устойчивости к вирусу табачной мозаики N». Труды Национальной академии наук Соединенных Штатов Америки. 97 (26): 14789–94. Bibcode:2000PNAS ... 9714789D. Дои:10.1073 / pnas.97.26.14789. ЧВК 18997. PMID 11121079.
- ^ Шорты с. 809.
- ^ Соосаар Дж. Л., Бурч-Смит ТМ, Динеш-Кумар СП (октябрь 2005 г.). «Механизмы устойчивости растений к вирусам». Обзоры природы. Микробиология. 3 (10): 789–98. Дои:10.1038 / nrmicro1239. PMID 16132037. S2CID 27311732.
- ^ Ломоносов Г.П. (2011). «Вирусные частицы и использование таких частиц в био- и нанотехнологиях». Последние достижения в вирусологии растений. Caister Academic Press. ISBN 978-1-904455-75-2.
- ^ Wommack KE, Colwell RR (март 2000 г.). «Вириопланктон: вирусы в водных экосистемах». Обзоры микробиологии и молекулярной биологии. 64 (1): 69–114. Дои:10.1128 / MMBR.64.1.69-114.2000. ЧВК 98987. PMID 10704475.
- ^ Bergh O, Børsheim KY, Bratbak G, Heldal M (август 1989 г.). «Большое количество вирусов, обнаруженных в водной среде». Природа. 340 (6233): 467–68. Bibcode:1989Натура.340..467Б. Дои:10.1038 / 340467a0. PMID 2755508. S2CID 4271861.
- ^ Шорс с. 834–35.
- ^ Бикл Т.А., Крюгер Д.Х. (июнь 1993 г.). «Биология рестрикции ДНК». Микробиологические обзоры. 57 (2): 434–50. Дои:10.1128 / MMBR.57.2.434-450.1993. ЧВК 372918. PMID 8336674.
- ^ Баррангу Р., Фремо С., Дево Х., Ричардс М., Боявал П., Муано С. и др. (Март 2007 г.). «CRISPR обеспечивает приобретенную устойчивость к вирусам у прокариот». Наука. 315 (5819): 1709–12. Bibcode:2007Научный ... 315.1709B. Дои:10.1126 / science.1138140. HDL:20.500.11794/38902. PMID 17379808. S2CID 3888761.
- ^ Brouns SJ, Jore MM, Lundgren M, Westra ER, Slijkhuis RJ, Snijders AP, et al. (Август 2008 г.). «Малые РНК CRISPR направляют противовирусную защиту прокариот». Наука. 321 (5891): 960–64. Bibcode:2008Sci ... 321..960B. Дои:10.1126 / science.1159689. ЧВК 5898235. PMID 18703739.
- ^ Мохика Ф.Дж., Родригес-Валера Ф. (сентябрь 2016 г.). «Открытие CRISPR у архей и бактерий». Журнал FEBS. 283 (17): 3162–69. Дои:10.1111 / фев.13766. HDL:10045/57676. PMID 27234458. S2CID 42827598.
- ^ Прангишвили Д., Гаррет Р.А. (апрель 2004 г.). «Исключительно разнообразные морфотипы и геномы гипертермофильных вирусов кренархей» (PDF). Сделки Биохимического Общества. 32 (Pt 2): 204–08. Дои:10.1042 / BST0320204. PMID 15046572.
- ^ Mojica FJ, Díez-Villaseñor C, García-Martínez J, Soria E (февраль 2005 г.). «Промежуточные последовательности регулярно расположенных прокариотических повторов происходят из чужеродных генетических элементов». Журнал молекулярной эволюции. 60 (2): 174–82. Bibcode:2005JMolE..60..174M. Дои:10.1007 / s00239-004-0046-3. PMID 15791728. S2CID 27481111.
- ^ Макарова К.С., Гришин Н.В., Шабалина С.А., Вольф Ю.И., Кунин Е.В. (март 2006 г.). «Предполагаемая иммунная система прокариот, основанная на РНК-интерференции: компьютерный анализ предсказанного ферментативного механизма, функциональные аналогии с эукариотической РНКи и гипотетические механизмы действия». Биология Директ. 1: 7. Дои:10.1186/1745-6150-1-7. ЧВК 1462988. PMID 16545108.
- ^ ван дер Ост Дж, Вестра ER, Джексон Р.Н., Виденхефт Б. (июль 2014 г.). «Раскрытие структурных и механических основ систем CRISPR-Cas». Обзоры природы. Микробиология. 12 (7): 479–92. Дои:10.1038 / nrmicro3279. ЧВК 4225775. PMID 24909109.
- ^ Давила-Рамос С., Кастелан-Санчес Х.Г., Мартинес-Авила Л., Санчес-Карбенте, доктор медицины, Перальта Р., Эрнандес-Мендоса А и др. (2019). «Обзор вирусной метагеномики в экстремальных условиях». Границы микробиологии. 10: 2403. Дои:10.3389 / fmicb.2019.02403. ЧВК 6842933. PMID 31749771.
- ^ Чжан Цюйи, Гуй Дж.Ф. (декабрь 2018 г.). «Разнообразие, эволюционный вклад и экологическая роль водных вирусов». Наука Китая. Науки о жизни. 61 (12): 1486–1502. Дои:10.1007 / s11427-018-9414-7. PMID 30443861. S2CID 53564176.
- ^ Weitz JS, Вильгельм SW (2013). «Море вирусов». Ученый. 27 (7): 35–39.
- ^ Suttle CA (сентябрь 2005 г.). «Вирусы в море». Природа. 437 (7057): 356–61. Bibcode:2005Натура.437..356S. Дои:10.1038 / природа04160. PMID 16163346. S2CID 4370363.
- ^ Вильгельм С.В., Саттл Калифорния (1999). «Вирусы и круговорот питательных веществ в море: вирусы играют решающую роль в структуре и функциях водных пищевых сетей». Бионаука. 49 (10): 781–88. Дои:10.2307/1313569. JSTOR 1313569.
- ^ Шелфорд Э.Дж., Саттл Калифорния (2018). «Опосредованный вирусами перенос азота от гетеротрофных бактерий к фитопланктону». Биогеонауки. 15 (3): 809–15. Bibcode:2018BGeo ... 15..809S. Дои:10.5194 / bg-15-809-2018.
- ^ а б c d Suttle CA (октябрь 2007 г.). «Морские вирусы - основные игроки в глобальной экосистеме». Обзоры природы. Микробиология. 5 (10): 801–12. Дои:10.1038 / nrmicro1750. PMID 17853907. S2CID 4658457.
- ^ Wigington CH, Sonderegger D, Brussaard CP, Buchan A, Finke JF, Fuhrman JA и др. (Январь 2016 г.). «Пересмотр взаимосвязи между морским вирусом и численностью микробных клеток» (PDF). Природная микробиология. 1 (15024): 15024. Дои:10.1038 / nmicrobiol.2015.24. PMID 27572161. S2CID 52829633.
- ^ Brussaard CP (2004). «Вирусный контроль популяций фитопланктона - обзор». Журнал эукариотической микробиологии. 51 (2): 125–38. Дои:10.1111 / j.1550-7408.2004.tb00537.x. PMID 15134247. S2CID 21017882.
- ^ Роббинс Дж. (13 апреля 2018 г.). «Триллионы и триллионы вирусов падают с неба каждый день». Нью-Йорк Таймс. Получено 14 апреля 2018.
- ^ Reche I, D'Orta G, Mladenov N, Winget DM, Suttle CA (апрель 2018 г.). «Скорость осаждения вирусов и бактерий над пограничным слоем атмосферы». Журнал ISME. 12 (4): 1154–62. Дои:10.1038 / с41396-017-0042-4. ЧВК 5864199. PMID 29379178.
- ^ Холл А.Дж., Джепсон П.Д., Гудман С.Дж., Харконен Т. (2006). «Вирус фокиновой чумы в Северном и Европейском морях - данные и модели, природа и воспитание». Биологическое сохранение. 131 (2): 221–29. Дои:10.1016 / j.biocon.2006.04.008.
- ^ Forterre P, Philippe H (июнь 1999 г.). «Последний универсальный общий предок (LUCA), простой или сложный?». Биологический бюллетень. 196 (3): 373–75, обсуждение 375–77. Дои:10.2307/1542973. JSTOR 1542973. PMID 11536914.
- ^ Кольер П. 8
- ^ Лодиш Х, Берк А, Зипурски С.Л., Мацудаира П., Балтимор Д., Дарнелл Дж. (2000). «Вирусы: структура, функции и использование». Молекулярная клеточная биология (4-е изд.). Нью-Йорк: У. Х. Фриман.
- ^ Мацузаки С., Рашель М., Учияма Дж., Сакураи С., Удихара Т., Курода М. и др. (Октябрь 2005 г.). «Бактериофаготерапия: оздоравливающая терапия против бактериальных инфекционных заболеваний». Журнал инфекций и химиотерапии. 11 (5): 211–19. Дои:10.1007 / s10156-005-0408-9. PMID 16258815. S2CID 8107934.
- ^ Глеба Ю.Ю., Гирич А (2011). "Растительные вирусные векторы для экспрессии белков". Последние достижения в вирусологии растений. Caister Academic Press. ISBN 978-1-904455-75-2.
- ^ Джефферсон А., кадет В. Е., Хильшер А. (сентябрь 2015 г.). «Механизмы генетически модифицированных вирусов осповакцины для лечения рака». Критические обзоры в онкологии / гематологии. 95 (3): 407–16. Дои:10.1016 / j.critrevonc.2015.04.001. PMID 25900073.
- ^ Каримхани С., Гонсалес Р., Деллавалле Р.П. (август 2014 г.). «Обзор новых методов лечения меланомы». Американский журнал клинической дерматологии. 15 (4): 323–37. Дои:10.1007 / s40257-014-0083-7. PMID 24928310. S2CID 38864550.
- ^ «FDA одобряет инъекционную иммунотерапию меланомы Amgen». Рейтер. 27 октября 2015 г.. Получено 24 января 2020.
- ^ Берк Дж., Ниева Дж., Борад MJ, Брайтбах CJ (август 2015 г.). «Онколитические вирусы: перспективы клинической разработки». Текущее мнение в вирусологии. 13: 55–60. Дои:10.1016 / j.coviro.2015.03.020. PMID 25989094.
- ^ Фишлехнер М, Донат Э (2007). «Вирусы как строительные блоки для материалов и устройств». Angewandte Chemie. 46 (18): 3184–93. Дои:10.1002 / anie.200603445. PMID 17348058.
- ^ Сото С.М., Блюм А.С., Вора Г.Дж., Лебедев Н., Мидор С.Е., Вон А.П. и др. (Апрель 2006 г.). «Усиление флуоресцентного сигнала карбоцианиновых красителей с использованием созданных вирусных наночастиц». Журнал Американского химического общества. 128 (15): 5184–89. Дои:10.1021 / ja058574x. PMID 16608355.
- ^ Блюм А.С., Сото С.М., Уилсон С.Д., Брауэр Т.Л., Поллак С.К., Шулл Т.Л. и др. (Июль 2005 г.). «Спроектированный вирус как каркас для трехмерной самосборки на наноуровне». Маленький. 1 (7): 702–06. Дои:10.1002 / smll.200500021. PMID 17193509.
- ^ Виолончель J, Пол А.В., Виммер Э. (август 2002 г.). «Химический синтез кДНК полиовируса: создание инфекционного вируса в отсутствие естественной матрицы». Наука. 297 (5583): 1016–18. Bibcode:2002Sci ... 297.1016C. Дои:10.1126 / science.1072266. PMID 12114528. S2CID 5810309.
- ^ Коулман Дж. Р., Папамихаил Д., Скиена С., Футчер Б., Виммер Е., Мюллер С. (июнь 2008 г.). «Ослабление вируса за счет изменений в масштабе генома в смещении пар кодонов». Наука. 320 (5884): 1784–87. Bibcode:2008Sci ... 320.1784C. Дои:10.1126 / science.1155761. ЧВК 2754401. PMID 18583614.
- ^ «База данных вирусного генома NIH». Ncbi.nlm.nih.gov. Получено 15 ноября 2017.
- ^ Жилинскас Р.А. (август 2017 г.). «Краткая история программ биологического оружия и использования патогенов животных в качестве боевых биологических агентов». Revue Scientifique et Technique (Международное бюро эпизоотии). 36 (2): 415–422. Дои:10.20506 / rst.36.2.2662. PMID 30152475.
- ^ а б c Артенштейн А.В., Грабенштейн Д.Д. (октябрь 2008 г.). «Противооспенные вакцины для биозащиты: необходимость и возможность». Экспертный обзор вакцин. 7 (8): 1225–37. Дои:10.1586/14760584.7.8.1225. PMID 18844596. S2CID 33855724.
Библиография
- Кольер Л., Баловс А., Сассман М. (1998). Махи, Б., Кольер Л.А. (ред.). Микробиология и микробные инфекции Топли и Вильсона. Вирусология. 1 (Девятое изд.). ISBN 0-340-66316-2.
- Диммок Нью-Джерси, Истон А.Дж., Леппард К. (2007). Введение в современную вирусологию (Шестое изд.). Блэквелл Паблишинг. ISBN 978-1-4051-3645-7.
- Книп Д.М., Хоули П.М., Гриффин Д.Е., Лэмб Р.А., Мартин М.А., Ройзман Б., Straus SE (2007). Области вирусологии. Липпинкотт Уильямс и Уилкинс. ISBN 978-0-7817-6060-7.
- Шорс Т (2017). Понимание вирусов. Джонс и Бартлетт Издательство. ISBN 978-1-284-02592-7.


