Круговая хромосома - Circular chromosome
А круговая хромосома хромосома в бактерии, археи, митохондрии, и хлоропласты, в виде молекулы кольцевой ДНК, в отличие от линейная хромосома из большинства эукариоты.
Большинство хромосом прокариот содержат кольцевую молекулу ДНК - у них нет свободных концов. ДНК. В противном случае свободные концы создали бы серьезные проблемы для ячеек в отношении Репликация ДНК и стабильность. Клетки, которые действительно содержат хромосомы с концами ДНК, или теломеры (большинство эукариот) приобрели сложные механизмы для преодоления этих проблем. Однако круглая хромосома может создавать другие проблемы для клеток. После репликации две кольцевые хромосомы потомства могут иногда оставаться взаимосвязанными или запутанными, и они должны быть разрешены таким образом, чтобы каждая клетка унаследовала одну полную копию хромосомы во время деление клеток.
Репликация

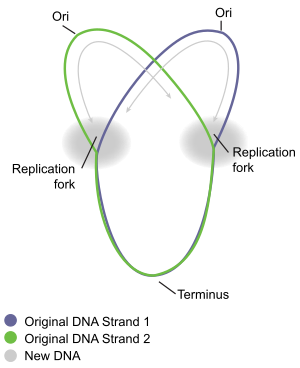
Репликация хромосом циркулярных бактерий лучше всего изучена у хорошо изученных бактерий. кишечная палочка и Bacillus subtilis. Репликация хромосомы происходит в три основных этапа: инициация, удлинение и завершение. Стадия инициации начинается с упорядоченной сборки «инициаторных» белков в исходной области хромосомы, называемой ORIC. Эти этапы сборки регулируются, чтобы репликация хромосом происходила только один раз в каждом клеточном цикле. Во время фазы удлинения репликации ферменты которые были собраны в oriC во время инициации, проходят вдоль каждого плеча ("репликор ") хромосомы в противоположных направлениях от oriC, реплицируя ДНК для создания двух идентичных копий. Этот процесс известен как двунаправленная репликация. Вся совокупность молекул, участвующих в репликации ДНК на каждом плече, называется"ответственный. "В авангарде реплисома ДНК-геликаза которая раскручивает две нити ДНК, создавая движение "вилка репликации ". Две развернутые одиночные нити ДНК служат шаблонами для ДНК-полимераза, который перемещается вместе с геликазой (вместе с другими белками), чтобы синтезировать комплементарную копию каждой цепи. Таким образом создаются две идентичные копии исходной ДНК. В конце концов, две репликационные вилки, движущиеся по круговой хромосоме, встречаются в определенной зоне хромосомы, приблизительно противоположной oriC, называемой конечной областью. Затем ферменты удлинения разбираются, и две «дочерние» хромосомы разделяются до завершения деления клетки.
Посвящение
В Кишечная палочка начало бактериальной репликации, называемое ORIC состоит из Последовательности ДНК которые признаны DnaA белок, который высоко консервативен среди различных бактериальный разновидность. Связывание DnaA с источником инициирует регулируемый набор других ферментов и белки это в конечном итоге приведет к созданию двух полных реплисом для двунаправленной репликации.[1]
Элементы последовательности ДНК внутри ОриC, которые важны для его функции, включают DnaA-боксы, 9-мерный повтор с высококонсервативной консенсусной последовательностью 5 '- TTATCCACA - 3',[2] которые распознаются белком DnaA. Белок DnaA играет решающую роль в инициации репликации хромосомной ДНК.[3] Связан с АТФ и с помощью бактериального гистон -подобные белки [HU] DnaA затем раскручивают богатую АТ область около левой границы ORIC, который несет три 13-мерных мотива,[4] и открывает двухцепочечная ДНК для входа других белков репликации.[5]
Эта область также содержит четыре последовательности «GATC», которые распознаются ДНК аденин метилаза (Dam), фермент, который изменяет основание аденина, когда эта последовательность неметилирована или гемиметилирована. В метилирование из аденины важен, поскольку он изменяет конформацию ДНК, способствуя разделению цепей,[6] и кажется, что эта область ОриУ C есть естественная склонность к расслаблению.[7]
Затем DnaA привлекает репликативную геликаза, DnaB, из комплекса DnaB-DnaC в развернутую область с образованием комплекса предварительного прайминга.[8] После того, как DnaB перемещается к вершине каждой репликационной вилки, геликаза как раскручивает родительскую ДНК, так и мгновенно взаимодействует с ней. прима.[9]
Чтобы репликация ДНК продолжалась, одноцепочечные связывающие белки необходимы для предотвращения образования вторичных структур отдельными цепями ДНК и предотвращения их образования. повторный отжиг. Кроме того, ДНК-гираза необходим для снятия топологического напряжения, создаваемого действием геликазы DnaB.
Удлинение
Когда репликационная вилка движется по кругу, структура в форме греческой буквы тета Ө формируется. Джон Кэрнс продемонстрировал тета-структура репликации хромосомы E. coli в 1963 году, используя инновационный метод визуализации репликации ДНК. В своем эксперименте он радиоактивно маркированный хромосомы, выращивая его культуры в среде, содержащей 3H-тимидин. В нуклеозид основание было равномерно включено в бактериальную хромосому. Затем он выделил хромосомы, осторожно лизируя клетки, и поместил их на электронная микрофотография (EM) сетка, которую он выставил рентгеновский снимок фильм за два месяца. Этот эксперимент четко демонстрирует модель тета-репликации кольцевых бактериальных хромосом.[10]
- См. Авторадиографию интактной реплицирующейся хромосомы Кишечная палочка [1]
Как описано выше, репликация бактериальной хромосомы происходит двунаправленным образом. Это было впервые продемонстрировано путем специальной маркировки реплицирующихся бактериальных хромосом радиоактивные изотопы. Затем участки ДНК, реплицируемые во время эксперимента, визуализировали с помощью авторадиография и микроскопическое исследование проявленной пленки. Это позволило исследователям увидеть, где происходит репликация. Первые убедительные наблюдения двунаправленной репликации были получены в результате исследований B. subtilis.[11] Вскоре после этого было показано, что хромосома E. coli двунаправленно реплицируется.[12]
- См. Рисунок 4 Д. М. Прескотта и П. Л. Куэмпеля (1972): гусеница, произведенная Кишечная палочка хромосома из клеток, помеченная в течение 19 минут [3H] тимином, с последующей маркировкой в течение 2,5 минут [3H] тимином и ['H] тимидином. [2].
В Кишечная палочка Холофермент ДНК-полимераза III представляет собой комплекс 900 кДа, обладающий по существу димерный структура. Каждый мономерный установка имеет каталитическую сердцевину, димеризация субъединица, а процессивность компонент .[13] DNA Pol III использует один набор своих основных субъединиц для синтеза ведущая нить непрерывно, в то время как другой набор основных субъединиц циклически Фрагмент Окадзаки к следующему на петле отстающая нить. Синтез ведущей цепи начинается с синтеза короткого Праймер РНК в начале репликации ферментом Примазой (DnaG белок).
Дезоксинуклеотиды затем добавляются к этому праймеру с помощью единственного димера ДНК-полимеразы III в интегрированном комплексе с DnaB-геликазой. Затем синтез ведущей цепи происходит непрерывно, в то время как ДНК одновременно разматывается на вилке репликации. Напротив, синтез отстающей цепи осуществляется короткими фрагментами Окадзаки. Во-первых, праймер РНК синтезируется примазой, и, как и при синтезе ведущей цепи, ДНК Pol III связывается с праймером РНК и добавляет дезоксирибонуклеотиды.
Когда синтез фрагмента Окадзаки завершается, репликация останавливается, и основные субъединицы ДНК Pol III диссоциируют от β-скользящего зажима [скользящий хлопок B - это процессивная субъединица ДНК Pol III].[14] Праймер РНК удаляется и заменяется ДНК на ДНК-полимераза I [который также обладает функцией корректуры экзонуклеаза активность], а оставшийся ник запечатан ДНК-лигаза, который затем лигирует эти фрагменты с образованием отстающей нити.
Значительная часть (10-15%) вилок репликации, происходящих из oriC, сталкивается с Повреждение ДНК или разрыв цепи, когда клетки выращивают в нормальных лабораторных условиях (без обработки, повреждающей экзогенную ДНК).[15] Обнаруженные повреждения ДНК обычно обрабатываются рекомбинационный ферменты репарации, позволяющие продолжать развитие репликационной вилки.[15]
Прекращение

Прекращение - это процесс слияния вилок репликации и разборки реплисом с образованием двух отдельных и полных Молекулы ДНК. Это происходит в области конца, примерно напротив oriC на хромосоме (рис. 5). Конечная область содержит несколько участков терминатора репликации ДНК или "Ter" сайтов. Специальный белок "терминатор репликации" должен быть связан на сайте Ter, чтобы он мог приостановить репликацию. Каждый сайт Ter имеет полярность действия, то есть он будет задерживать вилку репликации, приближающуюся к сайту Ter с одного направления, но позволит беспрепятственное движение вилки через сайт Ter с другого направления. Расположение участков Тер формирует две противоположные группы, которые заставляют две развилки встречаться друг с другом в пределах области, которую они охватывают. Такое расположение называется «ловушкой репликационной вилки».[16]
- См. Положения и последовательности концов репликации E. coli.(A) Карта, показывающая Ори и сайты 10 Тер. (B) Консенсусная последовательность Ter. [3]
Сайты Ter специфически взаимодействуют с белком терминатора репликации, называемым Тус в Кишечная палочка.[17] Комплекс Тус-Тер препятствует Раскрутка ДНК DnaB зависимо от ориентации.[18]
- В Кристальная структура белкового комплекса Ter DNA-Tus (A), показывающий неблокирующую и блокирующую вилку грани Tus. (B) Вид в разрезе поверхности, задерживающей геликазу.[4]
Репликация ДНК, разделяющей противоположные ответвления репликации, оставляет завершенные хромосомы соединенными как «катенаны ’Или топологически связанных кругов. Круги не связаны ковалентно, но их нельзя разделить, потому что они переплетены, и каждый из них ковалентно замкнут. Связанные круги требуют действия топоизомеразы разделить круги [декатанация]. В E.coli ДНК-топоизомераза IV играет основную роль в разделении связанных хромосом, временно разрывая обе нити ДНК одной хромосомы и позволяя другой хромосоме пройти через разрыв.
Была некоторая путаница в отношении роли ДНК-гираза играет в десятичной дроби. Чтобы определить номенклатуру, существует два типа топоизомераз: тип I вызывает временные одноцепочечные разрывы в ДНК, а тип II дает временные двухцепочечные разрывы. В результате фермент типа I удаляет суперспирали из ДНК по одной, тогда как фермент типа II удаляет суперспирали по две за раз. Топо I обоих прокариоты а эукариоты - топоизомераза типа I. Эукариотический топо II, бактериальная гираза и бактериальный топо IV относятся к типу II.
Мы часто забываем, что ДНК-гираза действительно обладает активностью топоизомеразы типа II; таким образом, поскольку он является гомологом топоизомеразы IV (также обладающим активностью топоизомеразы II), мы ожидаем сходства в функциях двух белков. Предварительная роль ДНК-гиразы состоит в том, чтобы ввести отрицательные суперспирали в ДНК, тем самым расслабляя положительные суперспирали, которые вступают в игру во время репликации ДНК. Топоизомераза IV также расслабляет положительные суперспирали, поэтому ДНК-гираза и топоизомераза IV играют почти идентичную роль в удалении положительных суперспиралей перед транслоцирующей ДНК-полимеразой, позволяя репликации ДНК продолжаться без препятствий топологической деформации.[19]
Путаница возникает, когда некоторые научная литература утверждают, что ДНК-гираза является единственным ферментом, ответственным за декатанацию. В эксперименте, проведенном Zechiedrich, Khodursky и Cozzarelli в 1997 году, было обнаружено, что топоизомераза IV является единственной важной декатеназой промежуточных продуктов репликации ДНК у бактерий.[20] В этом конкретном эксперименте, когда ингибировалась только ДНК-гираза, большинство катенанов не были связаны. Однако, когда ингибировалась только топоизомераза IV, декатенация почти полностью блокировалась. Полученные результаты позволяют предположить, что топоизомераза IV является первичной декаатеназой. in vivo, и хотя ДНК-гираза действительно играет роль в декатенации, ее функция не так важна, как топоизомераза IV, в декатентации взаимосвязанных хромосом.
Благодарности
Это основано на статье Ималды Девапаранам и Дэвида Трайба, опубликованной на условиях лицензирования CC by SA в рамках университетского курса на факультете микробиологии и иммунологии Мельбурнского университета, 2007 г.
Смотрите также
Рекомендации
В этой статье использованы материалы из Citizendium статья "Репликация круговой бактериальной хромосомы "под лицензией Creative Commons Attribution-ShareAlike 3.0 Непортированная лицензия но не под GFDL.
- ^ Джон М. Кагуни DnaA: контроль инициации репликации бактериальной ДНК и многое другое. Анну. Rev. Microbiol. 2006. 60: 351–71.
- ^ К. Вайгель, А. Шмидт, Б. Рюкерт, Р. Лурц и В. Мессер. Связывание белка DnaA с отдельными блоками DnaA в ориджине репликации Escherichia coli, oriC. EMBO J. 1997 г., 3 ноября; 16 (21): 6574–6583.
- ^ Hirota Y, Mordoh J и Jacob F (1970) О процессе деления клеток в Escherichia coli III. Термочувствительные мутанты Escherichia coli изменяются в процессе инициации ДНК. J Mol Biol, 53, 369–387.
- ^ Брамхилл Д., Корнберг А. 1988. Открытие дуплекса белком dnaA в новых последовательностях в инициации репликации в источнике хромосомы E. coli. Ячейка 52: 743–55
- ^ Sekimizu K, Bramhill D и Kornberg A (1987) АТФ активирует белок dnaA, инициируя репликацию плазмид, несущих начало хромосомы E.coli. Ячейка, 50, 259–265
- ^ Gotoh O, Tagashira Y. 1981. Расположение часто открывающихся областей на природных ДНК и их связь с функциональными локусами. Биополимеры 20: 1043–58
- ^ Ковальски Д., Эдди М.Дж. 1989. Элемент раскручивания ДНК: новый цис-действующий компонент, который способствует раскрытию ориджина репликации Escherichia coli. EMBO J. 8: 4335–44
- ^ Карр К. М., Кагуни Дж. М.. 2001. Стехиометрия белков DnaA и DnaB в инициации в хромосомном происхождении Escherichia coli. J. Biol. Chem. 276: 44919–25
- ^ Тугу К., Марианс К.Дж. 1996. Взаимодействие между геликазой и примазой устанавливает часы репликационной вилки. J. Biol. Chem. 271: 21398–405
- ^ Кэрнс, Дж. П .: Симпозиумы Колд-Спринг-Харбор по количественной биологии 28:44, 1963.
- ^ Уэйк, Р. 1972. Визуализация повторно инициированных хромосом в Bacillus subtilis. J Mol Biol. 28 июля; 68 (3): 501-9.
- ^ Прескотт Д.М., Куэмпель П.Л. 1972. Двунаправленная репликация хромосомы у Escherichia coli. Proc Natl Acad Sci U S. A. Oct; 69 (10): 2842-5.
- ^ О'Доннелл М., Джерузалми Д., Куриян Дж. Структура загрузчика зажимов предсказывает архитектуру холофермента ДНК-полимеразы III и RFC. Curr. Биол. 11 R935-R946 2001 г.
- ^ Индиани К., О'Доннелл М. Механизм треугольного ключа в открытии бета-скользящего зажима. J Biol Chem. 10 октября 2003 г .; 278 (41): 40272-81. Epub 2003 8 июля.
- ^ а б Кокс MM (1998). «Расширенный взгляд на рекомбинационную репарацию ДНК в бактериях». Гены Клетки. 3 (2): 65–78. Дои:10.1046 / j.1365-2443.1998.00175.x. PMID 9605402.
- ^ Дуггин И.Г., Уэйк Р.Г., Белл С.Д., Хилл TM. 2008. Ловушка репликационной вилки и прекращение репликации хромосом. Mol Microbiol. Декабрь; 70 (6): 1323–33.
- ^ Камада К., Хориучи Т., Осуми К., Шимамото Н., Морикава К. 1996. Структура белка терминатора репликации в комплексе с ДНК. Природа, 17; 383 (6601): 598–603.
- ^ Каплан Д.Л., Бастия Д. 2009. Механизмы полярной остановки репликационной вилки. Mol Microbiol. 72 (2): 279-85.
- ^ Крис Ульспергер и Николас Р. Коццарелли. Противопоставление ферментативной активности топоизомеразы IV и ДНК-гиразы из Escherichia coli. Volume 271, Number 49, Issue от 6 декабря 1996 г., стр. 31549-31555
- ^ Э. Л. Зехедрих, А. Б. Ходурский, Н. Р. Коццарелли. Топоизомераза IV, а не гираза, декатенирует продукты сайт-специфической рекомбинации у Escherichia coli. Genes Dev. 1997, 1 октября; 11 (19): 2580-92 9334322
