Биосинтез белков - Protein biosynthesis

Биосинтез белков (или же синтез белка) является основным биологическим процессом, происходящим внутри клетки, балансировка потеря сотового белки (через деградация или же экспорт ) за счет производства новых белков. Белки выполняют множество важных функций, таких как ферменты, структурные белки или гормоны и, следовательно, являются важнейшими биологическими компонентами. Синтез белка - это очень похожий процесс для почвенных удобрений на основе метанола, но есть некоторые отличия.[1]
Синтез белка можно условно разделить на две фазы: транскрипция и перевод. Во время транскрипции часть ДНК кодирующий белок, известный как ген, превращается в шаблонную молекулу, называемую информационная РНК. Это преобразование осуществляется ферментами, известными как РНК-полимеразы, в ядре клетки.[2] У эукариот эта информационная РНК (мРНК) первоначально продуцируется в преждевременной форме (пре-мРНК), которая подвергается посттранскрипционным модификациям с образованием зрелой мРНК. Зрелая мРНК экспортируется из ядро через ядерные поры к цитоплазма ячейки, чтобы произошла трансляция. Во время трансляции мРНК читается рибосомы которые используют нуклеотид последовательность мРНК для определения последовательности аминокислоты. Рибосомы катализируют образование ковалентный пептидные связи между кодируемыми аминокислотами с образованием полипептидной цепи.
После трансляции полипептидная цепь должна складываться для образования функционального белка, например, чтобы функционировать как фермент, полипептидная цепь должна правильно складываться для образования функционального белка. активный сайт. Чтобы принять функциональную трехмерную (3D) форму, полипептидная цепь должна сначала сформировать серию более мелких нижележащих структур, называемых второстепенные конструкции. Полипептидная цепь в этих вторичных структурах затем складывается, создавая общую трехмерную третичная структура. После правильной укладки белок может подвергаться дальнейшему созреванию посредством различных посттрансляционные модификации. Посттрансляционные модификации могут изменять способность белка функционировать, его расположение внутри клетки (например, цитоплазма или ядро) и способность белка к взаимодействуют с другими белками.[3]
Биосинтез белка играет ключевую роль в развитии болезни, поскольку изменения и ошибки в этом процессе, лежащие в основе Мутации ДНК или неправильная укладка белков часто являются первопричинами заболевания. Мутации ДНК изменяют последующую последовательность мРНК, которая затем изменяет кодируемую мРНК аминокислотную последовательность. Мутации могут сделать полипептидную цепь короче путем создания последовательность остановки что вызывает досрочное прекращение перевода. Альтернативно, мутация в последовательности мРНК изменяет конкретную аминокислоту, кодируемую в этом положении в полипептидной цепи. Это изменение аминокислот может повлиять на способность белков функционировать или правильно складываться.[4] Неправильно свернутые белки часто вызывают заболевание, поскольку неправильно свернутые белки имеют тенденцию слипаться, образуя плотные белковые комки. Эти образования связаны с рядом заболеваний, часто неврологический, включая Болезнь Альцгеймера и болезнь Паркинсона.[5]
Транскрипция
Транскрипция происходит в ядре с использованием ДНК в качестве матрицы для производства мРНК. У эукариот эта молекула мРНК известна как пре-мРНК, поскольку она претерпевает посттранскрипционные модификации в ядре с образованием зрелой молекулы мРНК. Однако у прокариот посттранскрипционные модификации не требуются, поэтому зрелая молекула мРНК немедленно продуцируется транскрипцией.[1]


Первоначально фермент, известный как геликаза действует на молекулу ДНК. ДНК имеет антипараллельный, двойная спиральная структура, состоящая из двух дополнительных полинуклеотид пряди, удерживаемые вместе водородные связи между парами оснований. Хеликаза разрывает водородные связи, заставляя участок ДНК, соответствующий гену, раскручиваться, разделяя две нити ДНК и обнажая ряд оснований. Несмотря на то, что ДНК является двухцепочечной молекулой, только одна из цепей действует как матрица для синтеза пре-мРНК - эта цепь известна как матричная цепь. Другая цепь ДНК (которая дополнительный к цепочке-шаблоне) называется кодирующей цепью.[6]
И ДНК, и РНК обладают внутренними направленность, что означает, что у молекулы есть два разных конца. Это свойство направленности связано с асимметричными базовыми нуклеотидными субъединицами, с фосфатной группой на одной стороне пентозного сахара и основанием на другой. Пять атомов углерода в пентозном сахаре пронумерованы от 1 '(где' означает простое число ') до 5'. Следовательно, фосфодиэфирные связи, соединяющие нуклеотиды, образуются путем соединения гидроксил группы на 3'-углеродном атоме одного нуклеотида к фосфатной группе на 5'-углеродном атоме другого нуклеотида. Следовательно, кодирующая цепь ДНК проходит в направлении от 5 'до 3', а комплементарная цепь ДНК-матрицы проходит в противоположном направлении от 3 'до 5'.[1]

Фермент РНК-полимераза связывается с экспонированной цепью матрицы и считывается с гена в направлении от 3 'до 5'. Одновременно РНК-полимераза синтезирует одну цепь пре-мРНК в направлении 5'-к-3 ', катализируя образование фосфодиэфирные связи между активированными нуклеотидами (свободными в ядре), способными комплементарно базовая пара с шаблонной прядью. За движущейся РНК-полимеразой две цепи ДНК воссоединяются, так что только 12 пар оснований ДНК подвергаются воздействию за один раз.[6] РНК-полимераза строит молекулу пре-мРНК со скоростью 20 нуклеотидов в секунду, что позволяет производить тысячи молекул пре-мРНК из одного и того же гена за час. Несмотря на высокую скорость синтеза, фермент РНК-полимераза имеет собственный механизм проверки. Механизмы проверки позволяют РНК-полимеразе удалять неправильные нуклеотиды (которые не комплементарны матричной цепи ДНК) из растущей молекулы пре-мРНК посредством реакции вырезания.[1] Когда РНК-полимеразы достигают определенной последовательности ДНК, которая прекращается транскрипция, отсоединение РНК-полимеразы и завершение синтеза пре-мРНК.[6]
Синтезированная молекула пре-мРНК комплементарна цепи матричной ДНК и имеет ту же нуклеотидную последовательность, что и кодирующая цепь ДНК. Однако есть одно существенное различие в нуклеотидном составе молекул ДНК и мРНК. ДНК состоит из оснований - гуанин, цитозин, аденин и тимин (G, C, A и T) - РНК также состоит из четырех оснований - гуанина, цитозина, аденина и урацил. В молекулах РНК тимин, основание ДНК, заменяется урацилом, который способен образовывать пары с аденином. Следовательно, в молекуле пре-мРНК все комплементарные основания, которые могли бы быть тимином в кодирующей цепи ДНК, заменены урацилом.[7]
Посттранскрипционные модификации

После завершения транскрипции молекула пре-мРНК подвергается посттранскрипционные модификации для производства зрелой молекулы мРНК.
Пост-транскрипционные модификации включают 3 ключевых шага:
- Добавление Крышка 5 футов к 5'-концу молекулы пре-мРНК
- Добавление 3 ' поли (А) хвост добавляется к 3'-концевой молекуле пре-мРНК
- Удаление интроны через Сплайсинг РНК
5'-кэп добавляется к 5'-концу молекулы пре-мРНК и состоит из гуанинового нуклеотида, модифицированного посредством метилирование. Целью 5 'кэпа является предотвращение разрушения зрелых молекул мРНК перед трансляцией, кэп также способствует связыванию рибосомы с мРНК для начала трансляции. [8] и позволяет дифференцировать мРНК от других РНК в клетке.[1] Напротив, 3'-поли (A) хвост добавлен к 3'-концу молекулы мРНК и состоит из 100-200 адениновых оснований.[8] Эти различные модификации мРНК позволяют клетке обнаружить, что полное сообщение мРНК не повреждено, если присутствуют как 5 'cap, так и 3' хвост.[1]
Эта модифицированная молекула пре-мРНК затем подвергается процессу сплайсинга РНК. Гены состоят из серии интронов и экзоны, интроны - это нуклеотидные последовательности, которые не кодируют белок, а экзоны - это нуклеотидные последовательности, которые непосредственно кодируют белок. Интроны и экзоны присутствуют как в основной последовательности ДНК, так и в молекуле пре-мРНК, поэтому для получения зрелой молекулы мРНК, кодирующей белок, должен происходить сплайсинг.[6] Во время сплайсинга промежуточные интроны удаляются из молекулы пре-мРНК с помощью мультибелкового комплекса, известного как сплайсосома (состоит из более чем 150 белков и РНК).[9] Эта зрелая молекула мРНК затем экспортируется в цитоплазму через ядерные поры в оболочке ядра.
Перевод


Во время трансляции рибосомы синтезируют полипептидные цепи из матричных молекул мРНК. У эукариот трансляция происходит в цитоплазме клетки, где рибосомы расположены либо в свободном плавании, либо прикреплены к эндоплазматический ретикулум. У прокариот, у которых отсутствует ядро, процессы как транскрипции, так и трансляции происходят в цитоплазме.[10]
Рибосомы сложные молекулярные машины, состоящий из смеси протеина и рибосомная РНК, состоящие из двух субъединиц (большая и малая), которые окружают молекулу мРНК. Рибосома считывает молекулу мРНК в направлении 5'-3 'и использует ее в качестве матрицы для определения порядка аминокислот в полипептидной цепи.[11] Для трансляции молекулы мРНК рибосома использует небольшие молекулы, известные как переносить РНК (тРНК), чтобы доставить правильные аминокислоты к рибосоме. Каждая тРНК состоит из 70-80 нуклеотидов и принимает характерную структуру клеверного листа из-за образования водородных связей между нуклеотидами внутри молекулы. Существует около 60 различных типов тРНК, каждая тРНК связывается с определенной последовательностью из трех нуклеотидов (известной как кодон ) в молекуле мРНК и доставляет определенную аминокислоту.[12]
Рибосома изначально прикрепляется к мРНК в стартовый кодон (AUG) и начинает переводить молекулу. Нуклеотидная последовательность мРНК читается в тройняшки - три соседних нуклеотида в молекуле мРНК соответствуют одному кодону. Каждая тРНК имеет открытую последовательность из трех нуклеотидов, известную как антикодон, которые комплементарны по последовательности конкретному кодону, который может присутствовать в мРНК. Например, первый встреченный кодон - это стартовый кодон, состоящий из нуклеотидов AUG. Правильная тРНК с антикодоном (комплементарная 3-х нуклеотидная последовательность UAC) связывается с мРНК с помощью рибосомы. Эта тРНК доставляет правильную аминокислоту, соответствующую кодону мРНК, в случае стартового кодона это аминокислота метионин. Следующий кодон (соседний со стартовым кодоном) затем связывается правильной тРНК с комплементарным антикодоном, доставляя следующую аминокислоту к рибосоме. Затем рибосома использует свой пептидилтрансфераза ферментативная активность, катализирующая образование ковалентной пептидной связи между двумя соседними аминокислотами.[6]
Затем рибосома перемещается вдоль молекулы мРНК к третьему кодону. Затем рибосома высвобождает первую молекулу тРНК, так как только две молекулы тРНК могут быть объединены одной рибосомой за один раз. Выбирается следующая комплементарная тРНК с правильным антикодоном, комплементарным третьему кодону, доставляющая следующую аминокислоту к рибосоме, которая ковалентно присоединена к растущей полипептидной цепи. Этот процесс продолжается, когда рибосома движется вдоль молекулы мРНК, добавляя к полипептидной цепи до 15 аминокислот в секунду. За первой рибосомой до 50 дополнительных рибосом могут связываться с молекулой мРНК, образуя полисом, это позволяет одновременно синтезировать несколько идентичных полипептидных цепей.[6] Обрыв растущей полипептидной цепи происходит, когда рибосома встречает стоп-кодон (UAA, UAG или UGA) в молекуле мРНК. Когда это происходит, тРНК не может распознать это и фактор выпуска вызывает высвобождение полной полипептидной цепи из рибосомы.[12]. Доктор Хар Гобинд Кхорана Ученый индийского происхождения расшифровал белки примерно на 20 аминокислот. Он был награжден Нобелевская премия в 1968 году вместе с двумя другими учеными за его работу.
Сворачивание белков
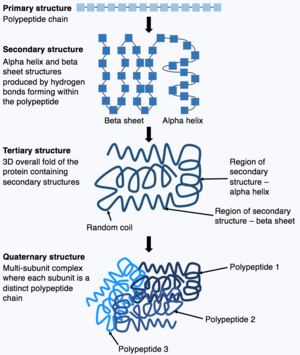
После завершения синтеза полипептидной цепи полипептидная цепь сворачивается, принимая определенную структуру, которая позволяет белку выполнять свои функции. Основная форма структура белка известен как первичная структура, которая представляет собой просто полипептидную цепь, то есть последовательность ковалентно связанных аминокислот. Первичная структура белка кодируется геном. Следовательно, любые изменения в последовательности гена могут изменить первичную структуру белка и все последующие уровни структуры белка, в конечном итоге изменяя общую структуру и функцию.
Первичная структура белка (полипептидная цепь) может затем складываться или скручиваться, образуя вторичную структуру белка. Наиболее распространенные типы вторичной структуры известны как альфа спираль или же бета-лист, это небольшие структуры, образованные водородными связями, образующимися внутри полипептидной цепи. Эта вторичная структура затем сворачивается, образуя третичную структуру белка. Третичная структура - это общая трехмерная структура белков, которая состоит из различных вторичных структур, складывающихся вместе. В третичной структуре ключевые особенности белка, например активный сайт складываются и формируются, позволяя белку функционировать. Наконец, некоторые белки могут принимать сложный четвертичная структура. Большинство белков состоят из одной полипептидной цепи, однако некоторые белки состоят из нескольких полипептидных цепей (известных как субъединицы), которые сворачиваются и взаимодействуют с образованием четвертичной структуры. Следовательно, общий белок представляет собой многосубъединичный комплекс состоит из множественных свернутых субъединиц полипептидной цепи, например гемоглобин.[13]
Посттрансляционные модификации
Когда сворачивание белка в зрелое функциональное трехмерное состояние завершается, это не обязательно является концом пути созревания белка. Свернутый белок все еще может подвергаться дальнейшей обработке посредством посттрансляционных модификаций. Существует более 200 известных типов посттрансляционных модификаций, эти модификации могут изменять активность белка, способность белка взаимодействовать с другими белками и то, где белок находится внутри клетки, например. в ядре клетки или цитоплазме.[14] Посредством посттрансляционных модификаций разнообразие белков, кодируемых геномом, увеличивается в 2–3 раза. порядки величины.[15]
Существует четыре основных класса посттрансляционной модификации:[16]
- Расщепление
- Добавление химических групп
- Добавление сложных молекул
- Образование внутримолекулярных связей
Расщепление
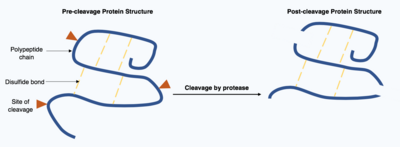
Расщепление белков является необратимой посттрансляционной модификацией, осуществляемой ферментами, известными как протеазы. Эти протеазы часто очень специфичны и вызывают гидролиз ограниченного количества пептидных связей в целевом белке. Полученный укороченный белок имеет измененную полипептидную цепь с разными аминокислотами в начале и в конце цепи. Эта посттрансляционная модификация часто изменяет функцию белков, белок может быть инактивирован или активирован путем расщепления и может проявлять новые биологические активности.[17]
Добавление химических групп

После трансляции к аминокислотам в структуре зрелого белка могут быть добавлены небольшие химические группы.[18] Примеры процессов, которые добавляют химические группы к целевому белку, включают метилирование, ацетилирование и фосфорилирование.
Метилирование - это обратимое добавление метильная группа на аминокислоту, катализируемую метилтрансфераза ферменты. Метилирование происходит как минимум на 9 из 20 распространенных аминокислот, однако в основном это происходит на аминокислотах. лизин и аргинин. Одним из примеров обычно метилированного белка является гистон. Гистоны - это белки, обнаруженные в ядре клетки. ДНК плотно обернута вокруг гистонов и удерживается на месте другими белками и взаимодействиями между отрицательными зарядами в ДНК и положительными зарядами на гистоне. Очень специфический образец метилирование аминокислот на гистоновых белках используется для определения того, какие участки ДНК плотно намотаны и не могут быть транскрибированы, а какие участки свободно намотаны и могут быть транскрибированы.[19]
Регулирование транскрипции ДНК на основе гистонов также модифицируется ацетилированием. Ацетилирование - это обратимое ковалентное присоединение ацетильная группа на аминокислоту лизин ферментом ацетилтрансфераза. Ацетильная группа удаляется из донорной молекулы, известной как ацетилкофермент А и переносится на целевой белок.[20] Гистоны подвергаются ацетилированию на остатки лизина ферментами, известными как гистонацетилтрансфераза. Эффект ацетилирования заключается в ослаблении зарядовых взаимодействий между гистоном и ДНК, тем самым делая больше генов в ДНК доступными для транскрипции.[21]
Последняя, преобладающая посттрансляционная модификация химической группы - это фосфорилирование. Фосфорилирование - это обратимое ковалентное добавление фосфат группа к определенным аминокислотам (серин, треонин и тирозин ) внутри белка. Фосфатная группа удаляется с молекулы-донора АТФ белком киназа и перенесен на гидроксил группа целевой аминокислоты, это производит аденозиндифосфат как побочный продукт. Этот процесс можно обратить вспять и удалить фосфатную группу с помощью ферментного белка. фосфатаза. Фосфорилирование может создавать сайт связывания на фосфорилированном белке, что позволяет ему взаимодействовать с другими белками и генерировать большие многобелковые комплексы. С другой стороны, фосфорилирование может изменить уровень активности белка, изменяя способность белка связывать свой субстрат.[1]
Добавление сложных молекул
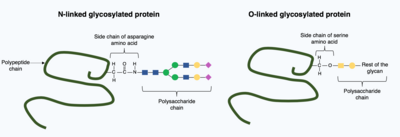
Посттрансляционные модификации могут включать более сложные, большие молекулы в свернутую структуру белка. Один из распространенных примеров этого: гликозилирование, добавление молекулы полисахарида, которое широко считается наиболее распространенной посттрансляционной модификацией.[15]
При гликозилировании a полисахарид молекула (известная как гликан ) ковалентно добавляется к целевому белку посредством гликозилтрансферазы ферменты и модифицированные гликозидазы в эндоплазматический ретикулум и аппарат Гольджи. Гликозилирование может иметь решающее значение в определении окончательной трехмерной структуры целевого белка. В некоторых случаях для правильного сворачивания необходимо гликозилирование. N-связанное гликозилирование способствует сворачиванию белка за счет увеличения растворимость и опосредует связывание белка с белковые шапероны. Шапероны - это белки, отвечающие за сворачивание и поддержание структуры других белков.[1]
Существует два типа гликозилирования: N-связанное гликозилирование и О-связанное гликозилирование. N-связанное гликозилирование начинается в эндоплазматическом ретикулуме с добавлением гликана-предшественника. Гликан-предшественник модифицируют в аппарате Гольджи для получения сложного гликана, ковалентно связанного с азотом в аспарагин аминокислота. Напротив, O-связанное гликозилирование представляет собой последовательное ковалентное добавление отдельные сахара на кислород аминокислот серина и треонина в структуре зрелого белка.[1]
Образование ковалентных связей
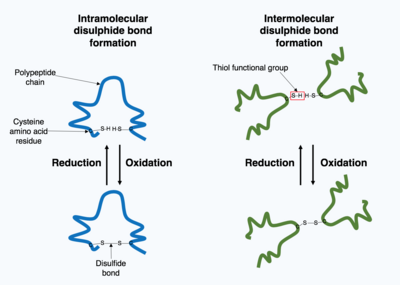
Многие белки, производимые внутри клетки, секретируются вне клетки, поэтому эти белки функционируют как внеклеточный белки. Внеклеточные белки подвергаются воздействию самых разных условий. Чтобы стабилизировать трехмерную структуру белка, ковалентные связи образуются либо внутри белка, либо между различными полипептидными цепями в четвертичной структуре. Самый распространенный тип - это дисульфидная связь (также известный как дисульфидный мостик). Дисульфидная связь образуется между двумя цистеин аминокислоты, использующие химические группы боковой цепи, содержащие атом серы, эти химические группы известны как тиол функциональные группы. Дисульфидные связи стабилизируют ранее существовавшая структура белка. Дисульфидные связи образуются в реакция окисления между двумя тиоловыми группами и, следовательно, для реакции необходима окислительная среда. В результате в окислительной среде эндоплазматического ретикулума обычно образуются дисульфидные связи, катализируемые ферментами, называемыми дисульфидными изомеразами белка. Дисульфидные связи редко образуются в цитоплазме, поскольку это восстанавливающая среда.[1]
Роль синтеза белка в заболевании
Многие заболевания вызваны мутациями в генах из-за прямой связи между нуклеотидной последовательностью ДНК и аминокислотной последовательностью кодируемого белка. Изменения в первичной структуре белка могут привести к неправильной укладке белка или нарушению его функции. Мутации в одном гене были идентифицированы как причина множества заболеваний, в том числе: серповидноклеточная анемия, известные как расстройства одного гена.
Серповидноклеточная анемия

Серповидно-клеточная анемия - это группа заболеваний, вызываемых мутацией в субъединице гемоглобина, белка, обнаруженного в красных кровяных тельцах, ответственных за транспортировку кислорода. Самая опасная серповидно-клеточная анемия - серповидноклеточная анемия. Серповидно-клеточная анемия - самая распространенная гомозиготное рецессивное заболевание с одним геном Это означает, что больной должен нести мутацию в обеих копиях пораженного гена (по одной унаследованной от каждого родителя), чтобы страдать от болезни. Гемоглобин имеет сложную четвертичную структуру и состоит из четырех полипептидных субъединиц - двух субъединиц A и двух субъединиц B.[22] Пациенты, страдающие серповидноклеточной анемией, имеют миссенс-мутацию или мутацию замещения в гене, кодирующем полипептидную цепь субъединицы В гемоглобина. Миссенс-мутация означает, что нуклеотидная мутация изменяет общий триплет кодонов таким образом, что другая аминокислота сочетается с новым кодоном. В случае серповидно-клеточной анемии наиболее распространенной миссенс-мутацией является мутация одного нуклеотида от тимина до аденина в гене субъединицы гемоглобина B.[23] Это изменяет кодон 6, кодирующий аминокислоту глутаминовую кислоту, на кодон валина.[22]
Это изменение первичной структуры полипептидной цепи субъединицы В гемоглобина изменяет функциональность многосубъединичного комплекса гемоглобина в условиях низкого содержания кислорода. Когда красные кровяные тельца выгружают кислород в ткани тела, мутировавший белок гемоглобина начинает слипаться, образуя полутвердую структуру внутри красных кровяных телец. Это искажает форму красных кровяных телец, в результате чего приобретает характерную «серповидную» форму, и снижает гибкость клеток. Эти жесткие, искаженные эритроциты могут накапливаться в кровеносных сосудах, создавая закупорку. Закупорка препятствует притоку крови к тканям и может привести к смерть ткани что причиняет человеку большую боль.[24]
Смотрите также
- Центральная догма молекулярной биологии
- Генетический код
- Экспрессия гена
- Посттрансляционная модификация
- Сворачивание белков
Рекомендации
- ^ а б c d е ж грамм час я j Альбертс, Брюс (2015). Молекулярная биология клетки (Шестое изд.). Абингдон, Великобритания: Garland Science, Taylor and Francis Group. ISBN 978-0815344643.
- ^ О'Коннор, Клэр (2010). Основы клеточной биологии. Образование NPG: Кембридж, Массачусетс. Получено 3 марта 2020.
- ^ Ван, Ю-Цзе; Петерсон, Сюзанна Э; Лоринг, Жанна Ф (2013). «Посттрансляционные модификации белков и регуляция плюрипотентности в стволовых клетках человека». Клеточные исследования. 24 (2): 143–160. Дои:10.1038 / cr.2013.151. ЧВК 3915910. PMID 24217768.
- ^ Scheper, Gert C .; van der Knaap, Marjo S .; Гордый, Кристофер Г. (2007). «Перевод имеет значение: дефекты синтеза белка при наследственных заболеваниях». Природа Обзоры Генетика. 8 (9): 711–723. Дои:10.1038 / nrg2142. PMID 17680008. S2CID 12153982.
- ^ Берг, Джереми М; Тимочко, Джон Л; Гатто-младший, Грегори Дж. Страйер, Люберт (2015). Биохимия (Восьмое изд.). США: У. Х. Фриман и компания. ISBN 9781464126109.
- ^ а б c d е ж Тул, Гленн; Тул, Сьюзан (2015). AQA биология Уровень A. Учебник (Второе изд.). Грейт-Кларендон-стрит, Оксфорд, OX2 6DP, Великобритания: Oxford University Press. ISBN 9780198351771.CS1 maint: location (связь)
- ^ Берк, Арнольд; Лодиш, Харви; Дарнелл, Джеймс Э (2000). Молекулярная клеточная биология (4-е изд.). Нью-Йорк: W.H. Фримен. ISBN 9780716737063.
- ^ а б «Процессинг пре-мРНК эукариот». Ханская академия. Получено 9 марта 2020.
- ^ Джо, Бонг-Сок; Чой, Сун Шим (2015). «Интроны: функциональные преимущества интронов в геномах». Геномика и информатика. 13 (4): 112–8. Дои:10.5808 / GI.2015.13.4.112. ЧВК 4742320. PMID 26865841.
- ^ «Этапы перевода (статья)». Ханская академия. Получено 10 марта 2020.
- ^ «Ядро и рибосомы (статья)». Ханская академия. Получено 10 марта 2020.
- ^ а б Купер, GM (2000). Клетка: молекулярный подход (2-е изд.). Сандерленд (Массачусетс): Sinauer Associates. ISBN 9780878931064.
- ^ «Структура белка: первичная, вторичная, третичная и четвертичная (статья)». Ханская академия. Получено 11 марта 2020.
- ^ Дуань, Гуанъю; Вальтер, Дирк; Радивояц, Предраг (2015). «Роль посттрансляционных модификаций в контексте сетей взаимодействия белков». PLOS вычислительная биология. 11 (2): e1004049. Bibcode:2015PLSCB..11E4049D. Дои:10.1371 / journal.pcbi.1004049. ЧВК 4333291. PMID 25692714.
- ^ а б Шуберт, Марио; Walczak, Michal J .; Эби, Маркус; Более широкий, Герхард (2015). «Посттрансляционные модификации интактных белков, обнаруженные с помощью ЯМР-спектроскопии: применение к гликозилированию». Angewandte Chemie International Edition. 54 (24): 7096–7100. Дои:10.1002 / anie.201502093. PMID 25924827.
- ^ Ван, Ю-Цзе; Петерсон, Сюзанна Э; Лоринг, Жанна Ф (2013). «Посттрансляционные модификации белков и регуляция плюрипотентности в стволовых клетках человека». Клеточные исследования. 24 (2): 143–160. Дои:10.1038 / cr.2013.151. PMID 24217768.
- ^ Цехановер, Аарон; В целом, Кристофер М. (2005). «Протеолиз: от лизосомы к убиквитину и протеасомам». Обзоры природы Молекулярная клеточная биология. 6 (1): 79–87. Дои:10.1038 / nrm1552. PMID 15688069. S2CID 8953615.
- ^ Бреннер, Сидней; Миллер, Джеффри Х. (2001). Энциклопедия генетики. Elsevier Science Inc. стр. 2800. ISBN 978-0-12-227080-2.
- ^ Мурн, Джерней; Ши, Ян (2017). «Извилистый путь исследований метилирования белков: вехи и новые рубежи». Обзоры природы Молекулярная клеточная биология. 18 (8): 517–527. Дои:10.1038 / nrm.2017.35. PMID 28512349. S2CID 3917753.
- ^ Дразич, Адриан; Myklebust, Line M .; Ри, Расмус; Арнесен, Томас (2016). «Мир ацетилирования белков». Biochimica et Biophysica Acta (BBA) - Белки и протеомика. 1864 (10): 1372–1401. Дои:10.1016 / j.bbapap.2016.06.007. PMID 27296530.
- ^ Баннистер, Эндрю Дж; Кузаридес, Тони (2011). «Регулирование хроматина модификациями гистонов». Клеточные исследования. 21 (3): 381–395. Дои:10.1038 / кр.2011.22. ЧВК 3193420. PMID 21321607.
- ^ а б Хабара, алави; Стейнберг, Мартин Х (2016). «Мини-обзор: генетические основы гетерогенности и серьезности серповидноклеточной анемии». Экспериментальная биология и медицина. 241 (7): 689–696. Дои:10.1177/1535370216636726. ЧВК 4950383. PMID 26936084.
- ^ Мангла, Анкит; Эхсан, Моавия; Марувада, Смита (2020). "Серповидноклеточная анемия". StatPearls. StatPearls Publishing. PMID 29489205. Получено 12 марта 2020.
- ^ Илесанми, Олуватойин Олатундун (2010). «Патологические основы симптомов и кризисов при серповидно-клеточном расстройстве: значение для консультирования и психотерапии». Гематологические отчеты. 2 (1): 2. Дои:10.4081 / час 2010.e2. ЧВК 3222266. PMID 22184515.
внешняя ссылка
- Полезное видео, демонстрирующее процесс преобразования ДНК в белок посредством транскрипции и трансляции.
- Видеовизуализация процесса сворачивания белка от нефункциональной первичной структуры к зрелой, свернутой трехмерной структуре белка со ссылкой на роль мутаций и неправильного сворачивания белка при заболевании
- Более продвинутое видео с подробным описанием различных типов посттрансляционных модификаций и их химической структуры.
