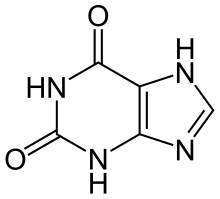
Ксантин - Xanthine
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК 3,7-дигидропурин-2,6-дион | |
| Другие имена 1ЧАС-Пурин-2,6-дион | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.000.653 |
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Свойства | |
| C5ЧАС4N4О2 | |
| Молярная масса | 152,11 г / моль |
| Внешность | Белое твердое вещество |
| Температура плавления | разлагается |
| 1 г / 14,5 л при 16 ° C 1 г / 1,4 л при 100 ° C | |
| Опасности | |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Ксантин (/ˈzæпθяп/ или /ˈzæпθаɪп/; архаично ксантовая кислота; систематическое название 3,7-дигидропурин-2,6-дион) это пурин база содержится в большинстве тканей и жидкостей человеческого тела, а также в других организмах.[2] Несколько стимуляторы получены из ксантина, в том числе кофеин, теофилин, и теобромин.[3][4]
Ксантин - это продукт, который деградация пуринов.[2]
- Он создан из гуанин от гуаниндезаминаза.
- Он создан из гипоксантин от ксантин оксидоредуктаза.
- Он также создан из ксантозин от пуриновая нуклеозид фосфорилаза.
Ксантин впоследствии превращается в мочевая кислота действием ксантиноксидаза фермент.[2]
Использование и изготовление
Ксантин используется как препарат, средство, медикамент предшественник для лекарств для людей и животных и производится как пестицид ингредиент.[2]
Клиническое значение
Производные ксантина (известные под общим названием ксантины) являются группой алкалоиды обычно используется из-за их эффектов как мягкий стимуляторы и в качестве бронходилататоры, особенно при лечении астма или грипп симптомы.[2] В отличие от других, более сильных стимуляторов, таких как симпатомиметические амины, ксантины в основном действуют, чтобы противостоять действиям аденозин, и повысить бдительность в Центральная нервная система.[2]
Токсичность
Метилированный ксантины (метилксантины), которые включают кофеин, аминофиллин, IBMX, параксантин, пентоксифиллин, теобромин, и теофиллин, влияют не только на дыхательные пути, но и в высоких концентрациях стимулируют частоту сердечных сокращений, силу сокращения и сердечную аритмию.[2] В высоких дозах они могут вызвать судороги, резистентные к противосудорожным средствам.[2] Метилксантины вызывают Желудочный сок и пепсин выделения в желудочно-кишечный тракт.[2] Метилксантины метаболизируются цитохром P450 в печени.[2]
При проглатывании, вдыхании или попадании в глаза ксантинов в больших количествах они могут быть вредными и могут вызывать аллергическая реакция если применяется тематически.[2]
Фармакология
В in vitro фармакологический исследования, ксантины действуют как:
- конкурентный неизбирательный ингибиторы фосфодиэстеразы которые повышают внутриклеточные лагерь, активировать PKA, ингибировать TNF-α[2][5][4] и лейкотриен[6] синтез и уменьшить воспаление и врожденный иммунитет[6] и
- неизбирательный аденозиновый рецептор антагонисты [7] которые подавляют вызывающие сонливость аденозин.[2]
Однако разные аналоги демонстрируют разную эффективность в отношении многочисленных подтипов, и был разработан широкий спектр синтетических ксантинов (некоторые из них неметилированные) в поисках соединений с большей селективностью к фермент фосфодиэстераза или аденозиновый рецептор подтипы.[2][8][9][10][11][12]

Кофеин: R1 = R2 = R3 = CH3
Теобромин: R1 = H, R2 = R3 = CH3
Теофиллин: R1 = R2 = CH3, Р3 = H
| имя | р1 | р2 | р3 | р8 | Номенклатура ИЮПАК | Нашел в |
|---|---|---|---|---|---|---|
| Ксантин | ЧАС | ЧАС | ЧАС | ЧАС | 3,7-дигидро-пурин-2,6-дион | Растения, животные |
| Кофеин | CH3 | CH3 | CH3 | ЧАС | 1,3,7-триметил-1ЧАС-пурин-2,6 (3ЧАС,7ЧАС) -диона | Кофе, гуарана, Йерба товарищ, чай, кола, Гуаюса, |
| Теобромин | ЧАС | CH3 | CH3 | ЧАС | 3,7-дигидро-3,7-диметил-1ЧАС-пурин-2,6-дион | Какао (шоколад ), Йерба товарищ, кола, Гуаюса, |
| Теофиллин | CH3 | CH3 | ЧАС | ЧАС | 1,3-диметил-7ЧАС-пурин-2,6-дион | Чай, какао (шоколад ), Йерба товарищ, кола |
| Параксантин | CH3 | ЧАС | CH3 | ЧАС | 1,7-диметил-7ЧАС-пурин-2,6-дион | Животные, употреблявшие кофеин |
| 8-хлоротеофиллин | CH3 | CH3 | ЧАС | Cl | 8-хлор-1,3-диметил-7ЧАС-пурин-2,6-дион | Синтетический фармацевтический ингредиент |
| 8-бромотеофиллин | CH3 | CH3 | ЧАС | Br | 8-бром-1,3-диметил-7ЧАС-пурин-2,6-дион | Памабром мочегонное средство |
| Дипрофиллин | CH3 | CH3 | C3ЧАС7О2 | ЧАС | 7- (2,3-дигидроксипропил) -1,3-диметил-3,7-дигидро-1ЧАС-пурин-2,6-дион | Синтетический фармацевтический ингредиент |
| IBMX | CH3 | C4ЧАС9 | ЧАС | ЧАС | 1-метил-3- (2-метилпропил) -7ЧАС-пурин-2,6-дион | |
| Мочевая кислота | ЧАС | ЧАС | ЧАС | О | 7,9-дигидро-1ЧАС-пурин-2,6,8 (3ЧАС) -трион | Побочный продукт пурин метаболизм нуклеотидов и нормальный компонент мочи |
Патология
Люди с редкими генетические нарушения в частности ксантинурия и Синдром Леша – Найхана, не имеют достаточного количества ксантиноксидазы и не могут превратить ксантин в мочевая кислота.[2]
Спекуляции на происхождении
Исследования, опубликованные в 2008 г., основаны на 12C /13C изотопные отношения из органические соединения найдено в Метеорит Мерчисон, предположил, что ксантин и родственные химические вещества, включая РНК составная часть урацил, были сформированы внеземной.[13][14] В августе 2011 г. отчет, основанный на НАСА учится с метеориты найдены на Земле, было опубликовано предположение, что ксантин и родственные органические молекулы, включая ДНК и РНК компоненты аденин и гуанин, были найдены в космическое пространство.[15][16][17]
Смотрите также
использованная литература
- ^ Индекс Merck, 11-е издание, 9968.
- ^ а б c d е ж г час я j k л м п о «Ксантин, CID 1188». PubChem, Национальная медицинская библиотека, Национальные институты здравоохранения США. 2019 г.. Получено 28 сентября 2019.
- ^ Спиллер, Джин А. (1998). Кофеин. Бока-Ратон: CRC Press. ISBN 0-8493-2647-8.
- ^ а б Кацунг, Бертрам Г. (1995). Базовая и клиническая фармакология. Восточный Норуолк, Коннектикут: Paramount Publishing. С. 310, 311. ISBN 0-8385-0619-4.
- ^ Marques LJ, Zheng L, Poulakis N, Guzman J, Costabel U (февраль 1999 г.). «Пентоксифиллин подавляет выработку TNF-альфа альвеолярными макрофагами человека». Am. J. Respir. Крит. Care Med. 159 (2): 508–11. Дои:10.1164 / ajrccm.159.2.9804085. PMID 9927365.
- ^ а б Петерс-Голден М., Канетти С., Манкузо П., Коффи М.Дж. (2005). «Лейкотриены: недооцененные медиаторы врожденного иммунного ответа». J. Immunol. 174 (2): 589–94. Дои:10.4049 / jimmunol.174.2.589. PMID 15634873.
- ^ Дэйли Дж. В., Якобсон К. А., Укена Д. (1987). «Аденозиновые рецепторы: разработка селективных агонистов и антагонистов». Прог Клин Биол Рес. 230 (1): 41–63. PMID 3588607.
- ^ Дэйли Дж. У., Пэджетт У. Л., Шамим М. Т. (июль 1986 г.). «Аналоги кофеина и теофиллина: влияние структурных изменений на сродство к аденозиновым рецепторам». Журнал медицинской химии. 29 (7): 1305–8. Дои:10.1021 / jm00157a035. PMID 3806581.
- ^ Дейли Дж. В., Якобсон К. А., Укена Д. (1987). «Аденозиновые рецепторы: разработка селективных агонистов и антагонистов». Прогресс в клинических и биологических исследованиях. 230: 41–63. PMID 3588607.
- ^ Дейли JW, Hide I, Müller CE, Shamim M (1991). «Аналоги кофеина: взаимосвязь структура-активность аденозиновых рецепторов». Фармакология. 42 (6): 309–21. Дои:10.1159/000138813. PMID 1658821.
- ^ Член парламента Гонсалес, Теран С., Тейейра М. (май 2008 г.). «Поиск новых лигандов-антагонистов аденозиновых рецепторов с точки зрения QSAR. Насколько мы близки?». Обзоры медицинских исследований. 28 (3): 329–71. Дои:10.1002 / med.20108. PMID 17668454.
- ^ Баральди П.Г., Тебризи М.А., Гесси С.П., Бореа (январь 2008 г.). «Антагонисты аденозиновых рецепторов: перевод медицинской химии и фармакологии в клиническую практику». Химические обзоры. 108 (1): 238–63. Дои:10.1021 / cr0682195. PMID 18181659.
- ^ Мартинс, З .; Botta, O .; Fogel, M. L .; Sephton, M. A .; Главин, Д. П .; Watson, J. S .; Dworkin, J. P .; Schwartz, A.W .; Эренфройнд, П. (2008). «Внеземные азотистые основания в метеорите Мерчисон». Письма по науке о Земле и планетах. 270 (1–2): 130–136. arXiv:0806.2286. Bibcode:2008E и PSL.270..130M. Дои:10.1016 / j.epsl.2008.03.026.
- ^ AFP Персонал (13 июня 2008 г.). "Мы все можем быть космическими пришельцами: учеба". AFP. Архивировано из оригинал 17 июня 2008 г.. Получено 2011-08-14.
- ^ Каллахан, М. П .; Smith, K. E .; Cleaves, H.J .; Ruzicka, J .; Stern, J.C .; Главин, Д. П .; House, C. H .; Дворкин, Дж. П. (2011). «Углеродистые метеориты содержат широкий спектр внеземных азотистых оснований». Труды Национальной академии наук. 108 (34): 13995–8. Bibcode:2011PNAS..10813995C. Дои:10.1073 / pnas.1106493108. ЧВК 3161613. PMID 21836052.
- ^ Стейгервальд, Джон (8 августа 2011 г.). «Исследователи НАСА: строительные блоки ДНК могут быть созданы в космосе». НАСА. Получено 2011-08-10.
- ^ ScienceDaily Staff (9 августа 2011 г.). «Строительные блоки ДНК могут быть созданы в космосе, - свидетельствуют данные НАСА». ScienceDaily. Получено 2011-08-09.

