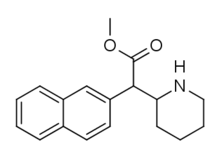
HDMP-28 - HDMP-28
 | |
| Легальное положение | |
|---|---|
| Легальное положение |
|
| Идентификаторы | |
| |
| Количество CAS |
|
| PubChem CID | |
| ChemSpider | |
| UNII | |
| Химические и физические данные | |
| Формула | C18ЧАС21NО2 |
| Молярная масса | 283,365 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| | |
HDMP-28 или же метилнафтидат это пиперидин основан стимулятор препарат, тесно связанный с метилфенидат, но с бензол кольцо заменено на нафталин. Это мощный ингибитор обратного захвата дофамина, в несколько раз эффективнее метилфенидата и непродолжительное действие,[1] и является структурный изомер другого мощного ингибитора обратного захвата дофамина, N, O-диметил-4- (2-нафтил) пиперидин-3-карбоксилат.

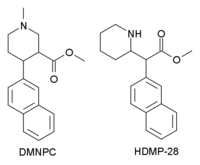
Большинство аналогов HDMP-28 имеют SERT Значения Ki в диапазоне> 10000 и поэтому являются селективными для обратного захвата дофамина и норадреналина, практически не влияя на серотонин. HDMP-28 также имеет высокое сродство к SERT и поэтому ведет себя как ингибитор тройного обратного захвата.[2]
| Ингибирование специфических аналогов при замещении CFT от связывания с DAT & RTI-55 от связывания с SERT | ||||||
| Ar | [3ЧАС]CFT DAT | [3H] DA Поглощение | [3ЧАС]РТИ-55 SERT | Ингибирование на 10 мкМ | D.R. | Потенция |
|---|---|---|---|---|---|---|
| Ph | 83.9 | 224 | >>10,000 | 19.6 | 2.7 | 1.00 |
| п-F | 35.0 | 142 | >10,000 | 36.9 | 4.1 | 3.33 |
| м-Cl | 5.1 | 23.0 | >10,000 | 45.5 | 4.5 | 2.42 |
| п-Мне | 33.0 | 126 | >10,000 | 45.0 | 3.8 | 0.74 |
| п-NH2 | 34.5 | 114 | >>10,000 | 7.9 | 3.3 | 2.18 |
| м, п-Cl2 | 5.3 (2.67)б | 7.0 | 1,064 (>10,000)б | 93.3 | 1.3 | 7.98 |
| β-Нафтил | 33.9б 11.0c | 53.0c | 71.6б | nd | 4.8c | — |
| Кокаин | 160 | 404 | 401 | nd | 2.5 | 0.41 |
| аSchweri, et al. (2002);[3] бДэвис и др. (2004);[4] cDeutsch, et al. (2001).[5] | ||||||
D.R. = Коэффициент дискриминации = [3H] DA ÷ [3H] CFT.
Низкий D.R. = вызывает привыкание, тогда как высокий D.R. = низкая склонность к самоуправлению.
Законность
HDMP-28 запрещен в Швейцарии с декабря 2015 года.[6]
Смотрите также
- 3,4-дихлорметилфенидат
- Этилфенидат
- HDEP-28
- Нафтилизопропиламин
- Нафирон
- 2β-пропаноил-3β- (2-нафтил) -тропан (WF-23)
- Изопропилфенидат
- Пропилфенидат
Рекомендации
- ^ Лил Дж. А., Ван З., Вулвертон В. Л., Франс Дж. Э., Грегг Т. К., Дэвис Н. М., Надер М. А. (октябрь 2003 г.). «Усиливающая эффективность психостимуляторов у макак-резусов: роль фармакокинетики и фармакодинамики». Журнал фармакологии и экспериментальной терапии. 307 (1): 356–66. Дои:10.1124 / jpet.103.049825. PMID 12954808. S2CID 5654856.
- ^ Дэвис Х.М., Хоппер Д.В., Хансен Т., Лю К., Чайлдерс С.Р. (апрель 2004 г.). «Синтез аналогов метилфенидата и их аффинности связывания на сайтах транспорта дофамина и серотонина». Письма по биоорганической и медицинской химии. 14 (7): 1799–802. Дои:10.1016 / j.bmcl.2003.12.097. PMID 15026075.
- ^ Швери MM, Deutsch HM, Massey AT, Holtzman SG (май 2002 г.). «Биохимическая и поведенческая характеристика новых аналогов метилфенидата». Журнал фармакологии и экспериментальной терапии. 301 (2): 527–35. Дои:10.1124 / jpet.301.2.527. PMID 11961053.
- ^ Дэвис Х.М., Хоппер Д.В., Хансен Т., Лю К., Чайлдерс С.Р. (апрель 2004 г.). «Синтез аналогов метилфенидата и их аффинности связывания на сайтах транспорта дофамина и серотонина». Письма по биоорганической и медицинской химии. 14 (7): 1799–802. Дои:10.1016 / j.bmcl.2003.12.097. PMID 15026075.
- ^ Deutsch HM, Ye X, Shi Q, Liu Z, Schweri MM (апрель 2001 г.). «Синтез и фармакология агентов лечения зависимости от места злоупотребления кокаином: новая синтетическая методология для аналогов метилфенидата, основанная на реакции Блейза». Европейский журнал медицинской химии. 36 (4): 303–11. Дои:10.1016 / s0223-5234 (01) 01230-2. PMID 11461755.
- ^ "Verordnung des EDI über die Verzeichnisse der Betäubungsmittel, psychotropen Stoffe, Vorläuferstoffe und Hilfschemikalien". Der Bundesrat.
