Дифторпин - Difluoropine
 | |
| Клинические данные | |
|---|---|
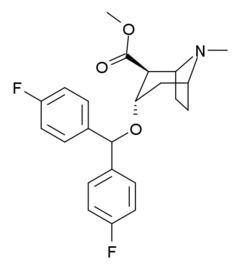
| Другие имена | (S) - (+) - 2β-Карбометокси-3α- (бис (4-фторфенил) метокси) тропан |
| Код УВД |
|
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| ChemSpider | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| Химические и физические данные | |
| Формула | C23ЧАС25F2NО3 |
| Молярная масса | 401,448 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| (проверять) | |
Дифторпин (О-620) это стимулятор препарат, синтезированный из тропинон, который действует как мощный и избирательный ингибитор обратного захвата дофамина. Дифторопин уникален среди ингибиторов обратного захвата дофамина, производных от тропана, тем, что активный стереоизомер представляет собой (S) энантиомер, а не (R) энантиомер, наоборот, по сравнению с естественным кокаин.[1] Это структурно связано с бензтропин и имеет аналогичный холинолитик и антигистаминный препарат эффекты в дополнение к его ингибирующему действию на обратный захват дофамина.[2]
Дифторпин оказывает стимулирующее действие на животных, хотя он значительно менее эффективен, чем многие другие сильнодействующие препараты. фенилтропан производные стимулирующие препараты, такие как ВЫИГРАТЬ 35 428 и РТИ-55.[3] Он показал многообещающие эффекты в облегчении симптомов болезнь Паркинсона в животной модели расстройства.[4]
По состоянию на 2008 год это не является явным незаконным в любой точке мира.[Обновить], но может считаться аналог контролируемого вещества кокаина на основании его химической структуры в некоторых юрисдикциях, таких как США, Канада, Австралия и Новая Зеландия.
Смотрите также
Рекомендации
- ^ Meltzer PC, Liang AY, Мадрас, BK (июнь 1994 г.). «Открытие необычно селективного и нового аналога кокаина: дифторпина. Синтез и ингибирование связывания в сайтах узнавания кокаина». Журнал медицинской химии. 37 (13): 2001–10. Дои:10.1021 / jm00039a014. PMID 8027983.
- ^ Кэмпбелл В.К., Копайтик Т.А., Ньюман А.Х., Кац Дж.Л. (ноябрь 2005 г.). «Оценка влияния гистаминергических действий на кокаиноподобные эффекты аналогов 3альфа-дифенилметокситропана». Журнал фармакологии и экспериментальной терапии. 315 (2): 631–40. Дои:10.1124 / jpet.105.090829. PMID 16055673. S2CID 40671768.
- ^ Кац Дж. Л., Изенвассер С., Клайн Р. Х., Аллен А. С., Ньюман А. Х. (январь 1999 г.). «Новые аналоги 3альфа-дифенилметокситропана: селективные ингибиторы захвата дофамина с поведенческими эффектами, отличными от эффектов кокаина». Журнал фармакологии и экспериментальной терапии. 288 (1): 302–15. PMID 9862785.
- ^ Мадрас Б.К., Фэи М.А., Гуле М., Лин З., Бендор Дж., Гудрич С. и др. (Ноябрь 2006 г.). «Ингибиторы переносчика дофамина (DAT) облегчают специфический паркинсонический дефицит у обезьян: связь с занятостью DAT in vivo». Журнал фармакологии и экспериментальной терапии. 319 (2): 570–85. Дои:10.1124 / jpet.106.105312. PMID 16885433. S2CID 7523758.
| Этот препарат, средство, медикамент статья, касающаяся нервная система это заглушка. Вы можете помочь Википедии расширяя это. |
