Хлорид железа (III) - Iron(III) chloride
 Хлорид железа (III) (гидрат) | |||
 Хлорид железа (III) (безводный) | |||
| |||
| Имена | |||
|---|---|---|---|
| Имена ИЮПАК Хлорид железа (III) Трихлорид железа | |||
Другие имена
| |||
| Идентификаторы | |||
| |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.028.846 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII |
| ||
| Номер ООН |
| ||
| |||
| |||
| Характеристики | |||
| FeCl 3 | |||
| Молярная масса |
| ||
| Внешность | Зелено-черный в отраженном свете; пурпурно-красный в проходящем свете; желтое твердое вещество в виде гексагидрата; коричневый как водн. решение | ||
| Запах | Незначительный HCl | ||
| Плотность |
| ||
| Температура плавления | 307,6 ° С (585,7 ° F, 580,8 К) (безводный) 37 ° С (99 ° F, 310 К) (гексагидрат)[1] | ||
| Точка кипения |
| ||
| 912 г / л (анх. или гексагидрат, 25 ° C)[1] | |||
| Растворимость в |
| ||
| +13,450·10−6 см3/ моль[2] | |||
| Вязкость | 12 сп (40% раствор) | ||
| Структура | |||
| Шестиугольный, 24 грн. | |||
| р3, № 148[3] | |||
а = 0.6065 нм, б = 0.6065 нм, c = 1.742 нм α = 90 °, β = 90 °, γ = 120 ° | |||
Формула единиц (Z) | 6 | ||
| Восьмигранный | |||
| Опасности[5][6][Примечание 1] | |||
| Паспорт безопасности | ICSC | ||
| Пиктограммы GHS |   | ||
| Сигнальное слово GHS | Опасность | ||
| H290, H302, H314, H318 | |||
| P234, P260, P264, P270, P273, P280, P301 + 312, P301 + 330 + 331, P303 + 361 + 353, P363, P304 + 340, P310, P321, P305 + 351 + 338, P390, P405, P406, P501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | Негорючий | ||
| NIOSH (Пределы воздействия на здоровье в США): | |||
REL (Рекомендуемые) | TWA 1 мг / м3[4] | ||
| Родственные соединения | |||
Другой анионы | |||
Другой катионы | |||
Связанный коагулянты | |||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Хлорид железа (III) представляет собой неорганическое соединение формулы (FeCl
3). Также называемый хлорид железа, это обычное соединение железа в степени окисления +3. В безводный соединение представляет собой твердое кристаллическое вещество с температурой плавления 307,6 ° C. Цвет зависит от угла обзора: в отраженном свете кристаллы кажутся темно-зелеными, но в проходящий свет они кажутся пурпурно-красными.
Структура и свойства
Безводный
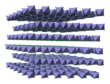
Безводный хлорид железа (III) имеет BiI3 структура, с восьмигранный Центры Fe (III), соединенные двухкоординатным хлоридом лиганды.[3]
Хлорид железа (III) имеет относительно низкую температуру плавления и кипит при температуре около 315 ° C. Пар состоит из димера Fe
2Cl
6 (ср. хлорид алюминия ), который все больше диссоциирует на мономерные FeCl
3 (с D3ч точечная группа молекулярная симметрия ) при более высокой температуре, конкурируя с его обратимым разложением с образованием хлорид железа (II) и хлор газ.[8]
Увлажняет
Помимо безводного материала, хлорид железа образует четыре гидрата. Все формы хлорида железа (III) содержат два или более хлорида в качестве лигандов, а три гидрата содержат FeCl.4−.[9]
- гексагидрат: FeCl3.6H2O имеет структурную формулу транс- [Fe (H2O)4Cl2] Cl.2H2О[10]
- FeCl3.2,5 ч2O имеет структурную формулу СНГ- [Fe (H2O)4Cl2] [FeCl4].ЧАС2О.
- дигидрат: FeCl3.2H2O имеет структурную формулу транс- [Fe (H2O)4Cl2] [FeCl4].
- FeCl3.3,5 ч2O имеет структурную формулу СНГ- [FeCl2(ЧАС2O)4] [FeCl4].3H2О.
Водный раствор
Водные растворы хлорида железа имеют характерный желтый цвет, в отличие от бледно-розовых растворов [Fe (H2O)6]3+. Согласно спектроскопическим измерениям, в водных растворах хлорида железа основными компонентами являются октаэдрический комплекс [FeCl2(ЧАС2O)4]+ (стереохимия не указана) и тетраэдрический [FeCl4]−.[9]
Подготовка
Безводный хлорид железа (III) может быть получен путем объединения элементов:[11]
Растворы хлорида железа (III) производятся в промышленных масштабах как из железа, так и из руды по замкнутому циклу.
- Растворение железная руда в соляная кислота
- Окисление хлорид железа (II) с хлор
- Окисление хлорид железа (II) с кислород
Небольшие количества могут быть получены реакцией железа с соляной кислотой, а затем с перекисью водорода. Перекись водорода является окислителем при превращении хлорида железа в хлорид железа.
Безводный хлорид железа (III) нельзя получить из гидрата нагреванием. Вместо этого твердое вещество разлагается на HCl и оксихлорид железа. Превращение может быть достигнуто обработкой тионилхлорид.[12] Точно так же обезвоживание может происходить с триметилсилилхлорид:[13]
Реакции

Хлорид железа (III) подвергается гидролизу с образованием сильно кислого раствора.[14][9]
При нагревании с оксид железа (III) при 350 ° С хлорид железа (III) дает оксихлорид железа, слоистое твердое тело и вставка хозяин.[15]
Безводная соль умеренно сильная. Кислота Льюиса, формируя аддукты с Базы Льюиса Такие как оксид трифенилфосфина; например., FeCl
3(OPPh
3)
2 где Ph - фенил. Он также реагирует с другими хлористый соли, чтобы придать желтый цвет четырехгранный [FeCl
4]−
ион. Соли [FeCl
4]−
в соляная кислота может быть извлечен в диэтиловый эфир.
Редокс-реакции
Хлорид железа (III) - мягкий окислитель, например, он способен окислять хлорид меди (I) к хлорид меди (II).
Он также реагирует с железом с образованием хлорида железа (II):
Традиционный синтез безводного хлорид железа сокращение FeCl3 с хлорбензол:[16]
С карбоксилат-анионами
Оксалаты быстро реагирует с водным хлоридом железа (III) с образованием [Fe (C
2О
4)
3]3−. Другой карбоксилат соли образуют комплексы; например., цитрат и тартрат.
С алкоксидами щелочных металлов
Щелочной металл алкоксиды реагируют с образованием комплексов алкоксидов металлов различной сложности.[17] Соединения могут быть димерными или тримерными.[18] В твердой фазе были описаны различные многоядерные комплексы для номинальной стехиометрической реакции между FeCl
3 и этоксид натрия:[19][20]
С металлоорганическими соединениями
Хлорид железа (III) в эфир раствор окисляется метиллитий LiCH
3 с образованием первого светло-зеленовато-желтого тетрахлорферрата лития (III) LiFeCl
4 раствора, а затем, при дальнейшем добавлении метиллития, тетрахлорферрат лития (II) Ли
2FeCl
4:[21][22]
В метильные радикалы соединяются сами с собой или реагируют с другими компонентами, чтобы дать в основном этан C
2ЧАС
6 и немного метан CH
4.
Использует
Промышленное
Хлорид железа (III) используется в очистка сточных вод и производство питьевой воды как коагулянт и флокулянт.[23] В этом приложении FeCl
3 в слабощелочной воде реагирует с гидроксид ион, чтобы сформировать хлопать гидроксида железа (III), или более точно сформулированный как FeO (ОН)−
, который может удалять взвешенные материалы.
Он также используется в качестве выщелачивающего агента в хлоридной гидрометаллургии,[24] например, при производстве Si из FeSi (процесс Силгрейна).[25]
Еще одно важное применение хлорида железа (III) - травление. медь в два этапа редокс реакция на хлорид меди (I) а затем в хлорид меди (II) в производстве печатные платы.[26]
Хлорид железа (III) используется в качестве катализатора реакции этилен с хлор, образуя этилендихлорид (1,2-дихлорэтан ), важный товарный химикат, который в основном используется для промышленного производства винилхлорид, то мономер для изготовления ПВХ.
Лабораторное использование
В лаборатории хлорид железа (III) обычно используется в качестве Кислота Льюиса за катализирование такие реакции как хлорирование из ароматические соединения и Реакция Фриделя – Крафтса ароматических углеводородов.[нужна цитата ] Он менее мощный, чем хлорид алюминия, но в некоторых случаях эта мягкость приводит к более высоким выходам, например, при алкилировании бензола:
В тест на хлорид железа традиционный колориметрический тест на фенолы, в котором используется 1% раствор хлорида железа (III), нейтрализованный едкий натр пока не образуется небольшой осадок FeO (OH).[27] Перед употреблением смесь фильтруют. Органическое вещество растворяется в воде, метанол или же этиловый спирт, затем добавляется раствор нейтрализованного хлорида железа (III) - временное или постоянное окрашивание (обычно пурпурное, зеленое или синее) указывает на присутствие фенола или енола.
Эта реакция используется в Точечный тест Триндера, который используется для обозначения присутствия салицилатов, в частности салициловая кислота, который содержит фенольную группу ОН.
Этот тест можно использовать для обнаружения присутствия гамма-гидроксимасляная кислота и гамма-бутиролактон,[28] что заставляет его становиться красно-коричневым.
Другое использование
Эта секция нужны дополнительные цитаты для проверка. (Январь 2020) (Узнайте, как и когда удалить этот шаблон сообщения) |
- Используется в безводной форме как сушильный реагент в некоторых реакциях.
- Используется для обнаружения фенольных соединений в органическом синтезе; например, проверка чистоты синтезированных Аспирин.
- Используется при очистке воды и сточных вод для осаждения фосфатов в виде фосфат железа (III).
- Используется при очистке сточных вод для контроля запаха.
- Используется американскими коллекционерами монет для определения дат Никель Баффало которые так сильно изношены, что даты больше не видно.
- Используется кузнецами и мастерами в узорная сварка протравливать металл, придавая ему контрастный эффект, чтобы увидеть слои или недостатки металла.
- Используется для травления widmanstatten образец в железе метеориты.
- Необходим для травления фотогравюра пластины для печати фото и изобразительного искусства в инталия и для травления ротогравюра цилиндры, используемые в полиграфической промышленности.
- Используется для изготовления печатные платы (ПП) травлением меди.
- Используется для снятия алюминиевого покрытия с зеркал.
- Используется для травления сложных медицинских устройств.
- Используется в ветеринарной практике для лечения чрезмерного купирования когтей животного, особенно когда это приводит к кровотечению.
- Реагирует с бромидом циклопентадиенилмагния в одном препарате ферроцен, металло-сэндвич-комплекс.[29]
- Иногда используется в технике Посуда раку обжиг, железо, окрашивающее керамическое изделие в оттенки розового, коричневого и оранжевого.
- Используется для испытания на стойкость к точечной и щелевой коррозии нержавеющих сталей и других сплавов.
- Используется вместе с NaI в ацетонитриле для мягкого восстановления органических азидов до первичных аминов.[30]
- Используется в модели тромбоза у животных.[31]
- Используется в системах хранения энергии.[32]
- Исторически он использовался для создания прямых позитивных чертежей.[33][34]
- Компонент модифицированного Решение Карнуа используется для хирургического лечения керато-кистозная одонтогенная опухоль (КОТ).
Безопасность
Хлорид железа (III) опасен, имеет сильную коррозию и кислоту. Безводный материал является мощным обезвоживающим агентом.
Хотя сообщения об отравлении людей редки, прием хлорида железа в организм может привести к серьезным заболеваниям и смертности. Несоответствующая маркировка и хранение приводят к случайному проглатыванию или ошибочной диагностике. Ранняя диагностика важна, особенно у серьезно отравленных пациентов.
Естественное явление
Природный аналог FeCl3 это редкий минерал молизит, обычно относящиеся к фумаролам вулканического и другого типа.[35][36]
Смотрите также
Примечания
Рекомендации
- ^ а б c d е ж Хейнс, Уильям М., изд. (2011). CRC Справочник по химии и физике (92-е изд.). Бока-Ратон, Флорида: CRC Press. п. 4.69. ISBN 1439855110.
- ^ Хейнс, Уильям М., изд. (2011). CRC Справочник по химии и физике (92-е изд.). Бока-Ратон, Флорида: CRC Press. п. 4.133. ISBN 1439855110.
- ^ а б Хашимото С., Форстер К., Мосс С.К. (1989). «Доработка структуры FeCl
3 кристалл с использованием тонкой пластинки образца ». J. Appl. Кристаллогр. 22 (2): 173. Дои:10.1107 / S0021889888013913. - ^ Карманный справочник NIOSH по химической опасности. "#0346". Национальный институт охраны труда и здоровья (NIOSH).
- ^ База данных по химической классификации HSNO, Управление по управлению экологическими рисками Новой Зеландии, получено 19 сен 2010
- ^ Различные поставщики, собранные Бейлорским стоматологическим колледжем, Техасский университет A&M. (дата обращения 19 сентября 2010 г.)
- ^ Классификация GHS - ID 831, Японский межведомственный комитет по СГС, 2006 г., получено 19 сен 2010
- ^ Холлеман А.Ф., Виберг Э. (2001). Wiberg N (ред.). Неорганическая химия. Сан-Диего: Academic Press. ISBN 978-0-12-352651-9.
- ^ а б c Саймон А. Коттон (2018). «Хлорид железа (III) и его координационная химия». Журнал координационной химии. 71 (21): 3415–3443. Дои:10.1080/00958972.2018.1519188. S2CID 105925459.
- ^ Линд, М. Д. (1967). «Кристаллическая структура гексагидрата хлористого железа». Журнал химической физики. 47 (3): 990–993. Bibcode:1967JChPh..47..990L. Дои:10.1063/1.1712067.
- ^ Tarr BR, Booth HS, Dolance A (1950). «Безводный хлорид железа (III)». В Одриет LF (ред.). Неорганические синтезы. 3. Книжная компания Макгроу-Хилл, Inc., стр. 191–194. Дои:10.1002 / 9780470132340.ch51. ISBN 9780470132340.
- ^ Pray AR, Heitmiller RF, Strycker S и др. (1990). «Безводные хлориды металлов». В Angelici RJ (ред.). Неорганические синтезы. 28. С. 321–323. Дои:10.1002 / 9780470132593.ch80. ISBN 9780470132593.
- ^ Boudjouk P, So JH, Ackermann MN, et al. (1992). «Сольватированные и несольватированные безводные хлориды металлов из гидратов хлоридов металлов». В Граймс RN (ред.). Неорганические синтезы. 29. С. 108–111. Дои:10.1002 / 9780470132609.ch26. ISBN 9780470132609.
- ^ Housecroft, C.E .; Шарп, А. Г. (2012). Неорганическая химия (4-е изд.). Прентис Холл. п. 747. ISBN 978-0-273-74275-3.
- ^ Киккава С., Канамару Ф., Коидзуми М. и др. (1984). «Слоистые интеркаляционные соединения». В Холт С.Л. младший (ред.). Неорганические синтезы. John Wiley & Sons, Inc., стр. 86–89. Дои:10.1002 / 9780470132531.ch17. ISBN 9780470132531.
- ^ П. Ковачич и Н. О. Брейс (1960). «Хлорид железа (II)». Неорганические синтезы. Неорг. Synth. Неорганические синтезы. 6. С. 172–173. Дои:10.1002 / 9780470132371.ch54. ISBN 9780470132371.
- ^ Турова Н.Ю., Туревская Е.П., Кесслер В.Г. и др., Ред. (2002). «12.22.1 Синтез». Химия алкоксидов металлов. Springer Science. п. 481. ISBN 0306476576.
- ^ Брэдли Д.К., Мехротра Р.К., Ротвелл I и др. (2001). «3.2.10. Алкоксиды более поздних 3-х металлов». Алкоксо- и арилоксопроизводные металлов. Сан-Диего: Academic Press. п. 69. ISBN 9780121241407. OCLC 162129468.
- ^ Майкл V, Grätz F, Huch V (2001). "Fe
9О
3(OC
2ЧАС
5)
21· C
2ЧАС
5ОЙ- Новый тип структуры незаряженного оксидно-алкоксидного кластера железа (III) ». Евро. J. Inorg. Chem. 2001 (2): 367. Дои:10.1002 / 1099-0682 (200102) 2001: 2 <367 :: AID-EJIC367> 3.0.CO; 2-V. - ^ Сейсенбаева Г.А., Гохиль С., Суслова Е.В. и др. (2005). «Повторный синтез этоксида железа (III): характеристика продуктов метатезиса галогенидов железа (III) и этоксида натрия». Неорг. Чим. Acta. 358 (12): 3506–3512. Дои:10.1016 / j.ica.2005.03.048.
- ^ Бертольд HJ, Spiegl HJ (1972). "Über die Bildung von Lithiumtetrachloroferrat (II)" Ли
2FeCl
4 bei der Umsetzung von Eisen (III) -хлорид мил литийметил (1: 1) в ätherischer Lösung ». Z. Anorg. Allg. Chem. (на немецком). 391 (3): 193–202. Дои:10.1002 / zaac.19723910302. - ^ Бертольд HJ, Spiegl HJ (1972). "Über die Bildung von Lithiumtetrachloroferrat (II)" Ли
2FeCl
4 bei der Umsetzung von Eisen (III) -хлорид мил литийметил (1: 1) в ätherischer Lösung ». Z. Anorg. Allg. Chem. (на немецком). 391 (3): 193–202. Дои:10.1002 / zaac.19723910302. - ^ Химикаты для очистки воды (PDF). Akzo Nobel Base Chemicals. 2007. Архивировано с оригинал (PDF) 13 августа 2010 г.. Получено 26 октября 2007.
- ^ Парк К. Х., Мохапатра Д., Редди Б. Р. (2006). «Исследование выщелачивания подкисленного хлорида железа сложного штейна (Cu – Ni – Co – Fe)». Технология разделения и очистки. 51 (3): 332–337. Дои:10.1016 / j.seppur.2006.02.013.
- ^ Dueñas Díez M, Fjeld M, Andersen E, et al. (2006). «Валидация модели компартментального баланса населения промышленного процесса выщелачивания: процесс Силгрейна». Chem. Англ. Sci. 61 (1): 229–245. Дои:10.1016 / j.ces.2005.01.047.
- ^ Гринвуд Н.Н., Эрншоу А. (1997). Химия элементов (2-е изд.). Оксфорд: Баттерворт-Хайнеманн. п. 1084. ISBN 9780750633659.
- ^ Фернисс Б.С., Ханнафорд А.Дж., Смит П.В. и др. (1989). Учебник практической органической химии Фогеля (5-е изд.). Нью-Йорк: Longman /Wiley. ISBN 9780582462366.
- ^ Чжан С.Ю., Хуан З.П. (2006). «Цветовой тест для экспресс-скрининга гамма-гидроксимасляной кислоты (ГОМК) и гамма-бутиролактона (ГБЛ) в питье и моче». Фа И Сюэ За Чжи. 22 (6): 424–7. PMID 17285863.
- ^ Кили Т.Дж., Паусон П.Л. (1951). «Новый тип железоорганического соединения». Природа. 168 (4285): 1040. Bibcode:1951 г., природа. 168,1039K. Дои:10.1038 / 1681039b0. S2CID 4181383.
- ^ Камаль А., Рамана К., Анкати Х. и др. (2002). «Мягкое и эффективное восстановление азидов до аминов: синтез конденсированных [2,1-б] хиназолины ». Tetrahedron Lett. 43 (38): 6861–6863. Дои:10.1016 / S0040-4039 (02) 01454-5.
- ^ Ценг М., Дозьер А., Харибабу Б. и др. (2006). «Трансэндотелиальная миграция иона трехвалентного железа в FeCl
3 повреждена общая сонная артерия мыши ". Тромб. Res. 118 (2): 275–280. Дои:10.1016 / j.thromres.2005.09.004. PMID 16243382. - ^ Manohar, Aswin K .; Ким, Кю Мин; Плихта, Эдвард; Хендриксон, Мэри; Роулингс, Сабрина; Нараянан, С. Р. (28 октября 2015 г.). «Высокоэффективная проточная батарея с окислительно-восстановительным окислением железа и хлоридом железа для крупномасштабного хранения энергии». Журнал Электрохимического общества. 163 (1): A5118. Дои:10.1149 / 2.0161601jes. ISSN 1945-7111.
- ^ Патент США 241713, Pellet H, "Метод подготовки бумаги", опубликовано в 1881 г.
- ^ Литце Э (1888 г.). Современные гелиографические процессы. Нью-Йорк: Компания Д. Ван Норстранда. стр.65.
- ^ https://www.mindat.org/min-2749.html
- ^ https://www.ima-mineralogy.org/Minlist.htm
дальнейшее чтение
- Лиде ДР, изд. (1990). CRC Справочник по химии и физике (71-е изд.). Анн-Арбор, Мичиган, США: CRC Press. ISBN 9780849304712.
- Стечер П.Г., Финкель М.Дж., Зигмунд Огайо, ред. (1960). Индекс химических веществ и лекарств Merck (7-е изд.). Рэуэй, Нью-Джерси, США: Merck & Co.
- Николс Д. (1974). Комплексы и переходные элементы первого ряда, Macmillan Press, Лондон, 1973. Текст по химии Макмиллана. Лондон: Macmillan Press. ISBN 9780333170885.
- Уэллс А.Ф. (1984). Структурная неорганическая химия. Оксфордские научные публикации (5-е изд.). Оксфорд, Великобритания: Издательство Оксфордского университета. ISBN 9780198553700.
- Март J (1992). Продвинутая органическая химия (4-е изд.). Нью-Йорк: John Wiley & Sons, Inc., стр.723. ISBN 9780471581482.
- Райх Х. Дж., Ригби Х. Дж., Ред. (1999). Кислые и основные реагенты. Справочник реагентов для органического синтеза. Нью-Йорк: John Wiley & Sons, Inc. ISBN 9780471979258.












![{ Displaystyle { ce {FeCl3 + 3 [C2H5O] - Na + -> Fe (OC2H5) 3 + 3 NaCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ddc3c55642250edf274b916c6006e34934890549)


![{ Displaystyle { ce {{[Fe (H2O) 6] ^ {3 +}} + 4HO ^ {-} -> {[Fe (H2O) 2 (HO) 4] ^ {-}} + 4H2O-> {[Fe (H2O) O (HO) 2] ^ {-}} + 6H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/99ae6eaddcd1e52696d8e29bb25401a3e7112601)


