Хлорид бериллия - Beryllium chloride
 | |
| Имена | |
|---|---|
| Название ИЮПАК Хлорид бериллия | |
| Идентификаторы | |
3D модель (JSmol ) |
|
| ChemSpider | |
| ECHA InfoCard | 100.029.197 |
PubChem CID | |
| Номер RTECS |
|
| |
| |
| Характеристики | |
| BeCl2 | |
| Молярная масса | 79,9182 г / моль |
| Внешность | Белые или желтые кристаллы |
| Плотность | 1,899 г / см3, твердый |
| Температура плавления | 399 ° С (750 ° F, 672 К) |
| Точка кипения | 482 ° С (900 ° F, 755 К) |
| 15,1 г / 100 мл (20 ° С) | |
| Растворимость | растворим в алкоголь, эфир, бензол, и пиридин слабо растворим в хлороформ и диоксид серы |
| Структура | |
| шестиугольник | |
| полимер | |
| Термохимия | |
Теплоемкость (C) | 7,808 Дж / К или 71,1 Дж / моль К |
Стандартный моляр энтропия (S | 63 Дж / моль К |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | -6,136 кДж / г или -494 кДж / моль |
Свободная энергия Гиббса (Δжграмм˚) | -468 кДж / моль |
Станд. Энтальпия горение (ΔcЧАС⦵298) | 16 кДж / моль |
| Опасности | |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) | 86 мг / кг (крыса, перорально) |
| NIOSH (Пределы воздействия на здоровье в США): | |
PEL (Допустимо) | TWA 0,002 мг / м3 C 0,005 мг / м3 (30 минут), с максимальным пиком 0,025 мг / м3 (как Be)[1] |
REL (Рекомендуемые) | Ca C 0,0005 мг / м3 (как Be)[1] |
IDLH (Непосредственная опасность) | Ca [4 мг / м3 (как Be)][1] |
| Родственные соединения | |
Другой анионы | Фторид бериллия Бериллий бромид Йодид бериллия |
Другой катионы | Хлорид магния Хлорид кальция Хлорид стронция Хлорид бария Хлорид радия |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Хлорид бериллия является неорганическое соединение с формула BeCl2. Это бесцветный, гигроскопичный твердое вещество, хорошо растворяющееся во многих полярных растворителях. Его свойства аналогичны свойствам хлорид алюминия, из-за бериллий диагональные отношения с алюминий.
Структура и синтез
Хлорид бериллия получают реакцией металла с хлором при высоких температурах:[2]
- Be + Cl2 → BeCl2
BeCl2 также может быть приготовлен карботермическое восстановление из оксид бериллия в присутствии хлора.[3] BeCl2 можно приготовить путем обработки бериллий с хлористый водород.
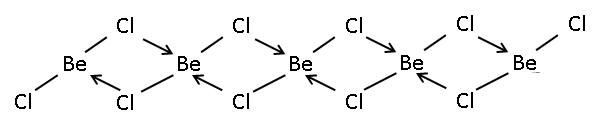
Твердое тело 1-мерный полимер состоящий из общих ребер тетраэдры.[4] В отличие, BeF2 это 3-х мерный полимер, по структуре схожий со структурой кварц. В газовой фазе BeCl2 существует как линейный мономер и мостовой димер с двумя мостиковыми атомами хлора, где атом бериллия 3-х координатный.[5] Линейная форма мономерной формы предсказывается VSEPR теория. Линейная форма контрастирует с мономерными формами некоторых из дигалогениды из более тяжелых членов группы 2, например CaF2, SrF2, BaF2, SrCl2, BaCl2, BaBr2, и BaI2, которые все нелинейны.[5]
Реакции
Хлорид бериллия устойчив в сухом воздухе. Хлорид бериллия - это Кислота Льюиса и использовался как катализатор в некоторых органических реакциях. Это гидролизует, развивающиеся хлористый водород:
- BeCl2 + 2H2О → Ве (ОН)2 + 2 HCl
Он образует тетрагидрат, BeCl2• 4H2O ([Be (H2O)4] Cl2). BeCl2 также растворим в кислородсодержащих растворителях, таких как эфиры.[6][7]
Приложения
Хлорид бериллия используется как сырье для электролиз бериллия, и как катализатор за Friedel-Crafts реакции.
Рекомендации
- ^ а б c Карманный справочник NIOSH по химической опасности. "#0054". Национальный институт охраны труда и здоровья (NIOSH).
- ^ Ирвинг Р. Танненбаум "Хлорид бериллия" Неорганические синтезы, 1957, т. 5, стр. 22. Дои:10.1002 / 9780470132364.ch7
- ^ Cotton, F. A .; Уилкинсон, Г. (1980) Продвинутая неорганическая химия John Wiley and Sons, Inc: Нью-Йорк, ISBN 0-471-02775-8.
- ^ Уэллс, А. Ф. (1984) Структурная неорганическая химия, Оксфорд: Clarendon Press. ISBN 0-19-855370-6.
- ^ а б Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ Лиде, Дэвид Р., изд. (2006). CRC Справочник по химии и физике (87-е изд.). Бока-Ратон, Флорида: CRC Press. ISBN 0-8493-0487-3.
- ^ Холлеман, А. Ф .; Виберг, Э. (2001) Неорганическая химия Academic Press: Сан-Диего, ISBN 0-12-352651-5
