Нитрат бериллия - Beryllium nitrate
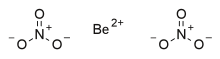 | |
| Имена | |
|---|---|
| Систематическое название ИЮПАК Нитрат бериллия | |
| Другие имена Динитрат бериллия | |
| Идентификаторы | |
| |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.033.678 |
| Номер ЕС |
|
PubChem CID | |
| UNII |
|
| Номер ООН | 2464 |
| |
| |
| Характеристики | |
| Быть (НЕТ3)2 | |
| Молярная масса | 133,021982 г / моль |
| Внешность | твердое вещество от белого до желтого |
| Запах | без запаха |
| Плотность | 1,56 г / см3 |
| Температура плавления | 60,5 ° С (140,9 ° F, 333,6 К) |
| Точка кипения | 142 ° С (288 ° F, 415 К) (разлагается) |
| 166 г / 100 мл | |
| Термохимия | |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | -700,4 кДж / моль |
| Опасности | |
| NIOSH (Пределы воздействия на здоровье в США): | |
PEL (Допустимо) | TWA 0,002 мг / м3 C 0,005 мг / м3 (30 минут), с максимальным пиком 0,025 мг / м3 (как Be)[1] |
REL (Рекомендуемые) | Ca C 0,0005 мг / м3 (как Be)[1] |
IDLH (Непосредственная опасность) | Ca [4 мг / м3 (как Be)][1] |
| Родственные соединения | |
Другой катионы | Нитрат магния Нитрат кальция Нитрат стронция Нитрат бария |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Нитрат бериллия, также известный как динитрат бериллия, является ионный бериллий соль из азотная кислота с химическая формула Быть (НЕТ3)2.[2] Каждый формульная единица состоит из одного Be2+ катион и два НЕТ3− анионы.
Опасности
Нитрат бериллия - токсичное химическое вещество,[2] как и все другие соединения бериллия. В малых дозах он также является раздражителем. При горении выделяет раздражающие или токсичные пары. Однако при массивном кратковременном воздействии острое пневмонит может наступить, но симптомы не проявляются в течение 3 дней.[2]
Подготовка
Нитрат бериллия можно получить путем реакции гидроксид бериллия в азотная кислота.[3]
- Будь (ОН)2 + 2 HNO3 → Быть (НЕТ3)2 + 2 часа2О
Рекомендации
- ^ а б c Карманный справочник NIOSH по химической опасности. "#0054". Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б c «Нитрат бериллия (ICSC)». IPCS INCHEM. Получено 13 сентября 2010.
- ^ Уолш, Кеннет (2009). Химия и переработка бериллия. ASM International. С. 121–122. ISBN 978-0-87170-721-5. Получено 3 января 2011.
Соли и ковалентные производные нитрат ион
| Этот неорганический сложный –Связанная статья является заглушка. Вы можете помочь Википедии расширяя это. |
