Платина (IV) хлорид - Platinum(IV) chloride
 | |
| Имена | |
|---|---|
| Название ИЮПАК Платина (IV) хлорид | |
| Идентификаторы | |
3D модель (JSmol ) |
|
| ChemSpider | |
| ECHA InfoCard | 100.033.300 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| PtCl4 | |
| Молярная масса | 336,89 г / моль |
| Внешность | коричнево-красный порошок |
| Плотность | 4,303 г / см3 (безводный) 2,43 г / см3 (пентагидрат) |
| Температура плавления | 370 ° С (698 ° F, 643 К) разлагается |
| Точка кипения | разлагается |
| 58,7 г / 100 мл (безводный) очень растворим (пентагидрат) | |
| Растворимость | безводный растворим в ацетон слабо растворим в этиловый спирт не растворим в эфир пентагидрат растворим в алкоголь, эфир |
| −93.0·10−6 см3/ моль | |
| Структура | |
| Квадратный плоский | |
| Опасности | |
Классификация ЕС (DSD) (устарело) | нет в списке |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) | 276 мг / кг (крыса, перорально) |
| Родственные соединения | |
Другой анионы | Бромид платины (IV) Платина (IV) фторид Сульфид платины (IV) |
Другой катионы | Хлорид иридия (IV) |
Родственные соединения | Платина (II) хлорид Платина (VI) фторид |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Платина (IV) хлорид это неорганическое соединение из платина и хлор с эмпирической формулой PtCl4. Это коричневое твердое вещество содержит платину в степени окисления 4+.
Структура
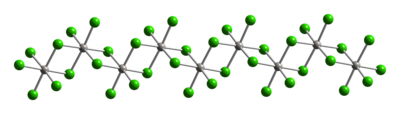
Типичные для Pt (IV) металлические центры имеют октаэдрическая координационная геометрия, {PtCl6}. Эта геометрия достигается за счет образования полимера, в котором половина хлоридных лигандов соединяется между платиновыми центрами. Благодаря своей полимерной структуре PtCl4 растворяется только после разрушения хлорида мостиковые лиганды. Таким образом, добавление HCl дает H2PtCl6. База Льюиса аддукты Pt (IV) типа цис-PtCl4L2 известны, но большинство из них получают окислением производных Pt (II).
 |
Образование и реакции
PtCl4 в основном встречается при обращении с платинохлористоводородная кислота, полученный растворением металлической Pt в царская водка. Отопление H2PtCl6 дает PtCl4:
- ЧАС2PtCl6 → PtCl4 + 2 HCl
Если удалить избыток кислот, PtCl4 кристаллизуется из водных растворов в крупных красных кристаллах пентагидрата PtCl4· 5 (H2O),[1] который может быть обезвожен путем нагревания примерно до 300 ° C в токе сухого хлора. Пентагидрат стабилен и используется как коммерческая форма PtCl.4.
Лечение PtCl4 с водным основанием дает [Pt (OH)6]2− ион. С метилом Реактивы Гриньяра с последующим частичным гидролизом, PtCl4 преобразуется в кубический кластер [Pt (CH3)3(ОЙ)]4.[2] При нагревании PtCl4 развивается хлор давать PtCl2:
- PtCl4 → PtCl2 + Cl2
Более тяжелые галогениды, PtBr4 и PtI4, также известны.
Рекомендации
- Коттон, С.А. Химия драгоценных металлов, Чепмен и Холл (Лондон): 1997. ISBN 0-7514-0413-6.
- ^ Джордж Сэмюэл Ньют (1920). Учебник неорганической химии.. Лонгманс, Грин и др. п. 694.
- ^ Greenwood, N. N .; И Эрншоу, А. (1997). Химия элементов (2-е изд.), Оксфорд: Баттерворт-Хайнеманн. ISBN 0-7506-3365-4.
| Этот неорганический сложный –Связанная статья является заглушка. Вы можете помочь Википедии расширяя это. |
