Хлорид железа (II) - Iron(II) chloride
 Состав безводного хлорида железа ( Fe, Cl) | |||
| |||
| Имена | |||
|---|---|---|---|
| Имена ИЮПАК Хлорид железа (II) Дихлорид железа | |||
| Другие имена Хлорное железо Рокюнит | |||
| Идентификаторы | |||
| |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.028.949 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| |||
| |||
| Характеристики | |||
| FeCl2 | |||
| Молярная масса | 126.751 г / моль (безводный) 198.8102 г / моль (тетрагидрат) | ||
| Внешность | Твердый загар (безводный) Бледно-зеленое твердое вещество (ди-тетрагидрат) | ||
| Плотность | 3.16 г / см3 (безводный) 2.39 г / см3 (дигидрат) 1.93 г / см3 (тетрагидрат) | ||
| Температура плавления | 677 ° С (1251 ° F, 950 К) (безводный) 120 ° C (дигидрат) 105 ° С (тетрагидрат) | ||
| Точка кипения | 1023 ° С (1873 ° F, 1296 К) (безводный) | ||
| 64.4 г / 100 мл (10 ° С), 68.5 г / 100 мл (20 ° С), 105.7 г / 100 мл (100 ° C) | |||
| Растворимость в THF | Растворимый | ||
| бревно п | −0.15 | ||
| +14750·10−6 см3/ моль | |||
| Структура | |||
| Моноклиника | |||
| Октаэдр в Fe | |||
| Фармакология | |||
| B03AA05 (ВОЗ) | |||
| Опасности | |||
| Паспорт безопасности | Паспорт безопасности хлорида железа (II) | ||
| NFPA 704 (огненный алмаз) | |||
| NIOSH (Пределы воздействия на здоровье в США): | |||
REL (Рекомендуемые) | TWA 1 мг / м3[1] | ||
| Родственные соединения | |||
Другой анионы | Фторид железа (II) Бромид железа (II) Иодид железа (II) | ||
Другой катионы | Хлорид кобальта (II) Хлорид марганца (II) Хлорид меди (II) | ||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Хлорид железа (II), также известный как хлорид железа, это химическое соединение формулы FeCl2. Это парамагнитный твердое вещество с высокой температурой плавления. Состав белый, но типичные образцы часто не совсем белые. FeCl2 кристаллизуется из воды как зеленоватый тетрагидрат, которая чаще всего встречается в торговле и лабораториях. Также есть дигидрат. Соединение хорошо растворяется в воде, давая бледно-зеленые растворы.
Производство

Гидратированные формы хлорида железа образуются при переработке отходов производство стали с соляная кислота. Такие растворы называют «отработанной кислотой» или «травильным раствором», особенно когда соляная кислота израсходована не полностью:
- Fe + 2 HCl → FeCl2 + H2
Отработанная кислота требует обработки в случае ее утилизации. Хлорид железа используется при производстве хлорида железа. Хлорид железа также можно использовать для регенерации соляной кислоты. Это также побочный продукт производства титана, так как некоторые титановые руды содержат железо.[3]
Безводный FeCl2
Хлорид железа получают добавлением порошка железа к раствору соляная кислота в метаноле. Эта реакция дает метанольный сольват дихлорида, который при нагревании в вакууме примерно до 160 ° C превращается в безводный FeCl2.[4] Показана чистая реакция:
- Fe + 2 HCl → FeCl2 + H2
FeBr2 и FeI2 можно приготовить аналогично.
Альтернативным синтезом безводного хлорида железа является восстановление FeCl3 с хлорбензол:[5]
- 2 FeCl3 + C6ЧАС5Cl → 2 FeCl2 + C6ЧАС4Cl2 + HCl
В одном из двух классических синтезов ферроцен, Уилкинсон генерированный FeCl2 на месте путем компропорционирования FeCl3 с железным порошком в THF.[6] Хлорид железа разлагается до хлорида железа при высоких температурах.
Увлажняет
Дигидрат, FeCl2(ЧАС2O)2, кристаллизуется из концентрированной соляной кислоты.[7] Дигидрат представляет собой координационный полимер. Каждый Fe-центр согласован с четырьмя двукратными мостиковые хлоридные лиганды. Октаэдр завершается парой взаимно транс акво-лиганды.[8]

Реакции
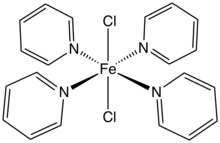
FeCl2 и его гидраты образуют комплексы со многими лигандами. Например, растворы гидратов реагируют с двумя молярными эквивалентами [(C2ЧАС5)4N] Cl дать соль [(C2ЧАС5)4N]2[FeCl4].[10]
Безводный FeCl2, который растворим в тетрагидрофуран (THF),[2] является стандартным предшественником в металлоорганическом синтезе. FeCl2 используется для создания Комплексы NHC на месте для реакции кросс-сочетания.[11]
Приложения
В отличие от родственных сульфат железа и хлорид железа, хлорид железа имеет несколько коммерческих применений. Помимо использования в лабораторном синтезе комплексов железа, хлорид железа служит для коагуляции и флокуляция агент в очистки сточных вод, особенно для отходов, содержащих хромат или сульфиды.[12] Он используется для контроля запаха при очистке сточных вод. Он используется в качестве прекурсора для производства различных сортов гематита, который может использоваться в различных пигментах. Это предшественник гидратированных оксидов железа (III), которые являются магнитными пигментами.[3] FeCl2 находит применение в качестве реагент в органический синтез. [13]
Естественное явление
Лоуренсит, (Fe, Ni) Cl2, является естественным аналогом и типичным (хотя и редко встречающимся) метеоритным минералом.[14] Естественная форма дигидрата: рокюнит - очень редкий минерал.[15] Родственные, но более сложные (в частности, основные или гидратированные) минералы гиббингит, дрониноит и кулигинит.
Рекомендации
- ^ Карманный справочник NIOSH по химической опасности. "#0346". Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б Cotton, F. A .; Удача, Р. Л .; Сын, К.-А. (1991). «Новые полиядерные соединения хлорида железа (II) с лигандами-донорами кислорода Часть I. Fe4Cl8(THF)6: синтез и определение рентгеновской структуры монокристаллов ». Неорганика Chimica Acta. 179: 11–15. Дои:10.1016 / S0020-1693 (00) 85366-9.CS1 maint: использует параметр авторов (связь)
- ^ а б Эгон Вильдермут, Ганс Старк, Габриэле Фридрих, Франц Людвиг Эбенхох, Бриджит Кюборт, Джек Сильвер, Рафаэль Ритупер «Соединения железа» в Энциклопедия промышленной химии Ульмана. Wiley-VCH, Винхайм, 2005.
- ^ Г. Винтер; Томпсон, Д. В .; Лое, Дж. Р. (1973). Галогениды железа (II). Неорг. Synth. Неорганические синтезы. 14. С. 99–104. Дои:10.1002 / 9780470132456.ch20. ISBN 9780470132456.
- ^ П. Ковачич и Н. О. Брейс (1960). «Хлорид железа (II)». Неорганические синтезы. Неорг. Synth. Неорганические синтезы. 6. С. 172–173. Дои:10.1002 / 9780470132371.ch54. ISBN 9780470132371.
- ^ Г. Уилкинсон (1963). «Ферроцен». Органический синтез.; Коллективный объем, 4, п. 473
- ^ К. Х .. Гейер; Л. Вунтнер (1957). 2-гидрат хлорида железа (II). Неорг. Synth. Неорганические синтезы. 5. С. 179–181. Дои:10.1002 / 9780470132364.ch48. ISBN 9780470132364.
- ^ Морозин, Б .; Грэбер, Э. Дж. (1965). «Кристаллические структуры дигидрата хлорида марганца (II) и железа (II)». Журнал химической физики. 42 (3): 898–901. Bibcode:1965ЖЧФ..42..898М. Дои:10.1063/1.1696078.
- ^ Баудиш, Оскар; Хартунг, Вальтер Х. (1939). «Тетрапиридино-хлорид железа (желтая соль)». Неорганические синтезы. Неорганические синтезы. 1. С. 184–185. Дои:10.1002 / 9780470132326.ch64. ISBN 9780470132326.
- ^ Н. С. Гилл, Ф. Б. Тейлор (1967). «Тетрахалоидные комплексы дипозитивных металлов в первой переходной серии». Неорганические синтезы. Неорг. Synth. Неорганические синтезы. 9. С. 136–142. Дои:10.1002 / 9780470132401.ch37. ISBN 9780470132401.
- ^ Би-Цзе Ли, Си-Ша Чжан, Чжан-Цзе Ши (2014). «Перекрестное связывание алкенил / арилкарбоксилатов с реактивами Гриньяра посредством активации связи С-О, катализируемой железом». Орг. Синтезатор. 91: 83–92. Дои:10.15227 / orgsyn.091.0083.CS1 maint: использует параметр авторов (связь)
- ^ Джамиль, Первез (1989). «Использование хлорида железа для контроля растворенных сульфидов в перехватывающих коллекторах». Журнал (Федерация по контролю за загрязнением воды). 61 (2): 230–236. JSTOR 25046917.
- ^ Эндрю Д. Уайт, Дэвид Г. Хилми (2009). «Хлорид железа (II)». Энциклопедия реагентов для органического синтеза. Дои:10.1002 / 047084289X.ri055.pub2. ISBN 978-0471936237.CS1 maint: использует параметр авторов (связь)
- ^ https://www.mindat.org/min-2351.html
- ^ https://www.mindat.org/min-3440.html


