Координационная геометрия - Coordination geometry
Период, термин координационная геометрия используется в ряде смежных областей химии и химии / физики твердого тела.
Молекулы
Координационная геометрия атома - это геометрический узор, образованный атомами вокруг центрального атома.
Неорганические координационные комплексы
В области неорганических координационных комплексов это геометрический узор, образованный атомами в лиганды которые связанный к центральному атому в молекула или координационный комплекс. Геометрическое расположение будет варьироваться в зависимости от количества и типа лигандов, связанных с металлическим центром, и от предпочтительной координации центрального атома, обычно металла в координационный комплекс. Число связанных атомов (т. Е. Число σ-связи между центральным атомом и лигандами) называется координационный номер Геометрический узор можно описать как многогранник где вершины многогранника - центры координирующих атомов лигандов.[1]
Предпочтение координации металла часто зависит от его степени окисления. Количество координационных связей (координационный номер ) может варьироваться от двух до 20 в Th (η5-C5ЧАС5)4.[2]
Одна из наиболее распространенных координационных геометрий - восьмигранный, где шесть лигандов координированы с металлом в симметричном распределении, что приводит к образованию октаэдр если провести линии между лигандами. Другие общие координационные геометрии: четырехгранный и квадратный плоский.
Теория кристаллического поля может быть использован для объяснения относительной стабильности соединений переходных металлов с различной координационной геометрией, а также наличия или отсутствия парамагнетизм, в то время как VSEPR может использоваться для комплексов элемент основной группы предсказывать геометрию.
Использование кристаллографии
В кристаллической структуре координационная геометрия атома - это геометрический образец координирующих атомов, где определение координирующих атомов зависит от используемой модели связи.[1] Например, в ионной структуре каменной соли каждый атом натрия имеет шесть ближайших соседних ионов хлора в октаэдрической геометрии, и каждый хлорид аналогичным образом имеет шесть ближайших соседних ионов натрия в октаэдрической геометрии. В металлы с объемно-центрированной кубической (ОЦК) структурой каждый атом имеет восемь ближайших соседей в кубической геометрии. В металлы с гранецентрированной кубической (ГЦК) структурой каждый атом имеет двенадцать ближайших соседей в кубооктаэдр геометрия.
Таблица координационных геометрий
Таблица встречающихся координационных геометрий показана ниже с примерами их появления в комплексах, обнаруженных в виде дискретных единиц в соединениях, и координационных сферах вокруг атомов в кристаллах (где нет дискретных комплексов).
| Координационный номер | Геометрия | Примеры дискретных (конечных) комплексных | Примеры в кристаллах (бесконечные твердые тела) | |
|---|---|---|---|---|
| 2 | линейный | Ag (CN)2− в KAg (CN)2 [3] | Ag в цианид серебра, Au в AuI [2] | |
| 3 | тригонально плоский |  | HgI3−[2] | О в TiO2 структура рутила[3] |
| 4 | четырехгранный |  | CoCl42−[2] | Zn и S в сульфид цинка, Si в диоксид кремния[3] |
| 4 | квадратный плоский |  | AgF4−[2] | CuO[3] |
| 5 | тригонально-бипирамидный |  | SnCl5−[3] | |
| 5 | квадратно-пирамидальный |  | InCl52− в (NEt4)2InCl5[2] | |
| 6 | восьмигранный |  | Fe (H2O)62+[2] | Na и Cl в NaCl[3] |
| 6 | тригонально-призматический |  | W (CH3)6[4] | Как в NiAs, Пн в MoS2[3] |
| 7 | пятиугольный бипирамидальный |  | ZrF73− в (NH4)3ZrF7[3] | Боль PaCl5 |
| 7 | закрытый восьмигранный |  | Минфин7−[5] | Ла в А-ля2О3 |
| 7 | закрытый тригонально-призматический | 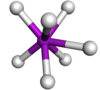 | TaF72− чернила2TaF7[3] | |
| 8 | квадратный антипризматический |  | TaF83− в Na3TaF8[3] Zr (H2O)84+ аквакомплекс[6] | Иодид тория (IV)[3] |
| 8 | додекаэдр (примечание: хотя это обычно термин используется правильный термин "бисдисфеноид"[3] или же "курносый дисфеноид "поскольку этот многогранник дельтаэдр ) |  | Пн (CN)84− чернила4[Пн (CN)8] .2H2О[3] | Zr в K2ZrF6[3] |
| 8 | двуглавый тригонально-призматический | 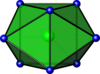 | ZrF84−[7] | PuBr3[3] |
| 8 | кубический | Хлорид цезия, фторид кальция | ||
| 8 | гексагональный бипирамидальный | 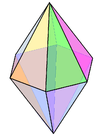 | N в Ли3N[3] | |
| 8 | восьмигранный, транс-двуглавый | Ni в арсенид никеля, NiAs; 6 Как соседи + 2 никелевых покрытия[8] | ||
| 8 | треугольная призматическая, треугольная грань двояковыпуклая | Ca в CaFe2О4[3] | ||
| 9 | трехшарошечная тригональная призматическая | 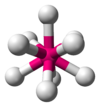 | [ReH9]2− в нонагидридорфенат калия[2] Чт (H2O)94+ аквакомплекс[6] | SrCl2.6H2O, Th в RbTh3F13[3] |
| 9 | закрытый квадратный антипризматический |  | [Чт (трополонат)4(ЧАС2O)][2] | La in LaTe2[3] |
| 10 | двуглавый квадратный антипризматический | Чт (С2О4)42− [2] | ||
| 11 | Чт в [ЧтIV(НЕТ3)4(ЧАС2O)3] (НЕТ3− двузубый) [2] | |||
| 12 | икосаэдр |  | Чт в Чт (НЕТ3)62− ион в Mg [Th (NO3)6] .8H2О [3] | |
| 12 | кубооктаэдр |  | ZrIV(η3- (BH4)4) | атомы в металлы с ГЦК например Ca[3] |
| 12 | антикубоктаэдр (треугольная ортобикупола ) |  | атомы в ГПУ металлы например Sc [3] | |
| 12 | двуглавый шестиугольный антипризматический | U (BH4)4[2] |
Наименование неорганических соединений
ИЮПАК представил многогранный символ как часть их Номенклатура неорганической химии IUPAC, рекомендации 2005 г. для описания геометрии атома в соединении.[9]
IUCr предложил символ, который в химической формуле отображается как верхний индекс в квадратных скобках. Например, CaF2 будет Ca[8cb]F2[4т], где [8cb] означает кубическую координацию, а [4t] означает тетраэдрическую. Эквивалентные символы в ИЮПАК: CU−8 и Т−4 соответственно.[1]
Символ IUPAC применим к комплексам и молекулам, тогда как предложение IUCr относится к кристаллическим твердым веществам.
Смотрите также
Рекомендации
- ^ а б c Х. Лима-де-Фариа; Э. Хеллнер; Ф. Либау; Э. Маковицкий; Э. Парте (1990). «Отчет Международного союза кристаллографической комиссии о подкомитете по кристаллографической номенклатуре по номенклатуре типов неорганических структур». Acta Crystallogr. А. 46: 1–11. Дои:10.1107 / S0108767389008834. Архивировано из оригинал на 2012-06-13. Получено 2008-09-12.
- ^ а б c d е ж грамм час я j k л Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v Уэллс А.Ф. (1984) Структурная неорганическая химия 5-е издание Oxford Science Publications ISBN 0-19-855370-6
- ^ Housecroft, C.E .; Шарп, А. Г. (2004). Неорганическая химия (2-е изд.). Прентис Холл. п. 725. ISBN 978-0-13-039913-7.
- ^ Каупп, Мартин (2001). ""Не-VSEPR "Структуры и соединения в системах d (0)". Angew Chem Int Ed Engl. 40 (1): 3534–3565. Дои:10.1002 / 1521-3773 (20011001) 40:19 <3534 :: AID-ANIE3534> 3.0.CO; 2- #.
- ^ а б Перссон, Ингмар (2010). «Гидратированные ионы металлов в водном растворе: насколько регулярны их структуры?». Чистая и прикладная химия. 82 (10): 1901–1917. Дои:10.1351 / PAC-CON-09-10-22. ISSN 0033-4545.
- ^ Джереми К. Бёрдетт; Роальд Хоффманн; Роберт С. Фэй (1978). «Восьмерка-координация». Неорганическая химия. 17 (9): 2553–2568. Дои:10.1021 / ic50187a041.
- ^ Дэвид Г. Петтифор, Связь и структура молекул и твердых тел, 1995, Oxford University Press,ISBN 0-19-851786-6
- ^ НОМЕНКЛАТУРА НЕОРГАНИЧЕСКОЙ ХИМИИ Рекомендации IUPAC 2005 ed. Н. Г. Коннелли и др. RSC Publishing http://www.chem.qmul.ac.uk/iupac/bioinorg/
