Диоксид хлора - Chlorine dioxide
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Диоксид хлора | |||
| Другие имена Оксид хлора (IV) | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.030.135 | ||
| Номер ЕС |
| ||
| Номер E | E926 (глазурь, ...) | ||
| 1265 | |||
| MeSH | Хлор + диоксид | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 9191 | ||
| |||
| |||
| Характеристики | |||
| ClО2 | |||
| Молярная масса | 67.45 г · моль−1 | ||
| Внешность | Газ от желтого до красноватого | ||
| Запах | Едкий | ||
| Плотность | 2.757 г дм−3[1] | ||
| Температура плавления | -59 ° С (-74 ° F, 214 К) | ||
| Точка кипения | 11 ° С (52 ° F, 284 К) | ||
| 8 г / л (при 20 ° С) | |||
| Растворимость | растворим в щелочах и серная кислота решения | ||
| Давление газа | > 1 атм[2] | ||
Закон Генри постоянный (kЧАС) | 4.01×10−2 атм м3 моль−1 | ||
| Кислотность (пKа) | 3.0(5) | ||
| Термохимия | |||
Стандартный моляр энтропия (S | 257,22 Дж К−1 моль−1 | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | 104,60 кДж / моль | ||
| Опасности | |||
| Главный опасности | Острая токсичность | ||
| Паспорт безопасности | Паспорт безопасности Архив. | ||
| Пиктограммы GHS |    | ||
| Сигнальное слово GHS | Опасность | ||
| H271, H314, H330 | |||
| P210, P220, P280, P283, P260, P264, P271, P284, P301, P330, P331, P311, P306, P360, P304, P340, P305, P351, P338, P371 + 380 + 375, P405, P403 + 233, P501 | |||
| NFPA 704 (огненный алмаз) | |||
| Смертельная доза или концентрация (LD, LC): | |||
LD50 (средняя доза ) | 94 мг / кг (перорально, крыса)[3] | ||
LCLo (самый низкий опубликованный ) | 260 частей на миллион (крыса, 2 часа)[4] | ||
| NIOSH (Пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 0,1 частей на миллион (0,3 мг / м3)[2] | ||
REL (Рекомендуемые) | TWA 0,1 частей на миллион (0,3 мг / м3) ST 0,3 частей на миллион (0,9 мг / м3)[2] | ||
IDLH (Непосредственная опасность) | 5 частей на миллион[2] | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Диоксид хлора это химическое соединение с формулой ClO2 который существует как желтовато-зеленый газ выше 11 ° C, красновато-коричневая жидкость при температуре от 11 ° C до -59 ° C и в виде ярко-оранжевых кристаллов ниже -59 ° C. Это окислитель, способный переносить кислород к различным субстратам, получая при этом один или несколько электронов за счет окисления-восстановления (редокс ). Это не гидролизовать когда он попадает в воду, и обычно с ним обращаются как с растворенным в воде газом. Потенциальные опасности, связанные с диоксидом хлора, включают опасность для здоровья, взрывоопасность и возгорание.[5] Обычно используется как отбеливать.
Диоксид хлора был открыт в 1811 году и широко используется для отбеливания в бумажной промышленности и для очистки питьевой воды. Более поздние разработки расширили его применение в пищевой промышленности, дезинфекции помещений и транспортных средств, уничтожении плесени, дезинфекции воздуха и борьбе с запахом, обработке бассейнов, стоматологических применениях и очищении ран.
Соединение обманным путем продавалось как лекарство от широкого спектра заболеваний, включая детский аутизм.[6] и COVID-19.[7][8][9] Детям, которым дали клизмы диоксида хлора как предполагаемое лекарство от детского аутизма страдали от опасных для жизни недугов.[6] В Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) заявило, что прием внутрь или другое внутреннее использование диоксида хлора (кроме, возможно, полоскания полости рта под наблюдением стоматолога) не приносит пользы для здоровья, и его не следует применять внутрь ни по какой причине.[10][11]
Структура и склеивание
Диоксид хлора - нейтральный соединение хлора. Он сильно отличается от элементарного хлора как по своей химической структуре, так и по поведению.[12] Одно из важнейших свойств диоксида хлора - его высокая растворимость в воде, особенно в холодной воде. Диоксид хлора не гидролизовать при попадании в воду; он остается растворенным газом в растворе. Диоксид хлора примерно в 10 раз более растворим в воде, чем хлор.[12]
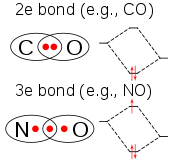
Молекула ClO2 имеет нечетное количество валентные электроны, а значит, это парамагнитный радикальный. Его электронная структура долгое время сбивала с толку химиков, потому что ни одна из возможных Структуры Льюиса очень удовлетворительно. В 1933 году Л. О. Броквей предложил структуру, включающую трехэлектронная связь.[13] Химик Линус Полинг развил эту идею и пришел к двум резонансные структуры включая двойную связь с одной стороны и одинарную связь плюс трехэлектронную связь с другой.[14] По мнению Полинга, последняя комбинация должна представлять некоторую связь, слабее чем двойная связь. В теория молекулярных орбиталей эта идея является обычным явлением, если третий электрон помещен на антисвязывающую орбиталь. Позже работа подтвердила, что самая высокая занятая молекулярная орбиталь действительно является не полностью заполненной разрыхляющей орбиталью.[15]
Подготовка
Диоксид хлора - это соединение, которое может очень сильно разлагаться при отделении от разбавляющих веществ. В результате часто предпочтительны способы приготовления, которые включают получение его растворов без прохождения стадии газовой фазы. Очень важно организовать безопасное обращение.
Окисление хлорита
В лаборатории ClO2 может быть получен окислением хлорит натрия с хлором:[16]
- 2 NaClO2 + Cl2 → 2 ClO2 + 2 NaCl
Традиционно диоксид хлора для дезинфекция аппликации были сделаны из натрия хлорит или хлорит натрия -гипохлорит метод:
- 2 NaClO2 + 2 HCl + NaOCl → 2 ClO2 + 3 NaCl + H2О
или хлорит натрия -соляная кислота метод:
- 5 NaClO2 + 4 HCl → 5 NaCl + 4 ClO2 + 2 часа2О
или хлорит -серная кислота метод:
- 4 ClO−
2 + 2 часа2ТАК4 → 2 ClO2 + HClO3 + 2 ТАК2−
4 + H2O + HCl
Все три метода позволяют производить диоксид хлора с высоким выходом конверсии хлорита. В отличие от других процессов, метод хлорит-серная кислота дает полностью свободный от хлора диоксид хлора, хотя при этом требуется на 25% больше хлорита для получения эквивалентного количества диоксида хлора. В качестве альтернативы, пероксид водорода может эффективно использоваться в небольших приложениях.[12]
Снижение хлората
В лаборатории диоксид хлора также можно получить реакцией хлорат калия с Щавелевая кислота:
- 2 KClO3 + 2 часа2C2О4 → K2C2О4 + 2 ClO2 + 2 СО2 + 2 часа2О
- 2 KClO3 + H2C2О4 + 2 часа2ТАК4 → 2 ХСО4 + 2 ClO2 + 2 СО2 + 2 часа2О
Более 95% диоксида хлора, производимого сегодня в мире, производится за счет сокращения хлорат натрия, для использования в отбеливание целлюлозы. Производится с высокой эффективностью в растворе сильной кислоты с подходящей Восстановитель Такие как метанол, пероксид водорода, соляная кислота или же диоксид серы.[12] Современные технологии основаны на метаноле или перекиси водорода, поскольку этот химический состав обеспечивает максимальную экономию и не приводит к совместному производству элементарного хлора. Общую реакцию можно записать как:[17]
- хлорат + кислота + восстановитель → диоксид хлора + побочные продукты
Как типичный пример, реакция хлорат натрия с соляная кислота в одном реакторе, как полагают, происходит по следующему пути:
- ClO−
3 + Cl−
+ ЧАС+
→ ClO−
2 + HOCl - ClO−
3 + ClO−
2 + 2 ЧАС+
→ 2 ClO
2 + ЧАС
2О - HOCl + Cl−
+ ЧАС+
→ Cl
2 + ЧАС
2О
что дает общую реакцию
- 2 ClO−
3 + 2 Cl−
+ 4 ЧАС+
→ 2 ClO
2 + Cl
2 + 2 ЧАС
2О.
Более важный с коммерческой точки зрения производственный маршрут использует метанол как восстановитель и серная кислота для кислотности. Два преимущества отказа от хлоридных процессов заключаются в отсутствии образования элементарного хлора и в том, что сульфат натрия, ценный химикат для целлюлозного завода, является побочным продуктом. Эти процессы на основе метанола обеспечивают высокую эффективность и могут быть очень безопасными.[12]
Вариант процесса с использованием хлората, перекиси водорода и серной кислоты все чаще используется с 1999 г. для очистки воды и других небольших дезинфекция применения, поскольку он производит продукт без хлора с высокой эффективностью.
Другие процессы
Очень чистый диоксид хлора можно также получить электролизом раствора хлорита:[18]
- 2 NaClO2 + 2 часа2O → 2 ClO2 + 2 NaOH + H2
Газообразный диоксид хлора высокой чистоты (7,7% в воздухе или азоте) может быть получен газо-твердым методом, при котором разбавленный газообразный хлор реагирует с твердым хлоритом натрия:[18]
- 2 NaClO2 + Cl2 → 2 ClO2 + 2 NaCl
Обработка свойств
При парциальном давлении выше 10 кПа[12] (или концентрации газовой фазы более 10% объема в воздухе при STP ), ClO2 может взрывоопасно распадаться на хлор и кислород. Разложение может быть инициировано светом, горячими точками, химической реакцией или ударным давлением. Таким образом, с газообразным диоксидом хлора никогда не обращаются в концентрированном виде, но почти всегда с ним обращаются как с растворенным в воде газом в диапазоне концентраций от 0,5 до 10 граммов на литр. Его растворимость увеличивается при более низких температурах, поэтому обычно используют охлажденную воду (5 ° C) при хранении в концентрациях выше 3 граммов на литр. Во многих странах, например в США, газообразный диоксид хлора нельзя транспортировать в любой концентрации, и он почти всегда производится на месте применения с использованием генератора диоксида хлора.[12] В некоторых странах,[который? ] растворы диоксида хлора с концентрацией менее 3 граммов на литр могут транспортироваться по суше, однако они относительно нестабильны и быстро портятся.
Использует
Диоксид хлора используется для отбеливание древесной массы и для дезинфекция (называется хлорирование ) муниципальной питьевой воды.[19][20]:4–1[21] В качестве дезинфицирующего средства он эффективен даже при низких концентрациях благодаря своим уникальным свойствам.[12][20]
Отбеливание
Диоксид хлора иногда используется для отбеливание древесной массы в комбинации с хлором, но он используется отдельно в последовательностях отбеливания ECF (без элементарного хлора). Применяется при умеренно кислой pH (От 3,5 до 6). Использование диоксида хлора сводит к минимуму количество хлорорганические соединения произведенные соединения.[22] Диоксид хлора (технология ECF) в настоящее время является наиболее важным методом отбеливания во всем мире. Около 95% всего отбеленного крафт-целлюлоза производится с использованием диоксида хлора в процессах отбеливания ECF.[23]
Диоксид хлора использовался для отбеливать мука.[24]
Очистка воды
В Ниагарский водопад, Нью-Йорк, водоочистная станция впервые использовала диоксид хлора для питьевая вода лечение в 1944 году для уничтожения "вкуса и запаха, производящих фенольные соединения ".[20]:4–17[21] Диоксид хлора был широко представлен в качестве дезинфицирующего средства для питьевой воды в 1956 году, когда Брюссель, Бельгия, перешла с хлора на диоксид хлора.[21] Его чаще всего используют при очистке воды в качестве предварительнойокислитель перед хлорированием питьевой воды для уничтожения природных примесей воды, которые в противном случае тригалометаны при воздействии свободного хлора.[25][26][27] Тригалометаны являются побочными продуктами канцерогенной дезинфекции[28] связано с хлорированием природных органических веществ в сырой воде.[27] Диоксид хлора также превосходит хлор при работе выше pH 7,[20]:4–33 в присутствии аммиака и аминов[нужна цитата ] и для контроля биопленок в системах распределения воды.[27] Диоксид хлора используется во многих промышленных системах очистки воды в качестве биоцид включая градирни, техническая вода и пищевая промышленность.[29]
Диоксид хлора менее агрессивен, чем хлор, и лучше подходит для контроля Легионелла бактерии.[21][30]Диоксид хлора превосходит некоторые другие методы вторичной дезинфекции воды тем, что диоксид хлора является EPA зарегистрированный биоцид, не подвержен отрицательному воздействию pH, не теряет эффективности со временем (бактерии не вырастут к нему устойчивыми) и не подвержен отрицательному воздействию кремнезем и фосфаты, которые обычно используются в качестве ингибиторов коррозии питьевой воды.
Он более эффективен в качестве дезинфицирующего средства, чем хлор, в большинстве случаев против патогенных агентов, передающихся через воду, таких как вирусы,[31] бактерии и простейшие - в том числе кисты из Лямблии и ооцисты из Криптоспоридиум.[20]:4–20–4–21
Использование диоксида хлора при очистке воды приводит к образованию побочного хлорита, содержание которого в питьевой воде в США в настоящее время ограничено до 1 части на миллион.[20]:4–33 Этот стандарт EPA ограничивает использование диоксида хлора в США относительно высококачественной водой, поскольку это сводит к минимуму концентрацию хлорита, или воду, которую необходимо обрабатывать коагулянтами на основе железа (железо может восстанавливать хлорит до хлорида).[нужна цитата ]
Использование в общественных кризисах
Диоксид хлора имеет множество применений в качестве окислителя или дезинфицирующего средства.[12] Диоксид хлора можно использовать для обеззараживания воздуха.[32] и был основным средством, используемым при дезактивации зданий в Соединенных Штатах после Атаки сибирской язвы в 2001 году.[33] После катастрофы ураган Катрина в Жители Нового Орлеана, Луизиана, и окружающее побережье Мексиканского залива диоксид хлора использовался для уничтожения опасных плесень из домов, затопленных паводковой водой.[34]
В борьбе с пандемией COVID-19 Агентство по охране окружающей среды США опубликовал список многих дезинфицирующие средства которые соответствуют его критериям для использования в экологических мерах против причинной коронавирус.[35][36] Некоторые из них основаны на хлорит натрия который активируется в диоксид хлора, хотя в каждом продукте используются разные составы. Многие другие продукты из списка EPA содержат гипохлорит натрия, который похож по названию, но не следует путать с хлоритом натрия, потому что они имеют очень разные механизмы химического действия.
Другие виды дезинфекции
Двуокись хлора можно использовать в качестве фумиганта для «дезинфекции» фруктов, таких как черника, малина и клубника, которые развивают плесень и дрожжи.[37]
Двуокись хлора может использоваться для дезинфекции птицы путем распыления или погружения после убоя.[38]
Диоксид хлора можно использовать для дезинфекции эндоскопы, например, под торговой маркой Tristel.[39] Он также доступен в виде тройки, состоящей из предшествующей предварительной очистки с поверхностно-активное вещество и последующее полоскание деионизированная вода и антиоксидант низкого уровня.[40]
Диоксид хлора может использоваться для контроля зебра и мидии квагги в водозаборниках.[20]:4–34
Было показано, что диоксид хлора эффективен при постельный клоп искоренение.[41]
Псевдомедицина
Двуокись хлора обманным путем продается как волшебное лекарство от целого ряда заболеваний, от рака мозга до СПИДа. Клизмы диоксида хлора - предполагаемое лекарство от детства аутизм, в результате чего жалобы в FDA сообщение об опасных для жизни реакциях,[42] и даже смерть.[43]Диоксид хлора переименован в различные торговые марки, включая, помимо прочего, MMS, Miracle Mineral Solution и протокол CD.[44] Нет научных оснований для медицинских свойств диоксида хлора, и FDA предостерегло от его использования.[45][46]
Другое использование
Диоксид хлора используется в качестве окислителя для разрушения фенолы в Сточные Воды потоков и для контроля запаха в очистителях воздуха заводов по переработке побочных продуктов животного происхождения.[20]:4–34 Он также доступен для использования в качестве дезодоранта для автомобилей и лодок в упаковках, вырабатывающих диоксид хлора, которые активируются водой и оставляются в лодке или машине на ночь.
Вопросы безопасности при использовании воды и пищевых добавок
Диоксид хлора токсичен, поэтому необходимы ограничения на его воздействие, чтобы гарантировать его безопасное использование. В Агентство по охране окружающей среды США установил максимальный уровень диоксида хлора в питьевой воде 0,8 мг / л.[47] В Управление по охране труда (OSHA), агентство Министерство труда США, установил 8-часовой допустимый предел воздействия 0,1 частей на миллион в воздухе (0,3 мг /м3 ) для людей, работающих с диоксидом хлора.[48]
30 июля 2010 г. и 1 октября 2010 г. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США предостерегло от использования этого продукта "Чудо-минеральная добавка »или« MMS », который при приготовлении в соответствии с инструкциями производит диоксид хлора. MMS был продан как средство для лечения различных состояний, включая ВИЧ, рак и т. д. аутизм, и прыщи. Предупреждения FDA проинформировали потребителей о том, что MMS может нанести серьезный вред здоровью, и заявили, что были получены многочисленные сообщения о тошноте, диарее, сильной рвоте и опасном для жизни низком кровяном давлении, вызванном обезвоживанием.[49][50] Это предупреждение было повторено в третий раз 12 августа 2019 г. и четвертый раз 8 апреля 2020 г., в котором говорилось, что употребление MMS равносильно употреблению отбеливателя, и призывали потребителей не использовать их и не давать эти продукты своим детям ни по какой причине. .[46]
Рекомендации
- ^ Хейнс, Уильям М. (2010). Справочник по химии и физике (91 изд.). Бока-Ратон, Флорида, США: CRC Press. п. 4–58. ISBN 978-1-43982077-3.
- ^ а б c d Карманный справочник NIOSH по химической опасности. "#0116". Национальный институт охраны труда и здоровья (NIOSH).
- ^ Добсон, Стюарт; Кэри, Ричард; Международная программа химической безопасности (2002 г.). Диоксид хлора (газ). Всемирная организация здоровья. п. 4. Получено 17 августа 2020.
- ^ «Диоксид хлора». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ «Токсикологический профиль диоксида хлора и хлорита» (PDF). Агентство регистрации токсичных веществ и заболеваний, HHS США. Архивировано из оригинал (PDF) на 2019-06-14.
- ^ а б «Родители травят своих детей отбеливателем, чтобы« вылечить »аутизм. Эти мамы пытаются его остановить».. Новости NBC. Получено 2019-05-21.
- ^ «Фейковые новости: диоксид хлора не остановит коронавирус». Новости Детройта. Получено 2020-04-03.
- ^ Фридман, Лиза (2020-04-03). "E.P.A. угрожает судебным иском против продавцов поддельных средств для очистки от коронавируса". Нью-Йорк Таймс. ISSN 0362-4331. Получено 2020-04-03.
- ^ Спенсер, Сарнак Хейл. «Те« лекарства »от коронавируса, о которых вы слышите? Они подделки. Не пейте диоксид хлора». США СЕГОДНЯ. Получено 2020-04-03.
- ^ «Отбеливатель не вылечит рак или аутизм, - предупреждает FDA». Новости NBC. Получено 2019-08-13.
- ^ Управление по контролю за продуктами и лекарствами (2019-08-12). «FDA предупреждает потребителей об опасных и потенциально опасных для жизни побочных эффектах Miracle Mineral Solution». fda.gov. Архивировано из оригинал на 2019-08-14. Получено 2019-08-16.
- ^ а б c d е ж грамм час я Vogt, H .; Balej, J .; Bennett, J. E .; Wintzer, P .; Шейх, С. А .; Gallone, P .; Васудеван, S .; Пелин, К. "Оксиды хлора и кислородные кислоты хлора". Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH.
- ^ Броквей, Л. О. (март 1933 г.). "Трехэлектронная связь в диоксиде хлора" (PDF). Труды Национальной академии наук. 19 (3): 303–307. Bibcode:1933ПНАС ... 19..303Б. Дои:10.1073 / пнас.19.3.303. ЧВК 1085967. PMID 16577512.
- ^ Полинг, Линус (1988). Общая химия. Минеола, Нью-Йорк: Dover Publications. ISBN 0-486-65622-5.
- ^ Flesch, R .; Plenge, J .; Рюль, Э. (2006). «Возбуждение и фрагментация диоксида хлора на уровне ядра». Международный журнал масс-спектрометрии. 249-250: 68–76. Bibcode:2006IJMSp.249 ... 68F. Дои:10.1016 / j.ijms.2005.12.046.
- ^ Derby, R. I .; Хатчинсон, У. С. (1953). Оксид хлора (IV). Неорганические синтезы. 4. С. 152–158. Дои:10.1002 / 9780470132357.ch51. ISBN 978-0-470-13235-7.
- ^ Ni, Y .; Ван, X. (1996). «Механизм процесса образования ClO2 на основе метанола». Международная конференция по отбеливанию целлюлозы. ТАППИ. С. 454–462.[постоянная мертвая ссылка ]
- ^ а б Уайт, Джордж В .; Уайт, Гео Клиффорд (1999). Справочник по хлорированию и альтернативным дезинфицирующим средствам (4-е изд.). Нью-Йорк: Джон Вили. ISBN 0-471-29207-9.
- ^ Swaddle, Томас Уилсон (1997). Неорганическая химия: промышленная и экологическая перспектива. Академическая пресса. стр.198 –199. ISBN 0-12-678550-3.
- ^ а б c d е ж грамм час Руководство по альтернативным дезинфицирующим средствам и окислителям, глава 4: Диоксид хлора (PDF), Агентство по охране окружающей среды США: Управление водных ресурсов, апрель 1999 г., архивировано с оригинала 5 сентября 2015 г., получено 2009-11-27CS1 maint: неподходящий URL (связь)
- ^ а б c d Блок, Сеймур Стэнтон (2001). Дезинфекция, стерилизация и консервация (5-е изд.). Липпинкотт, Уильямс и Уилкинс. п. 215. ISBN 0-683-30740-1.
- ^ Sjöström, E. (1993). Химия древесины: основы и приложения. Академическая пресса. ISBN 0-12-647480-X. OCLC 58509724.
- ^ «AET - Отчеты - Наука - Тенденции в мировом производстве беленой химической целлюлозы: 1990–2005 гг.». Архивировано из оригинал на 2017-07-30. Получено 2016-02-26.
- ^ Харрел, К. Г. (1952). «Созревающие и отбеливающие агенты в производстве муки». Промышленная и инженерная химия. 44 (1): 95–100. Дои:10.1021 / ie50505a030.
- ^ Сорлини, S .; Колливигнарелли, К. (2005). «Образование тригалометана при химическом окислении хлором, диоксидом хлора и озоном десяти итальянских природных вод». Опреснение. 176 (1–3): 103–111. Дои:10.1016 / j.desal.2004.10.022.
- ^ Li, J .; Ю, З .; Гао, М. (1996). «Пилотное исследование образования тригалометана в воде, обработанной диоксидом хлора». Чжунхуа Юйфан Исюэ Зачжи (Китайский журнал профилактической медицины) (на китайском языке). 30 (1): 10–13. PMID 8758861.
- ^ а б c Volk, C.J .; Hofmann, R .; Chauret, C .; Gagnon, G.A .; Рейнджер, G .; Эндрюс, Р. К. (2002). «Осуществление дезинфекции диоксидом хлора: Влияние изменения режима обработки на качество питьевой воды в полномасштабной системе распределения». Журнал экологической инженерии и науки. 1 (5): 323–330. Дои:10.1139 / s02-026.
- ^ Перейра, М. А .; Lin, L.H .; Lippitt, J.M .; Херрен, С. Л. (1982). «Тригалометаны как инициаторы и промоторы канцерогенеза». Перспективы гигиены окружающей среды. 46: 151–156. Дои:10.2307/3429432. JSTOR 3429432. ЧВК 1569022. PMID 7151756.
- ^ Andrews, L .; Ключ, А .; Martin, R .; Гроднер, Р .; Парк, Д. (2002). «Промывка креветок и раков диоксидом хлора - альтернатива водному хлору». Пищевая микробиология. 19 (4): 261–267. Дои:10.1006 / fmic.2002.0493.
- ^ Чжан, Чжэ; Макканн, Кэрол; Стаут, Джанет Э .; Пещинский, Стив; Ястребы, Роберт; Видич, Радисав; Ю., Виктор Л. (2007). «Безопасность и эффективность диоксида хлора для Легионелла контроль в больничной системе водоснабжения » (PDF). Инфекционный контроль и больничная эпидемиология. 28 (8): 1009–1012. Дои:10.1086/518847. PMID 17620253. Получено 2009-11-27.
- ^ Огата, Н .; Шибата, Т. (январь 2008 г.). «Защитный эффект газообразного диоксида хлора низкой концентрации против заражения вирусом гриппа А». Журнал общей вирусологии. 89 (пт 1): 60–67. Дои:10.1099 / vir.0.83393-0. PMID 18089729.
- ^ Zhang, Y.-L .; Zheng, S.-Y .; Чжи, К. (2007). «Обеззараживание воздуха диоксидом хлора в соках». Журнал окружающей среды и здоровья. 24 (4): 245–246.
- ^ «Обеззараживание спор сибирской язвы диоксидом хлора». Агентство по охране окружающей среды США. 2007 г.. Получено 2009-11-27.
- ^ Sy, Kaye V .; McWatters, Kay H .; Beuchat, Ларри Р. (2005). «Эффективность газообразного диоксида хлора в качестве дезинфицирующего средства для уничтожения сальмонеллы, дрожжей и плесени на чернике, клубнике и малине». Журнал защиты пищевых продуктов. Международная ассоциация защиты пищевых продуктов. 68 (6): 1165–1175. Дои:10.4315 / 0362-028x-68.6.1165. PMID 15954703.
- ^ «Откуда мы знаем, что дезинфицирующие средства должны убить коронавирус COVID-19». Новости химии и машиностроения. Получено 2020-03-28.
- ^ Агентство по охране окружающей среды США, OCSPP (13 марта 2020 г.). «Список N: дезинфицирующие средства для использования против SARS-CoV-2». Агентство по охране окружающей среды США. Получено 2020-03-28.
- ^ О'Брайан, Д. (2017). «Пакеты с диоксидом хлора могут сделать продукцию более безопасной и уменьшить порчу». Журнал AgResearch. Служба сельскохозяйственных исследований Министерства сельского хозяйства США (июль). Получено 2018-06-21.
- ^ "Правда о панике по поводу хлорированной курицы". Большой вопрос. 2019-05-29. Получено 2020-02-05.
- ^ Коутс, Д. (2001). «Оценка использования диоксида хлора (Tristel One-Shot) в автоматической моечной машине / дезинфекторе (Medivator), оснащенной генератором диоксида хлора для обеззараживания гибких эндоскопов». Журнал госпитальной инфекции. 48 (1): 55–65. Дои:10.1053 / jhin.2001.0956. PMID 11358471.
- ^ «Информация о продукте системы салфеток Tristel Wipes» (PDF). Этические агенты. Архивировано из оригинал (PDF) на 2016-04-15. Получено 2012-11-01.
- ^ Gibbs, S.G .; Lowe, J. J .; Smith, P.W .; Хьюлетт, А. Л. (2012). «Газообразный диоксид хлора как альтернатива борьбе с клопами». Инфекционный контроль и больничная эпидемиология. 33 (5): 495–9. Дои:10.1086/665320. PMID 22476276. S2CID 14105046.
- ^ Бартли, Лиза (2016-10-29). «Группа родителей SoCal тайно пытается вылечить детей с аутизмом с помощью отбеливателя». ABC 7 Новости. ABC. Получено 2019-03-24.
- ^ Райан, Фрэнсис (13.07.2016). «Фальшивые лекарства от аутизма, которые могут оказаться смертельными». Хранитель. Guardian Media Group. Получено 2019-03-24.
- ^ «Родители, которые дают своим детям отбеливать клизмы, чтобы« вылечить »их от аутизма». Vice.com. 2015-03-12. Получено 2018-04-05.
- ^ «FDA предупреждает потребителей о серьезном вреде от употребления чудо-минерального раствора (MMS)». 2011-02-03. Архивировано из оригинал на 2011-02-03. Получено 2018-04-05.
- ^ а б Управление по контролю за продуктами и лекарствами (2019-08-12). «FDA предупреждает потребителей об опасных и потенциально опасных для жизни побочных эффектах Miracle Mineral Solution». fda.gov. Архивировано из оригинал на 2019-08-14. Получено 2019-08-16.
- ^ «ATSDR: ToxFAQs ™ для диоксида хлора и хлорита».
- ^ «Руководство по безопасности и гигиене труда для диоксида хлора». Архивировано из оригинал на 2012-12-04. Получено 2012-12-08.
- ^ «Сообщения для прессы - FDA предупреждает потребителей о серьезном вреде от употребления чудо-минерального раствора (MMS)». Архивировано из оригинал на 2017-01-12.
- ^ "'Лечение Miracle превращается в мощный отбеливатель ». Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. 2015-11-20. В архиве из оригинала на 2017-11-01. Получено 2017-12-06.
внешняя ссылка
 СМИ, связанные с Диоксид хлора в Wikimedia Commons
СМИ, связанные с Диоксид хлора в Wikimedia Commons



