Торий - Thorium
 | |||||||||||||||||||||||||||||||||||||||||
| Торий | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение | /ˈθɔːrяəм/ | ||||||||||||||||||||||||||||||||||||||||
| Внешность | серебристый, часто с черным налетом | ||||||||||||||||||||||||||||||||||||||||
| Стандартный атомный вес Аг, стд(Чт) | 232.0377(4)[1] | ||||||||||||||||||||||||||||||||||||||||
| Торий в периодическая таблица | |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| Атомный номер (Z) | 90 | ||||||||||||||||||||||||||||||||||||||||
| Группа | группа н / д | ||||||||||||||||||||||||||||||||||||||||
| Период | период 7 | ||||||||||||||||||||||||||||||||||||||||
| Блокировать | f-блок | ||||||||||||||||||||||||||||||||||||||||
| Категория элемента | Актинид | ||||||||||||||||||||||||||||||||||||||||
| Электронная конфигурация | [Rn ] 6d2 7 с2 | ||||||||||||||||||||||||||||||||||||||||
| Электронов на оболочку | 2, 8, 18, 32, 18, 10, 2 | ||||||||||||||||||||||||||||||||||||||||
| Физические свойства | |||||||||||||||||||||||||||||||||||||||||
| Фаза вSTP | твердый | ||||||||||||||||||||||||||||||||||||||||
| Температура плавления | 2023 K (1750 ° С, 3182 ° F) | ||||||||||||||||||||||||||||||||||||||||
| Точка кипения | 5061 К (4788 ° С, 8650 ° F) | ||||||||||||||||||||||||||||||||||||||||
| Плотность (возлеr.t.) | 11,7 г / см3 | ||||||||||||||||||||||||||||||||||||||||
| Теплота плавления | 13.81 кДж / моль | ||||||||||||||||||||||||||||||||||||||||
| Теплота испарения | 514 кДж / моль | ||||||||||||||||||||||||||||||||||||||||
| Молярная теплоемкость | 26,230 Дж / (моль · К) | ||||||||||||||||||||||||||||||||||||||||
Давление газа
| |||||||||||||||||||||||||||||||||||||||||
| Атомные свойства | |||||||||||||||||||||||||||||||||||||||||
| Состояния окисления | +1, +2, +3, +4 (слабо базовый окись) | ||||||||||||||||||||||||||||||||||||||||
| Электроотрицательность | Шкала Полинга: 1,3 | ||||||||||||||||||||||||||||||||||||||||
| Энергии ионизации |
| ||||||||||||||||||||||||||||||||||||||||
| Радиус атома | эмпирический: 179,8вечера | ||||||||||||||||||||||||||||||||||||||||
| Ковалентный радиус | 206 ± 18 часов | ||||||||||||||||||||||||||||||||||||||||
| Другие свойства | |||||||||||||||||||||||||||||||||||||||||
| Естественное явление | изначальный | ||||||||||||||||||||||||||||||||||||||||
| Кристальная структура | гранецентрированная кубическая (fcc) | ||||||||||||||||||||||||||||||||||||||||
| Скорость звука тонкий стержень | 2490 м / с (при 20 ° C) | ||||||||||||||||||||||||||||||||||||||||
| Тепловое расширение | 11,0 мкм / (м · К) (при 25 ° C) | ||||||||||||||||||||||||||||||||||||||||
| Теплопроводность | 54,0 Вт / (м · К) | ||||||||||||||||||||||||||||||||||||||||
| Удельное электрическое сопротивление | 157 нОм · м (при 0 ° C) | ||||||||||||||||||||||||||||||||||||||||
| Магнитный заказ | парамагнитный[2] | ||||||||||||||||||||||||||||||||||||||||
| Магнитная восприимчивость | 132.0·10−6 см3/ моль (293 К)[3] | ||||||||||||||||||||||||||||||||||||||||
| Модуль для младших | 79 ГПа | ||||||||||||||||||||||||||||||||||||||||
| Модуль сдвига | 31 ГПа | ||||||||||||||||||||||||||||||||||||||||
| Объемный модуль | 54 ГПа | ||||||||||||||||||||||||||||||||||||||||
| коэффициент Пуассона | 0.27 | ||||||||||||||||||||||||||||||||||||||||
| Твердость по Моосу | 3.0 | ||||||||||||||||||||||||||||||||||||||||
| Твердость по Виккерсу | 295–685 МПа | ||||||||||||||||||||||||||||||||||||||||
| Твердость по Бринеллю | 390–1500 МПа | ||||||||||||||||||||||||||||||||||||||||
| Количество CAS | 7440-29-1 | ||||||||||||||||||||||||||||||||||||||||
| История | |||||||||||||||||||||||||||||||||||||||||
| Именование | после Тор, норвежский бог грома | ||||||||||||||||||||||||||||||||||||||||
| Открытие | Йенс Якоб Берцелиус (1829) | ||||||||||||||||||||||||||||||||||||||||
| Главный изотопы тория | |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
Торий слабо радиоактивный металлический химический элемент с символ Чт и атомный номер 90. Торий серебристый и тускнеет черный при контакте с воздухом, образуя диоксид тория; это умеренно сложно, податливый, и имеет высокий температура плавления. Торий - электроположительный актинид в химии которого преобладает +4 степень окисления; он довольно реактивен и может воспламеняться на воздухе при мелком измельчении.
Всем известный торий изотопы нестабильны. Самый стабильный изотоп, 232Че, есть период полураспада 14,05 миллиарда лет, или около возраст вселенной; он очень медленно распадается через альфа-распад, начиная с цепочка распада назвал ториевый ряд что заканчивается стабильным 208Pb. На Земле торий, висмут, и уран являются единственными тремя радиоактивными элементами, которые все еще встречаются в природе в больших количествах, поскольку первоэлементы.[а] По оценкам, это более чем в три раза больше, чем обильный как уран в земной коре, и в основном очищается от монацит пески как побочный продукт добычи редкоземельные металлы.
Торий был открыт в 1828 году норвежским минералогом-любителем. Мортен Трейн Эсмарк и идентифицирован шведским химиком Йенс Якоб Берцелиус, который назвал его в честь Тор, то Скандинавский бог грома. Первые его приложения были разработаны в конце 19 века. Радиоактивность тория была широко известна в первые десятилетия 20-го века. Во второй половине века торий был заменен во многих случаях из-за опасений по поводу его радиоактивности.
Торий до сих пор используется в качестве легирующего элемента в Сварка TIG электроды, но в полевых условиях постепенно заменяется на другой состав. Он также использовался в высококачественной оптике и научных приборах, использовался в некоторых радиолампах, а также в качестве источника света в газовые мантии, но это использование стало маргинальным. Он был предложен в качестве замены урана в качестве ядерного топлива в ядерные реакторы, и несколько ториевые реакторы были построены. Торий также используется для усиления магний, покрытие вольфрам проволока в электрооборудовании, контролирующая размер зерна вольфрама в электрические лампы, высокотемпературные тигли, в очках и используемые в линзах фотоаппаратов и научных приборов. Другие применения тория включают термостойкую керамику, авиационные двигатели, И в лампочки.
Объемные свойства
Торий умеренно мягкий, парамагнитный, яркий серебристый радиоактивный металл-актинид. в периодическая таблица, он находится справа от актиний, слева от протактиний, и ниже церий. Чистый торий очень пластичный и, как обычно для металлов, может быть холоднокатаные, обжатый, и нарисованный.[4] При комнатной температуре металлический торий имеет гранецентрированная кубическая Кристальная структура; у него есть две другие формы: одна при высокой температуре (более 1360 ° C; объемно-центрированная кубическая) и одна при высоком давлении (около 100 ГПа; Телоцентрированный тетрагональный ).[4]
Металлический торий имеет объемный модуль (мера сопротивления сжатию материала) 54ГПа, примерно так же, как банка (58,2 ГПа). Алюминий составляет 75,2 ГПа; по меди - 137,8 ГПа; для мягкой стали - 160–169 ГПа.[5] Торий примерно такой же твердый, как и мягкий стали, поэтому при нагревании его можно свернуть в листы и затянуть в проволоку.[6]
Торий почти вдвое меньше, чем уран и плутоний и сложнее обоих.[6] Это становится сверхпроводящий ниже 1,4K.[4] Тория температура плавления 1750 ° C выше, чем у актиния (1227 ° C) и протактиния (1568 ° C). В начале период 7, из франций Для тория точки плавления элементов увеличиваются (как и в другие периоды), потому что количество делокализованных электронов, вносимых каждым атомом, увеличивается с одного во франции до четырех в тории, что приводит к большему притяжению между этими электронами и ионами металла в качестве их заряда. увеличивается с одного до четырех. После тория наблюдается новая тенденция к понижению температуры плавления от тория до плутоний, где количество f-электронов увеличивается примерно с 0,4 до примерно 6: эта тенденция связана с растущей гибридизацией 5f- и 6d-орбиталей и образованием направленных связей, приводящих к более сложным кристаллическим структурам и ослаблению металлических связей.[6][7] (Счетчик f-электронов для металлического тория не является целым числом из-за перекрытия 5f – 6d.)[7] Среди актинидов до калифорний, который можно изучать в количествах, по крайней мере, миллиграммах, торий имеет самые высокие температуры плавления и кипения и второй по плотности; только актиний светлее.[b] Температура кипения тория 4788 ° C является пятой по величине среди всех элементов с известными температурами кипения.[c]
Свойства тория широко варьируются в зависимости от степени примесей в образце. Основная примесь обычно диоксид тория (ThO2); даже самые чистые образцы тория обычно содержат около десятой доли процента диоксида.[4] Экспериментальные измерения его плотности дают значения от 11,5 до 11,66 г / см.3: это немного ниже теоретически ожидаемого значения 11,7 г / см3 рассчитывается из тория параметры решетки возможно из-за микроскопических пустот, образующихся в металле при литье.[4] Эти значения лежат между значениями его соседнего актиния (10,1 г / см3) и протактиний (15,4 г / см3), часть тренда ранних актинидов.[4]
Торий может образовывать сплавы со многими другими металлами. Добавление небольшого количества тория улучшает механическую прочность магний, и торий-алюминиевые сплавы рассматривались как способ хранения тория в предполагаемых будущих ториевых ядерных реакторах. Формы тория эвтектические смеси с хром и уран, и это полностью смешивающийся как в твердом, так и в жидком состоянии состояния с зажигалкой конгенер церий.[4]
Изотопы
Все элементы, кроме двух, до висмут (элемент 83) имеет изотоп, который практически стабилен для всех целей («классически стабильный»), за исключением технеций и прометий (элементы 43 и 61). Все элементы из полоний (элемент 84) и далее радиоактивный. 232Это один из трех нуклидов за пределами висмута (два других 235U и 238U ) с периодом полураспада, измеряемым миллиардами лет; его период полураспада составляет 14,05 миллиарда лет, что примерно в три раза больше возраст земли, и немного длиннее, чем возраст вселенной. Четыре пятых тория, присутствующего при формировании Земли, сохранились до наших дней.[10][11][12] 232Th - единственный изотоп тория, встречающийся в природе в больших количествах.[10] Его стабильность объясняется закрытым ядерная подоболочка со 142 нейтронами.[13][14] Торий имеет характерный земной изотопный состав, с атомный вес 232.0377 (4). Это один из четырех радиоактивных элементов (наряду с висмутом, протактинием и ураном), которые встречаются на Земле в достаточно больших количествах, чтобы можно было определить стандартный атомный вес.[1]
Ядра тория восприимчивы к альфа-распад потому что сильное ядерное взаимодействие не может преодолеть электромагнитное отталкивание между их протонами.[15] Альфа-распад 232Th инициирует 4п цепочка распада который включает изотопы с массовое число делится на 4 (отсюда и название; его еще называют ториевым рядом по имени его прародителя). Эта цепочка последовательных альфа и бета-распад начинается с распада 232Че к 228Ra и оканчивается на 208Pb.[10] Любой образец тория или его соединений содержит следы этих дочерей, которые являются изотопами таллий, вести, висмут, полоний, радон, радий, и актиний.[10] Образцы природного тория можно химически очистить для извлечения полезных дочерних нуклидов, таких как 212Pb, который используется в ядерная медицина за лечение рака.[16][17] 227Th (альфа-излучатель с периодом полураспада 18,68 дней) также может использоваться при лечении рака, например целевые альфа-терапии.[18][19][20] 232Че тоже очень изредка подвергается спонтанное деление а не альфа-распад, и оставил доказательства этого в своих минералах (как захваченных ксенон газ, образовавшийся как продукт деления), но частичный период полураспада этого процесса очень велико более 1021 лет и преобладает альфа-распад.[21][22]

30 радиоизотопы охарактеризованы, массовое число которых колеблется от 209[23] к 238.[21] После 232Наиболее стабильными из них (с соответствующими периодами полураспада) являются 230Th (75380 лет), 229Th (7340 лет), 228Th (1,92 года), 234Чт (24.10 дней), и 227Чт (18,68 суток). Все эти изотопы встречаются в природе в виде следовые радиоизотопы из-за их присутствия в цепочках распада 232Чт, 235U, 238U и 237Np: последний из них длинный вымерший в природе из-за его короткого периода полураспада (2,14 миллиона лет), но постоянно производится в мельчайших следах из захват нейтронов в урановых рудах. Все остальные изотопы тория имеют период полураспада менее тридцати дней, а у большинства из них период полураспада менее десяти минут.[10]
В глубине морская вода изотоп 230Th составляет до 0,04% природного тория.[1] Это потому, что его родитель 238U растворим в воде, но 230Th нерастворим и выпадает в осадок. Урановые руды с низким содержанием тория могут быть очищены для получения образцов тория размером в грамм, из которых более четверти составляет 230Изотоп Th, поскольку 230Это одна из дочерей 238U.[21] В Международный союз теоретической и прикладной химии (IUPAC) реклассифицировал торий как бинуклидный элемент в 2013 году; раньше это считалось мононуклидный элемент.[1]
Торий имеет три известных ядерные изомеры (или метастабильные состояния), 216м1Чт, 216м2Че, и 229 кв.м.Чт. 229 кв.м.Th имеет самую низкую известную энергию возбуждения из всех изомеров,[24] измеряется, чтобы быть 7.6±0,5 эВ. Это настолько мало, что когда он подвергается изомерный переход, излучаемое гамма-излучение находится в ультрафиолетовый классифицировать.[25][26][d]
Различные изотопы тория химически идентичны, но имеют немного разные физические свойства: например, плотности чистого 228Чт, 229Чт, 230Че, и 232Ожидается, что Th соответственно составит 11,5, 11,6, 11,6 и 11,7 г / см3.3.[28] Изотоп 229Ожидается, что это будет расщепляющийся с голым критическая масса 2839 кг, хотя и со сталью отражатели это значение могло упасть до 994 кг.[28][e] 232Не расщепляется, но это плодородный поскольку он может быть преобразован в делящийся 233U захватом нейтронов и последующим бета-распадом.[28][29]
Радиометрическое датирование
Два метода радиометрического датирования включают изотопы тория: уран-ториевое датирование, основанный на распаде 234U к 230Че, и ионий-ториевое датирование, который измеряет отношение 232Че к 230Чт.[f] Они полагаются на тот факт, что 232Это изначальный радиоизотоп, но 230Th встречается только как промежуточный продукт распада в цепочке распада 238U.[30] Уран-ториевое датирование - это относительно короткий процесс из-за коротких периодов полураспада 234U и 230Относительно возраста Земли: он также сопровождается сестринским процессом, включающим альфа-распад 235U в 231Th, который очень быстро становится долгоживущим 231Па, и этот процесс часто используется для проверки результатов уран-ториевого датирования. Уран-ториевое датирование обычно используется для определения возраста карбонат кальция материалы, такие как образование или же коралл, потому что уран более растворим в воде, чем торий и протактиний, которые выборочно осаждаются на дно океана. отложения, где измеряются их отношения. Схема имеет диапазон в несколько сотен тысяч лет.[30][31] Ионий-ториевое датирование - это связанный процесс, в котором используется нерастворимость тория (как 232Че и 230Th) и, таким образом, его присутствие в океанических отложениях позволяет датировать эти отложения путем измерения отношения 232Че к 230Чт.[32][33] Оба этих метода датирования предполагают, что доля 230Че к 232Th является константой в течение периода, когда образовался слой осадка, что осадок еще не содержал торий до внесения вкладов от распада урана и что торий не может мигрировать внутри слоя отложений.[32][33]
Химия
В атоме тория 90 электронов, четыре из которых являются валентные электроны. Три атомные орбитали теоретически доступны для размещения валентных электронов: 5f, 6d и 7s.[34] Несмотря на положение тория в f-блок периодической таблицы, он имеет аномальный [Rn] 6d27 с2 электронная конфигурация в основном состоянии, поскольку подоболочки 5f и 6d в ранних актинидах очень близки по энергии, даже больше, чем подоболочки 4f и 5d лантаноидов: подоболочки 6d тория по энергии ниже, чем его подоболочки 5f, потому что его Подоболочки 5f плохо экранируются заполненными подоболочками 6s и 6p и дестабилизированы. Это связано с релятивистские эффекты, которые усиливаются у основания периодической таблицы, в частности релятивистские спин-орбитальное взаимодействие. Близость энергетических уровней 5f, 6d и 7s энергетических уровней тория приводит к тому, что торий почти всегда теряет все четыре валентных электрона и находится в своей наивысшей степени окисления +4. Это отличается от своего лантаноида, родственного церию, в котором +4 также является наивысшим возможным состоянием, но +3 играет важную роль и является более стабильным. Торий гораздо больше похож на переходные металлы цирконию и гафнию, чем церию, по его энергии ионизации и окислительно-восстановительному потенциалу, а, следовательно, и по его химическому составу: подобное поведение, подобное переходному металлу, является нормой для первой половины ряда актинидов.[35][36]

Несмотря на аномальную электронную конфигурацию для газообразных атомов тория, металлический торий показывает значительное участие 5f. Гипотетическое металлическое состояние тория с [Rn] 6d27 с2 конфигурация с орбиталями 5f над Уровень Ферми должно быть гексагональный плотно упакованный словно группа 4 элемента титан, цирконий и гафний, а не гранецентрированный кубик, как на самом деле. Настоящая кристаллическая структура может быть объяснена только тогда, когда задействованы состояния 5f, доказывающие, что торий, а не протактиний, в металлургическом отношении действует как первый актинид.[7]
Соединения четырехвалентного тория обычно бесцветные или желтые, как и соединения серебро или вести, как че4+ ион не имеет 5f или 6d электронов.[6] Таким образом, химия тория в основном связана с электроположительным металлом, образующим единый диамагнитный ион со стабильной конфигурацией благородного газа, что указывает на сходство между торием и элементы основной группы s-блока.[37][грамм] Торий и уран являются наиболее изученными радиоактивными элементами, поскольку их радиоактивность достаточно мала, чтобы не требовать специального обращения в лаборатории.[38]
Реактивность
Торий очень реактивный и электроположительный металл. С стандартный восстановительный потенциал −1,90 В для Th4+/ Th пара, она несколько более электроположительна, чем цирконий или алюминий.[39] Мелкодисперсный металлический торий может проявлять пирофорность, самовозгорающиеся на воздухе.[4] При нагревании на воздухе торий повороты зажечь и гореть ярким белым светом, чтобы произвести диоксид. В массе реакция чистого тория с воздухом протекает медленно, хотя коррозия может возникнуть через несколько месяцев; большинство образцов тория загрязнены диоксидом различной степени, что значительно ускоряет коррозию.[4] Такие образцы медленно тускнеют, становятся серыми и, наконец, черными на поверхности.[4]
В стандартная температура и давление, торий медленно разрушается водой, но не растворяется в большинстве распространенных кислот, за исключением соляная кислота, где он растворяется, оставляя черный нерастворимый остаток ThO (OH, Cl) H.[4][40] Растворяется в концентрированных азотная кислота содержащие небольшое количество каталитического фторид или же фторсиликат ионы;[4][41] если их нет, пассивация нитратом может происходить, как с ураном и плутонием.[4][42][43]

Чт4+: __ / F−: __
Неорганические соединения
Большинство бинарных соединений тория с неметаллами можно получить путем совместного нагревания элементов.[44] На воздухе торий горит с образованием ThO2, который имеет флюорит структура.[45] Диоксид тория - это огнеупорный материал, с самой высокой температурой плавления (3390 ° C) любого известного оксида.[46] Это несколько гигроскопичный легко реагирует с водой и многими газами;[47] легко растворяется в концентрированной азотной кислоте в присутствии фторида.[48]
При нагревании на воздухе диоксид тория излучает интенсивный синий свет; свет становится белым, когда ThO2 смешан со своим более легким гомологом диоксид церия (Исполнительный директор2, церия): это основа для его ранее распространенного применения в газовые мантии.[47] Для этого эффекта пламя не требуется: в 1901 году было обнаружено, что горячая газовая мантия Вельсбаха (с использованием ThO2 с 1% CeO2) оставался в состоянии «полного накала» при воздействии холодной негорючей смеси горючего газа и воздуха.[49] Свет, излучаемый диоксидом тория, имеет более высокую длину волны, чем свет черное тело выброс ожидается от накал при той же температуре эффект, называемый свечение. Это происходит потому, что ThO2 : Ce действует как катализатор рекомбинации свободные радикалы которые появляются в высокой концентрации в пламени, при снятии возбуждения выделяется большое количество энергии. Добавление 1% диоксида церия, как в газовых оболочках, усиливает эффект за счет увеличения излучательной способности в видимой области спектра; и поскольку церий, в отличие от тория, может находиться в нескольких состояниях окисления, его заряд и, следовательно, видимая излучательная способность будут зависеть от области пламени, в которой он находится (поскольку такие области различаются по своему химическому составу и, следовательно, насколько они окисляющие или восстанавливающие) .[49]
Несколько бинарных тория халькогениды и оксихалькогениды также известны с сера, селен, и теллур.[50]
Известны все четыре тетрагалогенида тория, а также некоторые низковалентные бромиды и йодиды:[51] все тетрагалогениды представляют собой гигроскопичные соединения с 8 координациями, которые легко растворяются в полярных растворителях, таких как вода.[52] Также известны многие родственные полигалогенид-ионы.[51] Тетрафторид тория имеет моноклинический кристаллическая структура как у тетрафторид циркония и тетрафторид гафния, где Th4+ ионы координированы с F− ионы в несколько искаженном квадратные антипризмы.[51] Вместо этого другие тетрагалогениды имеют додекаэдрическую геометрию.[52] Низшие йодиды ThI3 (черный) и ThI2 (окрашенные в золото) также могут быть получены восстановлением тетраиодида металлическим торием: они не содержат Th (III) и Th (II), но вместо этого содержат Th4+ и можно было бы более четко сформулировать как электрид соединения.[51] Многие полинарные галогениды с щелочными металлами, барий, таллий и аммоний известны как фториды, хлориды и бромиды тория.[51] Например, при лечении фторид калия и плавиковая кислота, Чт4+ образует сложный анион ThF2−
6, который выпадает в осадок в виде нерастворимой соли, K2ThF6.[41]
Бориды, карбиды, силициды и нитриды тория являются тугоплавкими материалами, такими же как уран и плутоний, и поэтому привлекают внимание как возможные ядерное топливо.[44] Все четыре тяжелее пниктогены (фосфор, мышьяк, сурьма, и висмут) также образуют бинарные соединения тория. Известны также германиды тория.[53] Торий реагирует с водородом с образованием гидридов тория ThH.2 и Чт4ЧАС15, последний из которых является сверхпроводящим ниже 7,5–8 К; при стандартной температуре и давлении он проводит электричество как металл.[54] Гидриды термически нестабильны и легко разлагаются под воздействием воздуха или влаги.[55]
Координационные соединения
В кислом водном растворе торий встречается как тетраположительный акваион [Чт (H2O)9]4+, у которого есть треугольная призматическая геометрия молекул:[56][57] при pH <3 в растворах солей тория преобладает этот катион.[56] Че4+ ион является самым большим из тетраположительных ионов актинида и в зависимости от координационного числа может иметь радиус от 0,95 до 1,14 Å.[56] Он довольно кислый из-за высокого заряда, чуть сильнее, чем сернистая кислота: таким образом, он имеет тенденцию к гидролизу и полимеризации (хотя и в меньшей степени, чем Fe3+ ), преимущественно до [Th2(ОЙ)2]6+ в растворах с pH 3 или ниже, но в более щелочных растворах полимеризация продолжается до тех пор, пока гелеобразный гидроксид Th (OH)4 образуется и выпадает в осадок (хотя для достижения равновесия могут потребоваться недели, поскольку полимеризация обычно замедляется перед осаждением).[58] Как твердая кислота Льюиса, Чт4+ отдает предпочтение жестким лигандам с атомами кислорода в качестве доноров: комплексы с атомами серы в качестве доноров менее стабильны и более склонны к гидролизу.[35]
Высокие координационные числа являются нормой для тория из-за его большого размера. Пентагидрат нитрата тория был первым известным примером координационного числа 11, тетрагидрат оксалата имеет координационное число 10, а борогидрид (впервые получен в Манхэттенский проект ) имеет координационный номер 14.[58] Эти соли тория известны своей высокой растворимостью в воде и полярных органических растворителях.[6]
Известны многие другие неорганические соединения тория с многоатомными анионами, такие как перхлораты, сульфаты, сульфиты, нитраты, карбонаты, фосфаты, ванадаты, молибдаты, и хроматы, и их гидратированные формы.[59] Они важны для очистки тория и удаления ядерных отходов, но большинство из них еще не полностью охарактеризовано, особенно в отношении их структурных свойств.[59] Например, нитрат тория образуется при реакции гидроксида тория с азотной кислотой: он растворим в воде и спиртах и является важным промежуточным продуктом при очистке тория и его соединений.[59] Комплексы тория с органическими лигандами, такими как оксалат, цитрат, и EDTA, намного стабильнее. В природных водах, содержащих торий, органические комплексы тория обычно встречаются в концентрациях на порядки выше, чем неорганические комплексы, даже когда концентрации неорганических лигандов намного выше, чем концентрации органических лигандов.[56]

Ториорганические соединения
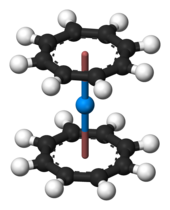
Большая часть работ по ортоорганическим соединениям была сосредоточена на циклопентадиенильные комплексы и циклооктатетраенилы. Как и многие из ранних и средних актинидов (до америций, а также ожидается для кюрий ), торий образует циклооктатетраенидный комплекс: желтый Th (C8ЧАС8)2, тороцен. это изотипический с более известным аналогичным соединением урана ураноцен.[60] Его можно приготовить, реагируя K2C8ЧАС8 с тетрахлоридом тория в тетрагидрофуран (THF) при температуре сухой лед, или реакцией тетрафторида тория с MgC8ЧАС8.[60] Неустойчив на воздухе, разлагается в воде или при 190 ° C.[60] Полусэндвич-компаунды также известны, например, (η8-C8ЧАС8) ThCl2(THF)2, который имеет структуру стула рояля и образуется в результате реакции торицена с тетрахлоридом тория в тетрагидрофуране.[35]
Самыми простыми из циклопентадиенилов являются Th (C5ЧАС5)3 и Th (C5ЧАС5)4: известно много производных. Первый (имеющий две формы: пурпурную и зеленую) является редким примером тория в формальной степени окисления +3;[60][61] формальная степень окисления +2 встречается в производной.[62] Хлоридное производное [Th (C5ЧАС5)3Cl] получают нагреванием тетрахлорида тория с ограничение К (С5ЧАС5) (также можно использовать циклопентадиенилы других одновалентных металлов). В алкил и арил производные получают из хлоридного производного и были использованы для изучения природы Th – C сигма-облигация.[61]
Другие ториорганические соединения изучены недостаточно. Тетрабензилторий, Th (CH2C6ЧАС5) и тетрааллилторий Th (C3ЧАС5)4, известны, но их структура не определена. Они медленно разлагаются при комнатной температуре. Торий образует монокапочный тригонально-призматический анион [Th (CH3)7]3−, гептаметилторат, который образует соль [Li (tmeda)]3[ThMe7] (tmeda = Я2NCH2CH2NMe2). Хотя одна метильная группа присоединена только к атому тория (расстояние Th – C 257,1 пм), а остальные шесть соединяют атомы лития и тория (расстояния Th – C 265,5–276,5 пм), они ведут себя в растворе одинаково. Тетраметилторий, Th (CH3)4, не известно, но его аддукты стабилизируются фосфин лиганды.[35]
Вхождение
Формирование
232Это первичный нуклид, существующий в нынешнем виде более десяти миллиардов лет; он был выкован в ядрах умирающих звезд через r-процесс и разбросаны по галактике сверхновые и нейтронные звезды слияния.[63][64] Буква «r» означает «быстрый захват нейтронов» и встречается в сверхновых с коллапсом ядра, где тяжелые зародышевые ядра, такие как 56Fe быстро захватывают нейтроны, наталкиваясь на капельная линия нейтронов, поскольку нейтроны захватываются намного быстрее, чем образующиеся нуклиды могут бета-распадом вернуться к стабильности. Захват нейтронов - единственный способ для звезд синтезировать элементы помимо железа из-за повышенной Кулоновские барьеры которые затрудняют взаимодействие между заряженными частицами при высоких атомных номерах, а также тот факт, что синтез за пределами 56Fe эндотермический.[65] Из-за резкой потери устойчивости прошлого 209Bi, r-процесс - единственный процесс звездного нуклеосинтеза, который может создавать торий и уран; все другие процессы слишком медленны, и промежуточные ядра альфа-распада не успевают захватить достаточно нейтронов, чтобы достичь этих элементов.[63][66][67]

Во Вселенной торий является одним из самых редких первичных элементов, потому что это один из двух элементов, которые могут быть произведены только в r-процессе (другой - уран), а также потому, что он медленно распадается вдали от момент его формирования. Единственные примордиальные элементы, более редкие, чем торий, - это тулий, лютеций, тантал и рений, элементы с нечетными номерами непосредственно перед третьим пиком содержания r-процесса вокруг тяжелых металлов платиновой группы, а также урана.[63][65][час] В далеком прошлом торий и уран были обогащены за счет распада изотопов плутония и кюрия, а торий был обогащен по сравнению с ураном за счет распада изотопов. 236U к 232Th и естественное истощение 235U, но эти источники уже давно распались и больше не вносят свой вклад.[68]
В земной коре тория гораздо больше: 8,1частей на миллион (ppm), это один из самых распространенных тяжелых элементов, почти такой же обильный, как свинец (13 ppm), и более распространенный, чем олово (2,1 ppm).[69] Это связано с тем, что торий может образовывать оксидные минералы, которые не проникают в ядро; это классифицируется как литофил. Обычные соединения тория также плохо растворяются в воде. Таким образом, даже если огнеупорные элементы имеют такое же относительное содержание на Земле, как и в Солнечной системе в целом, в коре более доступный торий, чем тяжелые металлы платиновой группы.[70]

На земле
Торий - 41-й элемент земной коры по распространенности. Природный торий обычно почти чистый 232Th, который является наиболее долгоживущим и наиболее стабильным изотопом тория, имеющий период полураспада, сопоставимый с возрастом Вселенной.[21] Его радиоактивный распад - самый крупный вклад в Внутреннее тепло Земли; другие основные вкладчики - короче живущие первичные радионуклиды, которые 238U, 40K и 235U в порядке убывания их вклада. (Во время формирования Земли 40K и 235U внесли гораздо больше в силу своего короткого периода полураспада, но они распались быстрее, оставив вклад от 232Че и 238U преобладает.)[75] Его распад приводит к постепенному уменьшению содержания тория на Земле: в настоящее время на планете содержится около 85% количества, присутствующего при образовании Земли.[46] Остальные природные изотопы тория намного короче; из них только 230Обычно это обнаруживается, встречается в светское равновесие со своим родителем 238U и составляет не более 0,04% природного тория.[21][я]
Торий встречается только в качестве второстепенного компонента большинства минералов, и по этой причине ранее считался редким.[77] Почва обычно содержит около 6 частей на миллион тория.[78]
В природе торий находится в степени окисления +4 вместе с ураном (IV), цирконий (IV), гафний (IV) и церий (IV), а также с скандий, иттрий, и трехвалентные лантаноиды, имеющие аналогичные ионные радиусы.[77] Из-за радиоактивности тория содержащиеся в нем минералы часто метамикт (аморфные), их кристаллическая структура была повреждена альфа-излучением тория.[79] Крайний пример - эканит, (Ca, Fe, Pb)2(Th, U) Si8О20, который почти никогда не встречается в неметамиктной форме из-за содержащегося в нем тория.[80]
Монацит (в основном фосфаты различных редкоземельных элементов) является наиболее важным коммерческим источником тория, поскольку он встречается в крупных месторождениях по всему миру, в основном в Индии, Южной Африке, Бразилии, Австралии и других странах. Малайзия. В среднем он содержит около 2,5% тория, хотя некоторые отложения могут содержать до 20%.[77][81] Монацит - химически инертный минерал, встречающийся в виде желтого или коричневого песка; его низкая реакционная способность затрудняет извлечение из него тория.[77] Алланит (главным образом силикаты-гидроксиды различных металлов) могут содержать торий 0,1–2% и циркон (в основном силикат циркония, ZrSiO4) до 0,4% тория.[77]
Диоксид тория встречается как редкий минерал. торианит. Поскольку он изотипен с диоксид урана эти два распространенных диоксида актинидов могут образовывать твердые растворы, и название минерала изменяется в соответствии с ThO2 содержание.[77][j] Торит (в основном силикат тория, ThSiO4), также имеет высокое содержание тория и является минералом, в котором торий был впервые обнаружен.[77] В минералах силиката тория Th4+ и SiO4−
4 ионы часто заменяются на M3+ (где M = Sc, Y или Ln) и фосфат (PO3−
4) ионы соответственно.[77] Из-за большой нерастворимости диоксида тория при высвобождении торий обычно не распространяется быстро в окружающей среде. Че4+ ион растворим, особенно в кислых почвах, и в таких условиях концентрация тория может достигать 40 ppm.[46]
История

Ошибочный отчет
В 1815 году шведский химик Йенс Якоб Берцелиус проанализировал необычный образец гадолинит из медного рудника в Фалунь, центральная Швеция. Он заметил пропитанные следы белого минерала, который он осторожно принял за землю (окись в современной химической номенклатуре) неизвестного элемента. Берцелиус уже открыл два элемента: церий и селен, но однажды он совершил публичную ошибку, объявив новый элемент, ганиум, это оказалось оксид цинка.[83] Берцелиус в частном порядке назвал предполагаемый элемент «торий» в 1817 году.[84] и его предполагаемый оксид "торина" после Тор, то Скандинавский бог грома.[85] В 1824 г., после того, как в Жилет-Агдер, Норвегия, он отказался от своих находок, поскольку минерал (позже названный ксенотайм ) оказались в основном ортофосфат иттрия.[29][83][86][87]
Открытие
В 1828 г. Мортен Трейн Эсмарк нашел черный минерал на Løvøya остров Телемарк графство, Норвегия. Он был норвежцем священник и любитель минералог который изучал минералы в Телемарке, где он служил викарий. Он обычно посылал самые интересные образцы, такие как этот, своему отцу, Йенс Эсмарк, известный минералог, профессор минералогии и геологии Королевский университет Фредерика в Христиании (сегодня называется Осло ).[88] Старший Эсмарк определил, что это неизвестный минерал, и отправил образец Берцелиусу для исследования. Берцелиус определил, что в нем есть новый элемент.[29] Он опубликовал свои результаты в 1829 году, выделив нечистый образец путем снижения KThF.5 с калий металл.[89][90][91] Берцелиус повторно использовал название предыдущего предполагаемого открытия элемента.[89][92] и назвал исходный минерал торитом.[29]

Берцелиус сделал некоторые первоначальные характеристики нового металла и его химических соединений: он правильно определил, что массовое отношение тория к кислороду оксида тория составляет 7,5 (его фактическое значение близко к этому, ~ 7,3), но он предположил, что новый элемент был двухвалентным. а не четырехвалентный, и таким образом подсчитали, что атомная масса была в 7,5 раз больше массы кислорода (120 аму ); на самом деле он в 15 раз больше.[k] Он определил, что торий очень электроположительный металл, впереди церия и позади циркония по электроположительности.[93] Металлический торий был впервые выделен в 1914 году голландскими предпринимателями Дирком Лели-младшим и Лодевейком Гамбургером.[l]
Первоначальная химическая классификация
В периодической таблице, опубликованной Дмитрий Менделеев в 1869 г. торий и редкоземельные элементы были помещены за пределы основной части таблицы в конце каждого вертикального периода после щелочноземельные металлы. Это отражало веру в то время, что торий и редкоземельные металлы двухвалентны. С более поздним признанием того, что редкоземельные элементы в основном трехвалентны, а торий четырехвалентен, Менделеев в 1871 году переместил церий и торий в группу IV, которая также содержала современные группа углерода (группа 14) и титановая группа (группа 4), потому что их максимальная степень окисления +4.[96][97] Церий вскоре был удален из основной части стола и помещен в отдельную серию лантанидов; торий остался в группе 4, так как он имел свойства, аналогичные своим предполагаемым более легким аналогам в этой группе, таким как титан и цирконий.[98][м]
Первое использование

Хотя торий был открыт в 1828 году, его первое применение датируется 1885 годом, когда австрийский химик Карл Ауэр фон Вельсбах изобрел газовая мантия - портативный источник света, который излучает свет от накала оксида тория при нагревании за счет сжигания газообразного топлива.[29] Впоследствии торий и его соединения нашли множество применений, включая керамику, угольные дуговые лампы, термостойкие тигли, а также в качестве катализаторов промышленных химических реакций, таких как окисление аммиака до азотной кислоты.[99]
Радиоактивность
Торий впервые обнаружил радиоактивность в 1898 году немецким химиком. Герхард Карл Шмидт а позже в том же году, независимо, польско-французский физик Мари Кюри. Это был второй элемент, который оказался радиоактивным после открытия в 1896 году радиоактивности урана французским физиком. Анри Беккерель.[100][101][102] С 1899 г. новозеландский физик Эрнест Резерфорд и американский инженер-электрик Роберт Боуи Оуэнс изучал излучение тория; первоначальные наблюдения показали, что они значительно различались. Было установлено, что эти изменения произошли от короткоживущей газообразной дочери тория, которая, как они обнаружили, является новым элементом. Этот элемент теперь называется радон, единственный из редких радиоэлементов, обнаруженных в природе как дочь тория, а не урана.[103]
После учета вклада радона Резерфорд теперь работает с британским физиком. Фредерик Содди, показал, как торий распадался с фиксированной скоростью с течением времени на ряд других элементов в работе, датированной 1900–1903 гг. Это наблюдение привело к идентификации период полураспада как один из результатов альфа-частица эксперименты, которые привели к теории распада радиоактивность.[104] Биологический эффект радиации был открыт в 1903 году.[105] Недавно обнаруженное явление радиоактивности взволновало как ученых, так и широкую общественность. В 1920-х годах радиоактивность тория рекламировалась как лекарство от ревматизм, сахарный диабет, и сексуальная импотенция. В 1932 году большинство из этих видов использования было запрещено в Соединенных Штатах после федерального расследования воздействия радиоактивности на здоровье.[106] 10 000 человек в США были введены торий во время рентгеновской диагностики; Позже выяснилось, что они страдают такими проблемами со здоровьем, как лейкемия и аномальные хромосомы.[46] К концу 1930-х гг. Общественный интерес к радиоактивности снизился.[106]

Дальнейшая классификация
Вплоть до конца 19 века химики единогласно считали торий и уран аналогами гафния и вольфрама; существование лантаноидов в шестом ряду было сочтено случайностью. В 1892 году британский химик Генри Бассетт постулировал второй сверхдлинный ряд периодической таблицы, содержащий известные и неоткрытые элементы, считая торий и уран аналогами лантаноидов. В 1913 г. датский физик Нильс Бор опубликовал теоретическая модель атома и его электронных орбиталей, которые вскоре получили широкое признание. Модель показала, что седьмая строка периодической таблицы также должна иметь заполнение f-оболочки перед d-оболочкой, которая была заполнена переходными элементами, как шестая строка с лантаноидами, предшествующими переходным металлам 5d.[96] The existence of a second inner transition series, in the form of the actinides, was not accepted until similarities with the electron structures of the lanthanides had been established;[107] Bohr suggested that the filling of the 5f orbitals may be delayed to after uranium.[96]
It was only with the discovery of the first трансурановые элементы, which from plutonium onward have dominant +3 and +4 oxidation states like the lanthanides, that it was realised that the actinides were indeed filling f-orbitals rather than d-orbitals, with the transition-metal-like chemistry of the early actinides being the exception and not the rule.[108] In 1945, when American physicist Гленн Т. Сиборг and his team had discovered the transuranic elements americium and curium, he proposed the actinide concept, realising that thorium was the second member of an f-block actinide series analogous to the lanthanides, instead of being the heavier congener of гафний in a fourth d-block row.[98][n]
Постепенный отказ от
In the 1990s, most applications that do not depend on thorium's radioactivity declined quickly due to safety and environmental concerns as suitable safer replacements were found.[29][111] Despite its radioactivity, the element has remained in use for applications where no suitable alternatives could be found. A 1981 study by the Национальная лаборатория Окриджа in the United States estimated that using a thorium gas mantle every weekend would be safe for a person,[111] but this was not the case for the dose received by people manufacturing the mantles or for the soils around some factory sites.[112] Some manufacturers have changed to other materials, such as yttrium.[113] As recently as 2007, some companies continued to manufacture and sell thorium mantles without giving adequate information about their radioactivity, with some even falsely claiming them to be non-radioactive.[111][114]
Атомная энергия

Thorium has been used as a power source on a prototype scale. The earliest thorium-based reactor was built at the Индийский энергетический центр находится в Бьюкенен, Нью-Йорк, Соединенные Штаты в 1962 г.[115] One of the largest supplies of thorium in the world is in the country of Индия, where there is not much uranium. In the 1950s, India targeted achieving energy independence with their three-stage nuclear power programme.[116][117] In most countries, uranium was relatively abundant and the progress of thorium-based reactors was slow; in the 20th century, three reactors were built in India and twelve elsewhere.[118] Large-scale research was begun in 1996 by the Международное агентство по атомной энергии to study the use of thorium reactors; a year later, the Министерство энергетики США started their research. Alvin Radkowsky из Тель-авивский университет в Израиль was the head designer of Шиппорт Атомная Электростанция in Pennsylvania, the first American civilian reactor to breed thorium.[119] He founded a consortium to develop thorium reactors, which included other laboratories: Raytheon Nuclear Inc. and Брукхейвенская национальная лаборатория в Соединенных Штатах, а Курчатовский институт в России.[120]
In the 21st century, thorium's potential for reducing nuclear proliferation and its напрасно тратить characteristics led to renewed interest in the thorium fuel cycle.[121][122][123] India has projected meeting as much as 30% of its electrical demands through thorium-based атомная энергия by 2050. In February 2014, Центр атомных исследований Бхабхи (BARC), in Мумбаи, India, presented their latest design for a "next-generation nuclear reactor" that burns thorium as its fuel ore, calling it the Advanced Heavy Water Reactor (AWHR). In 2009, the chairman of the Indian Atomic Energy Commission said that India has a "long-term objective goal of becoming energy-independent based on its vast thorium resources."
Ядерное оружие
When gram quantities of плутоний were first produced in the Манхэттенский проект, it was discovered that a minor isotope (240Пу ) underwent significant спонтанное деление, which brought into question the viability of a plutonium-fueled ядерное оружие пушечного типа. В то время как Лос-Аламос team began work on the implosion-type weapon to circumvent this issue, the Chicago team discussed reactor design solutions. Юджин Вигнер proposed to use the 240Pu-contaminated plutonium to drive the conversion of thorium into 233U in a special converter reactor. It was hypothesized that the 233U would then be usable in a gun-type weapon, though concerns about contamination from 232U were voiced. Progress on the implosion weapon was sufficient, and this converter was not developed further, but the design had enormous influence on the development of nuclear energy. It was the first detailed description of a highly enriched water-cooled, water-moderated reactor similar to future naval and commercial power reactors.[124]
Вовремя Холодная война the United States explored the possibility of using 232Th as a source of 233U to be used in a ядерная бомба; they fired a test bomb в 1955 г.[125] They concluded that a 233U-fired bomb would be a very potent weapon, but it bore few sustainable "technical advantages" over the contemporary uranium–plutonium bombs,[126] особенно с тех пор, как 233U is difficult to produce in isotopically pure form.[125]
Thorium metal was used in the radiation case of at least one nuclear weapon design deployed by the United States (the W71 ).[127]
Производство
| Страна | Резервы |
|---|---|
| Индия | 1070 |
| Бразилия | 632 |
| Австралия | 595 |
| Соединенные Штаты | 595 |
| Египет | 380 |
| индюк | 374 |
| Венесуэла | 300 |
| Канада | 172 |
| Россия | 155 |
| Южная Африка | 148 |
| Китай | 100 |
| Норвегия | 87 |
| Гренландия | 86 |
| Финляндия | 60.5 |
| Швеция | 50 |
| Казахстан | 50 |
| Другие страны | 1,725 |
| World total | 6579.5 |
The low demand makes working mines for extraction of thorium alone not profitable, and it is almost always extracted with the rare earths, which themselves may be by-products of production of other minerals.[128] The current reliance on monazite for production is due to thorium being largely produced as a by-product; other sources such as thorite contain more thorium and could easily be used for production if demand rose.[129] Present knowledge of the distribution of thorium resources is poor, as low demand has led to exploration efforts being relatively minor.[130] In 2014, world production of the monazite concentrate, from which thorium would be extracted, was 2,700 tonnes.[131]
The common production route of thorium constitutes concentration of thorium minerals; extraction of thorium from the concentrate; purification of thorium; and (optionally) conversion to compounds, such as thorium dioxide.[132]
Концентрация
There are two categories of thorium minerals for thorium extraction: primary and secondary. Primary deposits occur in acidic granitic magmas and pegmatites. They are concentrated, but of small size. Secondary deposits occur at the mouths of rivers in granitic mountain regions. In these deposits, thorium is enriched along with other heavy minerals.[39] Initial concentration varies with the type of deposit.[132]
For the primary deposits, the source pegmatites, which are usually obtained by mining, are divided into small parts and then undergo плавучесть. Alkaline earth metal carbonates may be removed after reaction with хлористый водород; then follow thickening, filtration, and calcination. The result is a concentrate with rare-earth content of up to 90%.[132] Secondary materials (such as coastal sands) undergo gravity separation. Magnetic separation follows, with a series of magnets of increasing strength. Monazite obtained by this method can be as pure as 98%.[132]
Industrial production in the 20th century relied on treatment with hot, concentrated sulfuric acid in cast iron vessels, followed by selective precipitation by dilution with water, as on the subsequent steps. This method relied on the specifics of the technique and the concentrate grain size; many alternatives have been proposed, but only one has proven effective economically: alkaline digestion with hot sodium hydroxide solution. This is more expensive than the original method but yields a higher purity of thorium; in particular, it removes phosphates from the concentrate.[132]
Acid digestion
Acid digestion is a two-stage process, involving the use of up to 93% серная кислота at 210–230 °C. First, sulfuric acid in excess of 60% of the sand mass is added, thickening the reaction mixture as products are formed. Then, fuming sulfuric acid is added and the mixture is kept at the same temperature for another five hours to reduce the volume of solution remaining after dilution. The concentration of the sulfuric acid is selected based on reaction rate and viscosity, which both increase with concentration, albeit with viscosity retarding the reaction. Increasing the temperature also speeds up the reaction, but temperatures of 300 °C and above must be avoided, because they cause insoluble thorium pyrophosphate to form. Since dissolution is very exothermic, the monazite sand cannot be added to the acid too quickly. Conversely, at temperatures below 200 °C the reaction does not go fast enough for the process to be practical. To ensure that no precipitates form to block the reactive monazite surface, the mass of acid used must be twice that of the sand, instead of the 60% that would be expected from stoichiometry. The mixture is then cooled to 70 °C and diluted with ten times its volume of cold water, so that any remaining monazite sinks to the bottom while the rare earths and thorium remain in solution. Thorium may then be separated by precipitating it as the phosphate at pH 1.3, since the rare earths do not precipitate until pH 2.[132]
Alkaline digestion
Alkaline digestion is carried out in 30–45% едкий натр solution at about 140 °C for about three hours. Too high a temperature leads to the formation of poorly soluble thorium oxide and an excess of uranium in the filtrate, and too low a concentration of alkali leads to a very slow reaction. These reaction conditions are rather mild and require monazite sand with a particle size under 45 μm. Following filtration, the filter cake includes thorium and the rare earths as their hydroxides, uranium as sodium diuranate, and phosphate as тринатрийфосфат. This crystallises trisodium phosphate decahydrate when cooled below 60 °C; uranium impurities in this product increase with the amount of диоксид кремния in the reaction mixture, necessitating recrystallisation before commercial use. The hydroxides are dissolved at 80 °C in 37% hydrochloric acid. Filtration of the remaining precipitates followed by addition of 47% sodium hydroxide results in the precipitation of thorium and uranium at about pH 5.8. Complete drying of the precipitate must be avoided, as air may oxidise cerium from the +3 to the +4 oxidation state, and the cerium(IV) formed can liberate free хлор from the hydrochloric acid. The rare earths again precipitate out at higher pH. The precipitates are neutralised by the original sodium hydroxide solution, although most of the phosphate must first be removed to avoid precipitating rare-earth phosphates. Экстракция растворителем may also be used to separate out the thorium and uranium, by dissolving the resultant filter cake in nitric acid. Наличие titanium hydroxide is deleterious as it binds thorium and prevents it from dissolving fully.[132]
Очищение
High thorium concentrations are needed in nuclear applications. In particular, concentrations of atoms with high neutron capture cross-sections must be very low (for example, гадолиний concentrations must be lower than one part per million by weight). Previously, repeated dissolution and recrystallisation was used to achieve high purity. Today, liquid solvent extraction procedures involving selective комплексообразование чт4+ are used. For example, following alkaline digestion and the removal of phosphate, the resulting nitrato complexes of thorium, uranium, and the rare earths can be separated by extraction with трибутилфосфат в керосин.[132]
Современные приложения
Non-radioactivity-related uses have been in decline since the 1950s[133] due to environmental concerns largely stemming from the radioactivity of thorium and its decay products.[29][111]
Most thorium applications use its dioxide (sometimes called "thoria" in the industry), rather than the metal. This compound has a melting point of 3300 °C (6000 °F), the highest of all known oxides; only a few substances have higher melting points.[46] This helps the compound remain solid in a flame, and it considerably increases the brightness of the flame; this is the main reason thorium is used in gas lamp mantles.[134] All substances emit energy (glow) at high temperatures, but the light emitted by thorium is nearly all in the видимый спектр, hence the brightness of thorium mantles.[49]
Energy, some of it in the form of visible light, is emitted when thorium is exposed to a source of energy itself, such as a cathode ray, heat, or ультрафиолетовый свет. This effect is shared by cerium dioxide, which converts ultraviolet light into visible light more efficiently, but thorium dioxide gives a higher flame temperature, emitting less Инфракрасный свет.[134] Thorium in mantles, though still common, has been progressively replaced with yttrium since the late 1990s.[135] According to the 2005 review by the United Kingdom's National Radiological Protection Board, "although [thoriated gas mantles] were widely available a few years ago, they are not any more."[136]
Во время производства раскаленный нити, recrystallisation of tungsten is significantly lowered by adding small amounts of thorium dioxide to the tungsten спекание powder before drawing the filaments.[133] A small addition of thorium to tungsten thermocathodes considerably reduces the рабочая функция электронов; as a result, electrons are emitted at considerably lower temperatures.[29] Thorium forms a one-atom-thick layer on the surface of tungsten. The work function from a thorium surface is lowered possibly because of the electric field on the interface between thorium and tungsten formed due to thorium's greater electropositivity.[137] Since the 1920s, thoriated tungsten wires have been used in electronic tubes and in the cathodes and anticathodes of X-ray tubes and rectifiers. Thanks to the reactivity of thorium with atmospheric oxygen and nitrogen, thorium also acts as a добытчик for impurities in the evacuated tubes. The introduction of transistors in the 1950s significantly diminished this use, but not entirely.[133] Thorium dioxide is used in газовая вольфрамовая дуговая сварка (GTAW) to increase the high-temperature strength of tungsten electrodes and improve arc stability.[29] Thorium oxide is being replaced in this use with other oxides, such as those of zirconium, cerium, and лантан.[138][139]
Thorium dioxide is found in heat-resistant ceramics, such as high-temperature laboratory crucibles,[29] either as the primary ingredient or as an addition to zirconium dioxide. An alloy of 90% платина and 10% thorium is an effective catalyst for oxidising аммиак to nitrogen oxides, but this has been replaced by an alloy of 95% platinum and 5% родий because of its better mechanical properties and greater durability.[133]

When added to стекло, thorium dioxide helps increase its показатель преломления и уменьшить dispersion. Such glass finds application in high-quality линзы for cameras and scientific instruments.[40] The radiation from these lenses can darken them and turn them yellow over a period of years and it degrades film, but the health risks are minimal.[140] Yellowed lenses may be restored to their original colourless state by lengthy exposure to intense ultraviolet radiation. Thorium dioxide has since been replaced in this application by rare-earth oxides, such as лантан, as they provide similar effects and are not radioactive.[133]
Thorium tetrafluoride is used as an anti-reflection material in multilayered optical coatings. It is transparent to electromagnetic waves having wavelengths in the range of 0.350–12 µm, a range that includes near ultraviolet, visible and средний инфракрасный свет. Its radiation is primarily due to alpha particles, which can be easily stopped by a thin cover layer of another material.[141] Replacements for thorium tetrafluoride are being developed as of the 2010s,[142] который включает в себя Lanthanum trifluoride.
Mag-Thor alloys (also called thoriated magnesium) found use in some aerospace applications, though such uses have been phased out due to concerns over radioactivity.
Potential use for nuclear energy
The main nuclear power source in a reactor is the neutron-induced fission of a nuclide; the synthetic fissile[e] ядра 233U и 239Pu can be разводится from neutron capture by the naturally occurring quantity nuclides 232Че и 238U. 235U occurs naturally and is also fissile.[143][144][o] In the thorium fuel cycle, the fertile isotope 232Th is bombarded by slow neutrons, undergoing neutron capture to become 233Th, which undergoes two consecutive beta decays to become first 233Па and then the fissile 233U:[29]
- 232
90Чт
+ 3n → 233
90Чт
+ γ + 2n 233
91Па
+ n 233
92U
Трансмутации в ториевый топливный цикл | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 237Np | ||||||||||||||
| ↑ | ||||||||||||||
| 231U | ← | 232U | ↔ | 233U | ↔ | 234U | ↔ | 235U | ↔ | 236U | → | 237U | ||
| ↓ | ↑ | ↑ | ↑ | |||||||||||
| 231Па | → | 232Па | ← | 233Па | → | 234Па | ||||||||
| ↑ | ↑ | |||||||||||||
| 230Чт | → | 231Чт | ← | 232Чт | → | 233Чт | ||||||||
| ||||||||||||||
233U is fissile and can be used as a nuclear fuel in the same way as 235U or 239Пу. Когда 233U undergoes nuclear fission, the neutrons emitted can strike further 232Th nuclei, continuing the cycle.[29] This parallels the uranium fuel cycle in быстрые реакторы-размножители куда 238U undergoes neutron capture to become 239U, beta decaying to first 239Np and then fissile 239Пу.[145]
Преимущества
Thorium is more abundant than uranium, and can satisfy world energy demands for longer.[146]
232Th absorbs neutrons more readily than 238U и 233U has a higher probability of fission upon neutron capture (92.0%) than 235U (85.5%) or 239Pu (73.5%).[147] It also releases more neutrons upon fission on average.[146] A single neutron capture by 238U produces transuranic waste along with the fissile 239Pu, but 232Th only produces this waste after five captures, forming 237Np. This number of captures does not happen for 98–99% of the 232Th nuclei because the intermediate products 233U or 235U undergo fission, and fewer long-lived transuranics are produced. Because of this, thorium is a potentially attractive alternative to uranium in mixed oxide fuels to minimise the generation of transuranics and maximise the destruction of плутоний.[148] Liquid fluoride thorium reactors (LFTR) have very little waste compared with reactors powered by uranium. LFTRs run at atmospheric pressure instead of 150 to 160 times atmospheric pressure currently needed.Thorium is less radioactive than uranium.
Thorium fuels result in a safer and better-performing активная зона реактора[29] because thorium dioxide has a higher melting point, higher теплопроводность, и более низкий коэффициент температурного расширения. It is more stable chemically than the now-common fuel uranium dioxide, because the latter oxidises to triuranium octoxide (U3О8), becoming substantially less dense.[149]
Недостатки
The used fuel is difficult and dangerous to reprocess because many of the daughters of 232Че и 233U are strong gamma emitters.[146] Все 233U production methods result in impurities of 232U, either from parasitic knock-out (n,2n) reactions on 232Чт, 233Pa, or 233U that result in the loss of a neutron, or from double neutron capture of 230Th, an impurity in natural 232Th:[150]
- 230
90Чт
+ п → 231
90Чт
+ γ 231
91Па
231
91Па
+ п → 232
91Па
+ γ 232
92U
232U by itself is not particularly harmful, but quickly decays to produce the strong gamma emitter 208Tl. (232Th follows the same decay chain, but its much longer half-life means that the quantities of 208Tl produced are negligible.)[151] These impurities of 232U make 233U easy to detect and dangerous to work on, and the impracticality of their separation limits the possibilities of распространение ядерного оружия с помощью 233U as the fissile material.[150] 233Pa has a relatively long half-life of 27 days and a high поперечное сечение for neutron capture. Thus it is a neutron poison: instead of rapidly decaying to the useful 233U, a significant amount of 233Pa converts to 234U and consumes neutrons, degrading the reactor efficiency. Чтобы этого избежать, 233Pa is extracted from the active zone of thorium реакторы на расплаве солей during their operation, so that it does not have a chance to capture a neutron and will only decay to 233U.[152]
The irradiation of 232Th with neutrons, followed by its processing, need to be mastered before these advantages can be realised, and this requires more advanced technology than the uranium and plutonium fuel cycle;[29] research continues in this area. Others cite the low commercial viability of the thorium fuel cycle:[153][154][155] the international Агентство по ядерной энергии predicts that the thorium cycle will never be commercially viable while uranium is available in abundance—a situation which may persist "in the coming decades".[156] The isotopes produced in the thorium fuel cycle are mostly not transuranic, but some of them are still very dangerous, such as 231Pa, which has a half-life of 32,760 years and is a major contributor to the long-term радиотоксичность of spent nuclear fuel.[152]
Опасности

Радиологический
Natural thorium decays very slowly compared to many other radioactive materials, and the emitted альфа-излучение cannot penetrate human skin. As a result, handling small amounts of thorium, such as those in gas mantles, is considered safe, although the use of such items may pose some risks.[157] Exposure to an aerosol of thorium, such as contaminated dust, can lead to increased risk of раки из легкое, поджелудочная железа, и кровь, as lungs and other internal organs can be penetrated by alpha radiation.[157] Internal exposure to thorium leads to increased risk of печень болезни.[158]
The decay products of 232Th include more dangerous radionuclides such as radium and radon. Although relatively little of those products are created as the result of the slow decay of thorium, a proper assessment of the radiological toxicity of 232Th must include the contribution of its daughters, some of which are dangerous гамма emitters,[159] and which are built up quickly following the initial decay of 232Th due to the absence of long-lived nuclides along the decay chain.[160] As the dangerous daughters of thorium have much lower melting points than thorium dioxide, they are volatilised every time the mantle is heated for use. In the first hour of use large fractions of the thorium daughters 224Ра, 228Ра, 212Pb, and 212Bi are released.[161] Most of the radiation dose by a normal user arises from inhaling the radium, resulting in a radiation dose of up to 0.2 миллизиверты per use, about a third of the dose sustained during a маммограмма.[162]
Немного ядерная безопасность agencies make recommendations about the use of thorium mantles and have raised safety concerns regarding their производство and disposal; the radiation dose from one mantle is not a serious problem, but that from many mantles gathered together in factories or landfills is.[158]
Биологические
Thorium is odourless and tasteless.[163] The chemical toxicity of thorium is low because thorium and its most common compounds (mostly the dioxide) are poorly soluble in water,[164] precipitating out before entering the body as the hydroxide.[165] Some thorium compounds are chemically moderately токсичный, especially in the presence of strong complex-forming ions such as citrate that carry the thorium into the body in soluble form.[160] If a thorium-containing object has been chewed or sucked, it loses 0.4% of thorium and 90% of its dangerous daughters to the body.[114] Three-quarters of the thorium that has penetrated the body accumulates in the скелет. Absorption through the skin is possible, but is not a likely means of exposure.[157] Thorium's low solubility in water also means that excretion of thorium by the kidneys and faeces is rather slow.[160]
Tests on the thorium uptake of workers involved in monazite processing showed thorium levels above recommended limits in their bodies, but no adverse effects on health were found at those moderately low concentrations. No chemical toxicity has yet been observed in the tracheobronchial tract and the lungs from exposure to thorium.[165] People who work with thorium compounds are at a risk of дерматит. It can take as much as thirty years after the ingestion of thorium for symptoms to manifest themselves.[46] Thorium has no known biological role.[46]
Химическая
Powdered thorium metal is pyrophoric: it ignites spontaneously in air.[4] В 1964 г. Министерство внутренних дел США listed thorium as "severe" on a table entitled "Ignition and explosibility of metal powders". Its ignition temperature was given as 270 °C (520 °F) for dust clouds and 280 °C (535 °F) for layers. Its minimum explosive concentration was listed as 0.075 oz/cu ft (0.075 kg/m3); the minimum igniting energy for (non-submicron) dust was listed as 5мДж.[166]
In 1956, the Sylvania Electric Products explosion occurred during reprocessing and burning of thorium sludge in Нью-Йорк, Соединенные Штаты. Nine people were injured; one died of complications caused by ожоги третьей степени.[167][168][169]
Exposure routes
Thorium exists in very small quantities everywhere on Earth although larger amounts exist in certain parts: the average human contains about 40 микрограммы of thorium and typically consumes three micrograms per day.[46] Most thorium exposure occurs through dust inhalation; some thorium comes with food and water, but because of its low solubility, this exposure is negligible.[160]
Exposure is raised for people who live near thorium deposits or radioactive waste disposal sites, those who live near or work in uranium, phosphate, or tin processing factories, and for those who work in gas mantle production.[170] Thorium is especially common in the Тамил Наду coastal areas of India, where residents may be exposed to a naturally occurring radiation dose ten times higher than the worldwide average.[171] It is also common in northern Бразильский coastal areas, from south Bahia к Гуарапари, a city with radioactive monazite sand beaches, with radiation levels up to 50 times higher than world average background radiation.[172]
Another possible source of exposure is thorium dust produced at weapons testing ranges, as thorium is used in the guidance systems of some missiles. This has been blamed for a high incidence of birth defects and cancer at Сальто-ди-Квирра на итальянском острове Сардиния.[173]
Смотрите также
Примечания
- ^ Висмут is very slightly radioactive, but its half-life (1.9×1019 years) is so long that its decay is negligible even over geological timespans.
- ^ Пока эйнштейний has been measured to have a lower density, this measurement was done on small, microgram-mass samples, and is likely because of the rapid self-destruction of the crystal structure caused by einsteinium's extreme radioactivity.[8]
- ^ Позади осмий, тантал, вольфрам, и рений;[4] higher boiling points are speculated to be found in the 6d transition metals, but they have not been produced in large enough quantities to test this prediction.[9]
- ^ Gamma rays are distinguished by their origin in the nucleus, not their wavelength; hence there is no lower limit to gamma energy derived from radioactive decay.[27]
- ^ а б А расщепляющийся nuclide is capable of undergoing fission (even with a low probability) after capturing a high-energy neutron. Some of these nuclides can be induced to fission with low-energy thermal neutrons with a high probability; они упоминаются как делящийся. А плодородный nuclide is one that could be bombarded with neutrons to produce a fissile nuclide. Критическая масса is the mass of a ball of a material which could undergo a sustained ядерная цепная реакция.
- ^ Название ionium за 230Th is a remnant from a period when different isotopes were not recognised to be the same element and were given different names.
- ^ Unlike the previous similarity between the actinides and the transition metals, the main-group similarity largely ends at thorium before being resumed in the second half of the actinide series, because of the growing contribution of the 5f orbitals to covalent bonding. The only other commonly-encountered actinide, uranium, retains some echoes of main-group behaviour. The chemistry of uranium is more complicated than that of thorium, but the two most common oxidation states of uranium are uranium(VI) and uranium(IV); these are two oxidation units apart, with the higher oxidation state corresponding to formal loss of all valence electrons, which is similar to the behaviour of the heavy main-group elements in the p-блок.[37]
- ^ An even number of either protons or neutrons generally increases nuclear stability of isotopes, compared to isotopes with odd numbers. Elements with odd atomic numbers have no more than two stable isotopes; even-numbered elements have multiple stable isotopes, with tin (element 50) having ten.[10]
- ^ Other isotopes may occur alongside 232Th, but only in trace quantities. If the source contains no uranium, the only other thorium isotope present would be 228Th, which occurs in the цепочка распада из 232Th (the thorium series ): the ratio of 228Th to 232Th would be under 10−10.[21] If uranium is present, tiny traces of several other isotopes will also be present: 231Че и 227Th from the decay chain of 235U (the актиниевый ряд ), and slightly larger but still tiny traces of 234Че и 230Th from the decay chain of 238U (the урановая серия ).[21] 229Th is also been produced in the decay chain of 237Np (the neptunium series ): all primordial 237Np is вымерший, but it is still produced as a result of nuclear reactions in uranium ores.[76] 229Th is mostly produced as a дочь of artificial 233U made by neutron irradiation из 232Th, and is extremely rare in nature.[21]
- ^ Thorianite refers to minerals with 75–100 mol% ThO2; uranothorianite, 25–75 mol% ThO2; thorian uraninite, 15–25 mol% ThO2; уранинит, 0–15 mol% ThO2.[77]
- ^ В то время редкоземельные элементы, among which thorium was found and with which it is closely associated in nature, were thought to be divalent; the rare earths were given атомный вес values two-thirds of their actual ones, and thorium and uranium are given values half of the actual ones.
- ^ The main difficulty in isolating thorium lies not in its chemical electropositivity, but in the close association of thorium in nature with the rare-earth elements and uranium, which collectively are difficult to separate from each other. Шведский химик Ларс Фредрик Нильсон Первооткрыватель скандия ранее уже пытался выделить металлический торий в 1882 году, но безуспешно добился высокой степени чистоты.[94] Lely и Hamburger получили металлический торий с чистотой 99% восстановлением хлорида тория металлическим натрием.[95] Более простой метод, ведущий к еще более высокой чистоте, был открыт в 1927 году американскими инженерами Джоном Марденом и Харви Рентшлером, включающий восстановление оксида тория кальцием в присутствии хлорида кальция.[95]
- ^ Торий также присутствует в таблице 1864 года британского химика. Джон Ньюлендс как последний и самый тяжелый элемент, поскольку первоначально считалось, что уран является трехвалентным элементом с атомной массой около 120: это половина его фактического значения, поскольку уран преимущественно шестивалентный. Он также фигурирует как самый тяжелый элемент в таблице 1864 года британского химика. Уильям Одлинг под титаном, цирконием и тантал. Он не фигурирует в периодических системах, опубликованных французским геологом. Александр-Эмиль Бегайе де Шанкуртуа в 1862 году немецко-американский музыкант Густав Хинрикс в 1867 г., или немецкий химик Юлиус Лотар Мейер в 1870 г., исключая редкоземельные элементы и торий.[96]
- ^ Заполнение подоболочки 5f от начала ряда актинидов было подтверждено в 1964 г., когда следующий элемент, резерфорд, был впервые синтезирован и обнаружил, что ведет себя как гафний, как и следовало ожидать, если бы к тому времени уже было завершено заполнение 5f-орбиталей.[109] Сегодня сходство тория с гафнием все еще иногда подтверждают, называя его «элементом псевдогруппы 4».[110]
- ^ Тринадцать делящихся изотопов актинида с периодом полураспада более года: 229Чт, 233U, 235U, 236Np, 239Пу, 241Пу, 242 кв.м.Являюсь, 243См, 245См, 247См, 249Cf, 251Cf, и 252Es. Из них только 235U встречается в природе, и только 233U и 239Pu можно вывести из ядер естественного происхождения за один нейтронный захват.[144]
Рекомендации
- ^ а б c d Мейя, Юрис; и другие. (2016). «Атомный вес элементов 2013 (Технический отчет IUPAC)». Чистая и прикладная химия. 88 (3): 265–91. Дои:10.1515 / pac-2015-0305.
- ^ Лиде, Д. Р., изд. (2005). «Магнитная восприимчивость элементов и неорганических соединений». CRC Справочник по химии и физике (PDF) (86-е изд.). CRC Press. С. 4–135. ISBN 978-0-8493-0486-6.
- ^ Уист, Р. (1984). CRC, Справочник по химии и физике. Издательство "Химическая резиновая компания". п. E110. ISBN 978-0-8493-0464-4.
- ^ а б c d е ж грамм час я j k л м п о Wickleder, Fourest & Dorhout, 2006 г. С. 61–63.
- ^ Gale, W. F .; Тотемайер, Т. К. (2003). Справочник Smithells Metals. Баттерворт-Хайнеманн. С. 15-2–15-3. ISBN 978-0-08-048096-1.
- ^ а б c d е Третьяков, Ю. Д., изд. (2007). Неорганическая химия в трех томах. Химия переходных элементов. 3. Академия. ISBN 978-5-7695-2533-9.
- ^ а б c Johansson, B .; Abuja, R .; Eriksson, O .; и другие. (1995). «Аномальная ГЦК кристаллическая структура металлического тория». Письма с физическими проверками. 75 (2): 280–283. Bibcode:1995PhRvL..75..280J. Дои:10.1103 / PhysRevLett.75.280. PMID 10059654.
- ^ Haire, R.G .; Байбарз, Р. Д. (1979). «Исследования металлического эйнштейния» (PDF). Le Journal de Physique. 40: C4–101. Дои:10.1051 / jphyscol: 1979431.
- ^ Фрике, Буркхард (1975). Сверхтяжелые элементы: прогноз их химических и физических свойств. Недавнее влияние физики на неорганическую химию. Структура и связь. 21. стр.89–144. Дои:10.1007 / BFb0116498. ISBN 978-3-540-07109-9. Получено 4 октября 2013.
- ^ а б c d е ж Audi, G .; Bersillon, O .; Blachot, J .; и другие. (2003). «Оценка ядерных и распадных свойств NUBASE» (PDF). Ядерная физика A. 729 (1): 3–128. Bibcode:2003НуФА.729 .... 3А. CiteSeerX 10.1.1.692.8504. Дои:10.1016 / j.nuclphysa.2003.11.001. Архивировано из оригинал (PDF) 24 июля 2013 г.
- ^ де Лаэтер, Джон Роберт; Бёльке, Джон Карл; Де Бьевр, Поль; Хидака, Хироши; Пайзер, Х. Штеффен; Росман, Кевин Дж. Р .; Тейлор, Филип Д. П. (2003). «Атомный вес элементов. Обзор 2000 г. (Технический отчет IUPAC)». Чистая и прикладная химия. 75 (6): 683–800. Дои:10.1351 / pac200375060683.
- ^ Международный союз теоретической и прикладной химии (2006). «Атомный вес элементов 2005 (Технический отчет IUPAC)» (PDF). Чистая и прикладная химия. 78 (11): 2051–2066. Дои:10.1351 / pac200678112051. Получено 27 июля 2017.
- ^ Надь, С. (2009). Радиохимия и ядерная химия. 2. Публикации EOLSS. п. 374. ISBN 978-1-84826-127-3.
- ^ Гриффин, Х.С. (2010). «Цепи естественного радиоактивного распада». In Vértes, A .; Nagy, S .; Klencsár, Z .; и другие. (ред.). Справочник по ядерной химии. Springer Science + Business Media. п. 668. ISBN 978-1-4419-0719-6.
- ^ Байзер, А. (2003). «Ядерные преобразования» (PDF). Концепции современной физики (6 изд.). McGraw-Hill Education. С. 432–434. ISBN 978-0-07-244848-1.
- ^ «AREVA Med начинает производство свинца-212 на новом предприятии» (Пресс-релиз). Areva. 2013. Получено 1 января 2017.
- ^ «Минеральный ежегодник 2012» (PDF). Геологическая служба США. Получено 30 сентября 2017.
- ^ Рамдал, Томас; Bonge-Hansen, Hanne T .; Райан, Олав Б .; Ларсен, Осмунд; Херстад, Гуннар; Сандберг, Марсель; Bjerke, Roger M .; Грант, Дерек; Бревик, Эллен М. (1 сентября 2016 г.). «Эффективный комплексообразователь тория-227». Письма по биоорганической и медицинской химии. 26 (17): 4318–4321. Дои:10.1016 / j.bmcl.2016.07.034. ISSN 0960-894X. PMID 27476138.
- ^ Deblonde, Gauthier J.-P .; Lohrey, Trevor D .; Бут, Корвин Х .; Картер, Кори П .; Паркер, Бернард Ф .; Ларсен, Осмунд; Смитс, Роджер; Райан, Олав Б .; Катбертсон, Алан С. (19 ноября 2018 г.). «Термодинамика раствора и кинетика комплексообразования металлов с хелатором гидроксипиридинона, разработанным для целевой альфа-терапии торием-227». Неорганическая химия. 57 (22): 14337–14346. Дои:10.1021 / acs.inorgchem.8b02430. ISSN 0020-1669. PMID 30372069.
- ^ Капитан Илья; Deblonde, Gauthier J.-P .; Руперт, Питер Б.; An, Dahlia D .; Или, Мари-Клэр; Ростан, Эмелин; Ralston, Corie Y .; Сильный, Роланд К .; Абергель, Ребекка Дж. (21 ноября 2016 г.). «Инженерное распознавание четырехвалентного циркония и тория с помощью хелаторно-белковых систем: на пути к гибким платформам лучевой терапии и визуализации». Неорганическая химия. 55 (22): 11930–11936. Дои:10.1021 / acs.inorgchem.6b02041. ISSN 0020-1669. PMID 27802058.
- ^ а б c d е ж грамм час Wickleder, Fourest & Dorhout, 2006 г. С. 53–55.
- ^ Bonetti, R .; Chiesa, C .; Guglielmetti, A .; и другие. (1995). «Первое наблюдение спонтанного деления и поиск кластерного распада 232Че ». Физический обзор C. 51 (5): 2530–2533. Bibcode:1995PhRvC..51.2530B. Дои:10.1103 / PhysRevC.51.2530. PMID 9970335.
- ^ Ikezoe, H .; Икута, Т .; Hamada, S .; и другие. (1996). "альфа-распад нового изотопа 209Че ». Физический обзор C. 54 (4): 2043–2046. Bibcode:1996PhRvC..54.2043I. Дои:10.1103 / PhysRevC.54.2043. PMID 9971554.
- ^ Ruchowska, E .; Płóciennik, W. A .; Ylicz, J .; и другие. (2006). "Ядерная структура 229Чт ». Физический обзор C. 73 (4): 044326. Bibcode:2006PhRvC..73d4326R. Дои:10.1103 / PhysRevC.73.044326. HDL:10261/12130.
- ^ Beck, B.R .; Беккер, Дж. А .; Beiersdorfer, P .; и другие. (2007). "Расщепление энергии в дублете основного состояния в ядре 229Чт ». Письма с физическими проверками. 98 (14): 142501. Bibcode:2007ПхРвЛ..98н2501Б. Дои:10.1103 / PhysRevLett.98.142501. PMID 17501268.
- ^ von der Wense, L .; Seiferle, B .; Laatiaoui, M .; и другие. (2016). "Прямое обнаружение 229Ядерные часы перехода ». Природа. 533 (7601): 47–51. arXiv:1710.11398. Bibcode:2016Натура.533 ... 47В. Дои:10.1038 / природа17669. PMID 27147026.
- ^ Фейнман, Р.; Leighton, R .; Сэндс, М. (1963). Лекции Фейнмана по физике. 1. Эддисон-Уэсли. С. 2–5. ISBN 978-0-201-02116-5. Получено 13 января 2018.
- ^ а б c «Оценка данных по безопасности ядерной критичности и пределов для актинидов на транспорте» (PDF). Институт радиозащиты и ядерной безопасности. п. 15. Архивировано из оригинал (PDF) 10 июля 2007 г.. Получено 20 декабря 2010.
- ^ а б c d е ж грамм час я j k л м п Wickleder, Fourest & Dorhout, 2006 г. С. 52–53.
- ^ а б «3–6: Датирование урана и тория» (PDF). Институт структуры и ядерной астрофизики, Университет Нотр-Дам. Получено 7 октября 2017.
- ^ Дэвис, О. «Уран-ториевое датирование». Департамент наук о Земле, Университет Аризоны. Архивировано из оригинал 28 марта 2017 г.. Получено 7 октября 2017.
- ^ а б Рафферти, Дж. П. (2010), Геохронология, датировка и докембрийское время: начало мира, каким мы его знаем, Геологическая история Земли, Розен Паблишинг, п. 150, ISBN 978-1-61530-125-6
- ^ а б Vértes, A. (2010), Nagy, S .; Klencsár, Z .; Lovas, R.G .; и другие. (ред.), Справочник по ядерной химии, 5 (2-е изд.), Springer Science + Business Media, стр. 800, ISBN 978-1-4419-0719-6
- ^ Wickleder, Fourest & Dorhout, 2006 г. С. 59–60.
- ^ а б c d Коттон, С. (2006). Химия лантаноидов и актинидов. Джон Уайли и сыновья.
- ^ Martin, W. C .; Hagan, L .; Читатель, Дж .; и другие. (1974). «Уровни земли и потенциал ионизации для атомов и ионов лантанидов и актинидов» (PDF). J. Phys. Chem. Ref. Данные. 3 (3): 771–779. Bibcode:1974JPCRD ... 3..771M. Дои:10.1063/1.3253147. Архивировано из оригинал (PDF) 4 марта 2016 г.. Получено 19 октября 2013.
- ^ а б Кинг, Р. Брюс (1995). Неорганическая химия элементов основных групп. Вайли-ВЧ. ISBN 978-0-471-18602-1.
- ^ Гринвуд и Эрншоу 1997, п. 1262.
- ^ а б Штолл 2005, п. 6.
- ^ а б Хаммонд, К. Р. (2004). Элементы, в Справочнике химии и физики (81-е изд.). CRC Press. ISBN 978-0-8493-0485-9.
- ^ а б Хайд, Э. К. (1960). Радиохимия тория (PDF). Национальная Академия Наук. Получено 29 сентября 2017.
- ^ Гринвуд и Эрншоу 1997, п. 1264.
- ^ Мур, Роберт Ли; Goodall, C.A .; Hepworth, J. L .; Уоттс, Р. А. (май 1957 г.). «Растворение тория в азотной кислоте. Кинетика реакции, катализируемой фторидом». Промышленная и инженерная химия. 49 (5): 885–887. Дои:10.1021 / ie50569a035.
- ^ а б Гринвуд и Эрншоу 1997, п. 1267.
- ^ Ямасита, Тошиюки; Нитани, Норико; Цудзи, Тошихидэ; Инагаки, Хироницу (1997). «Тепловые расширения NpO2 и некоторые другие диоксиды актинидов ». J. Nucl. Матер. 245 (1): 72–78. Bibcode:1997JNuM..245 ... 72Y. Дои:10.1016 / S0022-3115 (96) 00750-7.
- ^ а б c d е ж грамм час Эмсли, Дж. (2011). блоки emsley: руководство по элементам от А до Я. Oxford University Press. С. 544–548. ISBN 978-0-19-960563-7.
- ^ а б Wickleder, Fourest & Dorhout, 2006 г. С. 70–77.
- ^ Гринвуд и Эрншоу 1997, п. 1269.
- ^ а б c Айви, Х.Ф. (1974). «Кандолюминесценция и радикально-возбужденное свечение». Журнал Люминесценции. 8 (4): 271–307. Bibcode:1974JLum .... 8..271I. Дои:10.1016/0022-2313(74)90001-5.
- ^ Wickleder, Fourest & Dorhout, 2006 г. С. 95–97.
- ^ а б c d е Wickleder, Fourest & Dorhout, 2006 г. С. 78–94.
- ^ а б Гринвуд и Эрншоу 1997, п. 1271.
- ^ Wickleder, Fourest & Dorhout, 2006 г. С. 97–101.
- ^ Wickleder, Fourest & Dorhout, 2006 г. С. 64–66.
- ^ Гринвуд и Эрншоу 1997, п. 127.
- ^ а б c d Wickleder, Fourest & Dorhout, 2006 г. С. 117–134.
- ^ Перссон, И. (2010). «Гидратированные ионы металлов в водном растворе: насколько регулярны их структуры?». Чистая и прикладная химия. 82 (10): 1901–1917. Дои:10.1351 / PAC-CON-09-10-22.
- ^ а б Гринвуд и Эрншоу 1997, стр. 1275–1277.
- ^ а б c Wickleder, Fourest & Dorhout, 2006 г. С. 101–115.
- ^ а б c d Wickleder, Fourest & Dorhout, 2006 г. С. 116–117.
- ^ а б Гринвуд и Эрншоу 1997 С. 1278–1280.
- ^ Langeslay, Ryan R .; Fieser, Megan E .; Ziller, Joseph W .; Фурче, Филипп; Эванс, Уильям Дж. (2015). «Синтез, структура и реакционная способность кристаллических молекулярных комплексов {[C5ЧАС3(SiMe3)2]3Th}1− анион, содержащий торий в формальной степени окисления +2 ". Химическая наука. 6 (6): 517–521. Дои:10.1039 / C4SC03033H. ЧВК 5811171. PMID 29560172.
- ^ а б c Кэмерон, А. Г. У. (1973). «Изобилие элементов в Солнечной системе» (PDF). Обзоры космической науки. 15 (1): 121–146. Bibcode:1973ССРв ... 15..121С. Дои:10.1007 / BF00172440. Архивировано из оригинал (PDF) 21 октября 2011 г.
- ^ Фребель, Анна; Бирс, Тимоти С. (2018). «Формирование самых тяжелых элементов». Физика сегодня. 71 (1): 30–37. arXiv:1801.01190. Bibcode:2018ФТ .... 71а..30Ф. Дои:10.1063 / pt.3.3815. ISSN 0031-9228.
- ^ а б Roederer, I.U .; Kratz, K.-L .; Frebel, A .; и другие. (2009). «Конец нуклеосинтеза: производство свинца и тория в ранней галактике». Астрофизический журнал. 698 (2): 1963–1980. arXiv:0904.3105. Bibcode:2009ApJ ... 698.1963R. Дои:10.1088 / 0004-637X / 698/2/1963.
- ^ Burbidge, E.M .; Burbidge, G.R .; Fowler, W.A .; и другие. (1957). «Синтез элементов в звездах» (PDF). Обзоры современной физики. 29 (4): 547. Bibcode:1957РвМП ... 29..547Б. Дои:10.1103 / RevModPhys.29.547.
- ^ Клейтон, Д. (1968). Принципы звездной эволюции и нуклеосинтеза. McGraw-Hill Education. стр.577–591. ISBN 978-0-226-10953-4.
- ^ Штолл 2005, п. 2.
- ^ Гринвуд и Эрншоу 1997, п. 1294.
- ^ Альбаред, Ф. (2003). Геохимия: введение. Издательство Кембриджского университета. п. 17. ISBN 978-0-521-89148-6.
- ^ Тренн, Т. Дж. (1978). «Торуран (U-236) как вымерший естественный родитель тория: преждевременная фальсификация существенно правильной теории». Анналы науки. 35 (6): 581–597. Дои:10.1080/00033797800200441.
- ^ Diamond, H .; Фридман, А. М .; Gindler, J. E .; и другие. (1956). «Возможное наличие см247 или его дочери в природе ». Физический обзор. 105 (2): 679–680. Bibcode:1957ПхРв..105..679Д. Дои:10.1103 / PhysRev.105.679.
- ^ Rao, M. N .; Гопалан, К. (1973). «Кюрий-248 в ранней Солнечной системе». Природа. 245 (5424): 304–307. Bibcode:1973Натура.245..304Р. Дои:10.1038 / 245304a0.
- ^ Розенблатт, Д. Б. (1953). "Эффекты Первобытного Дара U236". Физический обзор. 91 (6): 1474–1475. Bibcode:1953ПхРв ... 91.1474Р. Дои:10.1103 / PhysRev.91.1474.
- ^ Gando, A .; Gando, Y .; Ichimura, K .; и другие. (2011). «Модель частичного радиогенного тепла Земли, выявленная с помощью измерений геонейтрино» (PDF). Природа Геонауки. 4 (9): 647–651. Bibcode:2011NatGe ... 4..647K. Дои:10.1038 / ngeo1205.
- ^ Пеппард, Д. Ф .; Mason, G.W .; Gray, P.R .; и другие. (1952). «Возникновение (4п + 1) Серия в природе ». Журнал Американского химического общества. 74 (23): 6081–6084. Дои:10.1021 / ja01143a074.
- ^ а б c d е ж грамм час я Wickleder, Fourest & Dorhout, 2006 г. С. 55–56.
- ^ Агентство регистрации токсичных веществ и заболеваний (2016). Торий (PDF) (Отчет). Получено 30 сентября 2017.
- ^ Вудхед, Дж. А. (1991). «Метамиктизация циркона: дозозависимые структурные характеристики» (PDF). Американский минералог. 76: 74–82.
- ^ Шиманский, Дж. Т. (1982). «Минералогическое исследование и определение кристаллической структуры неметамидного эканита ThCa.2Si8О20" (PDF). Канадский минералог. 20: 65–75.
- ^ Гринвуд и Эрншоу 1997, п. 1255.
- ^ "Битва Тора с гигантами". Google Искусство и культура. Получено 26 июн 2016.
- ^ а б Fontani, M .; Costa, M .; Орна, В. (2014). Утраченные элементы: теневая сторона Периодической таблицы. Издательство Оксфордского университета. п. 73. ISBN 978-0-19-938334-4.
- ^ Рябчиков, Д. И .; Гольбрайх Е. К. (2013). Аналитическая химия тория: Международная серия монографий по аналитической химии. Эльзевир. п. 1. ISBN 978-1-4831-5659-0.
- ^ Томсон, Т. (1831). Система химии неорганических тел.. 1. Болдуин и Крэдок и Уильям Блэквуд. п. 475.
- ^ Берцелиус, Дж. Дж. (1824 г.). "Undersökning af några Mineralier. 1. Phosphorsyrad Ytterjord" [Изучение некоторых минералов. 1-й фосфорный оксид иттрия.]. Kungliga Svenska Vetenskapsakademiens Handlingar (на шведском языке). 2: 334–338.
- ^ "Ксенотим- (Y)". База данных Миндат. Получено 7 октября 2017.
- ^ Сельбекк, Р. С. (2007). "Мортен Трейн Эсмарк". Магазин норске лексикон (на норвежском языке). Kunnskapsforlaget. Получено 16 мая 2009.
- ^ а б Уикс, М.Э. (1932). «Открытие элементов. XI. Некоторые элементы, выделенные с помощью калия и натрия: цирконий, титан, церий и торий». Журнал химического образования. 9 (7): 1231. Bibcode:1932JChEd ... 9.1231W. Дои:10.1021 / ed009p1231.
- ^ Берцелиус, Дж. Дж. (1829 г.). "Untersuchung eines neues Minerals und einer darin erhalten zuvor unbekannten Erde" [Исследование нового минерала и содержащейся в нем ранее неизвестной земли]. Annalen der Physik und Chemie (на немецком). 16 (7): 385–415. Bibcode:1829АнП .... 92..385Б. Дои:10.1002 / andp.18290920702. (современное цитирование: Annalen der Physik, т. 92, нет. 7. С. 385–415).
- ^ Берцелиус, Дж. Дж. (1829 г.). «Подземный минерал (торит), som innehåller en förut obekant jord» [Исследование нового минерала (торита), содержащегося в ранее неизвестной земле]. Kungliga Svenska Vetenskaps Akademiens Handlingar (на шведском языке): 1–30.
- ^ Шиллинг, Дж. (1902). "Die eigentlichen Thorit-Mineralien (Thorit und Orangit)" [Актуальные торитовые минералы (торит и орангит)]. Zeitschrift für Angewandte Chemie (на немецком). 15 (37): 921–929. Дои:10.1002 / ange.19020153703.
- ^ Лич, М. Р. "Интернет-база данных периодических таблиц: таблица электроотрицательности Берцелиуса". Получено 16 июля 2016.
- ^ Нильсон, Л. Ф. (1882). "Über Metallisches Thorium" [О металлическом тории]. Berichte der Deutschen Chemischen Gesellschaft (на немецком). 15 (2): 2537–2547. Дои:10.1002 / cber.188201502213.
- ^ а б Мейстер, Г. (1948). Производство редких металлов (PDF) (Отчет). Комиссия по атомной энергии США. Получено 22 сентября 2017.
- ^ а б c d Лич, М. Р. «Интернет-база данных периодических таблиц». Получено 14 мая 2012.
- ^ Дженсен, Уильям Б. (2003). «Место цинка, кадмия и ртути в Периодической таблице» (PDF). Журнал химического образования. 80 (8): 952–961. Bibcode:2003JChEd..80..952J. Дои:10.1021 / ed080p952. Архивировано из оригинал (PDF) 11 июня 2010 г.
- ^ а б Masterton, W. L .; Hurley, C.N .; Нет, Э. Дж. (2011). Химия: принципы и реакции (7-е изд.). Cengage Learning. п. 173. ISBN 978-1-111-42710-8.
- ^ Wickleder, Fourest & Dorhout, 2006 г., п. 52.
- ^ Кюри, М. (1898). "Rayons émis par les composés de l'uranium et du торий" [Лучи, излучаемые соединениями урана и тория]. Comptes Rendus (На французском). 126: 1101–1103. ПР 24166254M.
- ^ Шмидт, Г.С. (1898). "Über die vom Thorium und den Thoriumverbindungen ausgehende Strahlung" [О радиации, испускаемой соединениями тория и тория]. Verhandlungen der Physikalischen Gesellschaft zu Berlin (Труды Физического общества в Берлине) (на немецком). 17: 14–16.
- ^ Шмидт, Г. К. (1898). "Über die von den Thorverbindungen und einigen anderen Substanzen ausgehende Strahlung" [О излучении соединений тория и некоторых других веществ]. Annalen der Physik und Chemie (на немецком). 65 (5): 141–151. Bibcode:1898АнП ... 301..141С. Дои:10.1002 / andp.18983010512. (современное цитирование: Annalen der Physik, т. 301. С. 141–151 (1898)).
- ^ Резерфорд, Э.; Оуэнс, Р. Б. (1899 г.). «Ториевое и урановое излучение». Пер. R. Soc. Может. 2: 9–12.: «Излучение оксида тория не было постоянным, но изменялось самым причудливым образом», в то время как «Все соединения урана испускают удивительно постоянное излучение».
- ^ Симмонс, Дж. Г. (1996). The Scientific 100: рейтинг самых влиятельных ученых прошлого и настоящего. Кэрол. п.19. ISBN 978-0-8065-2139-8.
- ^ Фроман, Н. (1996). «Мария и Пьер Кюри и открытие полония и радия». nobelprize.org. Nobel Media AB. Получено 11 мая 2017.
- ^ а б Бернс, М. (1987). Регулирование низкоактивных радиоактивных отходов - наука, политика и страх. CRC Press. С. 24–25. ISBN 978-0-87371-026-8.
- ^ ван Спронсен, Дж. У. (1969). Периодическая система химических элементов. Эльзевир. С. 315–316. ISBN 978-0-444-40776-4..
- ^ Родс, Р. (2012). Создание атомной бомбы (25-летие изд.). Саймон и Шустер. С. 221–222, 349. ISBN 978-1-4516-7761-4.
- ^ Türler, A .; Букланов, Г. В .; Eichler, B .; и другие. (1998). «Доказательства релятивистских эффектов в химии 104-го элемента». Журнал сплавов и соединений. 271–273: 287. Дои:10.1016 / S0925-8388 (98) 00072-3.
- ^ Kratz, J. V .; Нагаме, Ю. (2014). «Жидкофазная химия сверхтяжелых элементов». В Schädel, M .; Шонесси, Д. (ред.). Химия сверхтяжелых элементов (2-е изд.). Springer-Verlag. п. 335. Дои:10.1007/978-3-642-37466-1. ISBN 978-3-642-37465-4.
- ^ а б c d Furuta, E .; Yoshizawa, Y .; Абураи, Т. (2000). «Сравнение радиоактивных и нерадиоактивных газовых мантий фонарей». J. Radiol. Prot. 20 (4): 423–431. Bibcode:2000JRP .... 20..423F. Дои:10.1088/0952-4746/20/4/305. PMID 11140713.
- ^ Департамент здравоохранения Нью-Джерси (1996 г.). «Здоровье и опасные отходы» (PDF). Руководство для практикующих по воздействию окружающей среды для пациентов. 1 (3): 1–8. Архивировано из оригинал (PDF) 15 апреля 2016 г.
- ^ Топкер, Терренс П. (1996). «Торий и иттрий в мантии газовых фонарей». Американский журнал физики. 64 (2): 109. Bibcode:1996AmJPh..64..109T. Дои:10.1119/1.18463.
- ^ а б Poljanc, K .; Steinhauser, G .; Sterba, J. H .; и другие. (2007). «За пределами низкой активности: на« нерадиоактивной »газовой мантии». Наука об окружающей среде в целом. 374 (1): 36–42. Bibcode:2007ScTEn.374 ... 36P. Дои:10.1016 / j.scitotenv.2006.11.024. PMID 17270253.
- ^ Казими, М. (2003). «Ториевое топливо для атомной энергетики». Американский ученый. Архивировано из оригинал 1 января 2017 г.. Получено 29 сентября 2017.
- ^ Majumdar, S .; Пурушотам, Д.С.С. (1999). «Опыт разработки ториевого топлива в Индии». Использование ториевого топлива: варианты и тенденции (PDF) (Отчет). Международное агентство по атомной энергии. Получено 7 октября 2017.
- ^ «Атомная энергетика в Индии». Всемирная ядерная ассоциация. 2017 г.. Получено 29 сентября 2017.
- ^ «IAEA-TECDOC-1450 Ториевый топливный цикл - потенциальные преимущества и проблемы» (PDF). Международное агентство по атомной энергии. 2005 г.. Получено 23 марта 2009.
- ^ Шиппорт Атомная электростанция. «Признанное историческое достижение: Атомная электростанция Шиппорт, национальный исторический памятник инженерной мысли» (PDF). п. 4. Архивировано из оригинал (PDF) 17 июля 2015 г.. Получено 24 июн 2006.
- ^ Образовательный фонд ядерной науки, Inc. Бюллетень ученых-атомщиков. С. 19–20. ISSN 0096-3402.
- ^ "IAEA-TECDOC-1349 Способность топливных циклов на основе тория ограничивать плутоний и снижать токсичность долгоживущих отходов" (PDF). Международное агентство по атомной энергии. 2002 г.. Получено 24 марта 2009.
- ^ Эванс, Б. (2006). «Ученый призывает перейти на торий». ABC News. Архивировано из оригинал 28 марта 2010 г.. Получено 17 сентября 2011.
- ^ Мартин, Р. (2009). "Уран - это последний век - введите торий, новую зеленую ядерную бомбу". Проводной. Получено 19 июн 2010.
- ^ Вайнберг, Элвин (1994). Первая ядерная эра: жизнь и времена технологического наладчика. Нью-Йорк: AIP Press. С. 36–38. ISBN 978-1-56396-358-2.
- ^ а б c «Торий». Всемирная ядерная ассоциация. 2017. Получено 21 июн 2017.
- ^ Вудс, В.К. (1966). LRL Интерес к U-233 (PDF) (Отчет). Battelle Memorial Institute. Дои:10.2172/79078. OSTI 79078.
- ^ «Классификационный бюллетень WNP-118» (PDF). Министерство энергетики США. 12 марта 2008 г.
- ^ Штолл 2005, п. 7.
- ^ Геологическая служба США (2012). «Торий» (PDF). Получено 12 мая 2017.
- ^ Джаярам, К. М. В. (1987). Обзор мировых ресурсов тория, стимулы для дальнейших исследований и прогноз потребностей в тории в ближайшем будущем (PDF) (Отчет). Департамент атомной энергии. Архивировано из оригинал (PDF) 28 июня 2011 г.
- ^ Торий. Статистика и информация (Отчет). Геологическая служба США. 2017. Получено 6 января 2018.
- ^ а б c d е ж грамм час Штолл 2005, п. 8.
- ^ а б c d е Штолл 2005, п. 32.
- ^ а б Штолл 2005, п. 31.
- ^ Матсон, Тим (2011). Книга неэлектрического освещения: классическое руководство по безопасному использованию свечей, топливных ламп, фонарей, газовых фонарей и каминных печей.. Countryman Press. п. 60. ISBN 978-1-58157-829-4.
- ^ Shaw, J .; Dunderdale, J .; Пэйнтер, Р.А. (9 июня 2005 г.). «Обзор потребительских товаров, содержащих радиоактивные вещества, в Европейском Союзе» (PDF). Департамент профессиональных услуг НРПБ.
- ^ Придхэм, Г.Дж. (2016). Электронные устройства и схемы. Содружество и международная библиотека: Отдел электротехники. Эльзевир. п. 105. ISBN 978-1-4831-3979-1.
- ^ Уттрахи, Дж. (2015). Weld Like a Pro: начиная с передовых технологий. CarTech Inc. стр. 42. ISBN 978-1-61325-221-5.
- ^ Джеффус, Л. (2016). Сварка: принципы и применение. Cengage Learning. п. 393. ISBN 978-1-305-49469-5.
- ^ «Торированный объектив камеры (ок. 1970-х годов)». Ассоциированные университеты Ок-Ридж. 1999 г.. Получено 29 сентября 2017.
- ^ Ранкур, JD (1996). Оптические тонкие пленки. Справочник пользователя. SPIE Press. п. 196. ISBN 978-0-8194-2285-9.
- ^ Kaiser, N .; Пулкер, Х. К. (2013). Покрытия для оптических помех. Springer. п. 111. ISBN 978-3-540-36386-6.
- ^ Ронен, Ю. (2006). «Правило определения делящихся изотопов». Ядерная наука и инженерия. 152 (3): 334–335. Дои:10.13182 / nse06-a2588. ISSN 0029-5639.
- ^ а б Ронен, Ю. (2010). «Несколько замечаний по делящимся изотопам». Анналы атомной энергетики. 37 (12): 1783–1784. Дои:10.1016 / j.anucene.2010.07.006.
- ^ "Плутоний". Всемирная ядерная ассоциация. 2017 г.. Получено 29 сентября 2017.
- ^ а б c Гринвуд и Эрншоу 1997, п. 1259.
- ^ «Интерактивная карта нуклидов». Брукхейвенская национальная лаборатория. Получено 12 августа 2013.
- ^ «Ториевое испытание начинается». Мировые ядерные новости. 2013. Получено 21 июля 2013.
- ^ «IAEA-TECDOC-1450 Ториевый топливный цикл - потенциальные преимущества и проблемы» (PDF). Международное агентство по атомной энергии. 2005 г.. Получено 23 марта 2009.
- ^ а б Лэнгфорд, Р. Э. (2004). Введение в оружие массового уничтожения: радиологическое, химическое и биологическое. Джон Вили и сыновья. п. 85. ISBN 978-0-471-46560-7.
- ^ Штолл 2005, п. 30.
- ^ а б Nakajima, Ts .; Гроулт, Х. (2005). Фторированные материалы для преобразования энергии. Эльзевир. С. 562–565. ISBN 978-0-08-044472-7.
- ^ Рис, Э. (2011). «Не верьте, что раскрутка тория - более экологичный вариант ядерной энергетики». Хранитель. Получено 29 сентября 2017.
- ^ Sovacool, B.K .; Валентин, С. В. (2012). Национальная политика в области ядерной энергетики: экономика, безопасность и управление. Рутледж. п. 226. ISBN 978-1-136-29437-2.
- ^ «Часто задаваемые вопросы по атомной энергии» (PDF). Аргоннская национальная лаборатория. 2014. Получено 13 января 2018.
- ^ Финдли, Т. (2011). Ядерная энергия и глобальное управление: обеспечение безопасности, защищенности и нераспространения. Рутледж. п. 9. ISBN 978-1-136-84993-0.
- ^ а б c «Торий: радиационная защита». Агентство по охране окружающей среды США. Архивировано из оригинал 1 октября 2006 г.. Получено 27 февраля 2016.
- ^ а б "Радиоактивность в мантии фонаря". Австралийское агентство радиационной защиты и ядерной безопасности. Архивировано из оригинал 14 октября 2007 г.. Получено 29 сентября 2017.
- ^ «Серия естественного распада: уран, радий и торий» (PDF). Аргоннская национальная лаборатория. 2005. Архивировано с оригинал (PDF) 17 августа 2016 г.. Получено 30 сентября 2017.
- ^ а б c d Штолл 2005, п. 35.
- ^ Luetzelschwab, J. W .; Гугинс, С. В. (1984). «Радиоактивность, выделяемая при горении кожухов газовых фонарей». Здоровье Phys. 46 (4): 873–881. Дои:10.1097/00004032-198404000-00013. PMID 6706595.
- ^ Huyskens, C.J .; Hemelaar, J. T .; Кикен, П. Дж. (1985). «Оценка доз воздействия радиоактивности в газовых оболочках». Sci. Total Environ. 45: 157–164. Bibcode:1985ScTEn..45..157H. Дои:10.1016/0048-9697(85)90216-5. PMID 4081711.
- ^ «Токсикологический профиль тория» (PDF). Агентство регистрации токсичных веществ и заболеваний Служба общественного здравоохранения США. 1990. стр. 4.
- ^ Меркель, Б .; Dudel, G .; и другие. (1988). Untersuchungen zur radiologischen Emission des Uran-Tailings Schneckenstein (PDF) (Отчет) (на немецком языке). Sächsisches Staatsministerium für Umwelt und Landesentwicklung. Архивировано из оригинал (PDF) 8 января 2013 г.
- ^ а б Штолл 2005, п. 34.
- ^ Jacobson, M .; Купер, А. Р .; Надь, Дж. (1964). Взрывоопасность металлических порошков (PDF) (Отчет). Министерство внутренних дел США. Получено 29 сентября 2017.
- ^ «Девять раненых в результате взрыва атомной лаборатории». Pittsburgh Post-Gazette. Ассошиэйтед Пресс. 1956. с. 2. Получено 29 сентября 2017.
- ^ «При взрыве в А-лаборатории радиационной угрозы не обнаружено». Санкт-Петербург Таймс. Ассошиэйтед Пресс. 1956. с. 2. Получено 29 сентября 2017.
- ^ Харрингтон, М. (2003). "Печальные воспоминания о взрыве в Сильвании 56 года". New York Newsday. Архивировано из оригинал 4 февраля 2012 г.. Получено 29 сентября 2017.
- ^ «Ториевый токсин» (PDF). Агентство регистрации токсичных веществ и заболеваний. Получено 29 сентября 2017.
- ^ «Сборник политических и законодательных положений, касающихся эксплуатации минералов пляжного песка». Департамент атомной энергии. Архивировано из оригинал 4 декабря 2008 г.. Получено 19 декабря 2008.
- ^ Pfeiffer, W.C .; Penna-Franca, E .; Ribeiro, C.C .; Nogueira, A. R .; Londres, H .; Оливейра, А. Э. (1981). «Измерения мощностей доз облучения окружающей среды на отдельных объектах в Бразилии». An. Акад. Бюстгальтеры. Ciênc. 53 (4): 683–691. PMID 7345962.
- ^ Альберичи, Эмма (29 января 2019 г.). «Суд над итальянскими военными заставляет подозревать связь между испытаниями оружия и врожденными дефектами на Сардинии». ABC News. Австралийская радиовещательная корпорация. Получено 29 января 2019.
Библиография
- Гринвуд, Н.; Эрншоу, А. (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- Столл, В. (2005). «Торий и соединения тория». Энциклопедия промышленной химии Ульмана. Wiley-VCH. Дои:10.1002 / 14356007.a27_001. ISBN 978-3-527-31097-5.
- Wickleder, M. S .; Fourest, B .; Дорхаут, П. К. (2006). «Торий». In Morss, L.R .; Эдельштейн, Н. М .; Фугер, Дж. (Ред.). Химия актинидных и трансактинидных элементов (PDF). 3 (3-е изд.). Springer-Verlag. С. 52–160. Дои:10.1007/1-4020-3598-5_3. ISBN 978-1-4020-3598-2. Архивировано из оригинал (PDF) 14 декабря 2017 г.
дальнейшее чтение
- Jordan, B.W .; Eggert, R .; Диксон, В .; и другие. (2014). «Торий: приводит ли изобилие коры к экономической доступности?» (PDF). Колорадская горная школа. Архивировано из оригинал (PDF) 30 июня 2017 г.. Получено 29 сентября 2017.
- Международное агентство по атомной энергии (2005 г.). Ториевый топливный цикл - потенциальные преимущества и проблемы
