Радиус атома - Atomic radius

В радиус атома из химический элемент это мера размера его атомы, обычно среднее или типичное расстояние от центра ядро к границе окружающей снаряды из электроны. Поскольку граница не является четко определенной физической сущностью, существуют различные неэквивалентные определения атомного радиуса. Три широко используемых определения атомного радиуса: Радиус Ван-дер-Ваальса, ионный радиус, и ковалентный радиус.
В зависимости от определения, термин может применяться только к изолированным атомам или также к атомам в конденсированное вещество, ковалентное связывание в молекулы, или в ионизированный и возбужденные состояния; и его значение может быть получено путем экспериментальных измерений или рассчитано на основе теоретических моделей. Значение радиуса может зависеть от состояния и контекста атома.[1]
Электроны не имеют определенных орбит или четко определенных диапазонов. Скорее их позиции должны быть описаны как распределения вероятностей которые постепенно сужаются по мере удаления от ядра, без резкого обрыва; они называются атомные орбитали или электронные облака. Более того, в конденсированных средах и молекулах электронные облака атомов обычно в некоторой степени перекрываются, и некоторые электроны могут перемещаться по большой области, охватывающей два или более атомов.
Согласно большинству определений радиусы изолированных нейтральных атомов составляют от 30 до 300. вечера (триллионных метра) или от 0,3 до 3 Ангстремс. Следовательно, радиус атома более чем в 10000 раз больше радиус его ядра (1–10 FM ),[2] и менее 1/1000 длина волны видимых свет (400–700 нм ).
Для многих целей атомы можно моделировать как сферы. Это только грубое приближение, но оно может дать количественные объяснения и предсказания для многих явлений, таких как плотность жидкостей и твердых тел, распространение жидкостей через молекулярные сита, расположение атомов и ионов в кристаллы, а размер и форма молекул.[нужна цитата ]
Атомные радиусы изменяются предсказуемым и объяснимым образом в периодическая таблица. Например, радиусы обычно уменьшаются вдоль каждого периода (строки) таблицы, начиная с щелочных металлов к благородные газы; и увеличивайте каждую группу (столбец). Радиус резко увеличивается между благородным газом в конце каждого периода и щелочным металлом в начале следующего периода. Эти тенденции изменения атомных радиусов (и различных других химических и физических свойств элементов) могут быть объяснены электронная оболочка теория атома; они предоставили важные доказательства для развития и подтверждения квантовая теория. Радиусы атомов уменьшаются по Периодической таблице, потому что по мере увеличения атомного номера количество протонов увеличивается по периоду, но дополнительные электроны добавляются только к той же квантовой оболочке. Следовательно, эффективный заряд ядра по отношению к самым удаленным электронам увеличивается, притягивая самые удаленные электроны ближе. В результате электронное облако сжимается и атомный радиус уменьшается.
История
В 1920 году, вскоре после того, как появилась возможность определять размеры атомов с помощью Рентгеновская кристаллография, было высказано предположение, что все атомы одного элемента имеют одинаковые радиусы.[3] Однако в 1923 году, когда стало доступно больше данных о кристаллах, было обнаружено, что приближение атома как сферы не обязательно выполняется при сравнении одного и того же атома в разных кристаллических структурах.[4]
Определения
Широко используемые определения атомного радиуса включают:
- Радиус Ван-дер-Ваальса: в принципе, это половина минимального расстояния между ядрами двух атомов элемента, которые не связаны с одной и той же молекулой.[5]
- Ионный радиус: номинальный радиус ионов элемента в определенном состоянии ионизации, рассчитанный из расстояния между атомными ядрами в кристаллических солях, которые включают этот ион. В принципе, расстояние между двумя соседними противоположно заряженными ионами ( длина из ионная связь между ними) должна равняться сумме их ионных радиусов.[5]
- Ковалентный радиус: номинальный радиус атомов элемента при ковалентно связанный к другим атомам, как это следует из разделения между атомными ядрами в молекулах. В принципе, расстояние между двумя атомами, которые связаны друг с другом в молекуле (длина этой ковалентной связи), должно равняться сумме их ковалентных радиусов.[5]
- Металлический радиус: номинальный радиус атомов элемента при соединении с другими атомами посредством металлические облигации.[нужна цитата ]
- Радиус Бора: радиус орбиты электрона с наименьшей энергией, предсказанный Модель Бора атома (1913).[6][7] Это применимо только к атомам и ионам с одним электроном, таким как водород, однократно ионизированный гелий, и позитроний. Хотя сама модель в настоящее время устарела, радиус Бора для атома водорода по-прежнему считается важной физической постоянной.
Эмпирически измеренный атомный радиус
В следующей таблице показаны эмпирически измеренные ковалентный радиусы элементов, опубликованные Дж. С. Слейтер в 1964 г.[8] Значения указаны в пикометры (pm или 1 × 10−12 м), с точностью около 5 м. Оттенок рамки варьируется от красного до желтого по мере увеличения радиуса; серый цвет указывает на отсутствие данных.
| Группа (столбец) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |
| Период (ряд) | |||||||||||||||||||
| 1 | ЧАС 25 | Он | |||||||||||||||||
| 2 | Ли 145 | Быть 105 | B 85 | C 70 | N 65 | О 60 | F 50 | Ne | |||||||||||
| 3 | Na 180 | Mg 150 | Al 125 | Si 110 | п 100 | S 100 | Cl 100 | Ar | |||||||||||
| 4 | K 220 | Ca 180 | Sc 160 | Ti 140 | V 135 | Cr 140 | Mn 140 | Fe 140 | Co 135 | Ni 135 | Cu 135 | Zn 135 | Ga 130 | Ge 125 | Так как 115 | Se 115 | Br 115 | Kr | |
| 5 | Руб. 235 | Sr 200 | Y 180 | Zr 155 | Nb 145 | Пн 145 | Tc 135 | RU 130 | Rh 135 | Pd 140 | Ag 160 | Компакт диск 155 | В 155 | Sn 145 | Sb 145 | Te 140 | я 140 | Xe | |
| 6 | CS 260 | Ба 215 | * | Hf 155 | Та 145 | W 135 | Re 135 | Операционные системы 130 | Ir 135 | Pt 135 | Au 135 | Hg 150 | Tl 190 | Pb 180 | Би 160 | По 190 | В | Rn | |
| 7 | Пт | Ра 215 | ** | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ц | Og | |
| Лантаноиды | * | Ла 195 | Ce 185 | Pr 185 | Nd 185 | Вечера 185 | См 185 | ЕС 185 | Б-г 180 | Tb 175 | Dy 175 | Хо 175 | Э 175 | Тм 175 | Yb 175 | Лу 175 | |||
| Актиниды | ** | Ac 195 | Чт 180 | Па 180 | U 175 | Np 175 | Пу 175 | Am 175 | См | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||
Объяснение общих тенденций
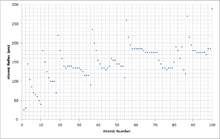
Изменение радиуса атома с увеличением атомный номер можно объяснить расположением электронов в оболочках фиксированной емкости. Оболочки обычно заполняются в порядке увеличения радиуса, так как отрицательно заряжен электроны притягиваются положительно заряженными протоны в ядре. По мере увеличения атомного номера вдоль каждой строки периодической таблицы дополнительные электроны переходят в ту же самую внешнюю оболочку; радиус которого постепенно сужается из-за увеличения заряда ядра. В благородном газе самая внешняя оболочка полностью заполнена; следовательно, дополнительный электрон следующего щелочного металла перейдет в следующую внешнюю оболочку, учитывая внезапное увеличение атомного радиуса.
Увеличивающийся заряд ядра частично уравновешивается увеличением количества электронов, явление, известное как защита; что объясняет, почему размер атомов обычно увеличивается в каждом столбце. Однако есть одно заметное исключение, известное как сокращение лантаноидов: блок элементов 5d намного меньше, чем можно было бы ожидать, из-за слабого экранирования 4f-электронов.
По сути, атомный радиус уменьшается через периоды из-за увеличения количества протонов. Следовательно, существует большее притяжение между протонами и электронами, потому что противоположные заряды притягиваются, и большее количество протонов создает более сильный заряд. Более сильное притяжение притягивает электроны ближе к протонам, уменьшая размер частицы. Следовательно, атомный радиус уменьшается. Вниз по группам атомный радиус увеличивается. Это потому, что существует больше уровней энергии и, следовательно, большее расстояние между протонами и электронами. Кроме того, защита электронов снижает притяжение, поэтому оставшиеся электроны могут уходить дальше от положительно заряженного ядра. Следовательно, размер (атомный радиус) увеличивается.
В следующей таблице приведены основные явления, влияющие на атомный радиус элемента:
| фактор | принцип | увеличиваться с ... | как правило | влияние на радиус |
|---|---|---|---|---|
| электронные оболочки | квантовая механика | главные и азимутальные квантовые числа | увеличивать каждый столбец | увеличивает атомный радиус |
| ядерный заряд | сила притяжения, действующая на электроны протонами в ядре | атомный номер | увеличиваются с каждым периодом (слева направо) | уменьшает атомный радиус |
| защита | сила отталкивания, действующая на электроны внешней оболочки внутренними электронами | количество электронов во внутренних оболочках | уменьшить влияние 2-го фактора | увеличивает атомный радиус |
Сокращение лантаноидов
Электроны в 4f-подоболочка, который постепенно заполняется от церий (Z = 58) в лютеций (Z = 71), не особенно эффективны при защите возрастающего ядерного заряда от более удаленных суб-оболочек. Элементы, следующие сразу за лантаноиды имеют атомные радиусы, которые меньше, чем можно было бы ожидать, и которые почти идентичны атомным радиусам элементов непосредственно над ними.[9] Следовательно гафний имеет практически такой же атомный радиус (и химический состав), что и цирконий, и тантал имеет атомный радиус, подобный ниобий, и так далее. Эффект сокращения лантаноидов заметен до платина (Z = 78), после чего маскируется релятивистский эффект известный как эффект инертной пары.
Из-за сокращения лантаноидов можно сделать 5 следующих наблюдений:
- Размер Ln3+ ионы регулярно убывают с атомным номером. Согласно с Правила фаянов, уменьшение размера Ln3+ ионов увеличивает ковалентный характер и снижает основной характер между Ln3+ и ОН− ионы в Ln (OH)3, до такой степени, что Yb (OH)3 и Лу (ОН)3 может с трудом растворяться в горячем концентрированном NaOH. Следовательно, порядок размера Ln3+ дано:
Ла3+ > Ce3+ > ..., ...> Лу3+. - Наблюдается закономерное уменьшение их ионных радиусов.
- Их тенденция действовать как восстановитель с увеличением атомного номера закономерно уменьшается.
- Второй и третий ряды переходных элементов d-блока довольно близки по свойствам.
- Следовательно, эти элементы встречаются вместе в природных минералах и их трудно разделить.
сокращение d-блока
Сокращение d-блока менее выражено, чем сокращение лантаноида, но возникает по той же причине. В этом случае именно плохая экранирующая способность 3d-электронов влияет на атомные радиусы и химический состав элементов, следующих сразу за первой строкой переходные металлы, от галлий (Z = 31) в бром (Z = 35).[9]
Расчетные атомные радиусы
В следующей таблице показаны атомные радиусы, рассчитанные на основе теоретических моделей, опубликованных Энрико Клементи и другие в 1967 году.[10] Значения указаны в пикометрах (пм).
| Группа (столбец) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |
| Период (ряд) | |||||||||||||||||||
| 1 | ЧАС 53 | Он 31 | |||||||||||||||||
| 2 | Ли 167 | Быть 112 | B 87 | C 67 | N 56 | О 48 | F 42 | Ne 38 | |||||||||||
| 3 | Na 190 | Mg 145 | Al 118 | Si 111 | п 98 | S 88 | Cl 79 | Ar 71 | |||||||||||
| 4 | K 243 | Ca 194 | Sc 184 | Ti 176 | V 171 | Cr 166 | Mn 161 | Fe 156 | Co 152 | Ni 149 | Cu 145 | Zn 142 | Ga 136 | Ge 125 | Так как 114 | Se 103 | Br 94 | Kr 88 | |
| 5 | Руб. 265 | Sr 219 | Y 212 | Zr 206 | Nb 198 | Пн 190 | Tc 183 | RU 178 | Rh 173 | Pd 169 | Ag 165 | Компакт диск 161 | В 156 | Sn 145 | Sb 133 | Te 123 | я 115 | Xe 108 | |
| 6 | CS 298 | Ба 253 | * | Hf 208 | Та 200 | W 193 | Re 188 | Операционные системы 185 | Ir 180 | Pt 177 | Au 174 | Hg 171 | Tl 156 | Pb 154 | Би 143 | По 135 | В 127 | Rn 120 | |
| 7 | Пт | Ра | ** | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ц | Og | |
| Лантаноиды | * | Ла 226 | Ce 210 | Pr 247 | Nd 206 | Вечера 205 | См 238 | ЕС 231 | Б-г 233 | Tb 225 | Dy 228 | Хо 226 | Э 226 | Тм 222 | Yb 222 | Лу 217 | |||
| Актиниды | ** | Ac | Чт | Па | U | Np | Пу | Am | См | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||
Заметки
- Разница между эмпирическими и экспериментальными данными: эмпирические данные в основном означают «происходящие из или основанные на наблюдении или опыте» или «полагающиеся только на опыт или наблюдение, часто без должного учета системных и теоретических данных».[11] По сути, это означает, что вы измерили его с помощью физических наблюдений и множества экспериментов, дающих те же результаты. Хотя обратите внимание, что значения не рассчитывается по формуле. Однако часто эмпирические результаты затем превращаются в уравнение оценки. С другой стороны, экспериментальные данные основаны только на теориях. Такие теоретические предсказания полезны, когда нет способов измерить радиусы экспериментально, если вы хотите предсказать радиус элемента, который еще не был обнаружен, или у него слишком короткий период полураспада.
Смотрите также
- Атомные радиусы элементов (страница данных)
- Химическая связь
- Ковалентный радиус
- Длина скрепления
- Стерическое препятствие
- Кинетический диаметр
использованная литература
- ^ Cotton, F. A .; Уилкинсон, Г. (1988). Продвинутая неорганическая химия (5-е изд.). Wiley. п. 1385. ISBN 978-0-471-84997-1.
- ^ Basdevant, J.-L .; Rich, J .; Спиро, М. (2005). Основы ядерной физики. Springer. п. 13, рис 1.1. ISBN 978-0-387-01672-6.
- ^ Брэгг, В. Л. (1920). «Расположение атомов в кристаллах». Философский журнал. 6. 40 (236): 169–189. Дои:10.1080/14786440808636111.
- ^ Вайкофф, Р. У. Г. (1923). "О гипотезе постоянных атомных радиусов". Труды Национальной академии наук Соединенных Штатов Америки. 9 (2): 33–38. Bibcode:1923ПНАС .... 9 ... 33Вт. Дои:10.1073 / pnas.9.2.33. ЧВК 1085234. PMID 16576657.
- ^ а б c Полинг, Л. (1945). Природа химической связи (2-е изд.). Издательство Корнельского университета. LCCN 42034474.
- ^ Бор, Н. (1913). «О строении атомов и молекул, часть I. - Связывание электронов положительными ядрами» (PDF). Философский журнал. 6. 26 (151): 1–24. Bibcode:1913ПМаг ... 26 .... 1Б. Дои:10.1080/14786441308634955. Получено 8 июн 2011.
- ^ Бор, Н. (1913). «О строении атомов и молекул, часть II. - Системы, содержащие только одно ядро» (PDF). Философский журнал. 6. 26 (153): 476–502. Bibcode:1913ПМаг ... 26..476Б. Дои:10.1080/14786441308634993. Получено 8 июн 2011.
- ^ Слейтер, Дж. К. (1964). «Атомные радиусы в кристаллах». Журнал химической физики. 41 (10): 3199–3205. Bibcode:1964ЖЧФ..41.3199С. Дои:10.1063/1.1725697.
- ^ а б Веселый, В. Л. (1991). Современная неорганическая химия (2-е изд.). Макгроу-Хилл. п. 22. ISBN 978-0-07-112651-9.
- ^ Clementi, E .; Raimond, D. L .; Райнхардт, У. П. (1967). "Константы экранирования атомов от функций SCF. II. Атомы с 37-86 электронами". Журнал химической физики. 47 (4): 1300–1307. Bibcode:1967ЖЧФ..47.1300С. Дои:10.1063/1.1712084.
- ^ https://www.merriam-webster.com/dictionary/empirical
