Гелий - Helium
 | ||||||||||||||||
| Гелий | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение | /ˈчасяляəм/ | |||||||||||||||
| Внешность | бесцветный газ с серым мутным свечением (или красновато-оранжевым, если используется особенно высокое напряжение) при помещении в электрическое поле | |||||||||||||||
| Стандартный атомный вес Аг, стд(Он) | 4.002602(2)[1] | |||||||||||||||
| Гелий в периодическая таблица | ||||||||||||||||
| ||||||||||||||||
| Атомный номер (Z) | 2 | |||||||||||||||
| Группа | группа 18 (благородные газы) | |||||||||||||||
| Период | период 1 | |||||||||||||||
| Блокировать | s-блок | |||||||||||||||
| Категория элемента | благородный газ | |||||||||||||||
| Электронная конфигурация | 1 с2 | |||||||||||||||
| Электронов на оболочку | 2 | |||||||||||||||
| Физические свойства | ||||||||||||||||
| Фаза вSTP | газ | |||||||||||||||
| Температура плавления | 0.95 K (-272,20 ° C, -457,96 ° F) (при 2,5 МПа) | |||||||||||||||
| Точка кипения | 4,222 К (-268,928 ° С, -452,070 ° F) | |||||||||||||||
| Плотность (на СТП) | 0,1786 г / л | |||||||||||||||
| в жидком состоянии (приm.p.) | 0,145 г / см3 | |||||||||||||||
| в жидком состоянии (приб.п.) | 0,125 г / см3 | |||||||||||||||
| Тройная точка | 2,177 К, 5,043 кПа | |||||||||||||||
| Критическая точка | 5,1953 К, 0,22746 МПа | |||||||||||||||
| Теплота плавления | 0.0138 кДж / моль | |||||||||||||||
| Теплота испарения | 0,0829 кДж / моль | |||||||||||||||
| Молярная теплоемкость | 20,78 Дж / (моль · К)[2] | |||||||||||||||
Давление газа (определяется ИТС-90 )
| ||||||||||||||||
| Атомные свойства | ||||||||||||||||
| Состояния окисления | 0 | |||||||||||||||
| Электроотрицательность | Шкала Полинга: нет данных | |||||||||||||||
| Энергии ионизации |
| |||||||||||||||
| Ковалентный радиус | 28 вечера | |||||||||||||||
| Радиус Ван-дер-Ваальса | 140 вечера | |||||||||||||||
| Другие свойства | ||||||||||||||||
| Естественное явление | изначальный | |||||||||||||||
| Кристальная структура | шестиугольный плотно упакованный (ГПУ) | |||||||||||||||
| Скорость звука | 972 РС | |||||||||||||||
| Теплопроводность | 0,1513 Вт / (м · К) | |||||||||||||||
| Магнитный заказ | диамагнитный[3] | |||||||||||||||
| Магнитная восприимчивость | −1.88·10−6 см3/ моль (298 К)[4] | |||||||||||||||
| Количество CAS | 7440-59-7 | |||||||||||||||
| История | ||||||||||||||||
| Именование | после Гелиос, Греческий Титан солнца | |||||||||||||||
| Открытие | Пьер Янссен, Норман Локьер (1868) | |||||||||||||||
| Первая изоляция | Уильям Рамзи, Пер Теодор Клев, Авраам Ланглет (1895) | |||||||||||||||
| Главный изотопы гелия | ||||||||||||||||
| ||||||||||||||||
Гелий (из Греческий: ἥλιος, романизированный: Гелиос, горит 'Солнце') химический элемент с символ Он и атомный номер 2. Это бесцветный, без запаха, без вкуса, нетоксичный, инертный, одноатомный газ, первый в благородный газ группа в периодическая таблица.[а] Его точка кипения самый низкий среди всех элементы. Гелий - второй по легкости и второй по величине обильный элемент в наблюдаемом вселенная (водород самый легкий и обильный). Он составляет около 24% от общей элементарной массы, что более чем в 12 раз превышает массу всех более тяжелых элементов вместе взятых. Его изобилие похоже на это как в солнце И в Юпитер. Это связано с очень высоким энергия связи ядра (на нуклон ) из гелий-4, по отношению к следующим трем элементам после гелия. Эта энергия связи гелия-4 также объясняет, почему он является продуктом обоих термоядерная реакция и радиоактивный распад. Большая часть гелия во Вселенной - это гелий-4, подавляющее большинство которого образовалось во время Большой взрыв. Большое количество нового гелия создается ядерным синтезом водорода в звезды.
Гелий назван в честь греческого Титан солнца, Гелиос. Впервые он был обнаружен как неизвестный желтый спектральная линия подпись в солнечном свете, во время солнечное затмение 1868 года к Жорж Райе,[11] Капитан К. Т. Хейг,[12] Норман Р. Погсон,[13] и лейтенант Джон Гершель,[14] и впоследствии было подтверждено французским астрономом, Жюль Янссен.[15] Janssen часто приписывают обнаружение элемента вместе с Норман Локьер. Янссен зарегистрировал спектральную линию гелия во время солнечного затмения 1868 года, а Локьер наблюдал ее из Великобритании. Локьер был первым, кто предположил, что линия связана с новым элементом, который он назвал. Формальный открытие элемента изготовлен в 1895 г. двумя Шведский химики, Пер Теодор Клев и Нильс Абрахам Ланглет, который обнаружил, что гелий выходит из уран руда, клевеит, который теперь рассматривается не как отдельный вид минералов, а как разновидность уранинита.[16][17] В 1903 г. были обнаружены большие запасы гелия в месторождения природного газа в некоторых частях Соединенных Штатов, которые на сегодняшний день являются крупнейшим поставщиком газа.
Жидкий гелий используется в криогеника (его крупнейшее разовое использование, поглощающее около четверти производства), особенно в охлаждение из сверхпроводящие магниты, при этом основное коммерческое приложение находится в МРТ сканеры. Другое промышленное использование гелия - в качестве газа для повышения давления и продувки, в качестве защитной атмосферы для дуговая сварка, а также в таких процессах, как выращивание кристаллов для получения кремниевые пластины - учет половины добытого газа. Хорошо известное, но второстепенное использование в качестве подъемный газ в шарики и дирижабли.[18] Как и в случае с любым газом, плотность которого отличается от плотности воздуха, вдыхание небольшого количества гелия временно изменяет тембр и качество звука. человеческий голос. В научных исследованиях поведение двух жидких фаз гелия-4 (гелия I и гелия II) важно для исследователей, изучающих квантовая механика (в частности, собственность сверхтекучесть ) и тем, кто смотрит на явления, такие как сверхпроводимость, произведенный в иметь значение возле абсолютный ноль.
На Земле относительно редко - 5,2. промилле по объему в атмосфера. В настоящее время большая часть земного гелия создается естественным путем. радиоактивный распад тяжелых радиоактивных элементов (торий и уран, хотя есть и другие примеры), поскольку альфа-частицы испускаемый такими распадами состоит из гелия-4 ядра. Этот радиогенный гелий улавливается натуральный газ в концентрациях до 7% по объему, из которых он извлекается в промышленных масштабах с помощью процесса низкотемпературного разделения, называемого фракционная перегонка. Раньше земной гелий был невозобновляемым ресурсом, потому что, попав в атмосферу, он быстро убегает в космос - считалось, что его не хватает.[19][20] Однако недавние исследования показывают, что гелий, образовавшийся глубоко под землей в результате радиоактивного распада, может накапливаться в запасах природного газа в больших, чем ожидалось, количествах.[21] в некоторых случаях из-за вулканической активности.[22]
История
Научные открытия
Первое свидетельство наличия гелия было обнаружено 18 августа 1868 года в виде ярко-желтой линии с длина волны 587,49 нм в спектр из хромосфера из солнце. Линия была обнаружена французским астрономом. Жюль Янссен в течение полное солнечное затмение в Гунтур, Индия.[23][24] Первоначально предполагалось, что эта линия будет натрий. 20 октября того же года английский астроном, Норман Локьер, наблюдал желтую линию в солнечном спектре, которую он назвал D3 потому что это было рядом с известным D1 и D2 Линия фраунгофера линии натрия.[25][26] Он пришел к выводу, что это было вызвано элементом Солнца, неизвестным на Земле. Локьер и английский химик Эдвард Франкленд назвал элемент греческим словом, обозначающим Солнце, ἥλιος (helios ).[27][28]

В 1881 г. итальянский физик Луиджи Палмьери впервые обнаружил гелий на Земле через его D3 спектральной линии, когда он анализировал материал, который был сублимированный во время недавнего извержения Гора Везувий.[29]


26 марта 1895 года шотландский химик, Сэр Уильям Рамзи, выделил гелий на Земле, обработав минерал клевеит (разнообразие уранинит не менее 10% редкоземельные элементы ) с минеральной кислоты. Рамзи искал аргон но после разделения азот и кислород из газа, освобожденного серная кислота, он заметил ярко-желтую линию, соответствующую букве D3 линия, наблюдаемая в спектре Солнца.[26][31][32][33] Эти образцы были идентифицированы как гелий Локьер и британский физик. Уильям Крукс.[34][35] Он был независимо выделен из клевеита в том же году химиками, Пер Теодор Клев и Авраам Ланглет, в Упсала, Швеция, которая собрала достаточно газа, чтобы точно определить атомный вес.[24][36][37] Гелий был также изолирован американским геохимиком, Уильям Фрэнсис Хиллебранд до открытия Рамзи, когда он заметил необычные спектральные линии во время тестирования образца минерала уранинита. Однако Хиллебранд приписал эти линии азоту.[38] Его поздравительное письмо Рамзи представляет собой интересный случай открытия и почти открытия в науке.[39]
В 1907 г. Эрнест Резерфорд и Томас Ройдс продемонстрировал, что альфа-частицы гелий ядра, позволяя частицам проникать через тонкую стеклянную стенку откачанной трубки, а затем создавая разряд в трубке, чтобы изучить спектр нового газа внутри.[40] В 1908 году голландский физик впервые сжижил гелий. Хайке Камерлинг-Оннес путем охлаждения газа до температуры менее 5 К (-268,15 ° C; -450,67 ° F).[41][42] Он попытался укрепить его, дополнительно снизив температуру, но ему это не удалось, потому что гелий не затвердевает при атмосферном давлении. Студент Оннеса Виллем Хендрик Кисом в итоге смог застыть на 1 см3 гелия в 1926 г. путем приложения дополнительного внешнего давления.[43][44]
В 1913 г. Нильс Бор опубликовал свою «трилогию»[45][46] по атомной структуре, что включало пересмотр Серия Пикеринга – Фаулера как центральное доказательство в поддержку его модель атома.[47][48] Эта серия названа в честь Эдвард Чарльз Пикеринг, опубликовавший в 1896 г. наблюдения ранее неизвестных линий в спектре звезды ζ Puppis[49] (теперь известно, что это происходит с Вольф – Райе и другие горячие звезды).[50] Пикеринг приписал наблюдение (строки 4551, 5411 и 10123).Å ) к новой форме водорода с полуцелыми уровнями перехода.[51][52] В 1912 г. Альфред Фаулер[53] удалось получить аналогичные линии из водородно-гелиевой смеси и поддержать вывод Пикеринга об их происхождении.[54] Модель Бора не допускает полуцелые переходы (как и квантовая механика), и Бор пришел к выводу, что Пикеринг и Фаулер были неправы, и вместо этого отнес эти спектральные линии к ионизированному гелию, He+.[55] Фаулер изначально был настроен скептически[56] но в конечном итоге был убежден[57] что Бор был прав,[45] и к 1915 году «спектроскописты окончательно перевели [серию Пикеринга – Фаулера] [с водорода] на гелий».[48][58] Теоретическая работа Бора над серией Пикеринга продемонстрировала необходимость «пересмотра проблем, которые, казалось, уже были решены в рамках классических теорий», и предоставила важное подтверждение его атомной теории.[48]
В 1938 г. русский физик Петр Леонидович Капица обнаружил, что гелий-4 почти нет вязкость при температурах около абсолютный ноль, явление, которое сейчас называется сверхтекучесть.[59] Это явление связано с Конденсация Бозе – Эйнштейна. В 1972 г. такое же явление наблюдалось в гелий-3, но при температурах, намного близких к абсолютному нулю, американские физики Дуглас Д. Ошерофф, Дэвид М. Ли, и Роберт С. Ричардсон. Считается, что явление в гелии-3 связано со спариванием гелия-3. фермионы сделать бозоны, по аналогии с Куперовские пары электронов, производящих сверхпроводимость.[60]
Добыча и использование

После бурения нефтяных скважин в 1903 г. в г. Декстер, Канзас произвел газовый гейзер, который не будет гореть, государственный геолог Канзаса Эразмус Хаворт собрали пробы выходящего газа и отнесли их обратно в Канзасский университет в Лоуренсе, где с помощью химиков Гамильтон Кэди и Дэвид Макфарланд, он обнаружил, что газ по объему состоит из 72% азота, 15% метан (а горючий процент только при достаточном количестве кислорода), 1% водород, и 12% - неидентифицируемый газ.[24][61] При дальнейшем анализе Кэди и Макфарланд обнаружили, что 1,84% пробы газа составлял гелий.[62][63] Это показало, что, несмотря на его общую редкость на Земле, гелий в больших количествах концентрировался под землей. Американские Великие равнины, доступный для экстракции как побочный продукт натуральный газ.[64]
Это позволило США стать ведущим поставщиком гелия в мире. По предложению сэра Ричард Трелфолл, то ВМС США спонсировал три небольших экспериментальных гелиевых завода во время Первой мировой войны. аэростаты заграждения с негорючим газом легче воздуха. Всего 5700 м3 (200 000 куб. Футов) 92% гелия было произведено в рамках программы, хотя ранее было получено менее кубического метра газа.[26] Часть этого газа была использована в первом в мире дирижабле, наполненном гелием, ВМС США. Дирижабль C-класса С-7, совершивший свой первый рейс из г. Хэмптон-роудс, Вирджиния, к Боллинг Филд в Вашингтоне, округ Колумбия, 1 декабря 1921 г.[65] почти за два года до первого жесткий гелиевый дирижабль Завод морской авиации -строенный USS Shenandoah, прилетел в сентябре 1923 г.
Хотя процесс экстракции с использованием низкотемпературных сжижение газа не был разработан вовремя, чтобы иметь значение во время Первой мировой войны, производство продолжалось. Гелий в основном использовался как подъемный газ в самолетах легче воздуха. Во время Второй мировой войны спрос на гелий для подъемного газа и на экранированную дугу увеличился. сварка. В гелиевый масс-спектрометр также был жизненно важен в атомной бомбе Манхэттенский проект.[66]
В правительство Соединенных Штатов создать Национальный гелиевый заповедник в 1925 г. Амарилло, Техас, с целью поставки военных дирижабли во время войны и коммерческих дирижаблей в мирное время.[26] Из-за Закон о гелии 1925 г., который запретил экспорт дефицитного гелия, на производство которого у США в то время была монополия, вместе с непомерно высокой стоимостью газа, Гинденбург, как и все немецкие Цеппелины, был вынужден использовать водород в качестве подъемного газа. Рынок гелия после Второй мировой войны находился в упадке, но в 1950-х годах резерв был расширен, чтобы обеспечить поставку гелия. жидкий гелий как хладагент для создания кислорода / водорода ракетное горючие (среди прочего) во время Космическая гонка и Холодная война. Использование гелия в США в 1965 году более чем в восемь раз превышало пиковое потребление военного времени.[67]
После «Поправок к Законам о гелии 1960 года» (Публичный закон 86–777), Горное бюро США организовал пять частных заводов по извлечению гелия из природного газа. За это сохранение гелия Программа Бюро построило трубопровод протяженностью 425 миль (684 км) от Буштон, Канзас, чтобы соединить эти заводы с правительственным частично истощенным газовым месторождением Клиффсайд недалеко от Амарилло, штат Техас. Эту гелий-азотную смесь вводили и хранили на газовом месторождении Клиффсайд до тех пор, пока она не потребовалась, после чего она была дополнительно очищена.[68]
К 1995 году было собрано миллиард кубометров газа, а резерв составлял 1,4 миллиарда долларов США в виде долга, что привело к Конгресс США в 1996 г. поэтапно ликвидировать заповедник.[24][69] Результирующий Закон о приватизации гелия 1996 г.[70] (Публичный закон 104–273) направил Министерство внутренних дел США чтобы опустошить резерв, продажи начнутся к 2005 году.[71]
Гелий, произведенный между 1930 и 1945 годами, имел чистоту около 98,3% (2% азота), что было достаточно для дирижаблей. В 1945 году для сварки было произведено небольшое количество гелия 99,9%. К 1949 году коммерческие количества гелия Grade A 99,95% были доступны.[72]
В течение многих лет Соединенные Штаты производили более 90% коммерческого гелия в мире, в то время как экстракционные заводы в Канаде, Польше, России и других странах производили остальное. В середине 1990-х годов новый завод в г. Арзев, Алжир, производящий 17 миллионов кубических метров (600 миллионов кубических футов), начал работу, при этом производства достаточно, чтобы покрыть все потребности Европы. Между тем, к 2000 году потребление гелия в США выросло до более чем 15 миллионов кг в год.[73] В 2004–2006 гг. Дополнительные заводы в г. Рас Лаффан, Катар, и Скикда, Алжир были построены. Алжир быстро стал вторым по величине производителем гелия.[74] За это время увеличилось как потребление гелия, так и затраты на его производство.[75] С 2002 по 2007 год цены на гелий выросли вдвое.[76]
По состоянию на 2012 год[Обновить], то Национальный гелиевый заповедник США приходится 30 процентов мирового гелия.[77] Ожидалось, что в 2018 году в резерве закончится гелий.[77] Несмотря на это, предложенный законопроект в Сенат США позволит заповеднику и дальше продавать газ. Другие крупные запасы были в Hugoton в Канзас, США и близлежащие газовые месторождения Канзаса и попрошайничает из Техас и Оклахома. Новые гелиевые заводы планировалось открыть в 2012 г. Катар, Россия и штат США Вайоминг, но не ожидалось, что они уменьшат дефицит.[77]
В 2013 году Катар запустил крупнейшую в мире гелиевую установку,[78] Хотя Катар дипломатический кризис 2017 сильно пострадало производство гелия там.[79] 2014 год был признан годом переизбытка гелия после многих лет известного дефицита.[80] Nasdaq сообщил (2015), что для Продукты Air, международной корпорации, которая продает газы для промышленного использования, объемы гелия остаются под экономическим давлением из-за ограничений с поставками сырья.[81]
Характеристики
Атом гелия
Эта секция нужны дополнительные цитаты для проверка. (Август 2020 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |

Гелий в квантовой механике
В перспективе квантовая механика, гелий - второй простейший атом моделировать, следуя атом водорода. Гелий состоит из двух электронов в атомные орбитали окружает ядро, содержащее два протона и (обычно) два нейтрона. Как и в механике Ньютона, никакая система, состоящая из более чем двух частиц, не может быть решена с помощью точного аналитического математического подхода (см. Проблема трех тел ) и гелий не исключение. Таким образом, требуются численно-математические методы даже для решения системы из одного ядра и двух электронов. Такой вычислительная химия были использованы методы для создания квантово-механической картины связывания электронов гелия с точностью до <2% от правильного значения за несколько вычислительных шагов.[82] Такие модели показывают, что каждый электрон в гелии частично экранирует ядро от другого, так что эффективный заряд ядра Z который видит каждый электрон, составляет около 1,69 единицы, а не 2 заряда классического «голого» ядра гелия.
Ядро атома гелия-4 идентично ядру альфа-частица. Эксперименты по рассеянию электронов при высоких энергиях показывают, что его заряд экспоненциально уменьшается от максимума в центральной точке, точно так же, как плотность заряда самого гелия. электронное облако. Эта симметрия отражает схожую физическую основу: пара нейтронов и пара протонов в ядре гелия подчиняются тем же квантово-механическим правилам, что и пара электронов гелия (хотя ядерные частицы подвержены другому потенциалу ядерной связи), так что все эти фермионы полностью занять 1 с орбитали попарно, ни один из них не обладает орбитальным угловым моментом, и каждый компенсирует собственный спин другого. Добавление еще одной из этих частиц потребовало бы углового момента и высвободило бы значительно меньше энергии (фактически, ни одно ядро с пятью нуклонами не является стабильным). Таким образом, такое расположение энергетически чрезвычайно устойчиво для всех этих частиц, и эта стабильность объясняет многие важные факты, касающиеся гелия в природе.
Например, стабильность и низкая энергия состояния электронного облака в гелии объясняют химическую инертность элемента, а также отсутствие взаимодействия атомов гелия друг с другом, что приводит к самым низким температурам плавления и кипения среди всех элементов.
Точно так же особая энергетическая стабильность ядра гелия-4, вызванная аналогичными эффектами, объясняет легкость образования гелия-4 в атомных реакциях, которые включают либо испускание тяжелых частиц, либо синтез. Некоторое количество стабильного гелия-3 (2 протона и 1 нейтрон) производится в реакциях синтеза из водорода, но это очень малая часть по сравнению с очень подходящим гелием-4.

Необычная стабильность ядра гелия-4 также важна. космологически: это объясняет тот факт, что в первые несколько минут после Большой взрыв Поскольку «суп» из свободных протонов и нейтронов, который первоначально был создан в соотношении примерно 6: 1, охладился до такой степени, что ядерное связывание стало возможным, почти все первые составные атомные ядра, которые образовались, были ядрами гелия-4. Связывание гелия-4 было настолько прочным, что образование гелия-4 потребляло почти все свободные нейтроны за несколько минут, прежде чем они могли бета-распадом, а также оставляло мало для образования более тяжелых атомов, таких как литий, бериллий или бор. Ядерная связь гелия-4 на нуклон сильнее, чем у любого из этих элементов (см. нуклеогенез и энергия связи ) и, таким образом, как только гелий был образован, не было энергии для создания элементов 3, 4 и 5. Для гелия было едва ли энергетически выгодно сливаться в следующий элемент с более низкой энергией на единицу. нуклон, углерод. Однако из-за отсутствия промежуточных элементов этот процесс требует, чтобы три ядра гелия столкнулись друг с другом почти одновременно (см. тройной альфа-процесс ). Таким образом, не было времени для образования значительного количества углерода в течение нескольких минут после Большого взрыва, до того, как ранняя расширяющаяся Вселенная остыла до температуры и давления, при которых синтез гелия с углеродом был невозможен. Это оставило раннюю Вселенную с очень похожим соотношением водорода / гелия, которое наблюдается сегодня (3 части водорода на 1 часть гелия-4 по массе), когда почти все нейтроны во Вселенной были захвачены гелием-4.
Таким образом, все более тяжелые элементы (включая те, которые необходимы для каменистых планет, таких как Земля, а также для углеродной или другой жизни) были созданы после Большого взрыва в звездах, которые были достаточно горячими, чтобы плавить сам гелий. Все элементы, кроме водорода и гелия, сегодня составляют всего 2% от массы атомной материи во Вселенной. Гелий-4, напротив, составляет около 23% обычного вещества Вселенной - почти все обычное вещество, не являющееся водородом.
Газовая и плазменная фазы

Гелий - второй наименее реактивный благородный газ после неон, и, следовательно, второй наименее реактивный из всех элементов.[83] это химически инертный и одноатомный во всех стандартных условиях. Из-за относительно низкой молярной (атомной) массы гелия его теплопроводность, удельная теплоемкость, и скорость звука в газовой фазе все больше, чем любой другой газ, кроме водород. По этим причинам и из-за небольшого размера одноатомных молекул гелия гелий распространяется через твердые тела в три раза быстрее воздуха и примерно на 65% быстрее водорода.[26]
Гелий наименее водо-растворимый одноатомный газ,[84] и один из наименее растворимых в воде газов (CF4, SF6, и C4F8 имеют более низкую растворимость мольных долей: 0,3802, 0,4394 и 0,2372 x2/10−5соответственно по сравнению с 0.70797 x2/10−5),[85] и гелий показатель преломления ближе к единице, чем у любого другого газа.[86] У гелия есть отрицательный Коэффициент Джоуля – Томсона при нормальной температуре окружающей среды, то есть при свободном расширении он нагревается. Только ниже своего Температура инверсии Джоуля – Томсона (примерно от 32 до 50 К при 1 атмосфере) охлаждает ли он при свободном расширении.[26] После предварительного охлаждения ниже этой температуры гелий может быть сжижен путем охлаждения расширением.
Больше всего внеземного гелия находится в плазма состояние, со свойствами, совершенно отличными от свойств атомарного гелия. В плазме электроны гелия не связаны с его ядром, что приводит к очень высокой электропроводности, даже если газ ионизирован лишь частично. На заряженные частицы сильно влияют магнитные и электрические поля. Например, в Солнечный ветер вместе с ионизированным водородом частицы взаимодействуют с земными магнитосфера, порождая Биркеланд течения и Аврора.[87]
Жидкий гелий

В отличие от любого другого элемента, гелий остается жидким до абсолютный ноль при нормальном давлении. Это прямой эффект квантовой механики: в частности, энергия нулевой точки системы слишком высоко, чтобы допустить замерзание. Для твердого гелия требуется температура 1–1,5 К (около –272 ° C или –457 ° F) при давлении около 25 бар (2,5 МПа).[88] Часто бывает трудно отличить твердый гелий от жидкого, поскольку показатель преломления двух фаз почти одинаковы. Твердое тело имеет острый температура плавления и имеет кристаллический структура, но очень сжимаемый; применение давления в лаборатории может уменьшить его объем более чем на 30%.[89] С объемный модуль из около 27 МПа[90] она в ~ 100 раз более сжимаема, чем вода. Твердый гелий имеет плотность 0.214±0,006 г / см3 при 1,15 К и 66 атм; расчетная плотность при 0 К и 25 бар (2,5 МПа) составляет 0.187±0,009 г / см3.[91] При более высоких температурах гелий затвердевает под достаточным давлением. При комнатной температуре для этого требуется около 114000 атм.[92]
Гелий I
Ниже его точка кипения 4,22 К (-268,93 ° C; -452,07 ° F) и выше лямбда-точка 2,1768 К (-270,9732 ° С; -455,7518 ° F), изотоп гелий-4 существует в обычном бесцветном жидком состоянии, называемом гелий I.[26] Как и другие криогенный В жидкостях гелий I кипит при нагревании и сжимается при понижении его температуры. Однако ниже лямбда-точки гелий не кипит и расширяется при дальнейшем понижении температуры.
Гелий I похож на газ показатель преломления 1,026, что делает его поверхность такой трудноразличимой, что всплывает Пенополистирол часто используются, чтобы показать, где находится поверхность.[26] Эта бесцветная жидкость имеет очень низкую вязкость и плотностью 0,145–0,125 г / мл (примерно от 0 до 4 К),[93] что составляет всего одну четвертую от ожидаемого значения классическая физика.[26] Квантовая механика необходимо для объяснения этого свойства, поэтому оба состояния жидкого гелия (гелий I и гелий II) называются квантовые жидкости, что означает, что они отображают атомные свойства в макроскопическом масштабе. Это может быть следствием того, что его температура кипения настолько близка к абсолютному нулю, что предотвращает случайное движение молекул (тепловая энергия ) от маскировки атомарных свойств.[26]
Гелий II
Жидкий гелий ниже его лямбда-точки (называемой гелий II) проявляет очень необычные характеристики. Из-за высокого теплопроводность, когда он кипит, он не пузырится, а испаряется прямо с его поверхности. Гелий-3 также есть сверхтекучий фаза, но только при гораздо более низких температурах; в результате о свойствах изотопа известно меньше.[26]

Гелий II является сверхтекучим, квантово-механическим состоянием (см .: макроскопические квантовые явления ) материи со странными свойствами. Например, когда он протекает через капилляры толщиной до 10−7 до 10−8 м не имеет измеримого вязкость.[24] Однако, когда измерения проводились между двумя движущимися дисками, наблюдалась вязкость, сопоставимая с вязкостью газообразного гелия. Текущая теория объясняет это с помощью двухжидкостная модель для гелия II. В этой модели жидкий гелий ниже лямбда-точки рассматривается как содержащий часть атомов гелия в основное состояние, которые являются сверхтекучими и текут с точно нулевой вязкостью, а также часть атомов гелия в возбужденном состоянии, которые ведут себя больше как обычная жидкость.[94]
в эффект фонтанастроится камера, которая соединяется с резервуаром с гелием II посредством спеченный диск, через который легко просачивается сверхтекучий гелий, но через который не может пройти несверхтекучий гелий. Если внутренняя часть контейнера нагревается, сверхтекучий гелий превращается в несверхтекучий гелий. Чтобы поддерживать равновесную долю сверхтекучего гелия, сверхтекучий гелий просачивается через него и увеличивает давление, заставляя жидкость фонтанировать из контейнера.[95]
Теплопроводность гелия II больше, чем у любого другого известного вещества, в миллион раз больше, чем у гелия I, и в несколько сотен раз больше, чем у гелия. медь.[26] Это потому, что теплопроводность происходит за счет исключительного квантового механизма. Большинство материалов, которые хорошо проводят тепло, имеют валентная полоса свободных электронов, которые служат для передачи тепла. Гелий II не имеет такой валентной зоны, но тем не менее хорошо проводит тепло. В поток тепла управляется уравнениями, аналогичными уравнениям волновое уравнение используется для характеристики распространения звука в воздухе. Когда вводится тепло, он движется со скоростью 20 метров в секунду при 1,8 К через гелий II в виде волн в явлении, известном как второй звук.[26]
Гелий II также проявляет эффект ползучести. Когда поверхность выходит за пределы уровня гелия II, гелий II движется по поверхности против силы сила тяжести. Гелий II выйдет из незапертого сосуда, ползая по бокам, пока не достигнет более теплой области, где он испарится. Он движется в 30нм -толстая пленка независимо от материала поверхности. Этот фильм называется Роллин фильм и назван в честь человека, который первым охарактеризовал эту черту, Бернар В. Роллин.[26][96][97] В результате такого ползучести и способности гелия II быстро просачиваться через крошечные отверстия очень трудно удерживать жидкий гелий. Если контейнер не будет тщательно сконструирован, гелий II будет ползать по поверхностям и через клапаны, пока не достигнет более теплого места, где он испарится. Волны, распространяющиеся по пленке Роллина, подчиняются тому же уравнению, что и гравитационные волны на мелководье, а не под действием силы тяжести, восстанавливающая сила - это сила Ван дер Ваальса.[98] Эти волны известны как третий звук.[99]
Изотопы
Известно девять изотопы гелия, но только гелий-3 и гелий-4 находятся стабильный. В атмосфере Земли один атом 3
Он на каждый миллион 4
Он.[24] В отличие от большинства элементов, изотопное содержание гелия сильно различается в зависимости от происхождения из-за различных процессов образования. Самый распространенный изотоп, гелий-4, производится на Земле альфа-распад более тяжелых радиоактивных элементов; Возникающие альфа-частицы представляют собой полностью ионизированные ядра гелия-4. Гелий-4 - необычайно стабильное ядро, потому что его нуклоны расположены в полные снаряды. Он также был образован в огромных количествах во время Нуклеосинтез Большого взрыва.[100]
Гелий-3 присутствует на Земле только в следовых количествах. Большая его часть присутствует с момента образования Земли, хотя некоторые из них падают на Землю в ловушке. космическая пыль.[101] Следы также производятся бета-распад из тритий.[102] Породы земной коры имеют изотопные отношения, изменяющиеся в десять раз, и эти отношения можно использовать для исследования происхождения горных пород и состава земной коры. мантия.[101] 3
Он в звездах гораздо больше, чем в результате ядерного синтеза. Таким образом, в межзвездная среда, доля 3
Он к 4
Он примерно в 100 раз выше, чем на Земле.[103] Внепланетный материал, такой как лунный и астероид реголит, имеют следы гелия-3 от бомбардировки солнечные ветры. В Луна На поверхности находится гелий-3 в концентрациях порядка 10 ppb, намного выше, чем примерно 5 ppt найдено в атмосфере Земли.[104][105] Некоторые люди, начиная с Джеральда Кульчински в 1986 году,[106] предложили исследовать Луну, добывать лунный реголит и использовать гелий-3 для слияние.
Жидкий гелий-4 можно охладить примерно до 1 К (-272,15 ° C; -457,87 ° F), используя охлаждение испарением в 1-к горшок. Подобное охлаждение гелия-3, имеющего более низкую температуру кипения, может достигать примерно 0,2 кельвина в гелий-3 холодильник. Равные смеси жидкости 3
Он и 4
Он ниже 0,8 К разделяются на две несмешивающиеся фазы из-за их несходства (они следуют разным квантовая статистика: атомы гелия-4 бозоны а атомы гелия-3 фермионы ).[26] Холодильники разбавления используйте эту несмешиваемость для достижения температуры в несколько милликельвинов.
Возможно изготовление экзотические изотопы гелия, которые быстро распадаются на другие вещества. Самый короткоживущий тяжелый изотоп гелия - гелий-5 с период полураспада из 7.6×10−22 s. Гелий-6 распадается, испуская бета-частица и имеет период полураспада 0,8 секунды. Гелий-7 также испускает бета-частицу, а также гамма-луч. Гелий-7 и гелий-8 создаются в определенных ядерные реакции.[26] Гелий-6 и гелий-8, как известно, проявляют ядерный ореол.[26]
Соединения

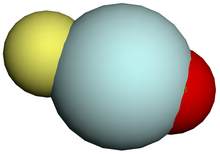
Гелий имеет валентность нулевого уровня и химически инертен при всех нормальных условиях.[89] Это электрический изолятор, если ионизированный. Как и другие благородные газы, гелий имеет метастабильную уровни энергии которые позволяют ему оставаться ионизированным в электрическом разряде с Напряжение ниже его потенциал ионизации.[26] Гелий может образовывать нестабильный соединения, известный как эксимеры, с вольфрамом, йодом, фтором, серой и фосфором, когда он подвергается воздействию тлеющий разряд, к бомбардировке электронами, или сводится к плазма другими способами. Молекулярные соединения HeNe, HgHe10, и WHe2, а молекулярные ионы Он+
2, Он2+
2, HeH+
, и HeD+
были созданы таким образом.[107] HeH+ также стабилен в основном состоянии, но чрезвычайно реактивен - это самый сильный Кислота Бренстеда известен, и поэтому может существовать только изолированно, так как он протонирует любую молекулу или противоанион, с которым контактирует. Этот метод также произвел нейтральную молекулу He2, который имеет большое количество ленточные системы, и HgHe, который, по-видимому, удерживается только поляризационными силами.[26]
Соединения Ван-дер-Ваальса гелия также может образовываться из криогенного газообразного гелия и атомов какого-либо другого вещества, например LiHe и Он2.[108]
Теоретически возможны и другие истинные соединения, такие как фторгидрид гелия (HHeF), который был бы аналогичен HArF, обнаруженный в 2000 году.[109] Расчеты показывают, что два новых соединения, содержащие гелий-кислородную связь, могут быть стабильными.[110] Два новых молекулярных вида, предсказанные с помощью теории, CsFHeO и N (CH3)4FHeO, являются производными метастабильного FHeO− теория аниона была впервые предложена в 2005 г. группой из Тайваня. В случае подтверждения экспериментом единственным оставшимся элементом без известных стабильных соединений будет неон.[111]
Атомы гелия внедрены в молекулы полого углеродного каркаса ( фуллерены ) нагреванием под высоким давлением. В эндоэдральные молекулы фуллерена сформированные устойчивы при высоких температурах. Когда образуются химические производные этих фуллеренов, гелий остается внутри.[112] Если гелий-3 используется, его легко наблюдать по гелию спектроскопия ядерного магнитного резонанса.[113] Сообщалось о многих фуллеренах, содержащих гелий-3. Хотя атомы гелия не связаны ковалентными или ионными связями, эти вещества обладают различными свойствами и определенным составом, как и все стехиометрические химические соединения.
Под высоким давлением гелий может образовывать соединения с различными другими элементами. Гелий-азотный клатрат (Курицы2)11) кристаллы были выращены при комнатной температуре и давлении ок. 10 ГПа в ячейка с алмазной наковальней.[114] В изоляционный электрид Na2Он было показано, что он термодинамически стабилен при давлениях выше 113 ГПа. Оно имеет флюорит структура.[115]
Возникновение и производство
Природное изобилие
Хотя гелий редко встречается на Земле, он является вторым по распространенности элементом в известной Вселенной, составляя 23% ее количества. барионный масса. Только водород более обильно.[24] Подавляющее большинство гелия образовано Нуклеосинтез Большого взрыва через одну-три минуты после Большого взрыва. Таким образом, измерения его распространенности вносят вклад в космологические модели. В звезды, он образован термоядерная реакция водорода в протон-протонные цепные реакции и Цикл CNO, часть звездный нуклеосинтез.[100]
в Атмосфера Земли объемная концентрация гелия составляет всего 5,2 частей на миллион.[116][117] Концентрация низкая и довольно постоянная, несмотря на непрерывное производство нового гелия, потому что большая часть гелия в атмосфере Земли убегает в космос несколькими процессами.[118][119][120] На Земле гетеросфера, часть верхних слоев атмосферы, гелий и другие более легкие газы являются наиболее распространенными элементами.
Большая часть гелия на Земле образуется в результате радиоактивный распад. Гелий в больших количествах содержится в минералах уран и торий, включая уранинит и его разновидности клевеит и уран,[16][121] карнотит и монацит (название группы; «монацит» обычно относится к монацит- (Ce) ),[122][123] потому что они испускают альфа-частицы (ядра гелия, He2+), с которой электроны немедленно объединяются, как только частица останавливается камнем. Таким образом, приблизительно 3000 метрических тонн гелия генерируются в год на всем протяжении литосфера.[124][125][126] В земной коре концентрация гелия составляет 8 частей на миллиард. В морской воде концентрация составляет всего 4 части на триллион. Также есть небольшие количества минеральных пружины, вулканический газ и метеоритное железо. Поскольку гелий улавливается под землей в условиях, в которых также происходит улавливание природного газа, наибольшие естественные концентрации гелия на планете находятся в природном газе, из которого извлекается большая часть коммерческого гелия. Концентрация варьируется в широком диапазоне от нескольких ppm до более 7% на небольшом газовом месторождении в Округ Сан-Хуан, Нью-Мексико.[127][128]
По состоянию на 2011 г.[Обновить] мировые запасы гелия оценивались в 40 миллиардов кубометров, из которых четверть приходилась на Газоконденсатное месторождение Южный Парс / Северный Купол принадлежат совместно Катар и Иран.[нужна цитата ] В 2015 и 2016 годах было объявлено, что дополнительные вероятные запасы находятся под Скалистыми горами в Северной Америке.[129] и в Восточноафриканский рифт.[130]
Современная добыча и распространение
Для крупномасштабного использования гелий извлекается фракционная перегонка из природного газа, который может содержать до 7% гелия.[131] Поскольку гелий имеет более низкую точка кипения чем любой другой элемент, низкая температура и высокое давление используются для сжижения почти всех других газов (в основном азот и метан ). Полученный сырой газообразный гелий очищается путем последовательного воздействия пониженных температур, при котором почти весь оставшийся азот и другие газы осаждаются из газовой смеси. Активированный уголь используется в качестве конечной стадии очистки, обычно приводящей к получению гелия Grade-A с чистотой 99,995%.[26] Основная примесь в гелии Grade-A: неон. На заключительном этапе производства большая часть производимого гелия сжижается с помощью криогенный процесс. Это необходимо для приложений, требующих жидкого гелия, а также позволяет поставщикам гелия снизить стоимость транспортировки на большие расстояния, поскольку самые большие контейнеры с жидким гелием имеют вместимость более чем в пять раз больше, чем самые большие прицепы с газообразным гелием.[74][132]
В 2008 году около 169 миллионов стандартные кубические метры (SCM) гелий был извлечен из природного газа или извлечен из запасов гелия, при этом примерно 78% из США, 10% из Алжира и большая часть оставшейся части из России, Польши и Катара.[133] К 2013 г. рост производства гелия в Катаре (в рамках компании РасГаз управляемый Air Liquide ) увеличил долю Катара в мировом производстве гелия до 25% и сделал его вторым по величине экспортером после США.[134]По оценкам, 54 миллиарда кубических футов (1,5×109 м3) месторождение гелия было обнаружено в Танзании в 2016 году.[135] Открыт крупный гелиевый завод в г. Нинся, Китай в 2020 году.[136]
В США большая часть гелия добывается из природного газа Hugoton и близлежащие газовые месторождения в Канзасе, Оклахома, и Пэнхэндл Филд в Техасе.[74][137] Большая часть этого газа когда-то отправлялась по трубопроводу в Национальный гелиевый заповедник, но с 2005 года этот резерв истощается и распродается, и ожидается, что он будет в значительной степени исчерпан к 2021 году,[134] под октябрь 2013 г. Закон об ответственном использовании и рациональном использовании гелия (HR 527).[138]
Распространение сырого природного газа через специальные полупроницаемые мембраны и другие барьеры - это еще один метод восстановления и очистки гелия.[139] В 1996 году в США доказано запасы гелия в таких газовых скважинных комплексах около 147 млрд стандартные кубические футы (4,2 млрд куб. М).[140] При темпах использования в то время (72 миллиона SCM в год в США; см. Круговую диаграмму ниже) этого было бы достаточно гелия примерно на 58 лет использования в США, и меньше этого (возможно, 80% времени) в мире. коэффициенты использования, хотя факторы экономии и обработки влияют на эффективные резервные числа.
Гелий необходимо извлекать из природного газа, потому что он присутствует в воздухе в размере лишь доли неона, но потребность в нем намного выше. Подсчитано, что если бы все производство неона было переоборудовано для экономии гелия, 0,1% мировых потребностей в гелии было бы удовлетворено. Точно так же только 1% мировой потребности в гелии может быть удовлетворен путем переоснащения всех установок воздушной дистилляции.[141] Гелий можно синтезировать путем бомбардировки литий или же бор протонами с высокой скоростью или бомбардировкой лития дейтроны, но эти процессы являются совершенно неэкономичным методом производства.[142]
Гелий коммерчески доступен в жидкой или газообразной форме. В виде жидкости он может поставляться в небольших изолированных контейнерах, называемых Дьюарс которые вмещают до 1000 литров гелия, или в больших контейнерах ISO с номинальной вместимостью до 42 м3 (около 11000 долларов США галлоны ). В газообразной форме небольшие количества гелия поставляются в баллонах высокого давления вместимостью до 8 м3.3 (около 282 стандартных кубических фута), в то время как большие объемы газа высокого давления поставляются в трубчатых прицепах вместимостью до 4860 м3.3 (приблизительно 172 000 стандартных кубических футов).
Защитники сохранения
По мнению защитников гелия, таких как физик, лауреат Нобелевской премии Роберт Коулман Ричардсон, написав в 2010 году, свободные рыночные цены на гелий способствовали «расточительному» использованию (например, для гелиевые шары ). Цены в 2000-х годах были снижены в связи с решением Конгресса США продать к 2015 году большие запасы гелия в стране.[143] По словам Ричардсона, цену нужно было умножить на 20, чтобы исключить чрезмерное расходование гелия. В своей книге Будущее гелия как природного ресурса (Routledge, 2012), Nuttall, Clarke & Glowacki (2012) также предложили создать Международное гелиевое агентство (IHA) для создания устойчивого рынка для этого драгоценного товара.[144]
Приложения

Расчетное использование фракционного гелия в США в 2014 г. по категориям. Общий объем использования составляет 34 миллиона кубических метров.[145]
Хотя воздушные шары - это, пожалуй, самое известное применение гелия, они составляют незначительную часть всего использования гелия.[69] Гелий используется для многих целей, для которых требуются некоторые его уникальные свойства, такие как низкий точка кипения, низкий плотность, низкий растворимость, высоко теплопроводность, или же инертность. Из общего объема производства гелия в мире в 2014 году, составляющего около 32 миллионов кг (180 миллионов стандартных кубических метров) гелия в год, наибольшее использование (около 32% от общего объема в 2014 году) приходится на криогенные приложения, большая часть которых связана с охлаждением сверхпроводящих магнитов в медицинский МРТ сканеры и ЯМР спектрометры.[146] Другими основными областями применения были системы нагнетания и продувки, сварка, поддержание контролируемой атмосферы и обнаружение утечек. Другие виды использования по категориям были относительно незначительными.[145]
Контролируемая атмосфера
Гелий используется в качестве защитного газа при выращивании кремний и германий кристаллы, в титан и цирконий производство, и в газовая хроматография,[89] потому что он инертен. В силу своей инертности термически и калорийно идеальный природа, высокая скорость звука, и высокая стоимость коэффициент теплоемкости, это также полезно в сверхзвуковые аэродинамические трубы[147] и импульсные устройства.[148]
Газовая вольфрамовая дуговая сварка
Гелий используется как защитный газ в дуговая сварка процессы с материалами, которые при температурах сварки загрязнены или ослаблены воздухом или азотом.[24] При сварке вольфрамовым электродом в газовой среде используется ряд инертных защитных газов, но вместо более дешевого используется гелий. аргон особенно для сварочных материалов с более высокой теплопроводность, подобно алюминий или же медь.
Незначительное использование
Обнаружение промышленных утечек

Одним из промышленных применений гелия является обнаружение утечки. Потому что гелий распространяется через твердые частицы в три раза быстрее, чем воздух, он используется как индикаторный газ для обнаружения утечки в высоковакуумном оборудовании (например, криогенных резервуарах) и контейнерах высокого давления.[149] Исследуемый объект помещается в камеру, которая затем откачивается и заполняется гелием. Гелий, выходящий через утечки, обнаруживается чувствительным устройством (гелиевый масс-спектрометр ), даже при величине утечки всего 10−9 мбар · л / с (10−10 Па · м3/ с). Процедура измерения обычно автоматическая и называется интегральным тестом гелия. Более простая процедура - заполнить тестируемый объект гелием и вручную найти утечки с помощью портативного устройства.[150]
Утечки гелия через трещины не следует путать с проникновением газа через сыпучий материал. Хотя для гелия задокументированы константы проницаемости (таким образом, рассчитываемая скорость проникновения) через стекла, керамику и синтетические материалы, инертные газы, такие как гелий, не проникают в большинство массивных металлов.[151]
Полет

Потому что это так легче воздуха, дирижабли а воздушные шары надувают гелием для поднимать. Хотя газообразный водород обладает большей плавучестью и не проникает через мембрану с меньшей скоростью, гелий имеет то преимущество, что он негорючий и действительно огнестойкий материал. Другое незначительное использование - в ракетная техника, где гелий используется в качестве незаполненный объем среда для вытеснения топлива и окислителей в резервуарах для хранения и для конденсации водорода и кислорода для получения ракетное горючие. Он также используется для продувки топлива и окислителя из наземного вспомогательного оборудования перед запуском и для предварительного охлаждения жидкого водорода в космические аппараты. Например, Сатурн V ракета, используемая в Программа Аполлон необходимо около 370000 м3 (13 миллионов кубических футов) гелия для запуска.[89]
Незначительное коммерческое и развлекательное использование
Гелий как дыхательный газ не имеет наркотические свойства, поэтому смеси гелия, такие как тримикс, гелиокс и heliair используются для глубокое погружение для уменьшения эффектов наркоза, которые усугубляются с увеличением глубины.[152][153] По мере того, как давление увеличивается с глубиной, плотность дыхательного газа также увеличивается, и обнаружено, что низкая молекулярная масса гелия значительно снижает усилие дыхания за счет снижения плотности смеси. Это снижает Число Рейнольдса потока, что приводит к уменьшению турбулентный поток и увеличение ламинарный поток, что требует меньшей работы дыхания.[154][155] На глубине менее 150 метров (490 футов) водолазы, дышащие гелиево-кислородными смесями, начинают испытывать тремор и снижение психомоторной функции, симптомы нервный синдром высокого давления.[156] Этому эффекту можно до некоторой степени противодействовать, добавляя некоторое количество наркотического газа, такого как водород или азот, в гелий-кислородную смесь.[157]
Гелий-неоновые лазеры газовый лазер малой мощности, излучающий красный луч, имел различные практические применения, в том числе считыватели штрих-кода и лазерные указки, прежде чем они были почти повсеместно заменены более дешевыми диодные лазеры.[24]
За инертность и высокую теплопроводность, нейтронная прозрачность, и поскольку он не образует радиоактивных изотопов в условиях реактора, гелий используется в качестве теплоносителя в некоторых газоохлаждаемых ядерные реакторы.[149]
Гелий, смешанный с более тяжелым газом, таким как ксенон, полезен для термоакустическое охлаждение из-за результирующего высокого коэффициент теплоемкости и низкий Число Прандтля.[158] Инертность гелия имеет экологические преимущества по сравнению с обычными холодильными системами, которые способствуют истощению озонового слоя или глобальному потеплению.[159]
Гелий также используется в некоторых жесткие диски.[160]
Научное использование
Использование гелия снижает искажающие эффекты колебаний температуры в пространстве между линзы в некоторых телескопы, из-за крайне низкого показатель преломления.[26] Этот метод особенно используется в солнечных телескопах, где вакуумная труба телескопа будет слишком тяжелой.[161][162]
Гелий - обычно используемый газ-носитель для газовая хроматография.
Возраст пород и минералов, содержащих уран и торий можно оценить, измерив уровень гелия с помощью процесса, известного как гелиевые датировки.[24][26]
Гелий при низких температурах используется в криогеника, и в некоторых приложениях криогеники. В качестве примеров приложений жидкий гелий используется для охлаждения некоторых металлов до чрезвычайно низких температур, необходимых для сверхпроводимость, например, в сверхпроводящие магниты за магнитно-резонансная томография. В Большой адронный коллайдер в ЦЕРН использует 96 метрических тонн жидкого гелия для поддержания температуры на уровне 1,9 К (-271,25 ° C; -456,25 ° F).[163]
Медицинское использование
Гелий был одобрен для медицинского использования в США в апреле 2020 года для людей и животных.[164][165]
Как загрязнитель
Несмотря на то, что он химически инертен, загрязнение гелием ухудшает работу микроэлектромеханические системы такие, что айфоны могут выйти из строя.[166]
Вдыхание и безопасность
Последствия
Нейтральный гелий при стандартных условиях не токсичен, не играет биологической роли и в следовых количествах содержится в крови человека.
В скорость звука в гелии почти в три раза превышает скорость звука в воздухе. Поскольку собственная резонансная частота заполненной газом полости пропорциональна скорости звука в газе, при вдыхании гелия происходит соответствующее увеличение резонансные частоты из голосовой тракт, который является усилителем вокального звука.[24][167] Это увеличение резонансной частоты усилителя (речевого тракта) дает повышенное усиление высокочастотных компонентов звуковой волны, создаваемой прямой вибрацией голосовых связок, по сравнению со случаем, когда голосовой ящик заполнен воздухом. . Когда человек говорит после вдыхания газообразного гелия, мышцы, которые управляют голосовым ящиком, продолжают двигаться так же, как когда голосовой ящик заполнен воздухом, поэтому основная частота (иногда называют подача ) от прямой вибрации голосовых связок не меняется.[168] Однако усиление, предпочтительное для высоких частот, вызывает изменение тембр усиленного звука, в результате чего вокал становится тростниковым, похожим на утку. Противоположный эффект - понижение резонансных частот - можно получить, вдыхая плотный газ, такой как гексафторид серы или же ксенон.
Опасности
Вдыхание гелия в чрезмерных количествах может быть опасным, поскольку гелий - это простое средство. удушающий и таким образом вытесняет кислород, необходимый для нормального дыхания.[24][169] Были зарегистрированы смертельные случаи, в том числе молодой человек, задохнувшийся в Ванкувере в 2003 году, и двое взрослых, задохнувшиеся в Южной Флориде в 2006 году.[170][171] В 1998 году австралийская девушка из Виктории потеряла сознание и временно потеряла сознание. посинел после вдыхания всего содержимого воздушного шара.[172][173][174]Вдыхание гелия непосредственно из баллонов под давлением или даже клапанов наполнения баллонов чрезвычайно опасно, так как высокая скорость потока и давление могут привести к баротравма, смертельный разрыв легочной ткани.[169][175]
Смерть от гелия случается редко. Первый зарегистрированный в СМИ случай произошел с 15-летней девушкой из Техаса, которая умерла в 1998 году от отравления гелием на вечеринке у друга; точный тип гелиевой смерти не установлен.[172][173][174]
В Соединенных Штатах в период с 2000 по 2004 год было зарегистрировано только два смертельных случая, включая человека, который умер в Северной Каролине от баротравмы в 2002 году.[170][175] Юноша задохнулся в Ванкувере в 2003 году, а у 27-летнего мужчины в Австралии после дыхания из баллона в 2000 году возникла эмболия.[170] С тех пор двое взрослых задохнулись в Южной Флориде в 2006 году.[170][171][176] В 2009 и 2010 годах были случаи, когда один юноша из Калифорнии был найден с сумкой на голове, прикрепленной к баллону с гелием,[177] и еще один подросток в Северной Ирландии умер от удушья.[178] В Игл-Пойнт, Орегон девочка-подросток умерла в 2012 году от баротравмы на вечеринке.[179][180][181] Позднее в том же году девушка из Мичигана умерла от гипоксии.[182]
4 февраля 2015 года стало известно, что во время записи их основного телешоу 28 января 12-летняя участница (имя не разглашается) японской певческой группы. 3Б Юниор страдал от воздушная эмболия, теряя сознание и впадая в кома в результате пузырьков воздуха, блокирующих приток крови к мозгу после вдыхания огромного количества гелия во время игры. Об инциденте стало известно только неделю спустя.[183][184] Персонал ТВ Асахи провела экстренную пресс-конференцию, чтобы сообщить, что участница была доставлена в больницу и демонстрирует признаки реабилитации, такие как движение глаз и конечностей, но ее сознание еще не полностью восстановилось. Полиция начала расследование в связи с пренебрежением мерами безопасности.[185][186]
Вопросы безопасности для криогенного гелия аналогичны вопросам безопасности. жидкий азот; его чрезвычайно низкие температуры могут привести к холодные ожоги, а степень расширения жидкости и газа может вызвать взрыв, если не установлены устройства для сброса давления. С контейнерами с газообразным гелием при температуре от 5 до 10 К следует обращаться как с жидким гелием из-за быстрого и значительного тепловое расширение что происходит, когда газообразный гелий при температуре менее 10 К нагревается до комнатная температура.[89]
При высоких давлениях (более 20 атм.МПа ), смесь гелия и кислорода (гелиокс ) может привести к нервный синдром высокого давления своего рода обратно-анестезирующий эффект; добавление небольшого количества азота к смеси может облегчить проблему.[187][156]
Смотрите также
Примечания
- ^ Некоторые авторы оспаривают размещение гелия в колонке с благородным газом, предпочитая размещать его выше. бериллий с щелочноземельные металлы. Они делают это на основании гелиевых единиц.2 электронная конфигурация, аналогичная нс2 валентные конфигурации щелочноземельных металлов и, кроме того, указывают на некоторые специфические тенденции, которые более регулярны для гелия, чем для бериллия.[5][6][7][8][9] Однако отнесение гелия к другим благородным газам остается почти универсальным, поскольку его необычайная инертность чрезвычайно близка к инертности других легких благородных газов - неона и аргона.[10]
Рекомендации
- ^ Мейя, Юрис; и другие. (2016). «Атомный вес элементов 2013 (Технический отчет IUPAC)». Чистая и прикладная химия. 88 (3): 265–91. Дои:10.1515 / pac-2015-0305.
- ^ Шуэн-Чен Хван, Роберт Д. Лейн, Дэниел А. Морган (2005). "Благородные газы". Энциклопедия химической технологии Кирка Отмера. Вайли. С. 343–383. DOI: 10.1002 / 0471238961.0701190508230114.a01.
- ^ Магнитная восприимчивость элементов и неорганических соединений, в Справочнике по химии и физике, 81-е издание, CRC press.
- ^ Weast, Роберт (1984). CRC, Справочник по химии и физике. Бока-Ратон, Флорида: Издательство Chemical Rubber Company. стр. E110. ISBN 0-8493-0464-4.
- ^ Грохала, Войцех (1 ноября 2017 г.). «О положении гелия и неона в Периодической таблице элементов». Основы химии. 20 (2018): 191–207. Дои:10.1007 / s10698-017-9302-7.
- ^ Бент Веберг, Либби (18 января 2019 г.). """Таблица Менделеева". Новости химии и машиностроения. 97 (3). Получено 27 марта 2020.
- ^ Грандинетти, Феличе (23 апреля 2013 г.). «Неон за вывесками». Химия природы. 5 (2013): 438. Bibcode:2013НатЧ ... 5..438Г. Дои:10.1038 / nchem.1631. PMID 23609097. Получено 27 марта 2019.
- ^ Курушкин, Михаил (2020). «Место гелия в Периодической таблице с точки зрения кристаллической структуры». IUCrJ. 7 (4): 577–578. Дои:10.1107 / S2052252520007769. ЧВК 7340260. PMID 32695406. Получено 19 июн 2020.
- ^ Лабарка, Мартин; Шриватс, Акаши (2016). «О размещении водорода и гелия в периодической системе: новый подход». Болгарский журнал естественнонаучного образования. 25 (4): 514–530. Получено 19 июн 2020.
- ^ Льюарс, Эррол Г. (5 декабря 2008 г.). Моделирование чудес: вычислительное ожидание новых молекул. Springer Science & Business Media. С. 69–71. ISBN 978-1-4020-6973-4. В архиве из оригинала 19 мая 2016 г.
- ^ Райе, Г. (1868) "Анализировать спектральные протуберанцы наблюдений, кулон l'éclipse totale de Soleil visible le 18 août 1868, à la presqu'île de Malacca" (Спектральный анализ выпуклостей, наблюдавшихся во время полного солнечного затмения 18 августа 1868 года с Малаккского полуострова), Comptes rendus ... , 67 : 757–759. С п. 758: "... je vis immédiatement une série de neuf lignes brillantes qui ... me semblent devoir être assimilées aux lignes Principales du Spectre Solaire, B, D, E, b, une ligne inconnue, F, et deux lignes du groupe G. " (... Я сразу увидел серию из девяти ярких линий, которые ... мне показалось, что их следует отнести к основным линиям солнечного спектра: B, D, E, b, неизвестная линия, F, и две линии группа G.)
- ^ Капитан К. Т. Хейг (1868) "Отчет о спектроскопических наблюдениях солнечного затмения 18 августа 1868 г." Труды Лондонского королевского общества, 17 : 74–80. С п. 74: «Могу сразу заявить, что я наблюдал спектры двух красных пламен, расположенных близко друг к другу, и в их спектрах две широкие яркие полосы, довольно резко очерченные, одна розовая, а другая светло-золотая».
- ^ Погсон подал свои наблюдения за затмением 1868 года в местное правительство Индии, но его отчет не был опубликован. (Биман Б. Нат, История гелия и зарождения астрофизики (Нью-Йорк, Нью-Йорк: Springer, 2013), п. 8. ) Тем не менее, Локьер процитировал из своего отчета. С п. 320 В архиве 17 августа 2018 г. Wayback Machine Локьера, Дж. Нормана (1896) "История гелия. Пролог", Природа, 53 : 319–322: «Погсон, говоря о затмении 1868 года, сказал, что желтая линия была« в точке D или около D. »»
- ^ Лейтенант Джон Гершель (1868 г.) «Отчет о солнечном затмении 1868 года, увиденном в Джамканди в Бомбее», Труды Лондонского королевского общества, 17 : 104–120. С п. 113: По мере приближения момента полного солнечного затмения «… Я зарегистрировал возрастающую яркость спектра в окрестности точки D, настолько большую, что фактически не позволяло проводить измерения этой линии до тех пор, пока подходящее облако не уменьшит свет. не готов предложить какое-либо объяснение этому ". С п. 117: «Я также считаю, что не может быть никаких сомнений в том, что ОРАНЖЕВАЯ ЛИНИЯ была идентична D, насколько это касается способности инструмента устанавливать любую такую идентичность».
- ^ В своем первоначальном докладе Французской академии наук о затмении 1868 года Янссен не упомянул желтую линию в солнечном спектре. Видеть:
- Янссен (1868) "Указание на результаты полученных результатов в Cocanada, кулон l'éclipse du mois d'août dernier, et à la suite de cette éclipse" (Информация о некоторых результатах, полученных на Коканаде во время затмения в августе прошлого года и после этого затмения), Comptes rendus ... , 67 : 838–839.
- Уилер М. Сирс, Гелий: исчезающий элемент (Гейдельберг, Германия: Springer, 2015), п. 44.
- Франсуаза Лоне и Сторм Данлоп, пер., Астроном Жюль Янссен: путешественник по небесной физике (Гейдельберг, Германия: Springer, 2012), п. 45.
- ^ а б "Клевейт". Mindat.org. Получено 14 февраля 2020.
- ^ "Уранинит". Mindat.org. Получено 14 февраля 2020.
- ^ Роза, Мелинда (октябрь 2008 г.). «Гелий: вверх, вверх и назад?». Фотонные спектры. В архиве из оригинала 22 августа 2010 г.. Получено 27 февраля 2010. Более авторитетную, но старую круговую диаграмму 1996 года, показывающую использование гелия в США по секторам, показывающую почти такой же результат, см. На диаграмме, воспроизведенной в разделе «Приложения» этой статьи.
- ^ Коннор, Стив (23 августа 2010 г.). «Почему в мире заканчивается гелий». Независимый. Лондон. В архиве из оригинала 27 сентября 2013 г.. Получено 16 сентября 2013.
- ^ Сигел, Итан (12 декабря 2012 г.). «Почему в мире закончится гелий». Начинается с ура. Scienceblogs.com. В архиве из оригинала 14 сентября 2013 г.. Получено 16 сентября 2013.
- ^ Сонди, Давид (24 августа 2015 г.). «Возможно, у нас все-таки не заканчивается гелий». www.gizmag.com. В архиве из оригинала 25 марта 2016 г.. Получено 1 апреля 2016.
- ^ Образец, Ян (28 июня 2016 г.). «Огромное открытие газообразного гелия в Восточной Африке предотвращает нехватку медицинских препаратов». Хранитель. В архиве из оригинала от 29 июня 2016 г.. Получено 29 июн 2016.
- ^ Кочхар, Р. К. (1991). «Французские астрономы в Индии в 17-19 веках». Журнал Британской астрономической ассоциации. 101 (2): 95–100. Bibcode:1991JBAA..101 ... 95K.
- ^ а б c d е ж грамм час я j k л Эмсли, Джон (2001). Строительные блоки природы. Оксфорд: Издательство Оксфордского университета. С. 175–179. ISBN 978-0-19-850341-5.
- ^ Локьер, Дж. Н. (октябрь 1868 г.). «Уведомление о наблюдении спектра солнечного протуберанца». Труды Лондонского королевского общества. 17: 91–92. Bibcode:1868RSPS ... 17 ... 91L. Дои:10.1098 / rspl.1868.0011. JSTOR 112357. S2CID 163097539. Получено 3 июн 2018.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты v ш Хэмпел, Клиффорд А. (1968). Энциклопедия химических элементов. Нью-Йорк: Ван Ностранд Рейнхольд. С. 256–268. ISBN 978-0-442-15598-8.
- ^ Харпер, Дуглас. "гелий". Интернет-словарь этимологии.
- ^ Томсон, Уильям (3 августа 1871 г.). «Инаугурационная речь сэра Уильяма Томсона». Природа. 4 (92): 261–278 [268]. Bibcode:1871Натура ... 4..261.. Дои:10.1038 / 004261a0. ЧВК 2070380. В архиве с оригинала 2 декабря 2016 г.. Получено 22 февраля, 2016.
Франкланд и Локьер находят желтые выступы, образующие очень четкую яркую линию недалеко от D, но до сих пор не отождествляемые с земным пламенем. Кажется, это указывает на новое вещество, которое они предлагают назвать гелием.
- ^ Пальмиери, Луиджи (1881). "La riga dell'Helium apparsa in una Recente sublimazione vesuviana" [Линия гелия появилась в недавно сублимированном материале [с горы] Везувий]. Rendiconto dell'Accademia delle Scienze Fisiche e Matematiche (Неаполь, Италия). 20: 223. В архиве из оригинала на 1 сентября 2018 г.. Получено 1 мая 2017.
Raccolsi alcun tempo fa una sostanza amorfa di consistenza butirracea e di colore giallo sbiadato sublimata sull'orlo di una fumarola prossima alla bocca di eruzione. Saggiata questa sublimazione allo spettroscopio, ho ravvisato le righe del sodio e del potassio ed una lineare ben distinta che corrisponde esattamente alla D3 Che è Quella dell'Helium. Do per ora il semplice annunzio del fatto, proponendomi di ritornare sopra questo argomento, dopo di aver sottoposta la sublimazione ad una analisi chimica. (Некоторое время назад я собрал аморфное вещество маслянистой консистенции и блеклого желтого цвета, которое сублимировалось на краю фумаролы возле устья извержения. Проанализировав это сублимированное вещество с помощью спектроскопа, я распознал линии натрия и калий и очень четкая линейная линия, которая точно соответствует D3, то есть гелия. А пока я просто констатирую этот факт, предлагая вернуться к этому предмету после того, как сублимат подвергнется химическому анализу.)
- ^ Кирк, Венди Л. «Клевит [не клевит] и гелий». Блог о музеях и коллекциях. Университетский колледж Лондона. В архиве из оригинала 18 октября 2018 г.. Получено 18 августа 2017.
- ^ Рамзи, Уильям (1895). "На газе, показывающем спектр гелия, предполагаемая причина D3, Одна из линий коронального спектра. Предварительная записка ». Труды Лондонского королевского общества. 58 (347–352): 65–67. Bibcode:1895RSPS ... 58 ... 65R. Дои:10.1098 / rspl.1895.0006. S2CID 129872109.
- ^ Рамзи, Уильям (1895). «Гелий, газообразный компонент некоторых минералов. Часть I». Труды Лондонского королевского общества. 58 (347–352): 81–89. Bibcode:1895RSPS ... 58 ... 80R. Дои:10.1098 / rspl.1895.0010.
- ^ Рамзи, Уильям (1895). «Гелий, газообразный компонент некоторых минералов. Часть II - Плотность». Труды Лондонского королевского общества. 59 (1): 325–330. Bibcode:1895RSPS ... 59..325R. Дои:10.1098 / rspl.1895.0097. S2CID 96589261.
- ^ Локьер, Дж. Норман (1895). «О новом газе, полученном из уранинита. Предварительная записка, часть II». Труды Лондонского королевского общества. 58 (347–352): 67–70. Дои:10.1098 / rspl.1895.0008.
- ^ Видеть:
- Крукс, Уильям (1895) «Спектр газа клевеита», Химические новости и журнал промышленной науки, 71 (1844) : 151.
- Крукс, Уильям (1895) «Спектр гелия», Химические новости и журнал промышленной науки, 72 (1865) : 87–89.
- ^ Ланглет, Н. А. (1895). "Das Atomgewicht des Heliums". Zeitschrift für Anorganische Chemie (на немецком). 10 (1): 289–292. Дои:10.1002 / zaac.18950100130.
- ^ Уивер, Э. Р. (1919). «Библиография гелиевой литературы». Промышленная и инженерная химия.
- ^ Гиллебранд (1890) «О наличии азота в уранините и о составе уранинита в целом», Бюллетень Геологической службы США, нет. 78. С. 43–79.
- ^ Мандей, Пэт (1999). Джон А. Гаррати; Марк К. Карнс (ред.). Биографическая запись W.F. Хиллебранд (1853–1925), геохимик и администратор Бюро стандартов США в американской национальной биографии. 10–11. Издательство Оксфордского университета. С. 808–9, 227–8.
- ^ Rutherford, E .; Ройдс, Т. (1908). «XXIV. Спектр излучения радия». Философский журнал. серия 6. 16 (92): 313–317. Дои:10.1080/14786440808636511.
- ^ Оннес, Х. Камерлинг (1908) «Сжижение гелия». Сообщения из физической лаборатории Лейденского университета, 9 (108) : 1–23.
- ^ ван Делфт, Дирк (2008). "Чашечка гелия, большая наука" (PDF). Физика сегодня. 61 (3): 36–42. Bibcode:2008ФТ .... 61с..36В. Дои:10.1063/1.2897948. Архивировано из оригинал (PDF) 25 июня 2008 г.. Получено 2008-07-20.
- ^ Видеть:
- Предварительное уведомление: Кисом У. Х. (17 июля 1926 г.) Письма в редакцию: «Затвердевание гелия». Природа, 118 : 81.
- Предварительное уведомление: Кисом, У. Х. (1926) «L'Hélium solidifié», В архиве 2016-10-22 на Wayback Machine Comptes rendus ... , 183 : 26.
- Кисом, У. Х. (1926) «Твердый гелий». Сообщения из физической лаборатории Лейденского университета, 17 (184) .
- ^ «Самый холодный». Time Inc. 10 июня 1929 г. В архиве из оригинала от 06.12.2008. Получено 2008-07-27.
- ^ а б Хойер, Ульрих (1981). «Строение атомов и молекул». В Хойере, Ульрих (ред.). Нильс Бор - Собрание сочинений: Том 2 - Работы по атомной физике (1912–1917). Амстердам: Издательская компания Северной Голландии. стр. 103–316 (особенно стр. 116–122). ISBN 978-0720418002.
- ^ Кеннеди, П. Дж. (1985). "Краткая биография". На французском языке A. P .; Кеннеди, П. Дж. (Ред.). Нильс Бор: столетний том. Издательство Гарвардского университета. С. 3–15. ISBN 978-0-674-62415-3.
- ^ Бор, Н. (1913). «О строении атомов и молекул, часть I» (PDF). Философский журнал. 26 (151): 1–25. Bibcode:1913ПМаг ... 26 .... 1Б. Дои:10.1080/14786441308634955. В архиве (PDF) из оригинала на 2019-04-04. Получено 2017-12-27.
Бор, Н. (1913). «О строении атомов и молекул, часть II: Системы, содержащие только одно ядро» (PDF). Философский журнал. 26 (153): 476–502. Bibcode:1913ПМаг ... 26..476Б. Дои:10.1080/14786441308634993. В архиве (PDF) с оригинала на 2017-12-15. Получено 2017-12-27.
Бор, Н. (1913). «О строении атомов и молекул, часть III: Системы, содержащие несколько ядер». Философский журнал. 26 (155): 857–875. Bibcode:1913ПМаг ... 26..857Б. Дои:10.1080/14786441308635031. - ^ а б c Роботти, Надя (1983). «Спектр ζ Puppis и историческая эволюция эмпирических данных». Исторические исследования в физических науках. 14 (1): 123–145. Дои:10.2307/27757527. JSTOR 27757527.
- ^ Пикеринг, Э. (1896 г.). «Звезды с пекулярным спектром. Новые переменные звезды в Крюке и Лебеде». Циркуляр обсерватории Гарвардского колледжа. 12: 1–2. Bibcode:1896 ХарСи..12 .... 1П. Также опубликовано как: Пикеринг, Э.; Флеминг, В. П. (1896 г.). «Звезды с пекулярным спектром. Новые переменные звезды в Крюке и Лебеде». Астрофизический журнал. 4: 369–370. Bibcode:1896ApJ ..... 4..369P. Дои:10.1086/140291.
- ^ Райт, У. Х. (1914).«Связь между звездами Вольфа – Райе и планетарными туманностями». Астрофизический журнал. 40: 466–472. Bibcode:1914ApJ .... 40..466Вт. Дои:10.1086/142138.
- ^ Пикеринг, Э. (1897). «Звезды с необычным спектром. Новые переменные звезды в Крюке и Лебеде». Astronomische Nachrichten. 142 (6): 87–90. Bibcode:1896АН .... 142 ... 87П. Дои:10.1002 / asna.18971420605. В архиве (PDF) из оригинала на 24.08.2019. Получено 2019-08-24.
- ^ Пикеринг, Э. (1897). «Спектр дзета-щенков». Астрофизический журнал. 5: 92–94. Bibcode:1897ApJ ..... 5 ... 92P. Дои:10.1086/140312.
- ^ Лакатош, Имре (1980). "Бор: исследовательская программа, развивающаяся на несовместимых основаниях". В Уорролле, Джон; Карри, Грегори (ред.). Методология научно-исследовательских программ. Издательство Кембриджского университета. С. 55–68. ISBN 9780521280310.
- ^ Фаулер, А. (1912). «Наблюдения основной и других серий линий в спектре водорода». Ежемесячные уведомления Королевского астрономического общества. 73 (2): 62–63. Bibcode:1912МНРАС..73 ... 62Ф. Дои:10.1093 / минрас / 73.2.62.
- ^ Бор, Н. (1913). «Спектры гелия и водорода». Природа. 92 (2295): 231–232. Bibcode:1913Натура..92..231Б. Дои:10.1038 / 092231d0. S2CID 11988018.
- ^ Фаулер, А. (1913). «Спектры гелия и водорода». Природа. 92 (2291): 95–96. Bibcode:1913Натура..92 ... 95F. Дои:10.1038 / 092095b0. S2CID 3972599.
- ^ Фаулер, А. (1913). "Ответ на: Спектры гелия и водорода". Природа. 92 (2295): 232–233. Bibcode:1913Натура..92..232F. Дои:10.1038 / 092232a0. S2CID 3981817.
- ^ Бор, Н. (1915). «Спектры водорода и гелия». Природа. 95 (6–7): 6–7. Bibcode:1915Натура..95 .... 6Б. Дои:10.1038 / 095006a0. S2CID 3947572.
- ^ Капица, П. (1938). «Вязкость жидкого гелия ниже λ-точки». Природа. 141 (3558): 74. Bibcode:1938Натура.141 ... 74К. Дои:10.1038 / 141074a0. S2CID 3997900.
- ^ Ошеров, Д. Д .; Richardson, R.C .; Ли, Д. М. (1972). "Свидетельства новой фазы твердого гена".3" (PDF). Phys. Rev. Lett. 28 (14): 885–888. Bibcode:1972PhRvL..28..885O. Дои:10.1103 / PhysRevLett.28.885. S2CID 89609083.
- ^ Макфарланд, Д. Ф. (1903). "Состав газа из скважины в Декстере, Кан". Труды Канзасской академии наук. 19: 60–62. Дои:10.2307/3624173. JSTOR 3624173.
- ^ «Открытие гелия в природном газе в Канзасском университете». Национальные исторические химические достопримечательности. Американское химическое общество. В архиве из оригинала от 26.02.2014. Получено 2014-02-21.
- ^ Cady, H.P .; Макфарланд, Д. Ф. (1906). «Гелий в природном газе». Наука. 24 (611): 344. Bibcode:1906 г., Наука .... 24..344Д. Дои:10.1126 / science.24.611.344. PMID 17772798.
- ^ Cady, H.P .; Макфарланд, Д. Ф. (1906). «Гелий в природном газе Канзаса». Труды Канзасской академии наук. 20: 80–81. Дои:10.2307/3624645. JSTOR 3624645.
- ^ Эмме, Юджин М. сост., изд. (1961). «Хронология воздухоплавания и космонавтики, 1920–1924». Аэронавтика и астронавтика: американская хронология науки и техники в исследовании космоса, 1915–1960. Вашингтон, округ Колумбия.: НАСА. С. 11–19.
- ^ Hilleret, Н. (1999). «Обнаружение утечек» (PDF). В С. Тернер (ред.). CERN Accelerator School, вакуумная технология: материалы: Конференц-центр Scanticon, Снекерстен, Дания, 28 мая - 3 июня 1999 г.. Женева, Швейцария: ЦЕРН. С. 203–212.
В основе метода обнаружения утечек гелия лежал Манхэттенский проект и беспрецедентные требования к герметичности, необходимые для заводов по обогащению урана. Требуемая чувствительность, необходимая для проверки герметичности, привела к выбору масс-спектрометра, разработанного доктором A.O.C. Ниер настроился на гелиевую массу.
- ^ Уильямсон, Джон Г. (1968). «Энергия Канзаса». Труды Канзасской академии наук. 71 (4): 432–438. Дои:10.2307/3627447. JSTOR 3627447.
- ^ "Консервационная распродажа гелия" (PDF). Федеральный регистр. 70 (193): 58464. 2005-10-06. В архиве (PDF) из оригинала 31.10.2008. Получено 2008-07-20.
- ^ а б Ствертка, Альберт (1998). Путеводитель по элементам: переработанное издание. Нью-Йорк; Oxford University Press, стр. 24. ISBN 0-19-512708-0
- ^ Pub.L. 104–273: Закон о приватизации гелия 1996 г. (текст) (pdf)
- ^ Управляющее резюме. nap.edu. 2000 г. Дои:10.17226/9860. ISBN 978-0-309-07038-6. В архиве из оригинала 27.03.2008. Получено 2008-07-20.
- ^ Mullins, P. V .; Гудлинг, Р. М. (1951). Гелий. Ежегодник горнодобывающего управления / полезных ископаемых, 1949 г., стр. 599–602. В архиве из оригинала от 06.12.2008. Получено 2008-07-20.
- ^ «Статистика конечного пользователя гелия» (PDF). Геологическая служба США. В архиве (PDF) из оригинала 21.09.2008. Получено 2008-07-20.
- ^ а б c Smith, E.M .; Goodwin, T. W .; Шиллингер, Дж. (2003). «Проблемы, связанные с поставками гелия во всем мире в следующем десятилетии». Достижения в криогенной технике. 49. А (710): 119–138. Bibcode:2004AIPC..710..119S. Дои:10.1063/1.1774674. S2CID 109060534.
- ^ Каплан, Карен Х. (июнь 2007 г.). «Нехватка гелия тормозит исследования и промышленность». Физика сегодня. Американский институт физики. 60 (6): 31–32. Bibcode:2007ФТ .... 60ф..31К. Дои:10.1063/1.2754594.
- ^ Basu, Sourish (октябрь 2007 г.). Yam, Филип (ред.). «Обновления: в воздух». Scientific American. 297 (4). Scientific American, Inc. стр. 18. Архивировано из оригинал на 2008-12-06. Получено 2008-08-04.
- ^ а б c Ньюкомб, Тим (21 августа 2012 г.). «Существует нехватка гелия - и это влияет не только на воздушные шары». Time.com. В архиве из оригинала 29 декабря 2013 г.. Получено 2013-09-16.
- ^ "Air Liquide | мировой лидер в области газов, технологий и услуг для промышленности и здравоохранения". 19 февраля 2015. Архивировано с оригинал на 2014-09-14. Получено 2015-05-25. Пресс-релиз Air Liquide.
- ^ «Беспорядки на Ближнем Востоке разрушают жизненно важный ресурс для ядерной энергии, космических полетов и воздушных шаров на день рождения». Washingtonpost.com. 26 июня 2017. В архиве из оригинала 26 июня 2017 г.. Получено 26 июн 2017.
- ^ http://www.gasworld.com/2015-what-lies-ahead-part-1/2004706.article В архиве 2015-01-17 на Wayback Machine Gasworld, 25 декабря 2014 г.
- ^ «Вырастет ли во втором квартале прогноз прибыли Air Products (APD)? - Блог аналитика». NASDAQ.com. 28 апреля 2015 года. В архиве с оригинала 15 июля 2019 г.. Получено 4 августа, 2019.
- ^ Уоткинс, Тайер. «Старая квантовая физика Нильса Бора и спектр гелия: модифицированная версия модели Бора». Государственный университет Сан-Хосе. В архиве из оригинала от 26 мая 2009 г.. Получено 2009-06-24.
- ^ Льюарс, Эррол Г. (2008). Моделирование чудес. Springer. С. 70–71. Bibcode:2008moma.book ..... L. ISBN 978-1-4020-6972-7.
- ^ Вайс, Рэй Ф. (1971). «Растворимость гелия и неона в воде и морской воде». J. Chem. Англ. Данные. 16 (2): 235–241. Дои:10.1021 / je60049a019.
- ^ Scharlin, P .; Battino, R .; Силла, Э .; Tuñón, I .; Паскуаль-Ахуир, Дж. Л. (1998). «Растворимость газов в воде: корреляция между растворимостью и количеством молекул воды в первой сольватной оболочке». Чистая и прикладная химия. 70 (10): 1895–1904. Дои:10.1351 / pac199870101895. S2CID 96604119.
- ^ Стоун, Джек А .; Стейскал, Алоис (2004). «Использование гелия в качестве эталона показателя преломления: исправление ошибок в газовом рефрактометре». Метрология. 41 (3): 189–197. Bibcode:2004Метро..41..189С. Дои:10.1088/0026-1394/41/3/012.
- ^ Бюлер, Ф .; Axford, W. I .; Chivers, H. J. A .; Мартин, К. (1976). «Изотопы гелия в северном сиянии». J. Geophys. Res. 81 (1): 111–115. Bibcode:1976JGR .... 81..111B. Дои:10.1029 / JA081i001p00111.
- ^ «Твердый гелий». Кафедра физики Университет Альберты. 2005-10-05. Архивировано из оригинал 31 мая 2008 г.. Получено 2008-07-20.
- ^ а б c d е Лиде, Д. Р., изд. (2005). CRC Справочник по химии и физике (86-е изд.). Бока-Ратон (Флорида): CRC Press. ISBN 0-8493-0486-5.
- ^ Грилли, Э. Р. (1973). «Соотношение давление-объем-температура в жидком и твердом 4He». Журнал физики низких температур. 11 (1–2): 33–52. Bibcode:1973JLTP ... 11 ... 33G. Дои:10.1007 / BF00655035. S2CID 189850188.
- ^ Хеншоу, Д. Б. (1958). «Структура твердого гелия по дифракции нейтронов». Письма с физическими проверками. 109 (2): 328–330. Bibcode:1958ПхРв..109..328Г. Дои:10.1103 / PhysRev.109.328.
- ^ Pinceaux, J.-P .; Maury, J.P .; Бессон, Ж.-М. (1979). «Затвердевание гелия при комнатной температуре под высоким давлением». Journal de Physique Lettres. 40 (13): 307–308. Дои:10.1051 / jphyslet: 019790040013030700.
- ^ Лиде, Д. Р., изд. (2005). CRC Справочник по химии и физике (86-е изд.). Бока-Ратон (Флорида): CRC Press. п. 6-120. ISBN 0-8493-0486-5.
- ^ Hohenberg, P.C .; Мартин, П. К. (2000). «Микроскопическая теория сверхтекучего гелия». Анналы физики. 281 (1–2): 636–705 12091211. Bibcode:2000AnPhy.281..636H. Дои:10.1006 / aphy.2000.6019.
- ^ Уорнер, Брент. «Введение в жидкий гелий». НАСА. Архивировано из оригинал на 2005-09-01. Получено 2007-01-05.
- ^ Fairbank, H.A .; Лейн, К. Т. (1949). «Скорость пленки Роллина в жидком гелии». Физический обзор. 76 (8): 1209–1211. Bibcode:1949ПхРв ... 76.1209Ф. Дои:10.1103 / PhysRev.76.1209.
- ^ Роллин, Б. В .; Саймон, Ф. (1939). «О« пленочном »явлении жидкого гелия II». Physica. 6 (2): 219–230. Bibcode:1939Phy ..... 6..219R. Дои:10.1016 / S0031-8914 (39) 80013-1.
- ^ Эллис, Фред М. (2005). «Третий звук». Уэслианская лаборатория квантовых жидкостей. В архиве из оригинала от 21.06.2007. Получено 2008-07-23.
- ^ Бергман, Д. (1949). «Гидродинамика и третий звук в тонких пленках He II». Физический обзор. 188 (1): 370–384. Bibcode:1969ПхРв..188..370Б. Дои:10.1103 / PhysRev.188.370.
- ^ а б Вайс, Ахим. «Элементы прошлого: нуклеосинтез Большого взрыва и наблюдение». Институт Макса Планка гравитационной физики. Архивировано из оригинал на 2010-07-29. Получено 2008-06-23.; Кок, Ален; Вангиони-Флам, Элизабет; Descouvemont, Пьер; Адахчур, Абдеррахим; Ангуло, Кармен (2004). «Обновленный нуклеосинтез Большого взрыва сопоставлен с наблюдениями WMAP и изобилием легких элементов». Астрофизический журнал. 600 (2): 544–552. arXiv:Astro-ph / 0309480. Bibcode:2004ApJ ... 600..544C. Дои:10.1086/380121. S2CID 16276658.
- ^ а б Андерсон, Дон Л .; Foulger, G.R .; Мейбом, А. (02.09.2006). «Основы гелия». MantlePlumes.org. В архиве из оригинала от 08.02.2007. Получено 2008-07-20.
- ^ Новик, Аарон (1947). «Период полураспада трития». Физический обзор. 72 (10): 972. Bibcode:1947ПхРв ... 72..972Н. Дои:10.1103 / PhysRev.72.972.2.
- ^ Застенкер, Г. Н .; Салерно, Э .; Buehler, F .; Bochsler, P .; Басси, М .; Агафонов, Ю. N .; Eisomont, N.A .; Храпченков, В. В .; и другие. (2002). «Изотопный состав и содержание межзвездного нейтрального гелия на основе прямых измерений». Астрофизика. 45 (2): 131–142. Bibcode:2002Ап ..... 45..131Z. Дои:10.1023 / А: 1016057812964. S2CID 116957905.
- ^ «Лунная добыча гелия-3». Институт технологии термоядерного синтеза Университета Висконсин-Мэдисон. 2007-10-19. В архиве из оригинала от 09.06.2010. Получено 2008-07-09.
- ^ Слюта, Э. Н .; Абдрахимов, А. М .; Галимов, Э. М. (2007). «Оценка вероятных запасов гелия-3 в лунном реголите» (PDF). Конференция по лунной и планетарной науке (1338): 2175. Bibcode:2007LPI .... 38.2175S. В архиве (PDF) из оригинала от 05.07.2008. Получено 2008-07-20.
- ^ Хедман, Эрик Р. (16 января 2006 г.). «Увлекательный час с Джеральдом Кульчински». Космический обзор. Архивировано из оригинал на 2011-01-09. Получено 2008-07-20.
- ^ Хиби, Джулиус В. (1939). "Massenspektrographische Untersuchungen an Wasserstoff- und Heliumkanalstrahlen (ЧАС+
3, ЧАС−
2, HeH+
, HeD+
, Он−
)". Annalen der Physik. 426 (5): 473–487. Bibcode:1939АнП ... 426..473Н. Дои:10.1002 / andp.19394260506. - ^ Фридрих, Бретислав (8 апреля 2013 г.). "Хрупкий союз между атомами Ли и Хэ". Физика. 6: 42. Bibcode:2013PhyOJ ... 6 ... 42F. Дои:10.1103 / Физика.6.42. HDL:11858 / 00-001M-0000-000E-F3CF-5. В архиве с оригинала 29 августа 2017 г.. Получено 24 августа 2019.
- ^ Вонг, Мин Ва (2000). «Прогнозирование метастабильного соединения гелия: HHeF». Журнал Американского химического общества. 122 (26): 6289–6290. Дои:10.1021 / ja9938175.
- ^ Грочала, В. (2009). «О химической связи между гелием и кислородом». Польский химический журнал. 83: 87–122.
- ^ «Коллапс химического благородства гелия, предсказанный польским химиком» (PDF). Архивировано из оригинал (PDF) на 2009-03-19. Получено 2009-05-15.
- ^ Сондерс, Мартин; Хименес-Васкес, Уго А .; Кросс, Р. Джеймс; Пореда, Роберт Дж. (1993). «Стабильные соединения гелия и неона: He @ C60 и Ne @ C60". Наука. 259 (5100): 1428–1430. Bibcode:1993Научный ... 259.1428S. Дои:10.1126 / science.259.5100.1428. PMID 17801275. S2CID 41794612.
- ^ Сондерс, Мартин; Хименес-Васкес, Уго А .; Кросс, Р. Джеймс; Мрочковски, Стэнли; Freedberg, Darón I .; Анет, Фрэнк А. Л. (1994). "Исследование внутренней части фуллеренов 3He ЯМР-спектроскопия эндоэдральных 3Он @ C60 и 3Он @ C70". Природа. 367 (6460): 256–258. Bibcode:1994Натура.367..256S. Дои:10.1038 / 367256a0. S2CID 4273677.
- ^ Vos, W. L .; Finger, L.W .; Хемли, Р. Дж .; Hu, J. Z .; Mao, H.K .; Схоутен, Дж. А. (1992). «Соединение Ван-дер-Ваальса высокого давления в твердых азотно-гелиевых смесях». Природа. 358 (6381): 46–48. Bibcode:1992Натура 358 ... 46В. Дои:10.1038 / 358046a0. S2CID 4313676.
- ^ Дун, Сяо; Оганов, Артем Р .; Гончаров, Александр Ф .; Ставру, Элиссайос; Лобанов, Сергей; Салех, Габриэле; Цянь, Гуан-Жуй; Чжу, Цян; Гатти, Карло; Deringer, Volker L .; Дронсковски, Ричард; Чжоу, Сян-Фэн; Пракапенко, Виталий Б .; Конопкова, Зузана; Попов, Иван А .; Болдырев, Александр I .; Ван, Хуэй-Тянь (2017). «Стабильное соединение гелия и натрия при высоком давлении». Химия природы. 9 (5): 440–445. arXiv:1309.3827. Bibcode:2017НатЧ ... 9..440Д. Дои:10.1038 / nchem.2716. ISSN 1755-4330. PMID 28430195. S2CID 20459726.
- ^ Оливер, Б. М .; Брэдли, Джеймс Г. (1984). «Концентрация гелия в нижних слоях атмосферы Земли». Geochimica et Cosmochimica Acta. 48 (9): 1759–1767. Bibcode:1984GeCoA..48.1759O. Дои:10.1016/0016-7037(84)90030-9.
- ^ "Атмосфера: Введение". JetStream - онлайн-школа погоды. Национальная служба погоды. 2007-08-29. Архивировано из оригинал 13 января 2008 г.. Получено 2008-07-12.
- ^ Ли-Свендсен, Ø .; Рис, М. Х. (1996). «Улет гелия из земной атмосферы: механизм истечения ионов». Журнал геофизических исследований. 101 (A2): 2435–2444. Bibcode:1996JGR ... 101.2435L. Дои:10.1029 / 95JA02208.
- ^ Штробель, Ник (2007). "Атмосфера". Астрономические заметки Ника Штробеля. Архивировано из оригинал на 2010-09-28. Получено 2007-09-25.
- ^ Дж. Брент Дэлримпл. "Насколько хороши эти аргументы молодой Земли?". В архиве из оригинала 2011-06-07. Получено 2011-02-13.
- ^ "Пичбленда". Mindat.org. Получено 14 февраля 2020.
- ^ «Монацит». Mindat.org. Получено 14 февраля 2020.
- ^ «Монацит- (Ce)». Mindat.org. Получено 14 февраля 2020.
- ^ Кук, Мелвин А. (1957). «Где радиогенный гелий Земли?». Природа. 179 (4552): 213. Bibcode:1957 г., природа 179..213C. Дои:10.1038 / 179213a0. S2CID 4297697.
- ^ Aldrich, L.T .; Ниер, Альфред О. (1948). "Появление Он3 в природных источниках гелия ». Phys. Rev. 74 (11): 1590–1594. Bibcode:1948ПхРв ... 74.1590А. Дои:10.1103 / PhysRev.74.1590.
- ^ Morrison, P .; Пайн, Дж. (1955). «Радиогенное происхождение изотопов гелия в горных породах». Летопись Нью-Йоркской академии наук. 62 (3): 71–92. Bibcode:1955НЯСА..62 ... 71М. Дои:10.1111 / j.1749-6632.1955.tb35366.x. S2CID 85015694.
- ^ Zartman, R.E .; Вассербург, Г. Дж .; Рейнольдс, Дж. Х. (1961). «Гелий, аргон и углерод в природных газах» (PDF). Журнал геофизических исследований. 66 (1): 277–306. Bibcode:1961JGR .... 66..277Z. Дои:10.1029 / JZ066i001p00277. В архиве (PDF) из оригинала на 2017-08-09. Получено 2019-01-29.
- ^ Бродхед, Рональд Ф. (2005). «Гелий в Нью-Мексико - спрос на геологические ресурсы и возможности разведки» (PDF). Геология Нью-Мексико. 27 (4): 93–101. Архивировано из оригинал (PDF) на 2012-03-30. Получено 2008-07-21.
- ^ «Пресс-релиз: Невыносимая легкость гелия ...» Европейская ассоциация геохимии. Архивировано из оригинал на 2015-09-06. Получено 5 марта 2017.
- ^ Наука, Ян (28 июня 2016 г.). «Огромное открытие газообразного гелия в Восточной Африке предотвращает нехватку медицинских препаратов». Хранитель. В архиве из оригинала 22 февраля 2017 г.. Получено 5 марта 2017.
- ^ Зима, Марк (2008). «Гелий: самое необходимое». Университет Шеффилда. В архиве из оригинала от 14.07.2008. Получено 2008-07-14.
- ^ Cai, Z .; и другие. (2007). Моделирование рынков гелия (PDF). Кембриджский университет. Архивировано из оригинал (PDF) на 2009-03-26. Получено 2008-07-14.
- ^ Гелий (PDF). Обзоры минерального сырья. Геологическая служба США. 2009. С. 74–75. В архиве (PDF) из оригинала от 14.08.2009. Получено 2009-12-19.
- ^ а б "Air Liquide и Linde в охоте за гелием, поскольку запасы Техаса иссякают". Блумберг. 2014 г. В архиве из оригинала на 2017-03-10. Получено 2017-03-07.
- ^ Бриггс, Хелен (28 июня 2016 г.). "Открытие гелия" изменит правила игры'". Новости BBC. В архиве из оригинала 28 июня 2016 г.. Получено 2016-06-28.
- ^ Чен, Стивен (28 июля 2020 г.). «Китай открывает первый крупномасштабный гелиевый завод, пытаясь снизить зависимость от импорта США». Южно-Китайская утренняя почта. Пекин, Китай. Получено 28 июл 2020.
- ^ Пирс, А. П., Готт, Г. Б., и Миттон, Дж. У. (1964). «Уран и гелий на газовом месторождении Панхандл в Техасе и прилегающих районах», Профессиональный документ геологической службы 454-G, Вашингтон: Типография правительства США
- ^ «Закон об ответственном применении и рациональном использовании гелия (HR 527)». Комитет палаты представителей по природным ресурсам. Комитет по природным ресурсам Палаты представителей США. Архивировано из оригинал на 2017-03-06. Получено 5 марта 2017.
- ^ Беляков, В. П .; Дургарьян, С.Г .; Мирзоян, Б.А. (1981). «Мембранные технологии - новое направление в промышленном разделении газов». Химическая и нефтяная инженерия. 17 (1): 19–21. Дои:10.1007 / BF01245721. S2CID 109199653.
- ^ Комитет по влиянию продаж, Таблица 4.2 В архиве 2014-09-10 на Wayback Machine
- ^ Комитет по влиянию продаж, см. стр. 40 В архиве 2014-05-29 в Wayback Machine для оценки общего теоретического производства гелия неоновыми и жидкостными установками
- ^ Dee, P. I .; Уолтон Э. Т. С. (1933). «Фотографическое исследование превращения лития и бора протонами и лития ионами тяжелого изотопа водорода» (PDF). Труды Лондонского королевского общества. 141 (845): 733–742. Bibcode:1933RSPSA.141..733D. Дои:10.1098 / rspa.1933.0151. S2CID 96565428.
- ^ Коннор, Стив (23 августа 2010 г.). «Ричард Коулман выступает против решения Конгресса США продать все поставки гелия к 2015 году». Лондон: Independent.co.uk. В архиве из оригинала 14 ноября 2010 г.. Получено 2010-11-27.
- ^ Наттолл, Уильям Дж .; Кларк, Ричард Х .; Гловацки, Бартек А. (2012). «Ресурсы: хватит тратить гелий». Природа. 485 (7400): 573–575. Bibcode:2012Натура.485..573Н. Дои:10.1038 / 485573a. PMID 22660302. S2CID 10351068.
- ^ а б Министерство внутренних дел США, Геологическая служба США (2015). «Гелий» (PDF). Обзор минерального сырья за 2014 год. С. 72–73. В архиве из оригинала от 04.04.2014. Получено 2014-05-31.
- ^ Распродажа гелия риски будущего предложения В архиве 2012-06-10 на Wayback Machine, Майкл Бэнкс, Мир физики, 27 января 2010 г., по состоянию на 27 февраля 2010 г.
- ^ Beckwith, I.E .; Миллер, К. Г. (1990). «Аэротермодинамика и переход в высокоскоростных аэродинамических трубах в НАСА Лэнгли». Ежегодный обзор гидромеханики. 22 (1): 419–439. Bibcode:1990АнРФМ..22..419Б. Дои:10.1146 / annurev.fl.22.010190.002223.
- ^ Моррис, К. (2001). Горение, вызванное ударом в высокоскоростных клиновых потоках (PDF). Диссертация Стэнфордского университета. Архивировано из оригинал (PDF) на 2009-03-04.
- ^ а б Консидайн, Гленн Д., изд. (2005). «Гелий». Энциклопедия химии Ван Ностранда. Wiley-Interscience. С. 764–765. ISBN 978-0-471-61525-5.
- ^ Габланян, М. Х. (1997). Высоковакуумная техника: практическое руководство. CRC Press. п. 493. ISBN 978-0-8247-9834-5.
- ^ Экин, Джек В. (2006). Экспериментальные методы низкотемпературных измерений. Издательство Оксфордского университета. ISBN 978-0-19-857054-7.
- ^ Fowler, B .; Ackles, K. N .; G, Порлье (1985). «Влияние наркоза инертным газом на поведение - критический обзор». Подводные биомедицинские исследования. 12 (4): 369–402. PMID 4082343. Архивировано из оригинал на 2010-12-25. Получено 2008-06-27.
- ^ Томас, Дж. Р. (1976). «Отмена азотного наркоза у крыс давлением гелия».. Подводный биомед. Res. 3 (3): 249–59. PMID 969027. Архивировано из оригинал на 2008-12-06. Получено 2008-08-06.
- ^ Мясник, Скотт Дж .; Джонс, Ричард Л .; Мэйн, Джонатан Р .; Хартли, Тимоти С .; Петерсен, Стюарт Р. (2007). «Нарушение дыхательной механики при упражнениях с автономным дыхательным аппаратом улучшается с помощью гелиокса». Европейский журнал прикладной физиологии. 101 (6): 659–69. Дои:10.1007 / s00421-007-0541-5. PMID 17701048. S2CID 7311649.
- ^ «Гелиокс21». Linde Gas Therapeutics. 27 января 2009 г. В архиве из оригинала 10 сентября 2011 г.. Получено 13 апреля 2011.
- ^ а б Hunger, W. L., Jr .; Беннетт П. Б. (1974). «Причины, механизмы и профилактика нервного синдрома высокого давления». Подводный биомед. Res. 1 (1): 1–28. ISSN 0093-5387. OCLC 2068005. PMID 4619860. Архивировано из оригинал на 2010-12-25. Получено 2008-04-07.
- ^ Rostain, J.C .; Gardette-Chauffour, M.C .; Lemaire, C .; Накет, Р. (1988). "Эффекты H2-He-O2 смесь на HPNS до 450 msw ». Подводный биомед. Res. 15 (4): 257–70. OCLC 2068005. PMID 3212843. Архивировано из оригинал на 2008-12-06. Получено 2008-06-24.
- ^ Белчер, Джеймс Р .; Слэйтон, Уильям V .; Распет, Ричард; Басс, Генри Э .; Лайтфут, Джей (1999). «Рабочие газы в термоакустических двигателях». Журнал акустического общества Америки. 105 (5): 2677–2684. Bibcode:1999ASAJ..105.2677B. Дои:10.1121/1.426884. PMID 10335618.
- ^ Махиджани, Арджун; Герни, Кевин (1995). Исправление озоновой дыры: наука, технологии и политика. MIT Press. ISBN 978-0-262-13308-1.
- ^ Галлахер, Шон (4 ноября 2013 г.). «Емкость диска баллонов HGST с гелиевым накопителем на 6 ТБ». Ars Technica. В архиве из оригинала 7 июля 2017 г.. Получено 14 июня, 2017.
- ^ Якобссон, Х. (1997). «Моделирование динамики Большого Земного Солнечного Телескопа». Астрономические и астрофизические исследования. 13 (1): 35–46. Bibcode:1997A & AT ... 13 ... 35J. Дои:10.1080/10556799708208113.
- ^ Engvold, O .; Dunn, R.B .; Smartt, R. N .; Ливингстон, В. К. (1983). «Испытания вакуума VS гелия в солнечном телескопе». Прикладная оптика. 22 (1): 10–12. Bibcode:1983ApOpt..22 ... 10E. Дои:10.1364 / AO.22.000010. PMID 20401118.
- ^ «LHC: факты и цифры» (PDF). ЦЕРН. Архивировано из оригинал (PDF) на 2011-07-06. Получено 2008-04-30.
- ^ «Гелий, USP: лекарства, одобренные FDA». Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Получено 30 апреля 2020.
- ^ «Письмо об одобрении FDA» (PDF). 14 апреля 2020 г.. Получено 30 апреля 2020.
- ^ Оберхаус, Даниэль (30 октября 2018 г.). «Почему утечка гелия вывела из строя каждый iPhone в медицинском учреждении». Материнская плата. Vice Media. В архиве из оригинала на 1 ноября 2018 г.. Получено 31 октября 2018.
- ^ Акерман, М. Дж .; Мейтленд, Г. (1975). «Расчет относительной скорости звука в газовой смеси». Подводная биомедицинская резервация. 2 (4): 305–10. PMID 1226588. Архивировано из оригинал на 2011-01-27. Получено 2008-08-09.
- ^ "Почему гелий делает ваш голос скрипучим?". 14 июля 2000 г. В архиве из оригинала 24 марта 2013 г.. Получено 2013-06-08.
- ^ а б Грассбергер, Мартин; Краускопф, Астрид (2007). «Суицидальная асфиксия гелием: отчет о трех случаях Suizid mit Helium Gas: Bericht über drei Fälle». Wiener Klinische Wochenschrift (на немецком и английском языках). 119 (9–10): 323–325. Дои:10.1007 / s00508-007-0785-4. PMID 17571238. S2CID 22894287.
- ^ а б c d Montgomery B .; Хейс С. (2006-06-03). «2 найдены мертвыми под спущенным воздушным шаром». Тампа Бэй Таймс. В архиве из оригинала 30.12.2013. Получено 2013-12-29.
- ^ а б «Два студента умирают, вдыхая гелий». CBC. 4 июня 2006 г. В архиве с оригинала 31 декабря 2013 г.. Получено 30 декабря 2013.
- ^ а б «Вдыхание гелия - это не до смеха - статья предоставлена BOC Gases». Ассоциация художников и поставщиков воздушных шаров компании Australasia Ltd. В архиве из оригинала 14.01.2014. Получено 2014-01-03.
- ^ а б «Опасности отравления гелием». Воздушные шары Лу. Архивировано из оригинал на 2014-01-04.
- ^ а б «Паспорт безопасности газообразного гелия». bouncetime. В архиве из оригинала от 22.04.2015. Получено 2014-01-03.
- ^ а б Энгбер, Дэниел (13.06.2006). "Держись подальше от этого шара!". Slate.com. В архиве с оригинала на 2011-10-20. Получено 2008-07-14.
- ^ Джозефсон, Д. (2000). «Имитировать Микки Мауса может быть опасно». BMJ: Британский медицинский журнал. 320 (7237): 732. ЧВК 1117755. PMID 10720344.
- ^ «Подросток умирает после вдыхания гелия». Новости KTLA. RIVERSIDE: ktla.com. 6 января 2010 г. Архивировано с оригинал 9 января 2012 г.. Получено 2010-11-19.
- ^ "Дань" гелиевой смерти "подростку из Ньютаунабби". BBC Online. 19 ноября 2010 г. В архиве из оригинала 20 ноября 2010 г.. Получено 2010-11-19.
- ^ Мазер, Кейт (24 февраля 2012 г.). «Родители девочки Игл-Пойнт, которая умерла от вдоха гелия, надеются спасти других от той же участи». Орегонский. В архиве из оригинала от 6 декабря 2013 г.. Получено 2013-06-08.
- ^ Барнард, Джефф (22 февраля 2012 г.). «Эшли Лонг, подросток из Орегона, умерла после вдыхания гелия на вечеринке Wild (ВИДЕО)». Huffington Post. В архиве с оригинала 31 декабря 2013 г.. Получено 30 декабря 2013.
- ^ Барнард, Джефф (23 февраля 2012 г.). «Девочка-подросток умерла от гелия на вечеринке». Сегодня. AP. Архивировано из оригинал на 2013-12-30. Получено 2013-12-30.
- ^ Газета Oxford Leader Newspaper, Sherman Publications, Inc., 3 декабря 2012 г.
- ^ "テ レ 朝 事故 で 分 か ム 変 声 缶 の 危 険 を 失 う ケ の 大半 が 子 ど も" (на японском языке). 5 февраля 2015. В архиве из оригинала 5 февраля 2015 г.. Получено 2015-02-05.
- ^ Рэйман, Ноа (5 февраля 2015 г.). "Юная звезда J-Pop ушла в кому после вдоха гелия для телешоу". Время. В архиве из оригинала 5 февраля 2015 г.. Получено 2015-02-06.
- ^ "ア イ ド ル が 収録 中 に 倒 れ 病院 搬 送 テ レ 朝 、 ヘ リ ウ ム ガ ス 吸引" (на японском языке). 4 апреля 2015 г. В архиве из оригинала 4 февраля 2015 г.. Получено 2015-02-04.
"テ レ ビ 番 組 収録 中 、 12 歳 イ ド ル が 意識 失 い 救急 ヘ リ ウ ム が 原因 か" (на японском языке). 4 февраля 2015. В архиве из оригинала 4 февраля 2015 г.. Получено 2015-02-04.
"テ レ 朝 謝罪 、 12 歳 ア イ ド ル い 救急 搬 送" (на японском языке). 4 февраля 2015. Архивировано с оригинал на 2015-02-04. Получено 2015-02-04.
«Юный кумир 3b в коме после вдыхания гелия в программе TV Asahi». 4 февраля 2015. В архиве из оригинала 4 февраля 2015 г.. Получено 2015-02-04.
"ア イ ド ル 救急 搬 送 騒 動 で 制作 社 が 実 績 削除 の 不可解" (на японском языке). 4 февраля 2015. В архиве из оригинала 4 февраля 2015 г.. Получено 2015-02-04. - ^ «Японская детская звезда в коме после неудачного гелиевого трюка». BBC. 5 февраля 2015. В архиве из оригинала 5 февраля 2015 г.. Получено 2015-02-06.
- ^ Rostain J.C .; Lemaire C .; Gardette-Chauffour M.C .; Doucet J .; Накет Р. (1983). «Оценка предрасположенности человека к нервному синдрому высокого давления». J Appl Physiol. 54 (4): 1063–70. Дои:10.1152 / jappl.1983.54.4.1063. PMID 6853282.
Библиография
- Бюро горного дела (1967). Ежегодник полезных ископаемых Минеральное топливо Год 1965. II. Правительственная типография США.
- Комитет по влиянию продажи Федерального резерва гелия; Комиссия по физическим наукам, математике и приложениям; Комиссия по инженерно-техническим системам; Национальный исследовательский совет (2000). Влияние продажи Федерального резерва гелия. Издательство национальных академий. ISBN 978-0-309-07038-6. Получено 2010-04-02.
- Эмсли, Джон (1998). Элементы (3-е изд.). Нью-Йорк: Издательство Оксфордского университета. ISBN 978-0-19-855818-7.
- Vercheval, J. (2003). «Термосфера: часть гетеросферы». Бельгийский институт космической аэрономии. Архивировано из оригинал на 2005-01-01. Получено 2008-07-12.
внешняя ссылка
Общий
- Бюро управления земельными ресурсами правительства США: источники, уточнение и дефицит. Немного истории с гелием.
- Публикации Геологической службы США по гелию начало 1996 г .: Гелий
- Где весь гелий? Сайт Ага
- Это элементаль - гелий
- Подкаст "Химия в ее стихии" (MP3) из Королевское химическое общество с Мир химии: Гелий
- Международные карты химической безопасности - гелий; включает информацию о здоровье и безопасности при случайном контакте с гелием
Более детально
- Гелий в Периодическая таблица видео (Ноттингемский университет)
- Гелий на Хельсинкский технологический университет; включает фазовые диаграммы давление-температура для гелия-3 и гелия-4
- Ланкастерский университет, Физика сверхнизких температур - включает краткое изложение некоторых низкотемпературных методов
Разное
- Физика в речи со звуковыми образцами, демонстрирующими неизменную высоту голоса
- Статья о гелии и других благородных газах
Нехватка гелия
- Предложение гелия Америки: варианты производства большего количества гелия из федеральных земель: надзорные слушания в Подкомитете по энергетическим и минеральным ресурсам Комитета по природным ресурсам Палаты представителей США, Сто тринадцатый Конгресс, первая сессия, четверг, 11 июля 2013 г.
- Гелиевая программа: неотложные проблемы, с которыми сталкивается BLM по хранению и продаже запасов гелия: свидетельские показания в Комитете по природным ресурсам, Палата представителей Счетная палата правительства
- Крамер, Дэвид (22 мая 2012 г.). «Законопроект Сената сохранит запасы гелия в США:« Мера »даст ученым первую долю гелия в случае возникновения дефицита. Веб-сайт Physics Today». Архивировано из оригинал 27 октября 2012 г.
- Ричардсон, Роберт С .; Чан, Моисей (2009). «Гелий, когда он кончится?» (PDF). Архивировано из оригинал (PDF) на 2015-06-14.

