Период (таблица Менделеева) - Period (periodic table)

А период в периодическая таблица это ряд химические элементы. Все элементы подряд имеют одинаковое количество электронные оболочки. Каждый следующий элемент в периоде имеет еще один протон и меньше металлический чем его предшественник. Так устроено, группы элементов в одном столбце имеют одинаковые химический и физические свойства, отражая периодический закон. Например, галогены находятся во втором-последнем столбце (группа 17 ) и обладают схожими свойствами, такими как высокая реакционная способность и тенденция к получению одного электрона для получения электронной конфигурации с благородным газом. По состоянию на 2020 год[Обновить]было открыто и подтверждено 118 элементов.
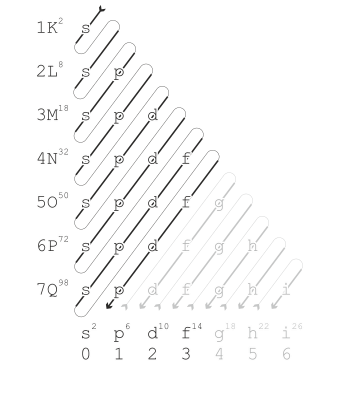
Современное квантовая механика объясняет эти периодические тенденции в свойствах с точки зрения электронные оболочки. По мере увеличения атомного номера оболочки заполняются электронами примерно в том порядке, который показан на диаграмме правила упорядочения. Наполнение каждой оболочки соответствует строке в таблице.
в s-блок и p-блок Периодической таблицы элементы в течение одного и того же периода, как правило, не демонстрируют тенденций и сходства в свойствах (группы с вертикальными тенденциями вниз более значительны). Однако в d-блок, тенденции в разные периоды становятся значительными, а в f-блок элементы показывают высокую степень сходства по периодам.
Периоды
В настоящее время в таблице Менделеева есть семь полных периодов, включающих 118 известных элементов. Любые новые элементы будут помещены в восьмой период; видеть расширенная таблица Менделеева.
Период 1
| Группа | 1 | 18 |
|---|---|---|
| Атомный # Имя | 1 ЧАС | 2 Он |
Первый период содержит меньше всего элементов, чем любой другой, всего два, водород и гелий. Поэтому они не следуют Правило октета, а скорее правило дуплета. Химически гелий ведет себя как благородный газ, и поэтому считается частью группа 18 элементов. Однако по своей ядерной структуре он относится к блок s, и поэтому иногда классифицируется как элемент группы 2, или одновременно 2 и 18. Водород легко теряет и приобретает электрон, и поэтому химически ведет себя как группа 1 и группа 17 элемент.
- Водород (H) - самый обильный химических элементов, составляющих примерно 75% элементарной массы Вселенной.[1] Ионизированный водород - это просто протон. Звезды в главная последовательность в основном состоят из водорода в его плазма государственный. Элементарный водород относительно редко встречается на земной шар, и промышленно производится из углеводороды Такие как метан. Водород может образовывать соединения с большинством элементов и присутствует в воды и большинство органические соединения.[2]
- Гелий (Он) существует только как газ кроме экстремальных условий.[3] Это второй по весу элемент и второй по распространенности во Вселенной.[4] Больше всего гелия образовалось в Большой взрыв, но новый гелий создается через термоядерная реакция водорода в звездах.[5] На земной шар, гелий относительно редок и встречается только как побочный продукт естественного разлагаться некоторых радиоактивных элементов.[6] Такой «радиогенный» гелий находится внутри натуральный газ в концентрациях до семи процентов по объему.[7]
Период 2
| Группа | 1 | 2 | 13 | 14 | 15 | 16 | 17 | 18 |
|---|---|---|---|---|---|---|---|---|
| Атомный # Имя | 3 Ли | 4 Быть | 5 B | 6 C | 7 N | 8 О | 9 F | 10 Ne |
Элементы периода 2 включают 2 с и 2p орбитали. Они включают в себя биологически наиболее важные элементы, помимо водорода: углерод, азот и кислород.
- Литий (Li) - самый легкий металл и наименее плотный твердый элемент.[8] В неионизированном состоянии он является одним из наиболее реактивных элементов, поэтому в природе встречается только в соединения. Это самый тяжелый изначальный элемент выкованы в больших количествах во время Большой взрыв.
- Бериллий (Be) имеет один из самых высоких точки плавления из всех легкие металлы. Небольшие количества бериллия были синтезированный во время Большого взрыва, хотя большая его часть разложившийся или вступили в реакцию внутри звезд, чтобы создать более крупные ядра, такие как углерод, азот или кислород. Бериллий классифицируется Международное агентство по изучению рака как канцероген группы 1.[9] От 1% до 15% людей чувствительны к бериллию, и у них может развиться воспалительная реакция. дыхательная система и кожа, называется хронической бериллиевой болезнью.[10]
- Бор (B) не встречается в природе как свободный элемент, но в таких соединениях, как бораты. Это важное растение микронутриент, необходим для прочности и развития клеточной стенки, деления клеток, развития семян и плодов, транспорта сахара и выработки гормонов,[11][12] хотя высокие уровни токсичны.
- Углерод (C) является четвертым по численности элементом во Вселенной по массе после водород, гелий и кислород[13] и это второй по распространенности элемент в организме человека по массе после кислорода,[14] третий по численности по количеству атомов.[15] Существует почти бесконечное количество соединений, которые содержат углерод из-за способности углерода образовывать длинные стабильные цепочки связей C — C.[16][17] Все органические соединения, необходимые для жизни, содержат по крайней мере один атом углерода;[16][17] В сочетании с водородом, кислородом, азотом, серой и фосфором углерод является основой всех важных биологических соединений.[17]
- Азот (N) встречается в основном как в основном инертный двухатомный газ, N2, что составляет 78% атмосферы Земли по объему. Это важный компонент белки и, следовательно, жизни.
- Кислород (O) составляет 21% атмосферы по объему и требуется для дыхание всеми (или почти всеми) животными, а также является основным компонентом воды. Кислород является третьим по распространенности элементом во Вселенной, а кислородные соединения доминируют в земной коре.
- Фтор (F) является наиболее реактивным элементом в неионизированном состоянии, и поэтому никогда не встречается в природе.
- Неон (Ne) - это благородный газ используется в неоновое освещение.
Период 3
| Группа | 1 | 2 | 13 | 14 | 15 | 16 | 17 | 18 |
|---|---|---|---|---|---|---|---|---|
| Атомный # Имя | 11 Na | 12 Mg | 13 Al | 14 Si | 15 п | 16 S | 17 Cl | 18 Ar |
Все три элемента периода встречаются в природе и имеют по крайней мере одну стабильный изотоп. Все, кроме благородного газа аргон необходимы для основ геологии и биологии.
- Натрий (Na) - это щелочной металл. Он присутствует в океанах Земли в больших количествах в виде хлорид натрия (столовая соль).
- Магний (Mg) - это щелочноземельный металл. Магний ионы находятся в хлорофилл.
- Алюминий (Al) - это постпереходный металл. Это самый распространенный металл на Земле. корка.
- Кремний (Si) - это металлоид. Это полупроводник, что делает его основным компонентом многих интегральные схемы. Диоксид кремния является основной составляющей песок. Как углерод к Биология, Кремний должен Геология.
- Фосфор (P) - это неметалл необходимо ДНК. Это очень реактивный, и поэтому никогда не встречается в природе как свободный элемент.
- Сера (S) - это неметалл. Он находится в двух аминокислоты: цистеин и метионин.
- Хлор (Cl) - это галоген. Он используется как дезинфицирующее средство, особенно в бассейны.
- Аргон (Ar) - это благородный газ, что делает его почти полностью инертным. Лампы накаливания часто заполнены благородными газами, такими как аргон, чтобы сохранить нити при высоких температурах.
Период 4
| Группа | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Атомный # Имя | 19 K | 20 Ca | 21 Sc | 22 Ti | 23 V | 24 Cr | 25 Mn | 26 Fe | 27 Co | 28 Ni | 29 Cu | 30 Zn | 31 Ga | 32 Ge | 33 В качестве | 34 Se | 35 Br | 36 Kr |
Период 4 включает биологически важные элементы калий и кальций, и является первым периодом в d-блок с зажигалкой переходные металлы. К ним относятся утюг, самый тяжелый элемент, выкованный в звезды главной последовательности и основной компонент Земли, а также другие важные металлы, такие как кобальт, никель, и медь. Почти у всех есть биологические роли.
Завершают четвертый период постпереходные металлы цинк и галлий, то металлоиды германий и мышьяк, а неметаллы селен, бром, и криптон.
Период 5
| Группа | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Атомный # Имя | 37 Руб. | 38 Sr | 39 Y | 40 Zr | 41 Nb | 42 Пн | 43 Tc | 44 RU | 45 Rh | 46 Pd | 47 Ag | 48 CD | 49 В | 50 Sn | 51 Sb | 52 Te | 53 я | 54 Xe |
Период 5 имеет такое же количество элементов, что и период 4, и следует той же общей структуре, но с одним дополнительным постпереходным металлом и одним меньше неметаллом. Из трех самых тяжелых элементов с биологической ролью два (молибден и йод ) находятся в этот период; вольфрам, в период 6, тяжелее, вместе с некоторыми из ранних лантаноиды. Период 5 также включает технеций, исключительно легкие радиоактивный элемент.
Период 6
| Группа | 1 | 2 | 3 (Лантаноиды ) | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Атомный # Имя | 55 CS | 56 Ба | 57 Ла | 58 Ce | 59 Pr | 60 Nd | 61 Вечера | 62 См | 63 Европа | 64 Б-г | 65 Tb | 66 Dy | 67 Хо | 68 Э | 69 Тм | 70 Yb | 71 Лу | 72 Hf | 73 Та | 74 W | 75 Re | 76 Операционные системы | 77 Ir | 78 Pt | 79 Au | 80 Hg | 81 Tl | 82 Pb | 83 Би | 84 По | 85 В | 86 Rn |
Период 6 - это первый период, включающий f-блок, с лантаноиды (также известный как редкоземельные элементы ), и включает в себя самые тяжелые устойчивые элементы. Многие из этих тяжелые металлы токсичны и некоторые радиоактивны, но платина и золото в значительной степени инертны.
Период 7
| Группа | 1 | 2 | 3 (Актиниды ) | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Атомный # Имя | 87 Пт | 88 Ра | 89 Ac | 90 Чт | 91 Па | 92 U | 93 Np | 94 Пу | 95 Являюсь | 96 См | 97 Bk | 98 Cf | 99 Es | 100 FM | 101 Мкр | 102 Нет | 103 Lr | 104 Rf | 105 Db | 106 Sg | 107 Bh | 108 Hs | 109 Mt | 110 Ds | 111 Rg | 112 Cn | 113 Nh | 114 Fl | 115 Mc | 116 Lv | 117 Ц | 118 Og |
Все элементы периода 7 являются радиоактивный. Этот период содержит самый тяжелый элемент, который встречается в природе на Земле, плутоний. Все последующие элементы этого периода были синтезированы искусственно. Пока пять из них (от америций к эйнштейний ) теперь доступны в макроскопических количествах, большинство из них чрезвычайно редки, поскольку были приготовлены в количествах микрограммов или меньше. Некоторые из более поздних элементов были идентифицированы только в лабораториях в количествах по несколько атомов за раз.
Хотя редкость многих из этих элементов означает, что экспериментальные результаты не очень обширны, периодические и групповые тенденции в поведении, по-видимому, менее четко определены для периода 7, чем для других периодов. Пока франций и радий действительно проявляют типичные свойства групп 1 и 2 соответственно, актиниды демонстрируют гораздо большее разнообразие поведения и степеней окисления, чем лантаноиды. Эти особенности 7 периода могут быть обусловлены множеством факторов, в том числе большой степенью спин-орбитальная связь и релятивистские эффекты, в конечном итоге вызванные очень высоким положительным электрическим зарядом от их массивных атомные ядра.
Период 8
Никакой элемент восьмого периода еще не синтезирован. А g-блок предсказано. Неясно, возможны ли все элементы, предсказанные для восьмого периода, на самом деле. Следовательно, восьмого периода может не быть.
Смотрите также
Рекомендации
- ^ Палмер, Дэвид (13 ноября 1997 г.). «Водород во Вселенной». НАСА. Получено 2008-02-05.
- ^ Веселый, Уильям Ли (9 августа 2019 г.). «водород». Британская энциклопедия.
- ^ «Гелий: физические свойства». WebElements. Получено 2008-07-15.
- ^ «Гелий: геологическая информация». WebElements. Получено 2008-07-15.
- ^ Кокс, Тони (1990-02-03). «Происхождение химических элементов». Новый ученый. Получено 2008-07-15.
- ^ «Предложение гелия сократилось: из-за нехватки производства некоторые отрасли промышленности и тусовщики вынуждены обходить стороной». Хьюстон Хроникл. 2006-11-05.
- ^ Браун, Дэвид (2008-02-02). «Гелий - новая цель в Нью-Мексико». Американская ассоциация геологов-нефтяников. Получено 2008-07-15.
- ^ Литий в WebElements.
- ^ "Монография МАИР, том 58". Международное агентство по изучению рака. 1993 г.. Получено 2008-09-18.
- ^ Информация о хронической бериллиевой болезни.
- ^ «Функции бора в питании растений» (PDF). www.borax.com/agriculture. U.S. Borax Inc. Архивировано с оригинал (PDF) на 20.03.2009.
- ^ Blevins, Dale G .; Лукашевский, Кристина М. (1998). «Функции бора в питании растений». Ежегодный обзор физиологии растений и молекулярной биологии растений. 49: 481–500. Дои:10.1146 / annurev.arplant.49.1.481. PMID 15012243.
- ^ Десять самых распространенных элементов во Вселенной, взятых из Топ-10 всего, 2006, Russell Ash, page 10. Проверено 15 октября 2008 г. В архиве 10 февраля 2010 г. Wayback Machine
- ^ Чанг, Раймонд (2007). Химия, Девятое издание. Макгроу-Хилл. п. 52. ISBN 0-07-110595-6.
- ^ Фрейтас-младший, Роберт А. (1999). Наномедицина. Landes Bioscience. Таблицы 3-1 и 3-2. ISBN 1-57059-680-8.
- ^ а б «Состав и номенклатура углеводородов». Университет Пердью. Получено 2008-03-23.
- ^ а б c Альбертс, Брюс; Александр Джонсон; Джулиан Льюис; Мартин Рафф; Кейт Робертс; Питер Уолтер. Молекулярная биология клетки. Наука о гирляндах.

