Хлорид индия (III) - Indium(III) chloride
 | |
| Имена | |
|---|---|
| Другие имена Хлорид индия Трихлорид индия | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.030.027 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 3260 |
| |
| |
| Характеристики | |
| InCl3 | |
| Молярная масса | 221,18 г / моль |
| Внешность | белые хлопья |
| Плотность | 3,46 г / см3 |
| Температура плавления | 586 ° С (1087 ° F, 859 К) |
| Точка кипения | 800 ° С (1470 ° F, 1070 К) |
| 195 г / 100 мл, экзотермический | |
| Растворимость в других растворителях | THF, Этиловый спирт |
| Структура | |
| Моноклиника, mS16 | |
| С12 / м1, №12 | |
| Опасности | |
| Главный опасности | Коррозионный |
| Паспорт безопасности | Внешний SDS |
| Пиктограммы GHS |   [1] [1] |
| Сигнальное слово GHS | Опасность[1] |
| H302, H314[1] | |
| P260, P303 + 361 + 353, P305 + 351 + 338, P301 + 330 + 331, P405, P501[1] | |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
Другой анионы | Фторид индия (III) Бромид индия (III) Иодид индия (III) |
Другой катионы | Хлорид алюминия Трихлорид галлия Хлорид таллия (III) |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Хлорид индия (III) это химическое соединение с формулой ВCl3. Этот соль представляет собой белое хлопьевидное твердое вещество с аппликациями в органический синтез как Кислота Льюиса. Это также наиболее доступное растворимое производное индия.[2]
Синтез и структура
Являясь относительно электроположительным металлом, индий быстро реагирует с хлором с образованием трихлорида. Трихлорид индия очень растворим и расплывается.[3] Сообщалось о синтезе с использованием электрохимической ячейки в смешанном метанол -бензол решение.[4]
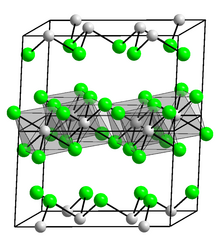
Нравиться AlCl3 и TlCl3, InCl3 кристаллизуется как слоистая структура, состоящая из плотноупакованного хлорида, содержащего слои октаэдрически согласованный В центрах (III)[5] структура, подобная той, что видна в YCl3.[6] В отличие, GaCl3 кристаллизуется в виде димеров, содержащих Ga2Cl6.[6] Расплавленный InCl3 проводит электричество,[5] тогда как AlCl3 не превращается в молекулярный димер, Al2Cl6.[7]
Реакции
InCl3 является кислотой Льюиса и образует комплексы с донором лиганды, L, InCl3L, InCl3L2, InCl3L3. Например, с ионом хлорида образует тетраэдрический InCl4−, тригонально-бипирамидный InCl52−, и октаэдрический InCl63−.[5]
В диэтиловый эфир раствор, InCl3 реагирует с гидрид лития, LiH, с образованием . Это нестабильное соединение разлагается ниже 0 ° C,[8] и реагирует на месте в органическом синтезе как восстановитель[9] и для получения комплексов третичного амина и фосфина Дюйм3.[10]
Триметилиндий, Во мне3, могут быть получены путем реакции InCl3 в диэтиловый эфир решение либо с Реактив Гриньяра или же метиллитий, Лайм. Триэтилиндий может быть приготовлен аналогичным образом, но с реактивом Гриньяра EtMgBr.[11]
InCl3 реагирует с металлическим индием при высокой температуре с образованием хлоридов индия с более низкой валентностью In5Cl9, В2Cl3 и InCl.[5]
Катализатор в химии
Хлорид индия - это кислота Льюиса катализатор в органические реакции Такие как Ацилирование Фриделя-Крафтса и Реакции Дильса-Альдера. В качестве примера последнего[12] реакция протекает в комнатная температура, при загрузке катализатора 1 мол.% в ацетонитрил -водная смесь растворителей. Первый шаг - это Конденсация Кневенагеля между барбитуровой кислотой и альдегидом; второй шаг - обратный электронный запрос Реакция Дильса-Альдера, что является многокомпонентная реакция N, N'-диметил-барбитуровая кислота, бензальдегид и этилвиниловый эфир. С катализатором сообщается химический выход составляет 90%, а процент транс-изомер составляет 70%. Без добавления катализатора выход падает до 65% с 50% транс-продукта.
Рекомендации
- ^ а б c d «Хлорид индия (III)». Американские элементы. Получено 15 мая, 2019.
- ^ Araki, S .; Хирашита Т. «Трихлорид индия» в Энциклопедии реагентов для органического синтеза (Эд: Л. Пакетт) 2004, J. Wiley & Sons, Нью-Йорк. Дои:10.1002 / 047084289X.
- ^ Трихлорид индия
- ^ Habeeb, J. J .; Так, Д. Г. "Электрохимический синтез комплексов индия (III)" Неорганические синтезы, 1979, том XIX, ISBN 0-471-04542-X
- ^ а б c d Эгон Виберг, Арнольд Фредерик Холлеман (2001) Неорганическая химия, Эльзевьер ISBN 0123526515
- ^ а б Уэллс, А.Ф. Структурная неорганическая химия, Оксфорд: Clarendon Press, 1984. ISBN 0-19-855370-6.
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ Энтони Джон Даунс (1993). Химия алюминия, галлия, индия и таллия. Springer. ISBN 0-7514-0103-X.
- ^ Металлы основной группы в органическом синтезе, том 1, изд. Хисаши Ямамото, Коитиро Осима, Wiley VCH, 2004 г., ISBN 3527305084
- ^ Металлы группы 13 Алюминий, галлий, индий и таллий: химические закономерности и особенности, Саймон Олдридж, Энтони Дж. Даунс, Wiley, 2011, ISBN 978-0-470-68191-6
- ^ Соединения основной группы in Inorganic Syntheses, vol 31, By Schultz, Neumayer, Marks; Под ред. Алан Х. Коули, John Wiley & Sons, Inc., 1997 г., ISBN 0471152889
- ^ Эффективный синтез новых пирано [2,3-d] - и фуропирано [2,3-d] пиримидинов посредством катализируемой индием многокомпонентной домино реакции Праджапати, Д. Мукут Гохайн, М. Журнал органической химии Байльштейна 2006, 2:11 Дои:10.1186/1860-5397-2-11







