Хлорид тантала (V) - Tantalum(V) chloride
 | |
| Имена | |
|---|---|
| Имена ИЮПАК Хлорид тантала (V) Пентахлорид тантала | |
| Идентификаторы | |
| |
3D модель (JSmol ) | |
| ECHA InfoCard | 100.028.869 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| TaCl5 | |
| Молярная масса | 358,213 г / моль |
| Внешность | белый моноклинический кристаллы[1] |
| Плотность | 3,68 г / см3 |
| Температура плавления | 216 ° С (421 ° F, 489 К) |
| Точка кипения | 239,4 ° С (462,9 ° F, 512,5 К) (разлагается) |
| реагирует | |
| Растворимость | хлороформ, CCl4 |
| +140.0×10−6 см3/ моль | |
| Структура | |
| Моноклиника, mS72 | |
| С2 / м, №12 | |
| Термохимия | |
Стандартный моляр энтропия (S | 221,75 Дж К−1 моль−1 |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | -858,98 кДж / моль |
| Опасности | |
| точка возгорания | Негорючий |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) | 1900 мг / кг (перорально, крыса) |
| Родственные соединения | |
Другой анионы | Фторид тантала (V) Бромид тантала (V) Иодид тантала (V) |
Другой катионы | Хлорид ванадия (IV) Ниобий (V) хлорид |
Родственные соединения | Хлорид тантала (III), Хлорид тантала (IV) |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Хлорид тантала (V), также известный как пентахлорид тантала, является неорганическое соединение с формулой TaCl5. Он принимает форму белого порошка и обычно используется в качестве исходного материала в тантал химия. Это легко гидролизует образовывать тантал (V) оксихлорид (TaOCl3) и в конечном итоге пятиокись тантала (Та2О5); для этого необходимо, чтобы он был синтезирован и обработан под безводный условия, используя безвоздушные методы.
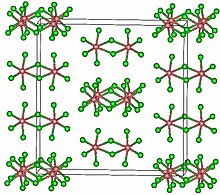
Структура
TaCl5 кристаллизуется в моноклинический космическая группа C2/м.[2] Десять атомов хлора образуют пару октаэдров, имеющих общее ребро. Атомы тантала занимают центры октаэдров и соединены двумя хлорными мостиковые лиганды. Димерная структура сохраняется в растворителях, не образующих комплексы, и в значительной степени в расплавленном состоянии. Однако в парообразном состоянии TaCl5 является мономерный. Этот мономер принимает тригонально-бипирамидная структура, как у PCl5.[3]
Физические свойства
Растворимость пентахлорида тантала несколько увеличивается для следующих серий: ароматические углеводороды:
Это отражается в углублении окраски растворов от бледно-желтого до оранжевого. Пентахлорид тантала менее растворим в циклогексан и четыреххлористый углерод чем в ароматических углеводородах. Такие растворы пентахлорида тантала также известны как плохие проводники электричества, что свидетельствует о слабой ионизации. TaCl5 очищается сублимация дать белые иголки.
Синтез
Пентахлорид тантала может быть получен реакцией порошкового металлического тантал с хлор газ при температуре от 170 до 250 ° C. Эту реакцию также можно провести с использованием HCl при 400 ° С.[4]
- 2 Та + 5 Cl2 → 2 TaCl5
- 2 Ta + 10 HCl → 2 TaCl5 + 5 часов2
Его также можно приготовить реакцией между пятиокись тантала и тионилхлорид при 240 ° C
- Та2О5 + 5 SOCl2 → 2 TaCl5 + 5 ТАК2
Пентахлорид тантала имеется в продаже, однако образцы могут быть загрязнены танталом (V). оксихлорид (TaOCl3), образующийся при гидролизе.
Реакции
TaCl5 является электрофильный и ведет себя как Катализатор Фриделя – Крафтса, похожий на AlCl3. Он образует аддукты с множеством Базы Льюиса.[5]
Простые аддукты
TaCl5 образует стабильные комплексы с эфиры:
- TaCl5 + R2O → TaCl5(ИЛИ ЖЕ2) (R = Me, Et)
TaCl5 также реагирует с пентахлорид фосфора и оксихлорид фосфора, первый является донором хлорида, а второй служит лигандом, связывающимся через кислород:
- TaCl5 + PCl5 → [PCl+
4][TaCl−
6] - TaCl5 + OPCl3 → [TaCl5(OPCl3)]
Пентахлорид тантала реагирует с третичные амины дать кристаллические аддукты.
- TaCl5 + 2 р3N → [TaCl5(NR3)]
Реакции замещения хлоридов
Пентахлорид тантала реагирует при комнатной температуре с избытком оксид трифенилфосфина дать оксихлориды:
- TaCl5 + 3 OPPh3 → [TaOCl3(OPPh3)]Икс ...
Предполагаемое начальное образование аддуктов между TaCl5 и гидроксильные соединения, такие как спирты, фенолы и карбоновые кислоты немедленно следует отщепление хлористого водорода и образование связей Ta – O:
- TaCl5 + 3 HOEt → TaCl2(OEt)3 + 3 HCl
В присутствии аммиак как HCl акцептора, все пять хлоридных лигандов замещаются с образованием Ta (OEt)5. Аналогично TaCl5 реагирует с метоксид лития в безводном метанол с образованием родственных метоксипроизводных:
- TaCl5 + 4 LiOMe → Ta (OMe)4Cl + 4 LiCl
Аммиак вытеснит большую часть хлоридных лигандов из TaCl5 отдать кластер. Хлорид медленнее вытесняется начальный или же вторичные амины но замена всех пяти хлоридных центров амидогруппами была достигнута за счет использования диалкиламидов лития, как показано на примере синтеза пентакис (диметиламидо) тантал:
- TaCl5 + 5 LiNMe2 → Ta (NMe2)5
Со спиртами пентахлорид реагирует с образованием алкоксиды. Как показано для приготовления этоксид тантала (V), такие реакции часто проводят в присутствии основания:
- 10 EtOH + Ta2Cl10 + 10 NH3 → Та2(OEt)10 + 10 NH4Cl
Пентахлорид тантала восстанавливается азотными гетероциклами, такими как пиридин.
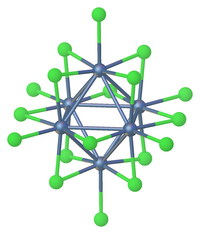
Снижение
Восстановление хлорида тантала (V) дает анионные и нейтральные кластеры, включая [Ta6Cl18]4− и [Ta6Cl14](ЧАС2O)4.[6]
Рекомендации
- ^ Лиде, Дэвид Р., изд. (2006). CRC Справочник по химии и физике (87-е изд.). Бока-Ратон, Флорида: CRC Press. ISBN 0-8493-0487-3.
- ^ Рабе, Сюзанна; Мюллер, Ульрих (2000). «Кристаллическая структура пентахлорида тантала (TaCl5)2". Z. Kristallogr. - Новый кристалл. Struct. 215 (1): 1–2. Дои:10.1515 / ncrs-2000-0102.
- ^ Ф. Фэйрброзер (1967). Химия ниобия и тантала. Эльзевир.
- ^ Янг, Ральф С.; Брубейкер, Карл Х. (1952). «Реакция тантала с хлористым водородом, бромоводородом и пентахлоридом тантала; действие водорода на пентахлорид тантала». Журнал Американского химического общества. 74 (19): 4967. Дои:10.1021 / ja01139a524.
- ^ Ф. А. Коттон, Г. Уилкинсон, Продвинутая неорганическая химия (4-е изд.), Wiley, New York, 1980.
- ^ Дурайсами, Тирумалай; Хэй, Дэниел Н. Т .; Мессерле, Луи (2014). «Октаэдрические кластеры гексатантала галогенидов». Неорганические синтезы: Том 36. Неорганические синтезы. 36. С. 1–8. Дои:10.1002 / 9781118744994.ch1. ISBN 9781118744994.
- ^ Thaxton, C.B .; Якобсон, Р. А. (1971). «Кристаллическая структура H2(Та6Cl18)(ЧАС2O)6". Неорганическая химия. 10: 1460–1463. Дои:10.1021 / ic50101a029.CS1 maint: использует параметр авторов (связь)
дальнейшее чтение
- Озин, Г. А .; Уолтон, Р. А. (1970). «Колебательные спектры и структуры комплексов 1: 1 ниобия и тантала, пентахлоридов и пентабромида тантала с ацето-, пердейтериоацето- и пропионитрилами в твердом состоянии и в растворе, а также колебательный анализ частиц MX.5, NC · CY3 (Y = H или D) ". J. Chem. Soc. А: 2236–2239. Дои:10,1039 / j19700002236.
- Bullock, J. I .; Parrett, F.W .; Тейлор, Н. Дж. (1973). «Некоторые комплексы галогенид металла – галогенид фосфора – алкилгалогенид. Часть II. Реакции с пентахлоридами ниобия, тантала и гексахлоридом вольфрама». J. Chem. Soc., Dalton Trans. (5): 522–524. Дои:10.1039 / DT9730000522.
- Orević, C .; Катович, В. (1970). «Координационные комплексы ниобия и тантала. Часть VIII. Комплексы ниобия (IV), ниобия (V) и тантала (V) со смешанными оксо, галогено, алкокси и 2,2'-бипиридиловыми лигандами». J. Chem. Soc. А: 3382–3386. Дои:10,1039 / j19700003382.
- Cowley, A .; Fairbrother, F .; Скотт, Н. (1958). "Галогениды ниобия (колумбия) и тантала. Часть V. Диэтиловые эфирные комплексы пентахлоридов и пентабромидов; растворимость пентаиодида тантала в эфире". J. Chem. Soc.: 3133–3137. Дои:10.1039 / JR9580003133.
