Рецептор эпидермального фактора роста - Epidermal growth factor receptor
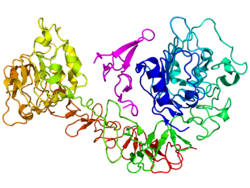
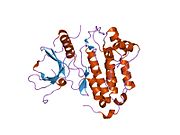
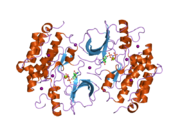
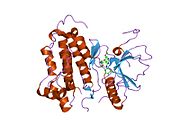
В рецептор эпидермального фактора роста (EGFR; ЭрбБ-1; HER1 у людей) является трансмембранный белок это рецептор для членов фактор роста эпидермиса семья (EGF family) из внеклеточный белок лиганды.[5]
Рецептор эпидермального фактора роста входит в состав Семейство рецепторов ErbB, подсемейство из четырех тесно связанных рецепторные тирозинкиназы: EGFR (ErbB-1), HER2 / neu (ЭрбБ-2), Ее 3 (ЭрбБ-3) и Ее 4 (ЭрбБ-4). При многих типах рака мутации, влияющие на экспрессию или активность EGFR, могут приводить к рак.[6]
Фактор эпидермального роста и его рецептор были открыты Стэнли Коэн из Университет Вандербильта. Коэн поделился 1986 Нобелевская премия по медицине с Рита Леви-Монтальчини за открытие факторы роста.
Недостаточная передача сигналов EGFR и других рецепторные тирозинкиназы у людей связана с такими заболеваниями, как болезнь Альцгеймера, а сверхэкспрессия связана с развитием большого количества опухолей. Прерывание передачи сигналов EGFR путем блокирования сайтов связывания EGFR на внеклеточном домене рецептора или ингибирования внутриклеточной активности тирозинкиназы может предотвратить рост опухолей, экспрессирующих EGFR, и улучшить состояние пациента.
Функция


Рецептор эпидермального фактора роста (EGFR) представляет собой трансмембранный белок который активируется связыванием его специфического лиганды, включая фактор роста эпидермиса и трансформирующий фактор роста α (TGFα)[7] ErbB2 не имеет известного прямого активации лиганд, и может находиться в активированном состоянии постоянно или становиться активным при гетеродимеризация с другими членами семьи, такими как EGFR. При активации лигандами факторов роста EGFR претерпевает переход из неактивного мономерный форма для активного гомодимер.[8] - хотя есть некоторые свидетельства того, что преформированные неактивные димеры также могут существовать до связывания лиганда.[нужна цитата ] Помимо образования гомодимеров после связывания лиганда, EGFR может спариваться с другим членом семейства рецепторов ErbB, таким как ErbB2 / Her2 / neu, чтобы создать активированный гетеродимер. Имеются также данные, позволяющие предположить, что формируются кластеры активированных EGFRs, хотя остается неясным, важно ли это кластеризация для самой активации или происходит после активации индивидуальных димеров.[нужна цитата ]
Димеризация EGFR стимулирует его внутреннюю внутриклеточную активность протеин-тирозинкиназы. Как результат, аутофосфорилирование из нескольких тирозин (Y) остатки на С-конце домен EGFR происходит. К ним относятся Y992, Y1045, Y1068, Y1148 и Y1173, как показано на диаграмме рядом.[9] Это аутофосфорилирование вызывает последующую активацию и передачу сигналов несколькими другими белками, которые связываются с фосфорилированными тирозинами посредством их собственного связывания фосфотирозина. SH2 домены. Эти нижерасположенные сигнальные белки инициируют несколько преобразование сигнала каскады, в основном MAPK, Акт и JNK пути, ведущие к Синтез ДНК и пролиферация клеток.[10] Такие белки модулируют такие фенотипы, как миграция клеток, адгезия, и распространение. Активация рецептора важна для врожденного иммунного ответа кожи человека. Киназный домен EGFR может также перекрестно фосфорилировать тирозиновые остатки других рецепторов, с которыми он агрегирован, и сам может быть активирован таким образом.
Биологические роли
EGFR необходим для протоковый развитие молочные железы,[11][12][13] и агонисты EGFR, например амфирегулин, TGF-α, а херегулин индуцирует как проток, так и лобулоальвеолярный развитие даже при отсутствии эстроген и прогестерон.[14][15]
Роль в заболевании человека
Рак
Мутации которые приводят к сверхэкспрессии EGFR (известной как повышающая регуляция или амплификация), были связаны с рядом раки, включая аденокарцинома легкого (40% случаев), анальный рак,[16] глиобластома (50%) и эпителиальные опухоли головы и шеи (80-100%).[17] Эти соматические мутации с участием EGFR приводят к его постоянной активации, что приводит к неконтролируемому делению клеток.[18] В глиобластома часто наблюдается специфическая мутация EGFR, называемая EGFRvIII.[19] Мутации, амплификации или неправильная регуляция EGFR или членов семьи вовлечены примерно в 30% всех эпителиальный раки.[нужна цитата ]
Воспалительное заболевание
Аберрантная передача сигналов EGFR участвует в псориазе, экземе и атеросклерозе.[20][21] Однако его точные роли в этих условиях не определены.
Моногенное заболевание
У одного ребенка с воспалением полиорганного эпителия обнаружена гомозиготная мутация потери функции в EGFR ген. Патогенность мутации EGFR подтверждена экспериментами in vitro и функциональным анализом биопсии кожи. Его тяжелый фенотип отражает результаты многих предыдущих исследований функции EGFR. Его клинические особенности включали папулопустулезную сыпь, сухость кожи, хроническую диарею, аномалии роста волос, затрудненное дыхание и дисбаланс электролитов.[22]
Заживление ран и фиброз
Было показано, что EGFR играет важную роль в TGF-beta1 зависимый фибробласт к миофибробласт дифференциация.[23][24] Абсолютное упорство миофибробласты в тканях может привести к прогрессированию ткани фиброз, нарушение функции ткани или органа (например, кожи гипертрофический или же келоид шрамы, цирроз печени, фиброз миокарда, хроническая болезнь почек ).
Медицинские приложения
Цель лекарства
Идентификация EGFR как онкоген привела к разработке противоопухолевых терапевтических средств, направленных против EGFR (так называемых «ингибиторов EGFR»), включая гефитиниб,[25] эрлотиниб, афатиниб, бригатиниб и икотиниб[26] для рака легких, и цетуксимаб за рак толстой кишки. Совсем недавно AstraZeneca разработала Осимертиниб, ингибитор тирозинкиназы третьего поколения.[27]
Многие терапевтические подходы нацелены на EGFR. Цетуксимаб и панитумумаб являются примерами моноклональное антитело ингибиторы. Однако первый из IgG1 тип, последний из IgG2 тип; последствия для антителозависимая клеточная цитотоксичность может быть совсем другим.[28] Другие моноклональные препараты, находящиеся в клинической разработке: залутумумаб, нимотузумаб, и матузумаб. Моноклональные антитела блокируют внеклеточный лиганд-связывающий домен. Когда сайт связывания заблокирован, сигнальные молекулы больше не могут прикрепляться к нему и активировать тирозинкиназу.
Другой метод заключается в использовании небольших молекул для ингибирования тирозинкиназы EGFR, которая находится на цитоплазматической стороне рецептора. Без киназной активности EGFR не может активироваться, что является предпосылкой для связывания нижележащих адаптерных белков. Якобы за счет остановки сигнального каскада в клетках, которые полагаются на этот путь роста, замедляется пролиферация и миграция опухоли. Гефитиниб, эрлотиниб, бригатиниб и лапатиниб (смешанный ингибитор EGFR и ERBB2) являются примерами малых молекул киназа ингибиторы.
CimaVax-EGF, активный вакцина ориентируясь на EGF как на основной лиганд EGF использует другой подход, повышая антитела против самого EGF, тем самым отрицая пролиферативный стимул для EGFR-зависимого рака;[29] он используется в качестве лечения рака против немелкоклеточный рак легкого (наиболее распространенная форма рака легких) на Кубе и проходит дальнейшие испытания на предмет возможного лицензирования в Японии, Европе и США.[30]
Существует несколько доступных количественных методов, которые используют обнаружение фосфорилирования белка для идентификации ингибиторов семейства EGFR.[31]
Новые препараты, такие как осимертиниб, гефитиниб, эрлотиниб и бригатиниб напрямую нацеливаться на EGFR. Пациенты были разделены на EGFR-положительные и EGFR-отрицательные в зависимости от того, обнаруживает ли тканевый тест мутацию. EGFR-положительные пациенты показали 60% -ный ответ, что превышает уровень ответа для обычной химиотерапии.[32]
Однако у многих пациентов развивается резистентность. Двумя основными источниками устойчивости являются мутация T790M и онкоген MET.[32] Однако по состоянию на 2010 г. не было ни единого мнения о принятом подходе к борьбе с устойчивостью, ни одобрения FDA конкретной комбинации. Отчет о результатах фазы II клинических испытаний для бригатиниб нацеленный на мутацию T790M, и бригатиниб получил статус прорывной терапии FDA в феврале 2015 года.
Самый распространенный вредное влияние ингибиторов EGFR, обнаруженных более чем у 90% пациентов, является папулопустулезный сыпь, распространяющаяся по лицу и туловищу; наличие сыпи коррелирует с противоопухолевым действием препарата.[33] У 10–15% пациентов последствия могут быть серьезными и требовать лечения.[34][35]
Некоторые тесты нацелены на прогнозирование пользы от лечения EGFR, поскольку Veristrat.[36]
В 2014 году сообщалось, что лабораторные исследования с использованием генно-инженерных стволовых клеток для нацеливания на EGFR у мышей оказались многообещающими.[37] EGFR является хорошо известной мишенью для моноклональных антител и специфических ингибиторов тирозинкиназы.[38]
Мишень для агентов визуализации
Были разработаны агенты визуализации, которые идентифицируют EGFR-зависимые раки с использованием меченого EGF.[39] Возможность визуализации экспрессии EGFR in vivo была продемонстрирована в нескольких исследованиях.[40][41]
Взаимодействия
Было показано, что рецептор эпидермального фактора роста взаимодействовать с:
- AR,[42][43]
- ARF4,[44]
- CAV1,[45]
- CAV3,[45]
- CBL,[46][47][48][49][50]
- CBLB,[47][51]
- CBLC,[52][53]
- CD44,[23]
- CDC25A,[54]
- CRK,[51][55]
- CTNNB1,[56][57][58]
- DCN,[59][60]
- EGF,[61][62]
- GRB14,[63]
- Grb2,[51][61][63][64][65][66][67][68][69][70]
- JAK2,[71]
- MUC1,[72][73]
- NCK1,[64][74][75]
- NCK2[64][76][77]
- PKC альфа,[78]
- PLCG1,[46][79]
- PLSCR1,[80]
- ПТПН1,[81][82]
- ПТПН11,[51][83]
- ПТПН6,[83][84]
- ПТПРК,[85]
- SH2D3A,[86]
- SH3KBP1,[87][88]
- SHC1,[51][89]
- SOS1,[69][90][91]
- Src,[71][92][93]
- STAT1,[71][94]
- STAT3,[71][95]
- STAT5A,[51][71]
- UBC,[48][49][96] и
- БЫЛ,[97]
- PAR2.[98]
У плодовых мух рецептор эпидермального фактора роста взаимодействует с Шпиц.[99]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000146648 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск ансамбля 89: ENSMUSG00000020122 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Хербст RS (2004). «Обзор биологии рецепторов эпидермального фактора роста». Международный журнал радиационной онкологии, биологии, физики. 59 (2 Дополнение): 21–6. Дои:10.1016 / j.ijrobp.2003.11.041. PMID 15142631.
- ^ Чжан Х., Березов А., Ван Ц., Чжан Г., Дребин Дж., Мурали Р., Грин М. И. (август 2007 г.). «Рецепторы ErbB: от онкогенов до таргетного лечения рака». Журнал клинических исследований. 117 (8): 2051–8. Дои:10.1172 / JCI32278. ЧВК 1934579. PMID 17671639.
- ^ Обратите внимание: полный список лигандов, способных активировать EGFR и других членов семейства ErbB, приведен в ErbB статья).
- ^ Yarden Y, Schlessinger J (март 1987 г.). «Эпидермальный фактор роста индуцирует быструю обратимую агрегацию очищенного рецептора эпидермального фактора роста». Биохимия. 26 (5): 1443–51. Дои:10.1021 / bi00379a035. PMID 3494473.
- ^ Вниз Дж., Паркер П., Уотерфилд, Мэриленд (1984). «Сайты аутофосфорилирования на рецепторе эпидермального фактора роста». Природа. 311 (5985): 483–5. Bibcode:1984Натура.311..483D. Дои:10.1038 / 311483a0. PMID 6090945. S2CID 4332354.
- ^ Ода К., Мацуока Ю., Фунахаши А., Китано Н. (2005). «Комплексная карта путей передачи сигналов рецептора эпидермального фактора роста». Молекулярная системная биология. 1 (1): E1 – E17. Дои:10.1038 / msb4100014. ЧВК 1681468. PMID 16729045.
- ^ Себастьян Дж., Ричардс Р.Г., Уокер М.П., Визен Дж.Ф., Верб З., Деринк Р., Хом Ю.К., Кунья Г.Р., ДиАугустин Р.П. (сентябрь 1998 г.). «Активация и функция рецептора эпидермального фактора роста и erbB-2 во время морфогенеза молочной железы». Рост и дифференциация клеток. 9 (9): 777–85. PMID 9751121.
- ^ Макбрайан Дж, Хаулин Дж, Наполетано С, Мартин Ф (июнь 2008 г.). «Амфирегулин: роль в развитии молочной железы и раке груди». Журнал биологии и неоплазии молочных желез. 13 (2): 159–69. Дои:10.1007 / s10911-008-9075-7. PMID 18398673. S2CID 13229645.
- ^ Sternlicht MD, Sunnarborg SW (июнь 2008 г.). «Ось ADAM17-амфирегулин-EGFR в развитии и раке молочной железы». Журнал биологии и неоплазии молочных желез. 13 (2): 181–94. Дои:10.1007 / s10911-008-9084-6. ЧВК 2723838. PMID 18470483.
- ^ Кенни Нью-Джерси, Боуман А., Корач К.С., Барретт Дж. К., Саломон Д.С. (май 2003 г.). «Влияние экзогенных эпидермально-подобных факторов роста на развитие и дифференциацию молочной железы у мышей с нокаутом рецептора эстрогена-альфа (ERKO)». Исследования и лечение рака груди. 79 (2): 161–73. Дои:10.1023 / а: 1023938510508. PMID 12825851. S2CID 30782707.
- ^ Кенни Нью-Джерси, Смит Г.Х., Розенберг К., Катлер М.Л., Диксон Р.Б. (декабрь 1996 г.). «Индукция протокового морфогенеза и лобулярной гиперплазии амфирегулином в молочной железе мыши». Рост и дифференциация клеток. 7 (12): 1769–81. PMID 8959346.
- ^ Уокер Ф., Абрамовиц Л., Бенабдеррахман Д., Дюваль Икс, Дескатуар В., Хенин Д., Лехи Т., Апарисио Т. (ноябрь 2009 г.). «Экспрессия рецептора фактора роста при плоскоклеточном поражении заднего прохода: модификации, связанные с онкогенным вирусом папилломы человека и вирусом иммунодефицита человека». Патология человека. 40 (11): 1517–27. Дои:10.1016 / j.humpath.2009.05.010. PMID 19716155.
- ^ Кумар В., Аббас А., Астер Дж. (2013). Основная патология Роббинса. Филадельфия: Эльзевьер / Сондерс. п. 179. ISBN 9781437717815.
- ^ Линч Т.Дж., Белл Д.В., Сорделла Р., Гурубхагаватула С., Окимото Р.А., Бранниган Б.В., Харрис П.Л., Хазерлат С.М., Супко Дж. Г., Халуска Ф. Г., Луис Д. Н., Кристиани Д. К., Сеттлман Дж., Хабер Д. А. (май 2004 г.). «Активирующие мутации в рецепторе эпидермального фактора роста, лежащие в основе реакции немелкоклеточного рака легкого на гефитиниб» (PDF). Медицинский журнал Новой Англии. 350 (21): 2129–39. Дои:10.1056 / NEJMoa040938. PMID 15118073.
- ^ Куан CT, Викстранд CJ, Бигнер Д.Д. (июнь 2001 г.). «Мутантный рецептор VIII EGF как молекулярная мишень в терапии рака». Эндокринный рак. 8 (2): 83–96. Дои:10.1677 / erc.0.0080083. PMID 11397666. S2CID 11790891.
- ^ Йост М., Кари С., Родек Ю. (2000). «Рецептор EGF - важный регулятор множества эпидермальных функций». Европейский журнал дерматологии. 10 (7): 505–10. PMID 11056418.
- ^ Dreux AC, Lamb DJ, Modjtahedi H, Ferns GA (май 2006 г.). «Рецепторы эпидермального фактора роста и их семейство лигандов: их предполагаемая роль в атерогенезе». Атеросклероз. 186 (1): 38–53. Дои:10.1016 / j.atherosclerosis.2005.06.038. PMID 16076471.
- ^ Кэмпбелл П., Мортон П. Е., Такеичи Т., Салам А., Робертс Н., Праудфут Л. Э., Меллерио Дж. Э., Амину К., Веллингтон С., Патил С. Н., Акияма М., Лю Л., Макмиллан Дж. Р., Аристодему С., Исида-Ямамото А., Абдул-Вахаб A, Петроф Дж., Фонг К., Харнчовонг С., Стоун К.Л., Харпер Дж. И., Маклин У.Х., Симпсон М.А., Парсонс М., МакГрат Дж. А. (октябрь 2014 г.). «Эпителиальное воспаление в результате наследственной мутации потери функции в EGFR». Журнал следственной дерматологии. 134 (10): 2570–8. Дои:10.1038 / jid.2014.164. ЧВК 4090136. PMID 24691054.
- ^ а б Мидгли А.С., Роджерс М., Халлетт МБ, Клейтон А., Боуэн Т., Филипс А.О., Стедман Р. (май 2013 г.). «Трансформация стимулированного фактором роста-β1 (TGF-β1) фибробласта в дифференцировку миофибробластов опосредуется рецептором эпидермального фактора роста (EGFR), поддерживаемым гиалуронаном (HA), и совместной локализацией CD44 в липидных рафтах». Журнал биологической химии. 288 (21): 14824–38. Дои:10.1074 / jbc.M113.451336. ЧВК 3663506. PMID 23589287.
- ^ Midgley AC, Bowen T, Phillips AO, Steadman R (апрель 2014 г.). «Ингибирование MicroRNA-7 восстанавливает возрастную потерю рецептора эпидермального фактора роста и гиалуронан-зависимую дифференцировку в фибробластах». Ячейка старения. 13 (2): 235–44. Дои:10.1111 / acel.12167. ЧВК 4331777. PMID 24134702.
- ^ Паез Дж. Г., Янне П. А., Ли Дж. К., Трейси С., Грейлих Х., Габриэль С., Херман П., Кэй Ф. Дж., Линдеман Н., Боггон Т. Дж., Наоки К., Сасаки Х., Фуджи Й., Эк MJ, Селлерс В. Р., Джонсон Б. Е., Мейерсон М. (Июнь 2004 г.). «Мутации EGFR при раке легких: корреляция с клиническим ответом на терапию гефитинибом». Наука. 304 (5676): 1497–500. Bibcode:2004Научный ... 304.1497P. Дои:10.1126 / science.1099314. PMID 15118125.
- ^ Лян В, Ву X, Фанг В, Чжао И, Ян И, Ху З, Сюэ Ц, Чжан Дж, Чжан Дж, Ма И, Чжоу Т, Янь И, Хоу Х, Цинь Т, Динлинь Х, Тиан И, Хуан П , Хуан И, Чжао Х, Чжан Л. (12 февраля 2014 г.). «Сетевой мета-анализ эрлотиниба, гефитиниба, афатиниба и икотиниба у пациентов с распространенным немелкоклеточным раком легкого, несущим мутации EGFR». PLOS ONE. 9 (2): e85245. Bibcode:2014PLoSO ... 985245L. Дои:10.1371 / journal.pone.0085245. ЧВК 3922700. PMID 24533047.
- ^ Greig SL (февраль 2016 г.). «Осимертиниб: первое глобальное одобрение». Наркотики. 76 (2): 263–73. Дои:10.1007 / s40265-015-0533-4. PMID 26729184. S2CID 45076898.
- ^ Ян Л., Бекман Р.А. (октябрь 2005 г.). «Фармакогенетика и фармакогеномика в разработке терапевтических онкологических антител». Биотехнологии. 39 (4): 565–8. Дои:10.2144/000112043. PMID 16235569.
- ^ Родригес П.К., Родригес Дж., Гонсалес Дж., Лаге А. (зима 2010 г.). «Клиническая разработка и перспективы CIMAvax EGF, кубинской вакцины для терапии немелкоклеточного рака легкого». Обзор MEDICC. 12 (1): 17–23. Дои:10.37757 / MR2010.V12.N1.4. PMID 20387330.
- ^ Патель Н (11 мая 2015 г.). «На Кубе есть вакцина против рака легких - и Америка этого хочет». Проводной. Получено 13 мая 2015.
- ^ Olive DM (октябрь 2004 г.). «Количественные методы анализа фосфорилирования белков при разработке лекарств». Экспертный обзор протеомики. 1 (3): 327–41. Дои:10.1586/14789450.1.3.327. PMID 15966829. S2CID 30003827.
- ^ а б Джекман Д.М., Миллер В.А., Чоффреди Л.А., Йеап Б.А., Янне П.А., Рили Г.Дж., Руис М.Г., Джакконе Г., Секвист Л.В., Джонсон Б.Е. (август 2009 г.). «Влияние рецептора эпидермального фактора роста и мутаций KRAS на клинические исходы у ранее нелеченных пациентов с немелкоклеточным раком легкого: результаты онлайн-реестра опухолей клинических испытаний». Клинические исследования рака. 15 (16): 5267–73. Дои:10.1158 / 1078-0432.CCR-09-0888. ЧВК 3219530. PMID 19671843.
- ^ Лю HB, Wu Y, Lv TF, Yao YW, Xiao YY, Yuan DM, Song Y (2013). «Кожная сыпь может предсказать реакцию на ингибитор тирозинкиназы EGFR и прогноз для пациентов с немелкоклеточным раком легкого: систематический обзор и метаанализ». PLOS ONE. 8 (1): e55128. Bibcode:2013PLoSO ... 855128L. Дои:10.1371 / journal.pone.0055128. ЧВК 3559430. PMID 23383079.
- ^ Гербер П.А., Меллер С., Имс Т., Бурен Б.А., Шрампф Х., Хетцер С., Эманн Л.М., Будах В., Бёльке Э., Матушек С., Волленберг А., Хоми Б. (2012). «Лечение сыпи, связанной с ингибиторами EGFR: ретроспективное исследование с участием 49 пациентов». Европейский журнал медицинских исследований. 17 (1): 4. Дои:10.1186 / 2047-783X-17-4. ЧВК 3351712. PMID 22472354.
- ^ Lacouture ME (октябрь 2006 г.). «Механизмы кожной токсичности ингибиторов EGFR». Обзоры природы. Рак. 6 (10): 803–12. Дои:10.1038 / nrc1970. PMID 16990857. S2CID 7782594.
- ^ Молина-Пинело С., пастор, доктор медицинских наук, Пас-Арес Л. (февраль 2014 г.). «VeriStrat: прогностический и / или предсказывающий биомаркер для пациентов с запущенным раком легких?». Экспертный обзор респираторной медицины. 8 (1): 1–4. Дои:10.1586/17476348.2014.861744. PMID 24308656. S2CID 44854672.
- ^ Стаки Д.В., Хингтген С.Д., Каракас Н., Рич Б.Е., Шах К. (февраль 2015 г.). «Разработка устойчивых к токсинам терапевтических стволовых клеток для лечения опухолей головного мозга». Стволовые клетки. 33 (2): 589–600. Дои:10.1002 / стержень.1874. ЧВК 4305025. PMID 25346520.
- ^ Роскоски Р-младший (2014). «Семейство протеин-тирозинкиназ и рака ErbB / HER». Pharmacol Res. 79: 34–74. Дои:10.1016 / j.phrs.2013.11.002. PMID 24269963.
- ^ Лукас Л.Дж., Теллез Калифорния, Кастильо М.Л., Ли К.Л., Хупман М.А., Виейра Л.С., Феррейра И., Раниеро Л., Хьюитт К.С. (май 2015 г.). «Разработка чувствительного, стабильного и специфичного для EGFR агента молекулярной визуализации для поверхностно-усиленной рамановской спектроскопии». Журнал Рамановской спектроскопии. 46 (5): 434–446. Bibcode:2015JRSp ... 46..434L. Дои:10.1002 / jrs.4678.
- ^ Лукас Л.Дж., Чен XK, Смит А.Дж., Корбелик М., Зенг, Гаитян Л., Ли П.В., Хьюитт К.С. (23 января 2015 г.). «Агрегация наночастиц в эндосомах и лизосомах производит спектроскопию комбинационного рассеяния с усилением поверхности». Журнал нанофотоники. 9 (1): 093094–1–14. Bibcode:2015JNano ... 9.3094L. Дои:10.1117 / 1.JNP.9.093094.
- ^ Андерссон К.Г., Оружени М., Гаруси Дж., Митран Б., Шталь С., Орлова А., Лёфблом Дж., Толмачев В. (декабрь 2016 г.). «Возможность визуализации экспрессии рецептора эпидермального фактора роста с помощью ZEGFR: 2377 аффитной молекулы, меченной 99mTc, с использованием цистеинсодержащего хелатора на основе пептидов». Международный журнал онкологии. 49 (6): 2285–2293. Дои:10.3892 / ijo.2016.3721. ЧВК 5118000. PMID 27748899.
- ^ Бонаккорси Л., Карлони В., Муратори М., Формигли Л., Зекки С., Форти Г., Балди Э. (октябрь 2004 г.). «Передача сигналов рецептора EGF (EGFR), способствующая инвазии, нарушается в андроген-чувствительных клетках рака простаты за счет взаимодействия между EGFR и рецептором андрогена (AR)». Международный журнал рака. 112 (1): 78–86. Дои:10.1002 / ijc.20362. HDL:2158/395766. PMID 15305378. S2CID 46121331.
- ^ Бонаккорси Л., Муратори М., Карлони В., Марчиани С., Формигли Л., Форти Дж., Балди Е. (август 2004 г.). «Рецептор андрогена связывается с рецептором эпидермального фактора роста в андроген-чувствительных клетках рака простаты». Стероиды. 69 (8–9): 549–52. Дои:10.1016 / j.steroids.2004.05.011. HDL:2158/395763. PMID 15288768. S2CID 23831527.
- ^ Ким С.В., Хаяши М., Ло Дж. Ф., Ян Й, Ю Дж. С., Ли Дж. Д. (январь 2003 г.). «Малая ГТФаза фактора 4 АДФ-рибозилирования опосредует активацию фосфолипазы D2, зависимую от рецептора эпидермального фактора роста». Журнал биологической химии. 278 (4): 2661–8. Дои:10.1074 / jbc.M205819200. PMID 12446727.
- ^ а б Couet J, Sargiacomo M, Lisanti MP (ноябрь 1997 г.). «Взаимодействие рецепторной тирозинкиназы EGF-R с кавеолинами. Связывание кавеолина негативно регулирует тирозин и серин / треонинкиназную активность». Журнал биологической химии. 272 (48): 30429–38. Дои:10.1074 / jbc.272.48.30429. PMID 9374534.
- ^ а б Творогов Д., Карпентер Г. (июль 2002 г.). «EGF-зависимая ассоциация фосфолипазы C-gamma1 с c-Cbl». Экспериментальные исследования клеток. 277 (1): 86–94. Дои:10.1006 / excr.2002.5545. PMID 12061819.
- ^ а б Эттенберг С.А., Кин М.М., Нау М.М., Франкель М., Ван Л.М., Пирс Дж. Х., Липковиц С. (март 1999 г.). «cbl-b ингибирует передачу сигналов рецептора эпидермального фактора роста». Онкоген. 18 (10): 1855–66. Дои:10.1038 / sj.onc.1202499. PMID 10086340.
- ^ а б Пеннок С., Ван Зи (май 2008 г.). «История двух Cbls: взаимодействие c-Cbl и Cbl-b в подавлении рецепторов эпидермального фактора роста». Молекулярная и клеточная биология. 28 (9): 3020–37. Дои:10.1128 / MCB.01809-07. ЧВК 2293090. PMID 18316398.
- ^ а б Умэбаяси К., Стенмарк Х, Йошимори Т. (август 2008 г.). «Ubc4 / 5 и c-Cbl продолжают убиквитинировать рецептор EGF после интернализации для облегчения полиубиквитинирования и деградации». Молекулярная биология клетки. 19 (8): 3454–62. Дои:10.1091 / mbc.E07-10-0988. ЧВК 2488299. PMID 18508924.
- ^ Нг К., Джексон Р.А., Бушдорф Дж. П., Сан К., Гай Г. Р., Сивараман Дж. (Март 2008 г.). «Структурная основа для новой интрапептидильной Н-связи и обратного связывания субстратов домена c-Cbl-TKB». Журнал EMBO. 27 (5): 804–16. Дои:10.1038 / emboj.2008.18. ЧВК 2265755. PMID 18273061.
- ^ а б c d е ж Шульце WX, Дэн Л., Манн М. (2005). «Фосфотирозиновый интерактом семейства киназ рецептора ErbB». Молекулярная системная биология. 1 (1): E1 – E13. Дои:10.1038 / msb4100012. ЧВК 1681463. PMID 16729043.
- ^ Ким М., Тэдзука Т., Сузики И., Сугано С., Хираи М., Ямамото Т. (октябрь 1999 г.). «Молекулярное клонирование и характеристика нового гена семейства cbl, cbl-c». Ген. 239 (1): 145–54. Дои:10.1016 / S0378-1119 (99) 00356-X. PMID 10571044.
- ^ Кин М.М., Эттенберг С.А., Нау М.М., Банерджи П., Куэлло М., Пеннингер Дж., Липковиц С. (июнь 1999 г.). "cbl-3: новый белок семейства cbl млекопитающих". Онкоген. 18 (22): 3365–75. Дои:10.1038 / sj.onc.1202753. PMID 10362357.
- ^ Ван З, Ван М., Лазо Дж. С., Карр Б. И. (май 2002 г.). «Идентификация рецептора эпидермального фактора роста как мишени протеинфосфатазы Cdc25A». Журнал биологической химии. 277 (22): 19470–5. Дои:10.1074 / jbc.M201097200. PMID 11912208.
- ^ Хашимото Ю., Катаяма Х, Киёкава Е., Ота С., Курата Т., Гото Н., Оцука Н., Шибата М., Мацуда М. (июль 1998 г.). «Фосфорилирование адапторного белка CrkII по тирозину 221 рецептором эпидермального фактора роста». Журнал биологической химии. 273 (27): 17186–91. Дои:10.1074 / jbc.273.27.17186. PMID 9642287.
- ^ Хазан РБ, Нортон Л (апрель 1998 г.). «Рецептор эпидермального фактора роста модулирует взаимодействие Е-кадгерина с актиновым цитоскелетом». Журнал биологической химии. 273 (15): 9078–84. Дои:10.1074 / jbc.273.15.9078. PMID 9535896.
- ^ Schroeder JA, Adriance MC, McConnell EJ, Thompson MC, Pockaj B, Gendler SJ (июнь 2002 г.). «Комплексы ErbB-бета-катенин связаны с инфильтрацией протоков молочной железы человека и трансгенными карциномами вируса опухоли молочной железы мыши (MMTV) -Wnt-1 и MMTV-c-Neu». Журнал биологической химии. 277 (25): 22692–8. Дои:10.1074 / jbc.M201975200. PMID 11950845.
- ^ Такахаши К., Сузуки К., Цукатани Ю. (июль 1997 г.). «Индукция фосфорилирования тирозина и ассоциации бета-катенина с рецептором EGF при триптическом переваривании покоящихся клеток при слиянии». Онкоген. 15 (1): 71–8. Дои:10.1038 / sj.onc.1201160. PMID 9233779.
- ^ Santra M, Reed CC, Iozzo RV (сентябрь 2002 г.). «Декорин связывается с узкой областью рецептора эпидермального фактора роста (EGF), частично перекрывающейся, но отличной от эпитопа, связывающего EGF». Журнал биологической химии. 277 (38): 35671–81. Дои:10.1074 / jbc.M205317200. PMID 12105206.
- ^ Iozzo RV, Moscatello DK, McQuillan DJ, Eichstetter I (февраль 1999 г.). «Декорин - биологический лиганд рецептора эпидермального фактора роста». Журнал биологической химии. 274 (8): 4489–92. Дои:10.1074 / jbc.274.8.4489. PMID 9988678.
- ^ а б Вонг Л., Деб Т. Б., Томпсон С. А., Уэллс А., Джонсон Г. Р. (март 1999 г.). «Дифференциальная потребность в COOH-концевой области рецептора эпидермального фактора роста (EGF) в амфирегулине и митогенной передаче сигналов EGF». Журнал биологической химии. 274 (13): 8900–9. Дои:10.1074 / jbc.274.13.8900. PMID 10085134.
- ^ Stortelers C, Souriau C, van Liempt E, van de Poll ML, van Zoelen EJ (июль 2002 г.). «Роль N-конца эпидермального фактора роста в связывании ErbB-2 / ErbB-3 изучается с помощью фагового дисплея». Биохимия. 41 (27): 8732–41. Дои:10.1021 / bi025878c. PMID 12093292.
- ^ а б Дэйли Р.Дж., Сандерсон Г.М., Джейн П.В., Сазерленд Р.Л. (май 1996 г.). «Клонирование и характеристика GRB14, нового члена семейства генов GRB7». Журнал биологической химии. 271 (21): 12502–10. Дои:10.1074 / jbc.271.21.12502. PMID 8647858.
- ^ а б c Braverman LE, Quilliam LA (февраль 1999 г.). «Идентификация Grb4 / Nckbeta, адаптерного белка, содержащего домен 2 и 3 гомологии src, имеющего сходные связывающие и биологические свойства с Nck». Журнал биологической химии. 274 (9): 5542–9. Дои:10.1074 / jbc.274.9.5542. PMID 10026169.
- ^ Благоев Б., Кратчмарова И., Онг С.Е., Нильсен М., Фостер Л.Дж., Манн М. (март 2003 г.). «Протеомическая стратегия для выяснения функциональных белок-белковых взаимодействий, применяемая к передаче сигналов EGF». Природа Биотехнологии. 21 (3): 315–8. Дои:10.1038 / nbt790. PMID 12577067. S2CID 26838266.
- ^ Онеяма С., Накано Х., Шарма С.В. (март 2002 г.). «UCS15A, новое низкомолекулярное лекарство, блокирующее белок-белковое взаимодействие, опосредованное SH3-доменом». Онкоген. 21 (13): 2037–50. Дои:10.1038 / sj.onc.1205271. PMID 11960376.
- ^ Окутани Т., Окабаяси Ю., Кидо Ю., Сугимото Ю., Сакагути К., Матуока К., Такенава Т., Касуга М. (декабрь 1994 г.). «Grb2 / Ash связывается непосредственно с тирозинами 1068 и 1086 и косвенно с тирозином 1148 активированных рецепторов эпидермального фактора роста человека в интактных клетках». Журнал биологической химии. 269 (49): 31310–4. PMID 7527043.
- ^ Tortora G, Damiano V, Bianco C, Baldassarre G, Bianco AR, Lanfrancone L, Pelicci PG, Ciardiello F (февраль 1997 г.). «Субъединица RIalpha протеинкиназы A (PKA) связывается с Grb2 и обеспечивает взаимодействие PKA с активированным рецептором EGF». Онкоген. 14 (8): 923–8. Дои:10.1038 / sj.onc.1200906. PMID 9050991.
- ^ а б Будай Л., Иган С.Е., Родригес Вичиана П., Кантрелл Д.А., Вниз J. (март 1994 г.). «Комплекс адапторного белка Grb2, фактора обмена Sos и 36-кДа мембраносвязанного тирозинфосфопротеина участвует в активации ras в Т-клетках». Журнал биологической химии. 269 (12): 9019–23. PMID 7510700.
- ^ Ловенштейн Э.Дж., Дейли Р.Дж., Батцер А.Г., Ли В., Марголис Б., Ламмерс Р., Ульрих А., Скольник Е.Ю., Бар-Саги Д., Шлессингер Дж. (Август 1992 г.). «Белок GRB2, содержащий SH2- и SH3-домены, связывает рецепторные тирозинкиназы с передачей сигналов ras». Клетка. 70 (3): 431–42. Дои:10.1016 / 0092-8674 (92) 90167-Б. PMID 1322798.
- ^ а б c d е Olayioye MA, Beuvink I., Horsch K, Daly JM, Hynes NE (июнь 1999 г.). «Индуцированная рецептором ErbB активация факторов транскрипции stat опосредуется тирозинкиназами Src». Журнал биологической химии. 274 (24): 17209–18. Дои:10.1074 / jbc.274.24.17209. PMID 10358079.
- ^ Шредер Дж. А., Томпсон М. С., Гарднер М. М., Гендлер С. Дж. (Апрель 2001 г.). «Трансгенный MUC1 взаимодействует с рецептором эпидермального фактора роста и коррелирует с активацией митоген-активируемой протеинкиназы в молочной железе мыши». Журнал биологической химии. 276 (16): 13057–64. Дои:10.1074 / jbc.M011248200. PMID 11278868.
- ^ Ли Й, Рен Дж, Ю В, Ли Кью, Кувахара Х, Инь Л., Каррауэй К.Л., Куфе Д. (сентябрь 2001 г.). «Рецептор эпидермального фактора роста регулирует взаимодействие антигена карциномы человека DF3 / MUC1 с c-Src и бета-катенином». Журнал биологической химии. 276 (38): 35239–42. Дои:10.1074 / jbc.C100359200. PMID 11483589.
- ^ Тан Дж., Фэн Г.С., Ли В. (октябрь 1997 г.). «Индуцированное прямое связывание адаптера белка Nck с белком p62, активирующим ГТФазу, с помощью эпидермального фактора роста». Онкоген. 15 (15): 1823–32. Дои:10.1038 / sj.onc.1201351. PMID 9362449.
- ^ Ли В., Ху П., Скольник Е. Ю., Ульрих А., Шлессингер Дж. (Декабрь 1992 г.). «Белок Nck, содержащий SH2- и SH3-домены, является онкогенным и является общей мишенью для фосфорилирования различными поверхностными рецепторами». Молекулярная и клеточная биология. 12 (12): 5824–33. Дои:10.1128 / MCB.12.12.5824. ЧВК 360522. PMID 1333047.
- ^ Чен М., Ше Х., Дэвис Э.М., Спайсер С.М., Ким Л., Рен Р., Ле Бо М.М., Ли В. (сентябрь 1998 г.). «Идентификация генов семейства Nck, хромосомная локализация, экспрессия и специфичность передачи сигналов». Журнал биологической химии. 273 (39): 25171–8. Дои:10.1074 / jbc.273.39.25171. PMID 9737977.
- ^ Ту И, Ли Ф, Ву Ц (декабрь 1998 г.). «Nck-2, новый адаптерный белок, содержащий гомологию Src2 / 3, который взаимодействует с LIM-единственным белком PINCH и компонентами сигнальных путей киназы рецептора фактора роста». Молекулярная биология клетки. 9 (12): 3367–82. Дои:10.1091 / mbc.9.12.3367. ЧВК 25640. PMID 9843575.
- ^ Готье М.Л., Торретто С., Ли Дж., Франческатти В., О'Дей Д.Х. (август 2003 г.). «Протеинкиназа Calpha отрицательно регулирует распространение и подвижность клеток в клетках рака молочной железы человека MDA-MB-231, расположенных ниже рецептора эпидермального фактора роста». Сообщения о биохимических и биофизических исследованиях. 307 (4): 839–46. Дои:10.1016 / S0006-291X (03) 01273-7. PMID 12878187.
- ^ Бедрин М.С., Аболафия С.М., Томпсон Дж. Ф. (июль 1997 г.). «Цитоскелетная ассоциация рецептора эпидермального фактора роста и ассоциированных сигнальных белков регулируется плотностью клеток в кишечных клетках IEC-6». Журнал клеточной физиологии. 172 (1): 126–36. Дои:10.1002 / (SICI) 1097-4652 (199707) 172: 1 <126 :: AID-JCP14> 3.0.CO; 2-A. PMID 9207933.
- ^ Сан Дж., Нанджундан М., Пайк Л.Дж., Видмер Т., Симс П.Дж. (май 2002 г.). «Фосфолипидная скрамблаза 1 плазматической мембраны обогащена липидными рафтами и взаимодействует с рецептором эпидермального фактора роста». Биохимия. 41 (20): 6338–45. Дои:10.1021 / bi025610l. PMID 12009895.
- ^ Сармиенто М., Пуйус Ю.А., Веттер С.В., Кенг Ю.Ф., Ву Л., Чжао Ю., Лоуренс Д.С., Альмо С.К., Чжан З.Й. (июль 2000 г.). «Структурные основы пластичности в распознавании субстрата протеинтирозинфосфатазы 1B». Биохимия. 39 (28): 8171–9. Дои:10.1021 / bi000319w. PMID 10889023.
- ^ Чжан З.Й., Уолш А.Б., Ву Л., Макнамара Д.Д., Добрусин Е.М., Миллер В.Т. (март 1996 г.). «Детерминанты распознавания субстрата в протеин-тирозинфосфатазе, PTP1». Журнал биологической химии. 271 (10): 5386–92. Дои:10.1074 / jbc.271.10.5386. PMID 8621392.
- ^ а б Томич С., Грейзер У., Ламмерс Р., Харитоненков А., Имянитов Э., Ульрих А., Бёмер Ф. Д. (сентябрь 1995 г.). «Ассоциация тирозинфосфатаз SH2-домена с рецептором эпидермального фактора роста в опухолевых клетках человека. Фосфатидная кислота активирует дефосфорилирование рецептора с помощью PTP1C». Журнал биологической химии. 270 (36): 21277–84. Дои:10.1074 / jbc.270.36.21277. PMID 7673163.
- ^ Кейлхак Х., Тенев Т., Ньякатура Э., Годовац-Циммерманн Дж., Нильсен Л., Зеедорф К., Бёмер Ф. Д. (сентябрь 1998 г.). «Фосфотирозин 1173 опосредует связывание протеин-тирозинфосфатазы SHP-1 с рецептором эпидермального фактора роста и ослабление передачи сигналов рецептора». Журнал биологической химии. 273 (38): 24839–46. Дои:10.1074 / jbc.273.38.24839. PMID 9733788.
- ^ Ван С.Е., Ву Ф.Й., Шин И, Цюй С., Артеага С.Л. (июнь 2005 г.). «Трансформирующий фактор роста {бета} (TGF- {бета}) - для функции TGF- {бета} необходим рецептор тирозинфосфатазы белка тирозинфосфатазы типа каппа». Молекулярная и клеточная биология. 25 (11): 4703–15. Дои:10.1128 / MCB.25.11.4703-4715.2005. ЧВК 1140650. PMID 15899872.
- ^ Лу И, Браш Дж, Стюарт Т.А. (апрель 1999 г.). «NSP1 определяет новое семейство адаптерных белков, связывающих рецепторы интегрина и тирозинкиназы с сигнальным путем N-концевой киназы / стресс-активируемой протеинкиназы c-Jun». Журнал биологической химии. 274 (15): 10047–52. Дои:10.1074 / jbc.274.15.10047. PMID 10187783.
- ^ Субейран П., Кованец К., Шимкевич И., Лэнгдон В. Ю., Дикич И. (март 2002 г.). «Комплекс Cbl-CIN85-эндофилин опосредует лиганд-индуцированное подавление рецепторов EGF». Природа. 416 (6877): 183–7. Bibcode:2002Натура.416..183С. Дои:10.1038 / 416183a. PMID 11894095. S2CID 635702.
- ^ Шимкевич И., Кованец К., Субейран П., Динарина А., Липковиц С., Дикич И. (октябрь 2002 г.). «CIN85 участвует в Cbl-b-опосредованном подавлении рецепторных тирозинкиназ». Журнал биологической химии. 277 (42): 39666–72. Дои:10.1074 / jbc.M205535200. PMID 12177062.
- ^ Сакагути К., Окабаяси Ю., Кидо Ю., Кимура С., Мацумура Ю., Инусима К., Касуга М. (апрель 1998 г.). «Фосфотирозинсвязывающий домен Shc преимущественно взаимодействует с рецепторами эпидермального фактора роста и опосредует активацию Ras в интактных клетках». Молекулярная эндокринология. 12 (4): 536–43. Дои:10.1210 / мэ.12.4.536. PMID 9544989.
- ^ Цянь X, Эстебан Л., Васс В.К., Упадхьяя К., Папажордж А.Г., Йенгер К., Уорд Дж. М., Лоуи Д. Р., Сантос Е. (февраль 2000 г.) «Факторы обмена, специфичные для Sos1 и Sos2 Ras: различия в экспрессии плаценты и сигнальных свойствах». Журнал EMBO. 19 (4): 642–54. Дои:10.1093 / emboj / 19.4.642. ЧВК 305602. PMID 10675333.
- ^ Qian X, Vass WC, Papageorge AG, Anborgh PH, Lowy DR (февраль 1998 г.). «N-конец фактора обмена Sos1 Ras: критические роли для доменов гомологии Dbl и плекстрина». Молекулярная и клеточная биология. 18 (2): 771–8. Дои:10.1128 / mcb.18.2.771. ЧВК 108788. PMID 9447973.
- ^ Кили С.Дж., Каландрелла С.О., Барретт К.Э. (апрель 2000 г.). «Карбахол-стимулированная трансактивация рецептора эпидермального фактора роста и митоген-активируемой протеинкиназы в клетках Т (84) опосредуется внутриклеточным Ca2 +, PYK-2 и p60 (src)». Журнал биологической химии. 275 (17): 12619–25. Дои:10.1074 / jbc.275.17.12619. PMID 10777553.
- ^ Сато К., Кимото М., Какумото М., Хориучи Д., Ивасаки Т., Токмаков А.А., Фуками Ю. (сентябрь 2000 г.). «Адаптерный белок Shc подвергается транслокации и опосредует повышающую регуляцию тирозинкиназы c-Src в EGF-стимулированных клетках A431». Гены в клетки. 5 (9): 749–64. Дои:10.1046 / j.1365-2443.2000.00358.x. PMID 10971656. S2CID 26366427.
- ^ Xia L, Wang L, Chung AS, Иванов С.С., Ling MY, Dragoi AM, Platt A, Gilmer TM, Fu XY, Chin YE (август 2002 г.). «Идентификация как положительных, так и отрицательных доменов в COOH-концевой области рецептора эпидермального фактора роста для преобразователя сигнала и активатора активации транскрипции (STAT)». Журнал биологической химии. 277 (34): 30716–23. Дои:10.1074 / jbc.M202823200. PMID 12070153.
- ^ Юань З.Л., Гуань Ю.Дж., Ван Л., Вэй В., Кейн А.Б., Чин Ю.Э. (ноябрь 2004 г.). «Центральная роль остатка треонина в петле p + 1 рецепторной тирозинкиназы в конститутивном фосфорилировании STAT3 в метастатических раковых клетках». Молекулярная и клеточная биология. 24 (21): 9390–400. Дои:10.1128 / MCB.24.21.9390-9400.2004. ЧВК 522220. PMID 15485908.
- ^ Сехат Б., Андерссон С., Гирнита Л., Ларссон О. (июль 2008 г.). «Идентификация c-Cbl как новой лигазы для рецептора инсулиноподобного фактора роста-I с различными ролями от Mdm2 в убиквитинировании рецептора и эндоцитозе». Исследования рака. 68 (14): 5669–77. Дои:10.1158 / 0008-5472.CAN-07-6364. PMID 18632619.
- ^ She HY, Rockow S, Tang J, Nishimura R, Skolnik EY, Chen M, Margolis B, Li W (сентябрь 1997 г.). «Белок синдрома Вискотта-Олдрича связан с адаптерным белком Grb2 и рецептором эпидермального фактора роста в живых клетках». Молекулярная биология клетки. 8 (9): 1709–21. Дои:10.1091 / mbc.8.9.1709. ЧВК 305731. PMID 9307968.
- ^ Цзян Ю., Лим Дж., Ву К.С., Сюй В., Суен Дж.Й., Фэрли Д.П. (ноябрь 2020 г.). «PAR2 индуцирует подвижность клеток рака яичников путем слияния трех сигнальных путей для трансактивации EGFR». Британский журнал фармакологии. (н / д) ((н / д)). Дои:10.1111 / bph.15332. PMID 33226635 Проверять
| pmid =ценить (помощь). - ^ Шило БЖ (март 2003 г.). «Передача сигналов по пути рецептора эпидермального фактора роста дрозофилы во время развития». Экспериментальные исследования клеток. 284 (1): 140–9. Дои:10.1016 / S0014-4827 (02) 00094-0. PMID 12648473.
дальнейшее чтение
- Карпентер Г (1987). «Рецепторы эпидермального фактора роста и митогенов других полипептидов». Ежегодный обзор биохимии. 56 (1): 881–914. Дои:10.1146 / annurev.bi.56.070187.004313. PMID 3039909.
- Бунстра Дж., Райкен П., Хамбель Б., Кремерс Ф., Ферклей А., ван Берген ан Хенегувен П. (май 1995 г.). «Фактор роста эпидермиса». Cell Biology International. 19 (5): 413–30. Дои:10.1006 / cbir.1995.1086. PMID 7640657. S2CID 20186286.
- Карпентер Г (август 2000 г.). «Рецептор EGF: связь для трафика и передачи сигналов». BioEssays. 22 (8): 697–707. Дои:10.1002 / 1521-1878 (200008) 22: 8 <697 :: AID-BIES3> 3.0.CO; 2-1. PMID 10918300.
- Филардо Э.Дж. (февраль 2002 г.). «Трансактивация рецептора эпидермального фактора роста (EGFR) эстрогеном через рецептор, связанный с G-белком, GPR30: новый сигнальный путь с потенциальным значением для рака груди». Журнал стероидной биохимии и молекулярной биологии. 80 (2): 231–8. Дои:10.1016 / S0960-0760 (01) 00190-X. PMID 11897506. S2CID 34995614.
- Тиганис Т. (январь 2002 г.). «Белковые тирозинфосфатазы: дефосфорилирование рецептора эпидермального фактора роста». IUBMB Life. 53 (1): 3–14. Дои:10.1080/15216540210811. PMID 12018405. S2CID 8376444.
- Ди Фьоре П.П., Scita G (октябрь 2002 г.). «Eps8 посреди GTPases». Международный журнал биохимии и клеточной биологии. 34 (10): 1178–83. Дои:10.1016 / S1357-2725 (02) 00064-X. PMID 12127568.
- Бенаим Дж., Вильялобо А. (август 2002 г.). «Фосфорилирование кальмодулина. Функциональные последствия» (PDF). Европейский журнал биохимии / FEBS. 269 (15): 3619–31. Дои:10.1046 / j.1432-1033.2002.03038.x. HDL:10261/79981. PMID 12153558.
- Leu TH, Maa MC (январь 2003 г.). «Функциональное значение взаимодействия между рецептором EGF и c-Src». Границы биологических наук. 8 (1–3): s28–38. Дои:10.2741/980. PMID 12456372. S2CID 20827945.
- Андерсон Н.Л., Андерсон Н.Г. (ноябрь 2002 г.). «Протеом плазмы человека: история, характер, диагностические перспективы». Молекулярная и клеточная протеомика. 1 (11): 845–67. Дои:10.1074 / mcp.R200007-MCP200. PMID 12488461.
- Кари С., Чан Т.О., Роша де Квадрос М., Родек Ю. (январь 2003 г.). «Нацеленность на рецептор эпидермального фактора роста при раке: апоптоз занимает центральное место». Исследования рака. 63 (1): 1–5. PMID 12517767.
- Bonaccorsi L, Muratori M, Carloni V, Zecchi S, Formigli L, Forti G, Baldi E (февраль 2003 г.). «Рецептор андрогенов и инвазия рака простаты». Международный журнал андрологии. 26 (1): 21–5. Дои:10.1046 / j.1365-2605.2003.00375.x. HDL:2158/252370. PMID 12534934.
- Reiter J, Maihle NJ (май 2003 г.). «Характеристика и экспрессия новых изоформ EGFR 60 и 110 кДа в плаценте человека». Летопись Нью-Йоркской академии наук. 995 (1): 39–47. Bibcode:2003НЯСА.995 ... 39р. Дои:10.1111 / j.1749-6632.2003.tb03208.x. PMID 12814937. S2CID 9377682.
- Адамс Т.Э., МакКерн Н.М., Уорд К.В. (июнь 2004 г.). «Передача сигналов рецептором инсулиноподобного фактора роста 1 типа: взаимодействие с рецептором эпидермального фактора роста». Факторы роста. 22 (2): 89–95. Дои:10.1080/08977190410001700998. PMID 15253384. S2CID 86844427.
- Фергюсон К.М. (ноябрь 2004 г.). «Активные и неактивные конформации рецептора эпидермального фактора роста». Сделки биохимического общества. 32 (Pt 5): 742–5. Дои:10.1042 / BST0320742. PMID 15494003.
- Chao C, Hellmich MR (декабрь 2004 г.). «Двунаправленная передача сигналов между рецепторами желудочно-кишечного пептидного гормона и рецептором эпидермального фактора роста». Факторы роста. 22 (4): 261–8. Дои:10.1080/08977190412331286900. PMID 15621729. S2CID 35208079.
- Карлссон Дж., Рен З.П., Вестер К., Сундберг А.Л., Хелдин Н.Е., Хесселагер Г., Перссон М., Гедда Л., Толмачев В., Лундквист Х., Бломквист Э., Нистер М. (март 2006 г.). «Планирование внутриполостной анти-EGFR радионуклидной терапии глиом. Обзор литературы и данные по экспрессии EGFR». Журнал нейроонкологии. 77 (1): 33–45. Дои:10.1007 / s11060-005-7410-z. PMID 16200342. S2CID 42293693.
- Скартоцци М., Пьерантони С., Берарди Р., Антоньоли С., Беарци И., Кашину С. (апрель 2006 г.). «Рецептор эпидермального фактора роста: многообещающая терапевтическая мишень для лечения колоректального рака». Аналитическая и количественная цитология и гистология. 28 (2): 61–8. PMID 16637508.
- Прудкин Л., Вистуба II (октябрь 2006 г.). «Аномалии рецепторов эпидермального фактора роста при раке легких. Патогенетические и клинические последствия». Анналы диагностической патологии. 10 (5): 306–15. Дои:10.1016 / j.anndiagpath.2006.06.011. PMID 16979526.
- Ахмед С.М., Салгия Р. (ноябрь 2006 г.). «Мутации рецептора эпидермального фактора роста и восприимчивость к таргетной терапии при раке легких». Респирология. 11 (6): 687–92. Дои:10.1111 / j.1440-1843.2006.00887.x. PMID 17052295. S2CID 38429131.
- Чжан X, Чанг А. (март 2007 г.). «Соматические мутации рецептора эпидермального фактора роста и немелкоклеточный рак легкого». Журнал медицинской генетики. 44 (3): 166–72. Дои:10.1136 / jmg.2006.046102. ЧВК 2598028. PMID 17158592.
- Коэнурам М., Саиф М.В. (2007). «Стратегии ингибирования рецепторов эпидермального фактора роста при раке поджелудочной железы: прошлое, настоящее и будущее». JOP. 8 (1): 4–15. PMID 17228128.
- Меллингхофф И.К., Cloughesy TF, Мишель П.С. (Январь 2007 г.). «PTEN-опосредованная устойчивость к ингибиторам киназы рецептора эпидермального фактора роста». Клинические исследования рака. 13 (2 Pt 1): 378–81. Дои:10.1158 / 1078-0432.CCR-06-1992. PMID 17255257.
- Накамура JL (апрель 2007 г.). «Рецептор эпидермального фактора роста в злокачественных глиомах: патогенез и терапевтическое значение». Мнение эксперта о терапевтических целях. 11 (4): 463–72. Дои:10.1517/14728222.11.4.463. PMID 17373877. S2CID 21947310.
внешняя ссылка
- Рецептор эпидермального фактора роста в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Обзор всей структурной информации, доступной в PDB за UniProt: P00533 (Рецептор эпидермального фактора роста человека) на PDBe-KB.