Пертузумаб - Pertuzumab
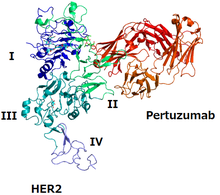 Структура HER2 и пертузумаб | |
| Моноклональные антитела | |
|---|---|
| Тип | Целое антитело |
| Источник | Гуманизированный (из мышь ) |
| Цель | HER2 |
| Клинические данные | |
| Торговые наименования | Perjeta |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | Внутривенно |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Идентификаторы | |
| Количество CAS | |
| ChemSpider |
|
| UNII | |
| КЕГГ | |
| ЧЭМБЛ | |
| | |
Пертузумаб (также называемый 2C4, торговое наименование Perjeta)[1] это моноклональное антитело используется в сочетании с трастузумаб и доцетаксел для лечения метастатических HER2 -положительный рак молочной железы; он также используется в той же комбинации, что и неоадъювантный при раннем HER2-положительном раке груди.[2]
Побочные эффекты у более чем половины людей, принимающих его, включают диарею, выпадение волос и потеря нейтрофилов; более 10% опыта потеря красных кровяных телец, гиперчувствительность или аллергическая реакция, инфузионные реакции, снижение аппетита, бессонница, нарушение вкусовых ощущений, воспаление ротовой полости или губ, запор, сыпь, болезнь ногтей и мышечные боли.[3] Беременным женщинам или планирующим забеременеть женщинам не следует принимать его, он не изучался на людях с определенными сердечными заболеваниями и должен применяться с осторожностью у таких людей, и его не следует использовать с антрациклин.[3] Неизвестно, взаимодействует ли пертузумаб с доксорубицин.[3]
Это первый в своем классе препарат под названием "ЕЕ ингибитор димеризации »- ингибирует димеризация HER2 с другими рецепторами HER, что предотвращает их сигнализация способами, которые способствуют росту и пролиферации клеток.[4]
Он был открыт и разработан Genentech, дочерняя компания Рош, и впервые был утвержден в 2012 году.[1][5]
Медицинское использование
Пертузумаб вводится внутривенно в сочетании с трастузумаб и доцетаксел в качестве лечения первой линии при HER2-положительном метастатическом раке груди.[2][3] Он также используется в той же комбинации, что и неоадъювантный (дается для уменьшения размера опухоли перед операцией или облучением) при HER2-положительном раке груди на ранней стадии; по состоянию на 2016 г. не было доказано, что это использование увеличивает выживаемость.[2]
По состоянию на 2016 год пертузумаб не изучался у людей с фракция выброса левого желудочка значение ≤ 50% от нормы, наличие в анамнезе застойной сердечной недостаточности или состояний, которые могут ухудшить левый желудочек действуют как неконтролируемая гипертония, недавние сердечные приступы или серьезная сердечная аритмия.[3] Следует соблюдать осторожность при сочетании пертузумаба с антрациклин.[3] Также нет данных о безопасности использования пертузумаба в сочетании с доксорубицин.[3]
Женщинам детородного возраста при приеме пертузумаба следует использовать противозачаточные средства; он может нанести вред плоду у беременных женщин и может выделяться с грудным молоком.[3]
Побочные эффекты
В клинических испытаниях комбинированной терапии из трех агентов при метастатическом раке молочной железы побочные эффекты, возникающие у более чем половины людей, принимавших ее, включали диарею, выпадение волос и потеря нейтрофилов; более 10% людей испытали потерю нейтрофилов с лихорадкой, и потеря лейкоцитов.[3] После отмены доцетаксела у некоторых людей наиболее частыми побочными эффектами были диарея (28,1%), инфекция верхних дыхательных путей (18,3%), сыпь (18,3%), головная боль (17,0%), усталость (13,4%), отек носа. проходы и горло (часто из-за простуды) (17,0%), слабость (13,4%), зуд (13,7%), боль в суставах (11,4%), тошнота (12,7%), боль в конечности (13,4%) , боли в спине (12,1%) и кашель (12,1%).[3]
В клинических испытаниях неоадъювантного применения комбинации более 50% людей имели выпадение волос и потеря нейтрофилов.[3]
В обоих случаях более 10% людей дополнительно испытали: потеря красных кровяных телец, гиперчувствительность или аллергическая реакция, инфузионные реакции, снижение аппетита, бессонница, нарушение вкусовых ощущений, воспаление ротовой полости или губ, запор, сыпь, болезнь ногтей и мышечные боли.[3]
Фармакология
Метаболизм пертузумаба напрямую не изучался; в основном антитела выводятся катаболизм. Средний клиренс пертузумаба составлял 0,235 л / день, а средний период полувыведения составлял 18 дней.[3]
Механизм действия
HER2 внеклеточный рецептор - а рецепторная тирозинкиназа - что при активации загорается преобразование сигнала через несколько путей которые стимулируют пролиферацию и рост клеток; чрезмерная экспрессия может вызвать неконтролируемый рост. HER2-положительный рак молочной железы вызывается амплификацией гена ERBB2, которая приводит к сверхэкспрессии HER2 примерно в 15-30% опухолей молочной железы.[6]
Как и многие рецепторы, HER2 обычно объединяет другой белок для своего функционирования (процесс, называемый димеризация ); он может связываться со вторым рецептором HER2 (действующим как гомодимер ) и он может гетеродимеризоваться с другим рецептором Ее семья. Самый мощный димер для активации сигнальных путей - это HER2 / HER3.[4]
В эпитоп поскольку пертузумаб является доменом HER2, где он связывается с HER3, а пертузумаб предотвращает образование димера HER2 / HER3, который блокирует передачу сигналов димером.[4][7] Трастузумаб другое моноклональное антитело против HER2; его эпитоп - это домен, в котором HER2 связывается с другим белком HER2.[4] Два mAb вместе препятствуют функционированию HER2.[4]
Химия и производство
Пертузумаб представляет собой иммуноглобулин G1 с вариабельной областью против белка HER2 человека, моноклональной тяжелой цепи 2С4 человека-мыши, дисульфидно связанной с моноклональной κ-цепью 2С4 человека-мыши.[8]
Производится рекомбинантно в CHO клетки.[2]
История
Моноклональное антитело 2C4, по-видимому, впервые было опубликовано в 1990 году учеными из Genentech,[9] в том же году, что F. Hoffmann-La Roche AG приобрела контрольный пакет акций Genentech.[10]
К 2003 году Genentech поняла, что 2C4 предотвращает димеризацию HER2 с другими рецепторами HER, и приступила к испытаниям фазы I, направленным на широкий спектр видов рака, а не только на те, которые со сверхэкспрессией HER2. Это был первый известный ингибитор димеризации HER.[11]
В 2005 году компания Genentech представила неудовлетворительные результаты испытаний фазы II пертузумаба в качестве единственного средства при раке простаты, груди и яичников, и заявила, что намерена продолжить разработку его в сочетании с другими препаратами от рака яичников.[12][13]
В 2007 году Genentech отказалась от торговой марки Omnitarg.[14][15]
В марте 2009 года «Рош» приобрела Genentech, купив акции, которые она еще не контролировала.[16][17]
В 2012 году были опубликованы результаты исследования CLEOPATRA, рандомизированного плацебо-контролируемого исследования III фазы пертузумаба в сочетании с трастузумаб и доцетаксел при HER2-положительном метастатическом раке молочной железы.[18] Позднее в том же году пертузумаб получил одобрение FDA США для лечения HER2-положительного метастатического рака груди.[5] Результаты исследования фазы II в неоадъювантной обстановке, NeoSphere, опубликованные в 2012 г.[19] и результаты исследования сердечной безопасности фазы II в той же популяции, Трифена, опубликованные в 2013 году.[20] FDA одобрило неоадъювантное показание в 2013 году.[21]
Пертузумаб был одобрен в Европе в 2013 году.[3]
Пертузумаб также изучался в Немелкоклеточный рак легкого но с 2016 года это указание было снято с производства.[1]
Общество и культура
По состоянию на 2016 год в США каждый цикл комбинации из трех препаратов, вводимый каждые три недели, стоит около 8 500 долларов, не включая расходы на вспомогательное лечение.[22]
В Великобритании ОТЛИЧНО Оценка в 2015 году сделала предварительный вывод о том, что комбинация лекарств не была рентабельной, и в мае 2016 года NICE отказался от этого препарата в условиях неоадъювантной терапии, главным образом потому, что было неизвестно, обеспечивает ли комбинация лекарств преимущество в выживаемости.[23][24][25] Впоследствии это решение было отменено шесть месяцев спустя, и пертузумаб стал первым новым лекарством от рака груди, одобренным NICE для повседневного использования. NHS финансирование почти через десять лет после того, как «Рош» пообещала предоставить препарат NHS с нераскрытой скидкой для пациентов в неоадъювантной обстановке и разделить долгосрочные финансовые риски.[26]
Рекомендации
- ^ а б c «Пертузумаб». AdisInsight. Получено 2 ноября 2016.
- ^ а б c d "Перьета Лейбл" (PDF). FDA. Март 2016 г.. Получено 2 ноября 2016.
- ^ а б c d е ж грамм час я j k л м п "UK Perjeta Label". Сборник электронных лекарств. 18 сентября 2015 г.. Получено 2 ноября 2016.
- ^ а б c d е Harbeck, N; и другие. (Март 2013 г.). «Ингибитор димеризации HER2 пертузумаб - механизм действия и клинические данные при раке груди». Уход за грудью (Базель, Швейцария). 8 (1): 49–55. Дои:10.1159/000346837. ЧВК 3971793. PMID 24715843.
- ^ а б «Сообщения для прессы - FDA одобряет Perjeta для лечения поздней стадии рака груди». FDA. 8 июня 2012 г.
- ^ Митри З., Константин Т., О'Реган Р. (2012). «Рецептор HER2 при раке груди: патофизиология, клиническое использование и новые достижения в терапии». Исследования и практика химиотерапии. 2012: 1–7. Дои:10.1155/2012/743193. ЧВК 3539433. PMID 23320171.
- ^ Badache, А; Хайнс, штат Невада (апрель 2004 г.). «Новое терапевтическое антитело маскирует ErbB2 для своих партнеров» (PDF). Раковая клетка. 5 (4): 299–301. Дои:10.1016 / с1535-6108 (04) 00088-1. PMID 15093533.
- ^ «Предлагаемое МНН: Список 89» (PDF). Информация ВОЗ о лекарствах. 17 (3). 2003.
- ^ Fendly, BM; и другие. (1 марта 1990 г.). «Характеристика мышиных моноклональных антител, реагирующих либо на рецептор эпидермального фактора роста человека, либо на продукт гена HER2 / neu» (PDF). Исследования рака. 50 (5): 1550–8. PMID 1689212., упоминается в Молина, Массачусетс; и другие. (15 июня 2001 г.). «Трастузумаб (герцептин), гуманизированное моноклональное антитело против рецептора Her2, ингибирует базальное и активированное расщепление эктодомена Her2 в клетках рака груди» (PDF). Исследования рака. 61 (12): 4744–9. PMID 11406546.
- ^ Фишер, Лоуренс М. (1 октября 2000 г.). "Genentech: оставшийся в живых". Нью-Йорк Таймс.
- ^ Albanell, J; Codony, J; Ровира, А; Мелладо, B; Гаскон, П. (2003). Механизм действия моноклональных антител против HER2: последние научные данные о трастузумабе и 2C4. Достижения экспериментальной медицины и биологии. 532. С. 253–68. Дои:10.1007/978-1-4615-0081-0_21. ISBN 978-0-306-47762-1. PMID 12908564.
- ^ "Пресс-релиз: данные клинической программы Omnitarg представлены на заседании Американского общества клинической онкологии". Genentech. 15 мая 2005 г.
- ^ «Омнитарг Genentech терпит неудачу на Фазе II». Фарма Таймс. 16 мая 2005 г.
- ^ «Исправление: письмо редакции». Новости онкологии рака: 3. Февраль 2012.
- ^ «Пресс-релиз: Рош в первой половине 2007 г.». Рош. 19 июля 2007 г.
- ^ Морс, Эндрю (10 мая 2006 г.). «Чугай сообщает о хороших перспективах выпуска лекарства от рака». Журнал "Уолл Стрит. Получено 26 сентября, 2008.
- ^ Штатные писатели (21 июля 2008 г.). "Рош делает ставку на Genentech на $ 43,7 млрд". Новости генной инженерии и биотехнологии. ISSN 1935-472X. Получено 26 сентября, 2008.
- ^ Базельга, Дж; Исследовательская группа КЛЕОПАТРА; и другие. (12 января 2012 г.). «Пертузумаб плюс трастузумаб плюс доцетаксел при метастатическом раке груди». Медицинский журнал Новой Англии. 366 (2): 109–19. Дои:10.1056 / nejmoa1113216. ЧВК 5705202. PMID 22149875.
- ^ Джанни, Л; и другие. (Январь 2012 г.). «Эффективность и безопасность неоадъювантного пертузумаба и трастузумаба у женщин с местнораспространенным, воспалительным или ранним HER2-положительным раком молочной железы (NeoSphere): рандомизированное многоцентровое открытое исследование фазы 2». Ланцет. Онкология. 13 (1): 25–32. Дои:10.1016 / с1470-2045 (11) 70336-9. PMID 22153890. цитируется в Товарищи, М; и другие. (Март 2015 г.). «Системная таргетная терапия her2-положительного рака груди на ранней стадии у женщин: систематический обзор данных для рекомендаций по системной терапии 2014 г., Онтарио». Текущая онкология (Торонто, Онтарио). 22 (Приложение 1): S114–22. Дои:10.3747 / co.22.2322. ЧВК 4381787. PMID 25848335.
- ^ Schneeweiss, A; и другие. (Сентябрь 2013). «Пертузумаб плюс трастузумаб в сочетании со стандартными неоадъювантными схемами химиотерапии, содержащими антрациклин и не содержащими антрациклинов, у пациентов с HER2-положительным раком груди на ранней стадии: рандомизированное исследование сердечной безопасности II фазы (TRYPHAENA)» (PDF). Анналы онкологии. 24 (9): 2278–84. Дои:10.1093 / annonc / mdt182. PMID 23704196.
- ^ «Сообщения для прессы - FDA одобряет Perjeta для лечения неоадъювантного рака груди». FDA. 30 сентября 2013 г.
- ^ Дурки, BY и др. (20 марта 2016 г.). «Экономическая эффективность пертузумаба при 2-положительном метастатическом раке молочной железы в отношении рецептора эпидермального фактора роста человека». Журнал клинической онкологии. 34 (9): 902–9. Дои:10.1200 / jco.2015.62.9105. ЧВК 5070553. PMID 26351332.
- ^ Fleeman, N; Багуст, А; Бил, S; Дван, К; Диксон, Р. Proudlove, C; Дундарь, Y (январь 2015). «Пертузумаб в комбинации с трастузумабом и доцетакселом для лечения HER2-положительного метастатического или местно рецидивирующего неоперабельного рака груди». Фармакоэкономика. 33 (1): 13–23. Дои:10.1007 / s40273-014-0206-2. PMID 25138171. S2CID 8470253.
- ^ «Рак груди (HER2-положительный, метастатический) - пертузумаб (с трастузумабом и доцетакселом) [ID523]». ОТЛИЧНО. 1 сентября 2016 г.. Получено 2 ноября 2016.
- ^ Макки, Селина (20 мая 2016 г.). «NICE отвергает препарат Perjeta от рака груди, созданный компанией Рош». Pharma Times.
- ^ Йип, Эми (22 ноября 2016 г.). «Хороший разворот и отказ от одобрения препарата Рош Perjeta для лечения HER2-положительного рака груди». Pharmalive.
дальнейшее чтение
- Дин Л. (2015). «Пертузумаб терапия и генотип ERBB2 (HER2)». В Pratt VM, McLeod HL, Rubinstein WS, et al. (ред.). Резюме по медицинской генетике. Национальный центр биотехнологической информации (NCBI). PMID 28520364. Идентификационный номер книжной полки: NBK315949.
