Каталитическая триада - Catalytic triad

А каталитическая триада представляет собой набор из трех согласованных аминокислоты что можно найти в активный сайт некоторых ферменты.[1][2] Каталитические триады чаще всего встречаются в гидролаза и трансфераза ферменты (например, протеазы, амидазы, эстеразы, ацилазы, липазы и β-лактамазы ). An Кислота -Основание -Нуклеофил триада - это общий мотив для образования нуклеофильного остатка для ковалентный катализ. В остатки формируют сеть реле заряда для поляризации и активации нуклеофила, который атакует субстрат, образуя ковалентный промежуточный, который затем гидролизованный выпустить товар и регенерировать свободный фермент. Нуклеофил чаще всего представляет собой серин или же цистеин аминокислота, но иногда треонин или даже селеноцистеин. В 3D структура фермента объединяет остатки триады в точной ориентации, даже если они могут находиться далеко друг от друга в последовательности (первичная структура ).[3]
А также дивергентная эволюция функции (и даже нуклеофила триады), каталитические триады демонстрируют одни из лучших примеров конвергентная эволюция. Химические ограничения на катализ привели к тому, что один и тот же каталитический раствор независимо развился по крайней мере в 23 отдельных надсемейства.[2] Их механизм действия следовательно, один из наиболее изученных в биохимия.[4][5]
История
Ферменты трипсин и химотрипсин были впервые очищены в 1930-х годах.[6] Серин в каждом из трипсина и химотрипсина был идентифицирован как каталитический нуклеофил (по диизопропилфторфосфат модификация) в 1950-х гг.[7] Строение химотрипсина было решено Рентгеновская кристаллография в 1960-х, показывая ориентацию каталитической триады в активном центре.[8] Другие протеазы секвенировали и выравнивали, чтобы выявить семейство родственных протеаз,[9][10][11] теперь называется семейством S1. Одновременно структуры эволюционно не связанных между собой папаин и субтилизин в протеазах обнаружены аналогичные триады. Механизм «реле заряда» для активации нуклеофила другими членами триады был предложен в конце 1960-х годов.[12] Поскольку больше протеазных структур было решено Рентгеновская кристаллография в 1970-х и 80-х, гомологичный (Такие как Протеаза TEV ) и аналогичные (например, папаиновые) триады.[13][14][15] В МЕРОПЫ Система классификации в 1990-х и 2000-х годах начала классифицировать протеазы на структурно связанный фермент надсемейства и таким образом действует как база данных конвергентной эволюции триад в более чем 20 суперсемействах.[16][17] Понимание того, как химические ограничения эволюции привели к слиянию стольких семейств ферментов в одной и той же триаде. геометрии сложилась в 2010-х гг.[2]
С момента их первоначального открытия их точный каталитический механизм исследовался все более и более детально. Особые разногласия в 1990-е и 2000-е гг. водородная связь с низким барьером способствовал катализу,[18][19][20] или обычный водородная связь достаточно, чтобы объяснить механизм.[21][22] Масштабная работа по ковалентному катализу и реле заряда, используемому каталитическими триадами, привела к тому, что этот механизм лучше всего охарактеризован во всей биохимии.[4][5][21]
Функция
Ферменты, содержащие каталитическую триаду, используют ее для одного из двух типов реакций: либо для расколоть подложка (гидролазы ) или перенести одну часть подложки на вторую подложку (трансферазы ). Триады представляют собой взаимозависимый набор остатков в активный сайт фермента и действуют совместно с другими остатками (например, сайт привязки и оксианионная дыра ) достигать нуклеофильный катализ. Эти триадные остатки действуют вместе, чтобы сделать нуклеофил член высоко реактивный, образуя ковалентный промежуточный продукт с субстратом, который затем растворяется для завершения катализа.
Механизм
Каталитические триады выступают ковалентный катализ с использованием остатка в качестве нуклеофила. Реакционная способность нуклеофильного остатка увеличивается за счет функциональные группы других членов триады. Нуклеофил поляризован и ориентирован основанием, которое само связывается и стабилизируется кислотой.
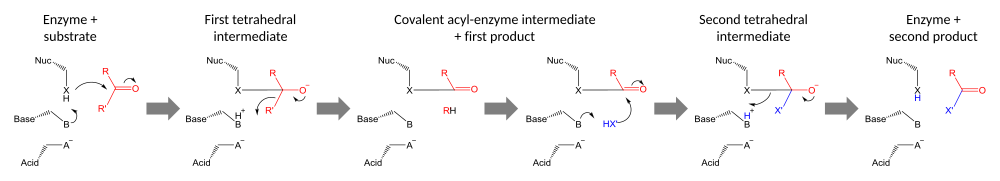
Катализ проводится в два этапа. Во-первых, активированный нуклеофил атакует карбонил углерода и заставляет карбонильный кислород принять электрон, что приводит к тетраэдрической средний. Накопление отрицательного заряда на этом промежуточном продукте обычно стабилизируется оксианионная дыра внутри активного сайта. Промежуточный продукт затем коллапсирует обратно в карбонил, выбрасывая первую половину субстрата, но оставляя вторую половину все еще ковалентно связанной с ферментом в виде промежуточное соединение ацил-фермента. Изгнание этого первого уходящая группа часто помогает донорство протона основанием.
Вторая стадия катализа - разделение промежуточного ацил-фермента путем атаки второго субстрата. Если этот субстрат - вода, то результатом будет гидролиз; если это органическая молекула, то результатом является перенос этой молекулы на первый субстрат. Атака этим вторым субстратом образует новый тетраэдрический промежуточный продукт, который разрешается путем выброса нуклеофила фермента, высвобождения второго продукта и регенерации свободного фермента.[23]
Идентичность членов триады

Нуклеофил
Боковая цепь нуклеофильного остатка выполняет ковалентный катализ на субстрат. В одинокая пара электронов, присутствующих на кислороде или сере, атакует электроположительный карбонил углерод.[3] 20 природные биологические аминокислоты не содержат достаточно нуклеофильных функциональных групп для многих сложных каталитические реакции. Включение нуклеофила в триаду увеличивает его реакционную способность для эффективного катализа. Наиболее часто используемые нуклеофилы - это гидроксил (ОН) серина и тиол / тиолат-ион (SH / S−) цистеина.[2] В качестве альтернативы, треониновые протеазы использовать вторичный гидроксил треонина, однако из-за стерическое препятствие дополнительной боковой цепи метильная группа такие протеазы используют свои N-Терминал амид в качестве основания, а не отдельная аминокислота.[1][24]
Использование кислорода или серы в качестве нуклеофильного атома вызывает незначительные различия в катализе. В сравнении с кислород, сера дополнительный d орбитальный делает его больше (на 0,4 Å)[25] и более мягкий, позволяет образовывать более длинные связи (dC-X и гX-H в 1,3 раза), и дает ему меньшее значение pKа (на 5 единиц).[26] Следовательно, серин в большей степени, чем цистеин, зависит от оптимальной ориентации членов кислотно-основной триады для снижения его pKа[26] для достижения согласованных депротонирование с катализом.[2] Низкий pKа цистеина работает в ущерб первому тетраэдрический промежуточный поскольку непродуктивное обращение исходной нуклеофильной атаки является более благоприятным продуктом распада.[2] Поэтому основание триады предпочтительно ориентировано на протонировать уходящей группы амида, чтобы гарантировать, что она выбрасывается, оставляя фермент серу ковалентно связанной с N-концом субстрата. Наконец, разделение ацил-фермента (для высвобождения С-конца субстрата) требует повторного протонирования серина, тогда как цистеин может уйти в виде S−. Стерически, сера цистеина также образует более длинные связи и имеет более объемный радиус Ван-дер-Ваальса[2] и если мутировавший к серину может быть захвачен в непродуктивных ориентациях в активном центре.[25]
Очень редко селен атом необычной аминокислоты селеноцистеин используется как нуклеофил.[27] Депротонированный Se− состояние сильно благоприятствует каталитической триаде.[27]
Основание
Поскольку никакие природные аминокислоты не являются сильно нуклеофильными, основание в каталитической триаде поляризует и депротонирует нуклеофил для увеличения его реакционной способности.[3] Кроме того, это протонирует первый товар в помощь уходящей группе.
Основанием чаще всего является гистидин, так как его pKа обеспечивает эффективный щелочной катализ, образование водородных связей с кислотным остатком и депротонирование нуклеофильного остатка.[1] β-лактамазы Такие как ТЕМ-1 использовать лизин остаток в качестве основы. Поскольку p лизинаKа настолько высок (pKа= 11), глутамат и несколько других остатков действуют как кислота, чтобы стабилизировать его депротонированное состояние во время каталитического цикла.[28][29] Треониновые протеазы используют свои N-концевой амид в качестве основания, поскольку стерическое скопление метила каталитического треонина не позволяет другим остаткам быть достаточно близкими.[30][31]
Кислота
Член кислотной триады образует водородную связь с основным остатком. Это выравнивает основной остаток, ограничивая его вращение боковой цепи, и поляризует его, стабилизируя его положительный заряд.[3] Две аминокислоты имеют кислую боковые цепи при физиологическом pH (аспартат или глутамат), поэтому они наиболее часто используются для этой триады.[3] Цитомегаловирус протеаза[b] использует пару гистидинов, один в качестве основания, как обычно, а другой в качестве кислоты.[1] Второй гистидин не является такой эффективной кислотой, как более распространенный аспартат или глутамат, что приводит к более низкой каталитической эффективности. В некоторых ферментах кислотный член триады менее необходим, а некоторые действуют только как диада. Например, папаин[c] использует аспарагин как его третий член триады, который ориентирует основание гистидина, но не действует как кислота. По аналогии, гепатит А вирусная протеаза[d] содержит заказанную воду в том месте, где должен быть остаток кислоты.
Примеры триад

Сер-Гис-Асп
Мотив серин-гистидин-аспартат является одним из наиболее подробно описанных каталитических мотивов в биохимии.[3] Примером триады является химотрипсин,[e] модельная сериновая протеаза из PA суперсемейство который использует свою триаду для гидролиза белковых цепей. Аспартат связан водородной связью с гистидином, увеличивая pKа азота имидазола от 7 до примерно 12. Это позволяет гистидину действовать как мощное общее основание и активировать сериновый нуклеофил. Он также имеет оксианионная дыра состоит из нескольких амидов основной цепи, которые стабилизируют накопление заряда на промежуточных соединениях. Основание гистидина помогает первой уходящей группе, отдавая протон, а также активирует гидролитический водный субстрат, отводя протон как оставшийся ОН− атакует промежуточный ацил-фермент.
Та же триада конвергентно развивалась в α / β гидролазы такие как некоторые липазы и эстеразы, тем не мение ориентация членов триады перевернут.[32][33] Кроме того, мозг ацетилгидролаза (который имеет ту же складку, что и маленький G-белок ) также была обнаружена эта триада. Эквивалент Сер-Гис-Glu триада используется в ацетилхолинэстераза.
Цис-Гис-Асп
Вторая наиболее изученная триада - это мотив цистеин-гистидин-аспартат.[2] Несколько семей цистеиновые протеазы используйте этот набор триад, например протеаза TEV[а] и папаин.[c] Триада действует аналогично триадам сериновых протеаз с некоторыми заметными отличиями. Из-за низкого уровня цистеинаKа, важность Asp для катализа варьируется, и некоторые цистеиновые протеазы эффективно являются Cys-His-диадами (например, вирус гепатита А протеаза), в то время как в других цистеин уже депротонирован до начала катализа (например, папаин).[34] Эта триада также используется некоторыми амидазами, такими как N-гликаназа для гидролиза непептидных связей C-N.[35]
Сер-Хис-Хис
Триада цитомегаловирус протеаза[b] использует гистидин в качестве членов как кислотной, так и основной триады. Удаление кислого гистидина приводит только к 10-кратной потере активности (по сравнению с более чем 10 000-кратной, когда аспартат удаляется из химотрипсина). Эта триада была интерпретирована как возможный способ создания менее активного фермента для контроля скорости расщепления.[24]
Сер-Глу-Асп
Необычная триада обнаружена в протеазах селдолизина.[f] Низкий pKа глутаматкарбоксилатной группы означает, что он действует как основание в триаде только при очень низком pH. Предполагается, что триада приспособление к конкретным средам, таким как кислый горячие источники (например. кумамолизин ) или ячейка лизосома (например. трипептидилпептидаза ).[24]
Cys-His-Ser
В эндотелиальный протеаза васогибин[грамм] использует цистеин в качестве нуклеофила, но серин для координации гистидинового основания.[36][37] Несмотря на то, что серин является слабой кислотой, он все же эффективен для ориентации гистидина в каталитической триаде.[36] Некоторые гомологи в качестве альтернативы содержат треонин вместо серина в кислотном месте.[36]
Thr-Nter, Ser-Nter и Cys-Nter
Треониновые протеазы, такие как протеасома субъединица протеазы[час] и орнитинацилтрансферазы[я] использовать вторичный гидроксил треонина аналогично использованию серина первичный гидроксил.[30][31] Однако из-за стерического вмешательства дополнительной метильной группы треонина основным членом триады является N-терминальный амид, который поляризует упорядоченную воду, которая, в свою очередь, депротонирует каталитический гидроксил для увеличения его реакционной способности.[1][24] Точно так же существуют эквивалентные конфигурации «только серин» и «только цистеин», такие как пенициллинацилаза грамм[j] и пенициллинацилаза V[k] которые эволюционно связаны с протеасомными протеазами. Опять же, они используют свои N-терминальный амид в качестве основания.[24]
Сер-СНГСер-Лис
Эта необычная триада встречается только в одном суперсемействе амидаз. В этом случае лизин поляризует средний серин.[38] Затем средний серин образует две сильные водородные связи с нуклеофильным серином, чтобы активировать его (одну с гидроксилом боковой цепи, а другую с амидом основной цепи). Средний серин находится в необычном СНГ ориентация для облегчения точных контактов с двумя другими остатками триады. Эта триада необычна еще и тем, что лизин и СНГ-серин действуют как основание при активации каталитического серина, но тот же лизин также выполняет роль кислотного члена, а также устанавливает ключевые структурные контакты.[38][39]
Sec-His-Glu
Редкая, но встречающаяся в природе аминокислота селеноцистеин (Sec), также может быть найден как нуклеофил в некоторых каталитических триадах.[27] Селеноцистеин похож на цистеин, но содержит селен атом вместо серы. Пример есть на активном сайте тиоредоксинредуктаза, который использует селен для восстановления дисульфида в тиоредоксине.[27]
Инженерные триады
В дополнение к встречающимся в природе типам каталитических триад, белковая инженерия был использован для создания вариантов ферментов с ненативными аминокислотами или полностью синтетическими аминокислотами.[40] Каталитические триады также были вставлены в некаталитические белки или имитаторы белков.
Субтилизин (сериновая протеаза) имеет кислородный нуклеофил, замененный каждым из серы,[41][42] селен,[43] или же теллур.[44] Цистеин и селеноцистеин были вставлены мутагенез, тогда как неприродная аминокислота, теллуроцистеин, был вставлен с помощью ауксотрофные клетки кормили синтетическим теллуроцистеином. Все эти элементы находятся в 16-м столбец таблицы Менделеева (халькогены ), поэтому обладают схожими свойствами.[45][46] В каждом случае изменение нуклеофила уменьшало активность протеазы фермента, но увеличивало другую активность. Нуклеофил серы улучшил работу ферментов трансфераза активность (иногда называемая субтилигазой). Нуклеофилы селена и теллура превратили фермент в оксидоредуктаза.[43][44] Когда нуклеофил протеазы TEV был преобразован из цистеина в серин, его протеазная активность сильно снижалась, но могла быть восстановлена с помощью направленная эволюция.[47]
Некаталитические белки использовались в качестве каркасов, в них были вставлены каталитические триады, которые затем были улучшены путем направленной эволюции. Триада Ser-His-Asp была вставлена в антитело,[48] а также ряд других белков.[49] Точно так же имитаторы каталитических триад были созданы в небольшие органические молекулы как диарил диселенид,[50][51] и отображается на более крупных полимерах, таких как Смолы Меррифилд,[52] и самособирающийся короткий пептид наноструктуры.[53]
Дивергентная эволюция
Сложность сети активных центров приводит к тому, что остатки, участвующие в катализе (и остатки, находящиеся в контакте с ними), сильно увеличиваются. эволюционно сохраненный.[54] Однако есть примеры дивергентной эволюции в каталитических триадах, как в катализируемой реакции, так и в остатках, используемых в катализе. Триада остается ядром активного центра, но эволюционно адаптированный выполнять разные функции.[55][56] Некоторые белки, называемые псевдоферменты, имеют некаталитические функции (например, регулирование путем ингибирующего связывания) и накопили мутации, которые инактивируют их каталитическую триаду.[57]
Изменения реакции
Каталитические триады выступают ковалентный катализ через промежуточный ацил-фермент. Если этот промежуточный продукт растворяется водой, происходит гидролиз субстрата. Однако если промежуточное соединение распадается путем атаки вторым субстратом, то фермент действует как трансфераза. Например, нападение ацил группа приводит к ацилтрансфераза реакция. Несколько семейств ферментов трансфераз произошли от гидролаз в результате адаптации, исключающей воду и способствующей атаке второго субстрата.[58] У разных членов суперсемейства α / β-гидролаз триада Ser-His-Asp настраивается окружающими остатками на выполнение по меньшей мере 17 различных реакций.[33][59] Некоторые из этих реакций также достигаются с помощью механизмов, которые изменили образование или разделение промежуточного ацил-фермента или которые не протекают через промежуточное соединение ацил-фермент.[33]
Кроме того, альтернативный механизм трансферазы был разработан амидофосфорибозилтрансферазы, имеющий два активных сайта.[l] В первом активном центре триада цистеина гидролизует глутамин субстрат для высвобождения свободного аммиака. Затем аммиак диффундирует через внутренний туннель в ферменте на второй активный центр, где он переносится на второй субстрат.[60][61]
Нуклеофильные изменения

Дивергентная эволюция остатков активного центра происходит медленно из-за сильных химических ограничений. Тем не менее, некоторая протеаза надсемейства эволюционировали от одного нуклеофила к другому. Это можно сделать вывод, когда надсемейство (с тем же складывать ) содержит семьи которые используют разные нуклеофилы.[47] Такие нуклеофильные переключения происходили несколько раз в течение эволюционной истории, однако механизмы, с помощью которых это происходит, все еще неясны.[17][47]
Внутри суперсемейства протеаз, которые содержат смесь нуклеофилов (например, Клан ПА ), семейства обозначены их каталитическими нуклеофилами (C = цистеиновые протеазы, S = сериновые протеазы).
| Надсемейство | Семьи | Примеры |
|---|---|---|
| Клан ПА | C3, C4, C24, C30, C37, C62, C74, C99 | Протеаза TEV (Вирус травления табака ) |
| S1, S3, S6, S7, S29, S30, S31, S32, S39, S46, S55, S64, S65, S75 | Химотрипсин (млекопитающие, например Bos taurus ) | |
| Клан PB | C44, C45, C59, C69, C89, C95 | Амидофосфорибозилтрансфераза предшественник (Homo sapiens ) |
| S45, S63 | Пенициллин G ацилаза предшественник (кишечная палочка ) | |
| Т1, Т2, Т3, Т6 | Протеасома архея, бета-компонент (Термоплазма ацидофильная ) | |
| Клан ПК | C26, C56 | Гамма-глутамилгидролаза (Раттус норвегикус ) |
| S51 | Дипептидаза E (кишечная палочка ) | |
| Клан PD | C46 | Протеин ежа (Drosophila melanogaster ) |
| N9, N10, N11 | Интеин -содержащий Протонная АТФаза V-типа каталитическая субъединица А (Saccharomyces cerevisiae ) | |
| Клан PE | P1 | Аминопептидаза DmpA (Ochrobactrum anthropi ) |
| Т5 | Орнитинацетилтрансфераза предшественник (Saccharomyces cerevisiae ) |
Псевдоферменты
Еще один подкласс вариантов каталитической триады: псевдоферменты, которые имеют триадные мутации, которые делают их каталитически неактивными, но способными функционировать как связывающие или структурные белки.[63][64] Например, гепарин -связывающий белок Азуроцидин является членом клана PA, но с глицином вместо нуклеофила и серином вместо гистидина.[65] По аналогии, RHBDF1 является гомологом семейства S54 ромбовидные протеазы с аланином вместо нуклеофильного серина.[66][67] В некоторых случаях псевдоферменты все еще могут иметь неповрежденную каталитическую триаду, но мутации в остальной части белка снимают каталитическую активность. В клан CA входят каталитически неактивные члены с мутировавшими триадами (кальпамодулин содержит лизин вместо цистеинового нуклеофила) и с интактными триадами, но инактивирует мутации в другом месте (тестин крысы сохраняет триаду Cys-His-Asn).[68]
| Надсемейство | Семьи, содержащие псевдоферменты | Примеры |
|---|---|---|
| Клан CA | C1, C2, C19 | Кальпамодулин |
| Клан CD | C14 | CFLAR |
| Клан SC | S9, S33 | Нейролигин |
| Клан SK | S14 | ClpR |
| Клан SR | S60 | Серотрансферрин домен 2 |
| Клан ST | S54 | RHBDF1 |
| Клан ПА | S1 | Азуроцидин 1 |
| Клан PB | Т1 | PSMB3 |
Конвергентная эволюция

В энзимология протеаз дает одни из самых ярких известных примеров конвергентной эволюции. Такое же геометрическое расположение триадных остатков встречается более чем в 20 отдельных ферментах. надсемейства. Каждое из этих суперсемейств является результатом конвергентной эволюции одного и того же расположения триад в разных структурная складка. Это связано с тем, что существуют ограниченные продуктивные способы организации трех остатков триады, ферментного скелета и субстрата. Эти примеры отражают внутренние химические и физические ограничения ферментов, что приводит эволюции к многократному и независимому поиску эквивалентных решений.[1][2]
Цистеиновые и сериновые гидролазы
К той же геометрии триады сходятся сериновые протеазы, такие как химотрипсин[e] и субтилизин надсемейства. Подобная конвергентная эволюция произошла с цистеиновыми протеазами, такими как вирусные C3 протеаза и папаин[c] надсемейства. Эти триады сходятся к почти одинаковому расположению из-за механистического сходства в механизмах протеолиза цистеина и серина.[2]
Семейства цистеиновых протеаз
Семейства сериновых протеаз
| Надсемейство | Семьи | Примеры |
|---|---|---|
| SB | S8, S53 | Субтилизин (Bacillus licheniformis ) |
| SC | S9, S10, S15, S28, S33, S37 | Пролил олигопептидаза (Sus scrofa ) |
| SE | S11, S12, S13 | D-Ala-D-Ala пептидаза C (кишечная палочка ) |
| SF | S24, S26 | Сигнальная пептидаза Я (кишечная палочка ) |
| SH | S21, S73, S77, S78, S80 | Цитомегаловирус сборка (человек герпесвирус 5) |
| SJ | S16, S50, S69 | Lon-A пептидаза (кишечная палочка ) |
| SK | S14, S41, S49 | Clp протеаза (кишечная палочка ) |
| ТАК | S74 | Саморасщепляющийся белок CIMCD отростка шейки фага GA-1 (Фаг Bacillus GA-1 ) |
| SP | S59 | Нуклеопорин 145 (Homo sapiens ) |
| SR | S60 | Лактоферрин (Homo sapiens ) |
| SS | S66 | Муреинтетрапептидаза LD-карбоксипептидаза (Синегнойная палочка ) |
| ST | S54 | Ромбовидный -1 (Drosophila melanogaster ) |
| PA | S1, S3, S6, S7, S29, S30, S31, S32, S39, S46, S55, S64, S65, S75 | Химотрипсин А (Bos taurus ) |
| PB | S45, S63 | Пенициллин G ацилаза предшественник (кишечная палочка ) |
| ПК | S51 | Дипептидаза E (кишечная палочка ) |
| PE | P1 | Аминопептидаза DmpA (Ochrobactrum anthropi ) |
| неназначенный | S48, S62, S68, S71, S72, S79, S81 |
Треониновые протеазы
Треониновые протеазы используют аминокислоту треонин в качестве каталитического нуклеофила. В отличие от цистеина и серина, треонин является вторичным гидроксилом (т.е. имеет метильную группу).Эта метильная группа сильно ограничивает возможные ориентации триады и субстрата, поскольку метил конфликтует либо с основной цепью фермента, либо с гистидиновым основанием.[2] Когда нуклеофил сериновой протеазы был мутирован в треонин, метил занимал смесь положений, большинство из которых препятствовало связыванию субстрата.[69] Следовательно, на нем находится каталитический остаток треониновой протеазы. N-терминал.[2]
Два эволюционно независимых суперсемейства ферментов с разными белковыми складками, как известно, используют N-концевой остаток в качестве нуклеофила: надсемейство PB (протеасомы с использованием складки Ntn)[30] и суперсемейство PE (ацетилтрансферазы используя свертку DOM)[31] Эта общность активный сайт структура в совершенно разных белковых складках указывает на то, что активный центр эволюционировал конвергентно в этих суперсемействах.[2][24]
Семейства треониновых протеаз
| Надсемейство | Семьи | Примеры |
|---|---|---|
| Клан PB | Т1, Т2, Т3, Т6 | Протеасома архея, бета-компонент (Термоплазма ацидофильная ) |
| Клан PE | Т5 | Орнитинацетилтрансфераза (Saccharomyces cerevisiae ) |
Смотрите также
Рекомендации
Примечания
- ^ а б c d Протеаза TEV МЕРОПЫ: клан PA, семья C4
- ^ а б Цитомегаловирусная протеаза МЕРОПЫ: клан SH, семья S21
- ^ а б c d Папаин МЕРОПЫ: клан CA, семья C1
- ^ Протеаза вируса гепатита А МЕРОПЫ: клан PA, семья C3
- ^ а б c Химотрипсин МЕРОПЫ: клан PA, семья S1
- ^ Селдолизин протеаза МЕРОПЫ: клан SB, семья 53
- ^ Вазохибиновая протеаза МЕРОПЫ: клан CA
- ^ а б Протеасома МЕРОПЫ: клан PB, семья T1
- ^ а б Орнитин ацилтрансферазы МЕРОПЫ: клан PE, семья T5
- ^ Пенициллинацилаза G МЕРОПЫ: клан PB, семья S45
- ^ Пенициллинацилаза V МЕРОПЫ: клан PB, семья C59
- ^ амидофосфорибозилтрансфераза МЕРОПЫ: клан PB, семья C44
- ^ Субтилизин МЕРОПЫ: клан SB, семья S8
- ^ Пролил олигопептидаза МЕРОПЫ: клан SC, семья S9
Цитаты
- ^ а б c d е ж Додсон Г., Влодавер А. (1998). «Каталитические триады и их родственники». Trends Biochem. Sci. 23 (9): 347–52. Дои:10.1016 / S0968-0004 (98) 01254-7. PMID 9787641.
- ^ а б c d е ж грамм час я j k л м Buller AR, Townsend CA (2013). «Внутренние эволюционные ограничения на структуру протеазы, ацилирование фермента и идентичность каталитической триады». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 110 (8): E653–61. Bibcode:2013PNAS..110E.653B. Дои:10.1073 / pnas.1221050110. ЧВК 3581919. PMID 23382230.
- ^ а б c d е ж Страйер Л., Берг Дж. М., Тимочко Дж. Л. (2002). «9 каталитических стратегий». Биохимия (5-е изд.). Сан-Франциско: W.H. Фримен. ISBN 9780716749554.
- ^ а б Перуц М (1992). Белковая структура. Новые подходы к болезни и терапии. Нью-Йорк: W.H. Фриман и Ко. ISBN 9780716770213.
- ^ а б Нейрат Х (1994). «Протеолитические ферменты прошлого и настоящего: вторая золотая эра. Воспоминания, специальный раздел в честь Макса Перуца». Protein Sci. 3 (10): 1734–9. Дои:10.1002 / pro.5560031013. ЧВК 2142620. PMID 7849591.
- ^ Оман К.П., Хоффман А., Кейзер HR (1990). «Эндотелин-индуцированное сужение сосудов и высвобождение предсердных натрийуретических пептидов у крыс». Acta Physiol. Сканд. 138 (4): 549–56. Дои:10.1111 / j.1748-1716.1990.tb08883.x. PMID 2141214.
- ^ Диксон Г. Х., Кауфман Д. Л., Нейрат Х. (1958). «Аминокислотная последовательность в области связывания диизопропилфосфорила в дип-трипсине». Варенье. Chem. Soc. 80 (5): 1260–1. Дои:10.1021 / ja01538a059.
- ^ Мэтьюз Б.В., Сиглер П.Б., Хендерсон Р. и др. (1967). «Трехмерная структура тозил-α-химотрипсина». Природа. 214 (5089): 652–656. Bibcode:1967Натура.214..652М. Дои:10.1038 / 214652a0. PMID 6049071.
- ^ Уолш К.А., Нейрат Х. (1964). «Трипсиноген и химотрипсиноген как гомологичные белки». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 52 (4): 884–9. Bibcode:1964ПНАС ... 52..884Вт. Дои:10.1073 / пнас.52.4.884. ЧВК 300366. PMID 14224394.
- ^ де Хаен К., Нейрат Н., Теллер, округ Колумбия (1975). «Филогения сериновых протеаз, связанных с трипсином, и их зимогенов. Новые методы исследования отдаленных эволюционных взаимоотношений». J. Mol. Биол. 92 (2): 225–59. Дои:10.1016/0022-2836(75)90225-9. PMID 1142424.
- ^ Леск А.М., Фордхэм В.Д. (1996). «Сохранение и изменчивость структур сериновых протеиназ семейства химотрипсинов». J. Mol. Биол. 258 (3): 501–37. Дои:10.1006 / jmbi.1996.0264. PMID 8642605.
- ^ Удар Д.М., Бирктофт Дж. Дж., Хартли Б.С. (1969). «Роль скрытой кислотной группы в механизме действия химотрипсина». Природа. 221 (5178): 337–40. Bibcode:1969Натура.221..337Б. Дои:10.1038 / 221337a0. PMID 5764436.
- ^ Горбаленя А.Е., Блинов В.М., Донченко А.П. (1986). «Кодируемая полиовирусом протеиназа 3C: возможная эволюционная связь между семействами клеточных сериновых и цистеиновых протеиназ». FEBS Lett. 194 (2): 253–7. Дои:10.1016/0014-5793(86)80095-3. PMID 3000829.
- ^ Базан Дж. Ф., Флеттерик Р. Дж. (1988). «Вирусные цистеиновые протеазы гомологичны трипсиноподобному семейству сериновых протеаз: структурные и функциональные последствия». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 85 (21): 7872–6. Bibcode:1988PNAS ... 85.7872B. Дои:10.1073 / pnas.85.21.7872. ЧВК 282299. PMID 3186696.
- ^ Фан Дж., Зданов А., Евдокимов А.Г. и др. (2002). «Структурные основы субстратной специфичности протеазы вируса травления табака». J. Biol. Chem. 277 (52): 50564–72. Дои:10.1074 / jbc.M207224200. PMID 12377789.
- ^ Ролингс Н.Д., Барретт А.Дж. (1993). «Эволюционные семейства пептидаз». Biochem. Дж. 290 (1): 205–18. Дои:10.1042 / bj2900205. ЧВК 1132403. PMID 8439290.
- ^ а б Роулингс Н.Д., Барретт А.Дж., Бейтман А. (2010). «MEROPS: база данных пептидаз». Nucleic Acids Res. 38 (supl_1): D227–33. Дои:10.1093 / nar / gkp971. ЧВК 2808883. PMID 19892822.
- ^ Фрей П.А., Уитт С.А., Тобин Дж.Б. (1994). «Низкобарьерная водородная связь в каталитической триаде сериновых протеаз». Наука. 264 (5167): 1927–30. Bibcode:1994Наука ... 264.1927F. Дои:10.1126 / science.7661899. PMID 7661899.
- ^ Ash EL, Sudmeier JL, De Fabo EC и др. (1997). «Низкобарьерная водородная связь в каталитической триаде сериновых протеаз? Теория против эксперимента». Наука. 278 (5340): 1128–32. Bibcode:1997 Наука ... 278.1128А. Дои:10.1126 / science.278.5340.1128. PMID 9353195.
- ^ Агбак П., Агбак Т. (2018). «Прямое доказательство наличия водородной связи с низким барьером в каталитической триаде сериновой протеазы». Sci. Rep. 8 (1): 10078. Bibcode:2018НатСР ... 810078A. Дои:10.1038 / s41598-018-28441-7. ЧВК 6031666. PMID 29973622.
- ^ а б Schutz CN, Warshel A (2004). «Пересмотр предложения о низкобарьерной водородной связи (LBHB): случай пары Asp ... His в сериновых протеазах». Белки. 55 (3): 711–23. Дои:10.1002 / prot.20096. PMID 15103633.
- ^ Варшел А, Папазян А (1996). «Энергетические соображения показывают, что водородные связи с низким барьером не обладают каталитическим преимуществом по сравнению с обычными водородными связями». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 93 (24): 13665–70. Bibcode:1996PNAS ... 9313665W. Дои:10.1073 / пнас.93.24.13665. ЧВК 19385. PMID 8942991.
- ^ Шафи Т. (2014). Эволюционируемость вирусной протеазы: экспериментальная эволюция катализа, надежность и специфичность (Кандидатская диссертация). Кембриджский университет. Дои:10.17863 / CAM.16528.
- ^ а б c d е ж Экичи О.Д., Паэтцель М., Далби Р.Э. (2008). «Нетрадиционные сериновые протеазы: варианты каталитической конфигурации триады Ser / His / Asp». Protein Sci. 17 (12): 2023–37. Дои:10.1110 / пс 035436.108. ЧВК 2590910. PMID 18824507.
- ^ а б McGrath ME, Wilke ME, Higaki JN и др. (1989). «Кристаллические структуры двух сконструированных тиоловых трипсинов». Биохимия. 28 (24): 9264–70. Дои:10.1021 / bi00450a005. PMID 2611228.
- ^ а б Полгар Л., Асбот Б. (1986). «Основное различие в катализаторах сериновых и цистеиновых протеиназ заключается в стабилизации заряда в переходном состоянии». J. Theor. Биол. 121 (3): 323–6. Дои:10.1016 / с0022-5193 (86) 80111-4. PMID 3540454.
- ^ а б c d Брандт В., Весьоханн Л.А. (2005). «Функциональная роль селеноцистеина (Sec) в механизме катализа больших тиоредоксинредуктаз: предположение об обмене каталитической триады, включая состояние Sec-His-Glu». ChemBioChem. 6 (2): 386–94. Дои:10.1002 / cbic.200400276. PMID 15651042.
- ^ Damblon C, Raquet X, Lian LY и др. (1996). «Каталитический механизм бета-лактамаз: ЯМР-титрование остатка лизина активного центра фермента ТЕМ-1». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 93 (5): 1747–52. Bibcode:1996PNAS ... 93.1747D. Дои:10.1073 / pnas.93.5.1747. ЧВК 39852. PMID 8700829.
- ^ Jelsch C, Lenfant F, Masson JM и др. (1992). «Бета-лактамаза TEM1 E. coli. Определение кристаллической структуры с разрешением 2,5 A». FEBS Lett. 299 (2): 135–42. Дои:10.1016/0014-5793(92)80232-6. PMID 1544485.
- ^ а б c Бранниган Дж. А., Додсон Дж., Дагглби Х. Дж. И др. (1995). «Белковая каталитическая основа с N-концевым нуклеофилом способна к самоактивации». Природа. 378 (6555): 416–9. Bibcode:1995Натура 378..416Б. Дои:10.1038 / 378416a0. PMID 7477383.
- ^ а б c Ченг Х, Гришин Н.В. (2005). «DOM-складка: структура с перекрещивающимися петлями, обнаруженная в DmpA, орнитинацетилтрансферазе и домене, связывающем кофактор молибдена». Protein Sci. 14 (7): 1902–10. Дои:10.1110 / пс. 051364905. ЧВК 2253344. PMID 15937278.
- ^ Sun Y, Yin S, Feng Y и др. (2014). «Молекулярная основа общего основного катализа каталитической триады α / β-гидролазы». J. Biol. Chem. 289 (22): 15867–79. Дои:10.1074 / jbc.m113.535641. ЧВК 4140940. PMID 24737327.
- ^ а б c Раувердинк А., Казлаускас Р. Дж. (2015). «Как одно и то же основное каталитическое оборудование катализирует 17 различных реакций: каталитическая триада серин-гистидин-аспартат складчатых ферментов α / β-гидролазы». ACS Catal. 5 (10): 6153–6176. Дои:10.1021 / acscatal.5b01539. ЧВК 5455348. PMID 28580193.
- ^ Беверидж AJ (1996). «Теоретическое исследование активных сайтов папаина и трипсина крысы S195C: последствия для низкой реактивности мутантных сериновых протеиназ». Protein Sci. 5 (7): 1355–65. Дои:10.1002 / pro.5560050714. ЧВК 2143470. PMID 8819168.
- ^ Аллен, доктор медицины, Бухбергер, Байкрофт, М. (2006). «Домен PUB функционирует как модуль связывания p97 в пептиде N-гликаназе человека». J. Biol. Chem. 281 (35): 25502–8. Дои:10.1074 / jbc.M601173200. PMID 16807242.
- ^ а б c Санчес-Пулидо Л., Понтинг CP (2016). «Вазохибины: новые трансглутаминазоподобные цистеиновые протеазы, обладающие неканонической каталитической триадой Cys-His-Ser». Биоинформатика. 32 (10): 1441–5. Дои:10.1093 / биоинформатика / btv761. ЧВК 4866520. PMID 26794318.
- ^ Сато Й, Сонода Х (2007). «Семейство вазохибинов: негативная система регуляции ангиогенеза, генетически запрограммированная в эндотелиальных клетках». Артер. Тромб. Васк. Биол. 27 (1): 37–41. Дои:10.1161 / 01.atv.0000252062.48280.61. PMID 17095714.
- ^ а б Шин С., Юн Ю.С., Ку Х.М. и др. (2003). «Характеристика новой каталитической триады Ser-cisSer-Lys в сравнении с классической триадой Ser-His-Asp». J. Biol. Chem. 278 (27): 24937–43. Дои:10.1074 / jbc.M302156200. PMID 12711609.
- ^ Серкейра Н.М., Мурти Н., Фернандес П.А. и др. (2017). «Механизм каталитической триады Ser- (цис) Ser-Lys пептидных амидаз». Phys. Chem. Chem. Phys. 19 (19): 12343–12354. Bibcode:2017PCCP ... 1912343C. Дои:10.1039 / C7CP00277G. PMID 28453015.
- ^ Тоскано, М.Д., Войчеховски К.Дж., Хилверт Д. (2007). «Минималистичный редизайн активного сайта: обучение новым трюкам старых ферментов». Энгью. Chem. 46 (18): 3212–36. Дои:10.1002 / anie.200604205. PMID 17450624.
- ^ Abrahmsén L, Tom J, Burnier J, et al. (1991). «Конструирование субтилизина и его субстратов для эффективного лигирования пептидных связей в водном растворе». Биохимия. 30 (17): 4151–9. CiteSeerX 10.1.1.461.9606. Дои:10.1021 / bi00231a007. PMID 2021606.
- ^ Джексон Д. Ю., Бернир Дж., Куан С. и др. (1994). «Разработанная пептидная лигаза для полного синтеза рибонуклеазы А с неприродными каталитическими остатками». Наука. 266 (5183): 243–7. Bibcode:1994Научный ... 266..243J. Дои:10.1126 / science.7939659. JSTOR 2884761. PMID 7939659.
- ^ а б Сайед Р., Ву З. П., Хогл Дж. М. и др. (1993). «Кристаллическая структура селеносубтилизина при разрешении 2,0-А». Биохимия. 32 (24): 6157–64. Дои:10.1021 / bi00075a007. PMID 8512925.
- ^ а б Мао С., Дун З., Лю Дж. И др. (2005). «Полусинтетический теллуросубтилизин с активностью глутатионпероксидазы». Варенье. Chem. Soc. 127 (33): 11588–9. Дои:10.1021 / ja052451v. PMID 16104720.
- ^ Девилланова Ф.А., Du Mont W (2013). Справочник по химии халькогенов. Vol. 1: новые перспективы серы, селена и теллура (2-е изд.). Кембридж: RSC. ISBN 9781849736237. OCLC 868953797.
- ^ Бурушян М (2010). «Электрохимия халькогенов». Электрохимия халькогенидов металлов. Монографии по электрохимии. Берлин, Гейдельберг: Springer. С. 57–75. Дои:10.1007/978-3-642-03967-6_2. ISBN 9783642039669.
- ^ а б c Шафи Т., Гатти-Лафранкони П., Минтер Р. и др. (2015). «Эволюция по восстановлению инвалидности ведет к химически универсальной протеазе, допускающей нуклеофилы». ChemBioChem. 16 (13): 1866–9. Дои:10.1002 / cbic.201500295. ЧВК 4576821. PMID 26097079.
- ^ Окочи Н., Като-Мурай М., Кадоносоно Т. и др. (2007). «Дизайн сериновой протеазоподобной каталитической триады на легкой цепи антитела, отображаемой на поверхности дрожжевых клеток». Appl. Microbiol. Biotechnol. 77 (3): 597–603. Дои:10.1007 / s00253-007-1197-0. PMID 17899065.
- ^ Раджагопалан С., Ван С., Ю К. и др. (2014). «Дизайн активированных серин-содержащих каталитических триад с точностью до атомного уровня». Nat. Chem. Биол. 10 (5): 386–91. Дои:10.1038 / nchembio.1498. ЧВК 4048123. PMID 24705591.
- ^ Бхоумик Д., Мугеш Г. (2015). «Введение каталитической триады увеличивает активность диарилдиселенидов, аналогичную глутатионпероксидазе». Орг. Biomol. Chem. 13 (34): 9072–82. Дои:10.1039 / C5OB01294E. PMID 26220806.
- ^ Бхоумик Д., Мугеш Г. (2015). «Понимание каталитического механизма синтетических миметиков глутатионпероксидазы». Орг. Biomol. Chem. 13 (41): 10262–72. Дои:10.1039 / c5ob01665g. PMID 26372527.
- ^ Nothling MD, Ganesan A, Condic-Jurkic K, et al. (2017). «Простая конструкция катализатора на основе ферментов на носителе на основе каталитической триады». Chem. 2 (5): 732–745. Дои:10.1016 / j.chempr.2017.04.004.
- ^ Гульсерен Г., Халилы М.А., Текинай А.Б. и др. (2016). «Каталитические супрамолекулярные самособирающиеся пептидные наноструктуры для гидролиза сложных эфиров». J. Mater. Chem. B. 4 (26): 4605–4611. Дои:10.1039 / c6tb00795c. HDL:11693/36666. PMID 32263403.
- ^ Halabi N, Rivoire O, Leibler S и др. (2009). «Белковые секторы: эволюционные единицы трехмерной структуры». Клетка. 138 (4): 774–86. Дои:10.1016 / j.cell.2009.07.038. ЧВК 3210731. PMID 19703402.
- ^ Мурзин А.Г. (1998). «Как далеко заходит дивергентная эволюция белков». Текущее мнение в структурной биологии. 8 (3): 380–387. Дои:10.1016 / S0959-440X (98) 80073-0. PMID 9666335.
- ^ Герлт Дж. А., Бэббит П. С. (2001). «Дивергентная эволюция ферментативной функции: механистически различные суперсемейства и функционально различные супрасемейства». Анну. Rev. Biochem. 70 (1): 209–46. Дои:10.1146 / annurev.biochem.70.1.209. PMID 11395407.
- ^ Мерфи Дж. М., Фархан Х., Айерс ПА (2017). «Биозомби: рост псевдоферментов в биологии». Biochem. Soc. Пер. 45 (2): 537–544. Дои:10.1042 / bst20160400. PMID 28408493.
- ^ Stehle F, Brandt W., Stubbs MT, et al. (2009). «Синапоилтрансферазы в свете молекулярной эволюции». Фитохимия. Эволюция метаболического разнообразия. 70 (15–16): 1652–62. Дои:10.1016 / j.phytochem.2009.07.023. PMID 19695650.
- ^ Димитриу П.С., Денесюк А., Такахаши С. и др. (2017). «Альфа / бета-гидролазы: уникальный структурный мотив координирует остатки каталитической кислоты в 40-кратных семействах белков». Белки. 85 (10): 1845–1855. Дои:10.1002 / prot.25338. PMID 28643343.
- ^ Смит JL (1998). «Глутамин PRPP амидотрансфераза: снимки фермента в действии». Текущее мнение в структурной биологии. 8 (6): 686–94. Дои:10.1016 / s0959-440x (98) 80087-0. PMID 9914248.
- ^ Smith JL, Zaluzec EJ, Wery JP, et al. (1994). «Структура аллостерического регуляторного фермента биосинтеза пуринов». Наука. 264 (5164): 1427–33. Bibcode:1994Sci ... 264.1427S. Дои:10.1126 / science.8197456. PMID 8197456.
- ^ «Кланы смешанного (C, S, T) каталитического типа». www.ebi.ac.uk. МЕРОПЫ. Получено 20 декабря 2018.
- ^ а б Фишер К., Рейнольдс С.Л. (2015). «Псевдопротеазы: механизмы и функции». Biochem. Дж. 468 (1): 17–24. Дои:10.1042 / BJ20141506. PMID 25940733.
- ^ Тодд А.Е., Оренго Калифорния, Торнтон Дж. М. (2002). «Последовательность и структурные различия между ферментными и неферментными гомологами». Структура. 10 (10): 1435–51. Дои:10.1016 / s0969-2126 (02) 00861-4. PMID 12377129.
- ^ Иверсен Л. Ф., Каструп Дж. С., Бьорн С. Е. и др. (1997). «Структура HBP, многофункционального белка со складкой сериновой протеиназы». Nat. Struct. Биол. 4 (4): 265–8. Дои:10.1038 / nsb0497-265. PMID 9095193.
- ^ Зеттл М., Адрайн С., Стрисовский К. и др. (2011). «Псевдопротеазы семейства ромбовидных используют механизм контроля качества ER для регулирования межклеточной передачи сигналов». Клетка. 145 (1): 79–91. Дои:10.1016 / j.cell.2011.02.047. ЧВК 3149277. PMID 21439629.
- ^ Лемберг МК, Адрайн С. (2016). «Неактивные ромбовидные белки: новые механизмы, влияющие на здоровье и болезни». Семин. Cell Dev. Биол. 60: 29–37. Дои:10.1016 / j.semcdb.2016.06.022. HDL:10400.7/759. PMID 27378062.
- ^ Ченг CY, Моррис I, Бардин CW (1993). «Тесты структурно родственны предшественнику цистеиновой протеиназы мыши, но лишены какой-либо протеазной / антипротеазной активности». Biochem. Биофиз. Res. Commun. 191 (1): 224–231. Дои:10.1006 / bbrc.1993.1206. PMID 8447824.
- ^ Пелк Л.А., Чен З., Гохара Д.В. и др. (2015). "Почему Ser, а не Thr брокеры катализируют трипсиновый фолд". Биохимия. 54 (7): 1457–64. Дои:10.1021 / acs.biochem.5b00014. ЧВК 4342846. PMID 25664608.