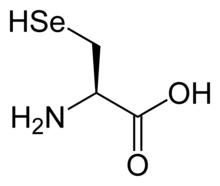
Селеноцистеин - Selenocysteine
 | |
| Имена | |
|---|---|
| Название ИЮПАК 2-амино-3-селанилпропановая кислота | |
| Другие имена L-Селеноцистеин; 3-Селанил-L-аланин; Селен цистеин | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.236.386 |
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C3ЧАС7NО2Se | |
| Молярная масса | 168.065 г · моль−1 |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Селеноцистеин (символ Сек или же U,[2] в более старых публикациях также как Se-Cys)[3] 21-й протеиногенная аминокислота.
Селеноцистеин естественным образом присутствует во всех трех области жизни, но не в каждой родословной, как строительный блок селенопротеины.[4] Селеноцистеин - это цистеин аналог с селен -содержащий селенол группа вместо сера -содержащий тиол группа.
Селеноцистеин присутствует в нескольких ферменты (Например глутатионпероксидазы, тетрайодтиронин 5 'дейодиназы, тиоредоксинредуктазы, формиатдегидрогеназы, глицинредуктазы, селенофосфат синтетаза 2, метионин-р-сульфоксидредуктаза B1 (SEPX1 ), и немного гидрогеназы ).
Селеноцистеин был открыт биохимиком Тресса Штадтман[5] на Национальные институты здоровья.
Биохимическое применение селеноцистеина было описано биохимиком Робертом Хондалом (Вермонтский университет ) и химик Ганс Райх (Университет Висконсина-Мэдисона ).[6]
Структура
Селеноцистеин имеет структуру, аналогичную структуре цистеин, но с атомом селен заменяя обычную серу, образуя селенол группа, которая депротонированный на физиологическом pH. (Как и другие природные протеиногенные аминокислоты, цистеин и селеноцистеин имеют L хиральность в старом D/L обозначение, основанное на гомологии D- и L-глицеральдегид. В новее р/S система обозначения хиральности, основанная на атомных номерах атомов около асимметричного углерода, они имеют р хиральность из-за присутствия серы или селена в качестве второго соседа асимметричного углерода. (Остальные хиральные аминокислоты, имеющие только более легкие атомы в этом положении, имеют S хиральность.)
Белки, содержащие один или несколько остатков селеноцистеина, называются селенопротеины. Большинство селенопротеинов содержат один остаток селеноцистеина. Селенопротеины, зависящие от каталитической активности селеноцистеина, называются селеноферменты.[7]Было обнаружено, что селеноферменты используют каталитическая триада структуры, влияющие на нуклеофильность селеноцистеина активного центра.[нужна цитата ]
Биология
Селеноцистеин имеет как более низкий пKа (5.43) и ниже потенциал сокращения чем цистеин. Эти свойства делают его очень подходящим для белков, которые участвуют в антиоксидант Мероприятия.[8]
Хотя он встречается в трех сферах жизни, он не универсален для всех организмов.[9] В отличие от других аминокислот, присутствующих в биологических белки, селеноцистеин не кодируется непосредственно в генетический код.[10] Вместо этого он кодируется особым образом с помощью UGA. кодон, который обычно стоп-кодон. Такой механизм называется переводческое кодирование[11] а его эффективность зависит от синтезируемого селенопротеина и трансляции факторы инициирования.[12] Когда клетки растут в отсутствие селена, трансляция селенопротеинов заканчивается на кодоне UGA, что приводит к усеченному нефункциональному ферменту. Кодон UGA кодирует селеноцистеин за счет присутствия последовательность вставки селеноцистеина (SECIS) в мРНК. Элемент SECIS определяется характерными нуклеотидными последовательностями и образцами спаривания оснований вторичной структуры. В бактерии, элемент SECIS обычно располагается сразу после кодона UGA в пределах рамки считывания селенопротеина.[13] В Археи И в эукариоты, элемент SECIS находится в 3 'нетранслируемая область (3'-UTR) мРНК и может направлять несколько кодонов UGA для кодирования остатков селеноцистеина.[14]
Опять же, в отличие от других аминокислот, в клетке не существует свободного пула селеноцистеина. Его высокая реактивность может вызвать повреждение клеток.[оригинальное исследование? ] Вместо этого клетки хранят селен в менее реакционной окисленной форме, селеноцистине, или в метилированной форме, селенометионине. Синтез селеноцистеина происходит на специализированных тРНК, который также включает его в растущие полипептиды.
Первичная и вторичная структура селеноцистеин-специфической тРНК, тРНКСек, отличаются от стандартных тРНК по нескольким параметрам, в первую очередь наличием 8-пар оснований (бактерии) или 10-пар оснований (эукариоты)[Археи? ] акцепторный стержень, длинное плечо вариабельной области и замены в нескольких хорошо консервативных положениях оснований. Селеноцистеиновые тРНК изначально заряжаются серином посредством серил-тРНК лигаза, но полученная Ser-тРНКСек не используется для перевода, потому что он не распознается нормальным коэффициентом удлинения перевода (EF-Tu в бактериях, eEF1A у эукариот).[Археи? ]
Скорее, связанный с тРНК сериловый остаток превращается в остаток селеноцистеина посредством пиридоксальфосфат -содержащий фермент селеноцистеинсинтаза. У эукариот и архей для преобразования тРНК-связанного серилового остатка в тРНК селеноцистеиниловый остаток необходимы два фермента: PSTK (О-фосфосерил-тРНК [Ser] Sec киназа) и селеноцистеинсинтаза.[15][16] Наконец, полученная Sec-тРНКСек специфически связывается с альтернативным фактором удлинения трансляции (SelB или mSelB (или eEFSec)), который целенаправленно доставляет его к рибосомам, транслирующим мРНК для селенопротеинов. Специфичность этого механизма доставки обусловлена наличием дополнительного белкового домена (у бактерий, SelB) или дополнительной субъединицы (SBP2 для эукариотических mSelB / eEFSec)[Археи? ] которые связываются с соответствующими вторичными структурами РНК, образованными элементами SECIS в мРНК селенопротеидов.
Селеноцистеин разлагается ферментом селеноцистеинлиаза в L-аланин и селенид.[17]
По состоянию на 2016 год известно, что пятьдесят четыре белка человека содержат селеноцистеин (селенопротеины).[18]
Производные селеноцистеина γ-глутамил-Se-метилселеноцистеин и Se-метилселеноцистеин встречаются в естественных условиях у растений родов Allium и Brassica.[19]
Приложения
Биотехнологические применения селеноцистеина включают использование 73Se-меченый Sec (период полураспада 73Se = 7,2 часа) в позитронно-эмиссионная томография (ПЭТ) исследования и 75Se-меченый Sec (период полураспада 75Se = 118,5 дней) в частности радиоактивная маркировка, облегчение определения фазы за счет многоволновая аномальная дифракция в Рентгеновская кристаллография белков путем введения только Sec или Sec вместе с селенометионин (SeMet) и включение конюшни 77Изотоп Se, имеющий ядерное вращение из 1/2 и может использоваться для высокого разрешения ЯМР, среди прочего.[4]
Смотрите также
- Пирролизин, другая аминокислота, не входящая в основной набор из 20.
- Селенометионин, другая селенсодержащая аминокислота, которая случайным образом замещена на метионин.
Рекомендации
- ^ Индекс Merck, 12-е издание, 8584
- ^ «Номенклатура и символика аминокислот и пептидов». Совместная комиссия IUPAC-IUB по биохимической номенклатуре. 1983 г. В архиве из оригинала от 9 октября 2008 г.. Получено 5 марта 2018.
- ^ «Совместная комиссия IUPAC-IUBMB по биохимической номенклатуре (JCBN) и Номенклатурный комитет IUBMB (NC-IUBMB)». Европейский журнал биохимии. 264 (2): 607–609. 17 августа 1999 г. Дои:10.1046 / j.1432-1327.1999.news99.x.
- ^ а б Йоханссон Л., Гафвелин Г., Арнер Э.С. (октябрь 2005 г.). «Селеноцистеин в белках - свойства и биотехнологическое использование». Biochimica et Biophysica Acta (BBA) - Общие предметы. 1726 (1): 1–13. Дои:10.1016 / j.bbagen.2005.05.010. HDL:10616/39311. PMID 15967579.
- ^ Stadtman TC (март 1974 г.). «Биохимия селена». Наука. 183 (4128): 915–22. Bibcode:1974Научный ... 183..915S. Дои:10.1126 / science.183.4128.915. PMID 4605100.
- ^ Reich HJ, Hondal RJ (апрель 2016 г.). «Почему природа выбрала селен». ACS Химическая биология. 11 (4): 821–841. Дои:10.1021 / acschembio.6b00031. PMID 26949981.
- ^ Рой Г., Сарма Б.К., Фаднис П.П., Мугеш Г. (2005). «Селенсодержащие ферменты у млекопитающих: химические перспективы» (PDF). Журнал химических наук. 117 (4): 287–303. Дои:10.1007 / BF02708441.
- ^ Бьюн Б.Дж., Кан Ю.К. (май 2011 г.). «Конформационные предпочтения и значение pK (a) остатка селеноцистеина». Биополимеры. 95 (5): 345–53. Дои:10.1002 / bip.21581. PMID 21213257.
- ^ Longtin R (апрель 2004 г.). «Забытый спор: селеноцистеин - это 21-я аминокислота?». Журнал Национального института рака. 96 (7): 504–5. Дои:10.1093 / jnci / 96.7.504. PMID 15069108.
- ^ Бёк А., Форчхаммер К., Хейдер Дж., Барон С. (декабрь 1991 г.). «Синтез селенопротеинов: расширение генетического кода». Тенденции в биохимических науках. 16 (12): 463–7. Дои:10.1016/0968-0004(91)90180-4. PMID 1838215.
- ^ Баранов П.В., Гестеланд РФ, Аткинс Дж.Ф. (март 2002 г.). «Перекодирование: трансляционные бифуркации в экспрессии генов». Ген. 286 (2): 187–201. Дои:10.1016 / S0378-1119 (02) 00423-7. PMID 11943474.
- ^ Донован Дж., Copeland PR (июль 2010 г.). «Эффективность включения селеноцистеина регулируется факторами инициации трансляции». Журнал молекулярной биологии. 400 (4): 659–64. Дои:10.1016 / j.jmb.2010.05.026. ЧВК 3721751. PMID 20488192.
- ^ Аткинс, Дж. Ф. (2009). Перекодирование: расширение правил декодирования улучшает экспрессию генов. Springer. п. 31. ISBN 978-0-387-89381-5.
- ^ Берри MJ, Banu L, Harney JW, Larsen PR (август 1993). «Функциональная характеристика эукариотических элементов SECIS, которые направляют вставку селеноцистеина в кодоны UGA». Журнал EMBO. 12 (8): 3315–22. Дои:10.1002 / j.1460-2075.1993.tb06001.x. ЧВК 413599. PMID 8344267.
- ^ Сюй XM, Карлсон BA, Mix H, Zhang Y, Saira K, Glass RS, Berry MJ, Gladyshev VN, Hatfield DL (январь 2007 г.). «Биосинтез селеноцистеина на его тРНК у эукариот». PLOS Биология. 5 (1): e4. Дои:10.1371 / journal.pbio.0050004. ЧВК 1717018. PMID 17194211.
- ^ Юань Дж., Палиура С., Салазар Дж. К., Су Д., О'Донохью П., Хон М. Дж., Кардосо А. М., Уитман В. Б., Сёлл Д. (декабрь 2006 г.). «РНК-зависимая конверсия фосфосерина в формы селеноцистеина у эукариот и архей». Труды Национальной академии наук Соединенных Штатов Америки. 103 (50): 18923–7. Bibcode:2006PNAS..10318923Y. Дои:10.1073 / pnas.0609703104. ЧВК 1748153. PMID 17142313.
- ^ Лабунский В.М., Хэтфилд Д.Л., Гладышев В.Н. (июль 2014 г.). «Селенопротеины: молекулярные пути и физиологические роли». Физиологические обзоры. 94 (3): 739–77. Дои:10.1152 / Physrev.00039.2013. ЧВК 4101630. PMID 24987004.
- ^ Romagné F, Santesmasses D, White L, Sarangi GK, Mariotti M, Hübler R, Weihmann A, Parra G, Gladyshev VN, Guigó R, Castellano S (январь 2014 г.). «SelenoDB 2.0: аннотация генов селенопротеинов у животных и их генетического разнообразия у людей». Исследования нуклеиновых кислот. 42 (Выпуск базы данных): D437-43. Дои:10.1093 / нар / gkt1045. ЧВК 3965025. PMID 24194593.
- ^ Блок, Э. (2010). Чеснок и другие луковые культуры: знания и наука. Королевское химическое общество. ISBN 978-0-85404-190-9.
дальнейшее чтение
- Зинони Ф., Биркманн А., Штадтман Т.С., Бёк А. (июль 1986 г.). «Нуклеотидная последовательность и экспрессия селеноцистеин-содержащего полипептида формиатдегидрогеназы (связанного с формиат-гидроген-лиазой) из Escherichia coli». Труды Национальной академии наук Соединенных Штатов Америки. 83 (13): 4650–4. Bibcode:1986PNAS ... 83.4650Z. Дои:10.1073 / пнас.83.13.4650. ЧВК 323799. PMID 2941757.
- Зинони Ф., Биркманн А., Лейнфельдер В., Бёк А. (май 1987 г.). «Котрансляционная вставка селеноцистеина в формиатдегидрогеназу из Escherichia coli, управляемая кодоном UGA». Труды Национальной академии наук Соединенных Штатов Америки. 84 (10): 3156–60. Bibcode:1987PNAS ... 84.3156Z. Дои:10.1073 / пнас.84.10.3156. ЧВК 304827. PMID 3033637.
- Конус Дж. Э., Дель Рио Р. М., Дэвис Дж. Н., Штадтман Т.С. (август 1976 г.). «Химическая характеристика селенопротеинового компонента клостридиальной глицинредуктазы: идентификация селеноцистеина как селенорганического фрагмента». Труды Национальной академии наук Соединенных Штатов Америки. 73 (8): 2659–63. Bibcode:1976PNAS ... 73.2659C. Дои:10.1073 / pnas.73.8.2659. ЧВК 430707. PMID 1066676.
- Fenyö D, Beavis RC (февраль 2016 г.). «Селеноцистеин: зачем ты?». Журнал протеомных исследований. 15 (2): 677–8. Дои:10.1021 / acs.jproteome.5b01028. PMID 26680273.
внешняя ссылка
| Scholia имеет тема профиль для Селеноцистеин. |
- Впервые уругвайский ученый обнаружил селеноцистеин в грибах (на испанском)

