Ремонт ДНК - DNA repair

Ремонт ДНК представляет собой набор процессов, посредством которых клетка выявляет и исправляет повреждение ДНК молекулы, кодирующие его геном.[1] В клетках человека оба нормальные метаболический виды деятельности и факторы окружающей среды, такие как радиация может вызвать повреждение ДНК, в результате чего 1 миллион индивидуальный молекулярные поражения на ячейку в сутки.[2] Многие из этих повреждений вызывают структурное повреждение молекулы ДНК и могут изменять или устранять способность клетки к расшифровывать то ген что кодирует пораженная ДНК. Другие поражения вызывают потенциально опасные мутации в геноме клетки, которые влияют на выживание ее дочерних клеток после того, как она подвергнется митоз. Как следствие, процесс восстановления ДНК постоянно активен, поскольку он реагирует на повреждение структуры ДНК. Когда нормальные процессы восстановления терпят неудачу, и когда клеточная апоптоз не происходит, может произойти непоправимое повреждение ДНК, включая двухцепочечные разрывы и Сшивки ДНК (межнитевые сшивки или ICL).[3][4] В конечном итоге это может привести к злокачественным опухолям или рак в соответствии с гипотеза двух ударов.
Скорость восстановления ДНК зависит от многих факторов, включая тип клетки, возраст клетки и внеклеточную среду. Клетка, в которой накоплено большое количество повреждений ДНК, или клетка, которая больше не может эффективно восстанавливать повреждения, нанесенные ее ДНК, может войти в одно из трех возможных состояний:
- необратимое состояние покоя, известное как старение
- клеточное самоубийство, также известное как апоптоз или же запрограммированная гибель клеток
- нерегулируемое деление клеток, которое может привести к образованию опухоль то есть раковый
Способность клетки к репарации ДНК жизненно важна для целостности ее генома и, следовательно, для нормального функционирования этого организма. Многие гены, которые, как было первоначально показано, влияют на срок жизни оказались вовлеченными в восстановление и защиту повреждений ДНК.[5]
2015 год Нобелевская премия по химии был присужден Томас Линдаль, Пол Модрич, и Азиз Санкар за их работу над молекулярными механизмами процессов репарации ДНК.[6][7]
Повреждение ДНК
Повреждение ДНК из-за факторов окружающей среды и нормального метаболический процессы внутри клетки происходят со скоростью от 10 000 до 1 000 000 молекулярных повреждений на клетку в день.[2] Хотя это составляет только 0,000165% от примерно 6 миллиардов оснований генома человека (3 миллиарда пар оснований), неизлечимые повреждения в критических генах (например, гены-супрессоры опухолей ) может препятствовать способности клетки выполнять свою функцию и значительно увеличивать вероятность опухоль формирование и способствовать неоднородность опухоли.
Подавляющее большинство повреждений ДНК влияет на первичная структура двойной спирали; то есть сами основания химически модифицированы. Эти модификации, в свою очередь, могут нарушить регулярную спиральную структуру молекул за счет введения ненативных химических связей или объемных аддуктов, которые не помещаются в стандартную двойную спираль. В отличие от белки и РНК, В ДНК обычно отсутствует третичная структура и поэтому на этом уровне не происходит повреждений или нарушений. Однако ДНК суперскрученный и намотанные на «упаковочные» белки, называемые гистоны (у эукариот), и обе надстройки уязвимы для эффектов повреждения ДНК.
Источники
Повреждения ДНК можно разделить на два основных типа:
- эндогенный повреждение, такое как атака активные формы кислорода образуются из нормальных побочных продуктов метаболизма (спонтанная мутация), особенно в процессе окислительное дезаминирование
- также включает ошибки репликации
- экзогенный ущерб, вызванный внешними факторами, такими как
- ультрафиолет [УФ 200–400 нм ] радиация от солнца или других источников искусственного света
- другие частоты излучения, в том числе рентгеновские лучи и гамма излучение
- гидролиз или тепловое нарушение
- определенный растение токсины
- рукотворный мутагенные химические вещества, особенно ароматный соединения, которые действуют как ДНК интеркалирующие агенты
- вирусы[8]
Репликация поврежденной ДНК до деления клетки может привести к включению неправильных оснований в противоположность поврежденным. Дочерние клетки, унаследовавшие эти неправильные основания, несут мутации, из которых исходная последовательность ДНК не восстанавливается (за исключением редкого случая обратная мутация, например, через преобразование гена ).
Типы
Существует несколько типов повреждений ДНК из-за эндогенных клеточных процессов:
- окисление баз [например, 8-оксо-7,8-дигидрогуанин (8-oxoG)] и образование разрывов цепи ДНК из активных форм кислорода,
- алкилирование баз (обычно метилирование ), например, образование 7-метилгуанозин, 1-метиладенин, 6-O-Methylguanine
- гидролиз баз, таких как дезаминирование, депуризация, и депиримидинация.
- «образование объемного аддукта» (например, аддукт бензо [a] пирендиол эпоксид-dG, аддукт аристолактама I-dA)
- несоответствие баз, из-за ошибок в Репликация ДНК, в котором неправильное основание ДНК вставлено на место во вновь формирующейся цепи ДНК, или основание ДНК пропускается или вставляется по ошибке.
- Повреждение моноаддукта, вызванное изменением единственного азотистого основания ДНК
- Повреждение диаддукта
Повреждения, вызванные экзогенными агентами, могут иметь разные формы. Вот несколько примеров:
- УФ-B свет вызывает сшивание между соседними основаниями цитозина и тимина, создавая димеры пиримидина. Это называется прямое повреждение ДНК.
- УФ-свет создает в основном свободные радикалы. Ущерб, причиненный свободными радикалами, называется непрямое повреждение ДНК.
- Ионизирующего излучения например, созданный в результате радиоактивного распада или в космические лучи вызывает разрывы в цепях ДНК. Ионизирующее излучение промежуточного уровня может вызвать непоправимое повреждение ДНК (что приведет к ошибкам репликации и транскрипции, необходимым для неоплазии, или может вызвать вирусные взаимодействия), что приведет к преждевременному старению и раку.
- Термическое нарушение при повышенной температуре увеличивается скорость депуризация (утрата пурин оснований из основной цепи ДНК) и одноцепочечные разрывы. Например, гидролитическая депуринизация наблюдается в термофильные бактерии, которые растут в горячие источники при 40–80 ° С.[9][10] Скорость депуринизации (300 пурин остатков на геном на поколение) слишком велико у этих видов, чтобы его можно было восстановить с помощью обычного механизма восстановления, следовательно, существует возможность адаптивный ответ не исключен.
- Промышленная химия Такие как винилхлорид и пероксид водорода и химические вещества окружающей среды, такие как полициклические ароматические углеводороды содержащиеся в дыме, саже и смоле создают огромное разнообразие аддуктов ДНК - этеновых оснований, окисленных оснований, алкилированных фосфотриэфиров и сшивание ДНК, Просто назвать несколько.
УФ-повреждение, алкилирование / метилирование, рентгеновское повреждение и окислительное повреждение являются примерами индуцированного повреждения. Самопроизвольное повреждение может включать потерю основы, дезаминирование, сахар. сморщивание кольца и таутомерный сдвиг. Конститутивное (спонтанное) повреждение ДНК, вызванное эндогенными оксидантами, можно определить по низкому уровню фосфорилирования гистона H2AX в необработанных клетках.[11]
Ядерное против митохондриального
В клетках человека и эукариотический клетки в целом, ДНК находится в двух клеточных местах - внутри ядро и внутри митохондрии. Ядерная ДНК (яДНК) существует как хроматин во время нерепликативных стадий клеточный цикл и конденсируется в агрегатные структуры, известные как хромосомы в течение деление клеток. В любом состоянии ДНК сильно уплотнена и свернута вокруг бусинчатых белков, называемых гистоны. Всякий раз, когда клетке необходимо выразить генетическую информацию, закодированную в ее яДНК, необходимая хромосомная область раскрывается, гены, расположенные в ней, экспрессируются, а затем область конденсируется обратно до ее конформации покоя. Митохондриальная ДНК (мтДНК) находится внутри митохондрий. органеллы, существует в нескольких копиях, а также тесно связан с рядом белков с образованием комплекса, известного как нуклеоид. Внутри митохондрий активные формы кислорода (ROS) или свободные радикалы, побочные продукты постоянного производства аденозинтрифосфат (ATP) через окислительного фосфорилирования, создают высокоокислительную среду, которая, как известно, повреждает мтДНК. Важнейшим ферментом в противодействии токсичности этих видов является супероксиддисмутаза, который присутствует как в митохондриях, так и в цитоплазма эукариотических клеток.
Старение и апоптоз
Старение - необратимый процесс, при котором клетка больше не разделяет, является защитной реакцией на сокращение концы хромосом. Теломеры - это длинные повторяющиеся области. некодирующая ДНК которые закрывают хромосомы и подвергаются частичной деградации каждый раз, когда клетка подвергается делению (см. Лимит Хейфлика ).[12] В отличие, покой это обратимое состояние клеточного покоя, не связанное с повреждением генома (см. клеточный цикл ). Старение клеток может служить функциональной альтернативой апоптозу в случаях, когда физическое присутствие клетки по пространственным причинам требуется организму.[13] который служит механизмом «последней инстанции» для предотвращения неправильной репликации клетки с поврежденной ДНК в отсутствие стимуляции роста. сотовая сигнализация. Нерегулируемое деление клеток может привести к образованию опухоли (см. рак ), что потенциально опасно для организма. Следовательно, индукция старения и апоптоза считается частью стратегии защиты от рака.[14]
Мутация
Важно различать повреждение ДНК и мутацию - два основных типа ошибок в ДНК. Повреждение ДНК и мутация принципиально разные. Повреждение приводит к физическим аномалиям в ДНК, таким как одно- и двухцепочечные разрывы, 8-гидроксидезоксигуанозин остатки и аддукты полициклических ароматических углеводородов. Повреждение ДНК может быть распознано ферментами и, таким образом, может быть правильно восстановлено, если избыточная информация, такая как неповрежденная последовательность в комплементарной цепи ДНК или в гомологичной хромосоме, доступна для копирования. Если в клетке сохраняется повреждение ДНК, транскрипция гена может быть предотвращена, и, таким образом, трансляция в белок также будет заблокирована. Репликация также может быть заблокирована или клетка может умереть.
В отличие от повреждения ДНК, мутация - это изменение последовательности оснований ДНК. Мутация не может быть распознана ферментами, если изменение основания присутствует в обеих цепях ДНК, и, таким образом, мутация не может быть исправлена. На клеточном уровне мутации могут вызывать изменения в функции и регуляции белков. Мутации реплицируются при репликации клетки. В популяции клеток частота мутантных клеток будет увеличиваться или уменьшаться в зависимости от воздействия мутации на способность клетки выживать и воспроизводиться.
Хотя повреждение ДНК и мутация явно отличаются друг от друга, они связаны, поскольку повреждение ДНК часто вызывает ошибки синтеза ДНК во время репликации или репарации; эти ошибки являются основным источником мутаций.
Учитывая эти свойства повреждения и мутации ДНК, можно видеть, что повреждение ДНК представляет собой особую проблему для неделящихся или медленно делящихся клеток, где не восстановленные повреждения будут накапливаться с течением времени. С другой стороны, в быстро делящихся клетках невосстановленное повреждение ДНК, которое не убивает клетку путем блокирования репликации, будет иметь тенденцию вызывать ошибки репликации и, следовательно, мутации. Подавляющее большинство мутаций, которые не являются нейтральными по своему действию, вредны для выживания клетки. Таким образом, в популяции клеток, составляющих ткань с реплицирующимися клетками, мутантные клетки будут иметь тенденцию к потере. Однако редкие мутации, которые обеспечивают преимущество в выживании, будут иметь тенденцию к клональному разрастанию за счет соседних клеток в ткани. Это преимущество клетки невыгодно для всего организма, потому что такие мутантные клетки могут вызывать рак. Таким образом, повреждение ДНК в часто делящихся клетках, поскольку оно вызывает мутации, является основной причиной рака. Напротив, повреждение ДНК в редко делящихся клетках, вероятно, является основной причиной старения.[15]
Механизмы
Клетки не могут функционировать, если повреждение ДНК нарушает целостность и доступность важной информации в геном (но клетки остаются внешне функциональными, когда несущественные гены отсутствуют или повреждены). В зависимости от типа повреждения, нанесенного двойной спиральной структуре ДНК, для восстановления утраченной информации было разработано множество стратегий восстановления. Если возможно, клетки используют немодифицированную комплементарную цепь ДНК или сестринскую. хроматида в качестве шаблона для восстановления исходной информации. Без доступа к шаблону ячейки используют подверженный ошибкам механизм восстановления, известный как транслезионный синтез в крайнем случае.
Повреждение ДНК изменяет пространственную конфигурацию спирали, и такие изменения могут быть обнаружены клеткой. Как только повреждение локализовано, определенные молекулы репарации ДНК связываются в месте повреждения или рядом с ним, побуждая другие молекулы связываться и образовывать комплекс, который позволяет осуществить репарацию.
Прямой разворот
Известно, что клетки устраняют три типа повреждений своей ДНК, химически обращая их вспять. Эти механизмы не требуют шаблона, поскольку типы повреждений, которым они противодействуют, могут возникать только на одной из четырех баз. Такие механизмы прямого обращения специфичны для типа нанесенного повреждения и не связаны с разрывом фосфодиэфирного остова. Формирование димеры пиримидина при облучении УФ-светом приводит к аномальной ковалентной связи между соседними пиримидиновыми основаниями. В фотореактивация процесс напрямую устраняет это повреждение под действием фермента фотолиаза, активация которой обязательно зависит от энергии, поглощенной из синий / УФ свет (300–500 нм длина волны ) для ускорения катализа.[16] Фотолиаза, старый фермент, присутствующий в бактерии, грибы, и большинство животные больше не работает у людей,[17] кто вместо этого использует эксцизионная репарация нуклеотидов для ремонта повреждений от УФ-излучения. Другой тип повреждений, метилирование гуаниновых оснований, напрямую устраняется протеин-метилгуанин-метилтрансферазой (MGMT), бактериальный эквивалент которой называется ogt. Это дорогостоящий процесс, потому что каждую молекулу MGMT можно использовать только один раз; то есть реакция стехиометрический скорее, чем каталитический.[18] Обобщенный ответ на метилирующие агенты у бактерий известен как адаптивный ответ и придает уровень устойчивости к алкилирующим агентам при длительном воздействии за счет активации ферментов репарации алкилирования.[19] Третий тип повреждений ДНК, обращаемых клетками, - это определенное метилирование оснований цитозина и аденина.
Однонитевое повреждение

Когда только одна из двух нитей двойной спирали имеет дефект, другую прядь можно использовать в качестве шаблона для коррекции поврежденной пряди. Чтобы восстановить повреждение одной из двух парных молекул ДНК, существует ряд иссечение механизмы, которые удаляют поврежденный нуклеотид и заменяют его неповрежденным нуклеотидом, комплементарным тому, который обнаружен в неповрежденной цепи ДНК.[18]
- Базовая эксцизионная пластика (BER): поврежденные одиночные основания или нуклеотиды чаще всего восстанавливаются путем удаления соответствующего основания или нуклеотида и последующей вставки правильного основания или нуклеотида. При базовой эксцизионной пластике a гликозилаза[20] Фермент удаляет поврежденное основание из ДНК, разрывая связь между основанием и дезоксирибозой. Эти ферменты удаляют одно основание, чтобы создать апуриновый или апиримидиновый сайт (Сайт AP ).[20] Ферменты под названием Эндонуклеазы AP Ник поврежденный каркас ДНК на сайте AP. Затем ДНК-полимераза удаляет поврежденную область, используя свою 5’-3 ’экзонуклеазную активность, и правильно синтезирует новую цепь, используя комплементарную цепь в качестве матрицы.[20] Затем разрыв закрывается ферментной ДНК-лигазой.[21]
- Эксцизионная репарация нуклеотидов (NER): объемные, искажающие спираль повреждения, такие как димеризация пиримидина повреждение, вызванное ультрафиолетовым излучением, обычно устраняется в три этапа. Сначала распознается повреждение, затем цепи ДНК длиной от 12 до 24 нуклеотидов удаляются как перед, так и после участка повреждения посредством эндонуклеазы, и удаленная область ДНК затем повторно синтезируется.[22] NER - это высоко эволюционно консервативный механизм репарации, который используется почти во всех эукариотических и прокариотических клетках.[22] У прокариот NER опосредуется УФ-белки.[22] У эукариот задействовано гораздо больше белков, хотя общая стратегия остается той же.[22]
- Исправление несоответствия системы присутствуют практически во всех ячейках для исправления ошибок, которые не исправляются корректура. Эти системы состоят как минимум из двух белков. Один обнаруживает несоответствие, а другой задействует эндонуклеазу, которая расщепляет вновь синтезированную цепь ДНК вблизи области повреждения. В Кишечная палочка , задействованными белками являются белки класса Mut: MutS, MutL и MutH. У большинства эукариот аналогом MutS является MSH, а аналогом MutL - MLH. MutH присутствует только в бактериях. Затем следует удаление поврежденной области экзонуклеазой, ресинтез ДНК-полимеразой и запечатывание разрывов ДНК-лигазой.[23]
Двухниточные разрывы

Двухцепочечные разрывы, при которых обе цепи двойной спирали разрываются, особенно опасны для клетки, поскольку они могут привести к перестройке генома. Фактически, когда двухцепочечный разрыв сопровождается перекрестным связыванием двух цепей в одной и той же точке, ни одна из цепей не может использоваться в качестве матрицы для механизмов репарации, так что клетка не сможет завершить митоз, когда Затем он делится и либо умирает, либо, в редких случаях, подвергается мутации.[3][4] Существуют три механизма восстановления двухцепочечных разрывов (DSB): негомологичное соединение концов (NHEJ), соединение концов, опосредованное микрогомологией (MMEJ) и гомологичная рекомбинация (HR).[18][24] В in vitro В системе MMEJ обнаруживается в клетках млекопитающих на уровнях 10-20% HR, когда также доступны механизмы HR и NHEJ.[25]

В NHEJ, ДНК-лигаза IV специализированный ДНК-лигаза который образует комплекс с кофактором XRCC4, непосредственно соединяет два конца.[26] Чтобы обеспечить точную репарацию, NHEJ полагается на короткие гомологичные последовательности, называемые микрогомологиями, присутствующими на однонитевых хвостах соединяемых концов ДНК. Если эти выступы совместимы, ремонт обычно выполняется аккуратно.[27][28][29][30] NHEJ также может вносить мутации во время ремонта. Потеря поврежденных нуклеотидов в месте разрыва может привести к делециям, а присоединение несовпадающих концов формирует вставки или транслокации. NHEJ особенно важен до того, как клетка реплицирует свою ДНК, поскольку нет матрицы, доступной для восстановления путем гомологичной рекомбинации. Есть "резервные" пути NHEJ в высших эукариоты.[31] Помимо своей роли в качестве хранителя генома, NHEJ требуется для соединения двухцепочечных разрывов, покрытых шпилькой, индуцированных во время V (D) J рекомбинация, процесс, который порождает разнообразие в В-клетка и Рецепторы Т-клеток в позвоночное животное иммунная система.[32]
Гомологичная рекомбинация требует наличия идентичной или почти идентичной последовательности, используемой в качестве матрицы для репарации разрыва. Ферментативный механизм, ответственный за этот процесс восстановления, почти идентичен механизму, отвечающему за хромосомный кроссовер во время мейоза. Этот путь позволяет восстановить поврежденную хромосому с помощью сестры. хроматида (доступен в G2 после репликации ДНК) или гомологичная хромосома как шаблон. DSB, вызванные механизмом репликации, пытающимся синтезировать через однонитевой разрыв или нерепарированное повреждение, вызывают коллапс вилка репликации и обычно восстанавливаются путем рекомбинации.
MMEJ начинается с ближнего боя конец резекции к MRE11 нуклеазы по обе стороны от двухцепочечного разрыва для выявления участков микрогомологии.[25] На дальнейших этапах[33] Поли (АДФ-рибоза) полимераза 1 (PARP1) является обязательным и может быть первым шагом в MMEJ. Происходит спаривание областей микрогомологии с последующим набором эндонуклеаза 1, специфичная для структуры лоскута (FEN1) для снятия свисающих закрылков. Затем следует набор XRCC1 –LIG3 к месту лигирования концов ДНК, что приводит к неповрежденной ДНК. MMEJ всегда сопровождается делецией, поэтому MMEJ является мутагенным путем репарации ДНК.[34]
В экстремофил Дейнококк радиодуранс обладает замечательной способностью выдерживать повреждения ДНК от ионизирующего излучения и другие источники. По крайней мере, две копии генома со случайными разрывами ДНК могут образовывать фрагменты ДНК через отжиг. Частично перекрывающиеся фрагменты затем используются для синтеза гомологичный регионы через перемещение D-петля которые могут продолжать наращивание, пока не найдут дополнительные партнерские нити. На последнем этапе есть кроссовер посредством RecA -зависимый гомологичная рекомбинация.[35]
Топоизомеразы вводят как одно-, так и двухцепочечные разрывы в процессе изменения состояния ДНК суперспирализация, что особенно часто встречается в регионах рядом с открытой вилкой репликации. Такие разрывы не считаются повреждением ДНК, потому что они являются естественным промежуточным звеном в биохимическом механизме топоизомеразы и немедленно восстанавливаются ферментами, которые их создали.
Транслезионный синтез
Синтез транслезии (TLS) - это процесс устойчивости к повреждению ДНК, который позволяет Репликация ДНК оборудование для репликации прошлых повреждений ДНК, таких как димеры тимина или же Сайты AP.[36] Это предполагает отказ от обычных ДНК-полимеразы для специализированных трансмезионных полимераз (например, ДНК-полимеразы IV или V из семейства Y-полимераз), часто с более крупными активными сайтами, которые могут облегчить вставку оснований напротив поврежденных нуклеотидов. Считается, что переключение полимеразы опосредуется, среди прочего, посттрансляционной модификацией репликации. процессивность фактор PCNA. Полимеразы транслезионного синтеза часто имеют низкую точность воспроизведения (высокая склонность к вставке неправильных оснований) на неповрежденные матрицы по сравнению с обычными полимеразами. Однако многие из них чрезвычайно эффективны при установке правильных оснований против определенных типов повреждений. Например, Pol η способствует безошибочному обходу поражений, вызванных УФ-облучение, в то время как Pol ι вводит мутации на этих сайтах. Известно, что Pol η добавляет первый аденин через Фотодимер Т ^ Т с помощью Базовая пара Уотсона-Крика а второй аденин будет добавлен в его син-конформации с использованием Спаривание оснований Хугстина. С точки зрения сотовой связи, рискуя появлением точечные мутации во время синтеза транслезии может быть предпочтительнее прибегнуть к более радикальным механизмам репарации ДНК, которые могут вызвать грубые хромосомные аберрации или гибель клеток. Короче говоря, в этом процессе задействованы специализированные полимеразы либо обход, либо восстановление повреждений в местах остановки репликации ДНК. Например, ДНК-полимераза человека эта может обходить сложные повреждения ДНК, такие как внутрицепочечное сшивание гуанин-тимин, G [8,5-Me] T, хотя она может вызывать целевые и полунацеленные мутации.[37] Паромита Райчаудхури и Ашис Басу[38] изучили токсичность и мутагенез одного и того же поражения в кишечная палочка путем репликации G [8,5-Me] T-модифицированной плазмиды в Кишечная палочка со специфическими нокаутами ДНК-полимеразы. Жизнеспособность штамма, лишенного pol II, pol IV и pol V, трех SOS-индуцибельных ДНК-полимераз, была очень низкой, что указывает на то, что синтез трансформации осуществляется в основном этими специализированными ДНК-полимеразами. Платформа обхода этих полимераз обеспечивается за счет Ядерный антиген пролиферирующих клеток (PCNA). В нормальных условиях PCNA, связанная с полимеразами, реплицирует ДНК. На сайте поражение, PCNA убиквитинируется или модифицируется RAD6 /RAD18 белки чтобы предоставить специализированным полимеразам платформу для обхода поражения и возобновления репликации ДНК.[39][40] После синтеза транслезии требуется удлинение. Это расширение может быть выполнено репликативной полимеразой, если TLS не содержит ошибок, как в случае Pol η, но если TLS приводит к несоответствию, для его расширения требуется специализированная полимераза; Pol ζ. Pol ζ уникален тем, что он может расширять концевые несоответствия, тогда как более процессивные полимеразы не могут. Таким образом, при обнаружении поражения репликационная вилка остановится, PCNA переключится с процессивной полимеразы на TLS-полимеразу, такую как Pol ι, чтобы исправить поражение, затем PCNA может переключиться на Pol ζ, чтобы увеличить несоответствие, и последняя PCNA переключится в процессивную полимеразу для продолжения репликации.
Глобальный ответ на повреждение ДНК
Клетки, подвергшиеся воздействию ионизирующего излучения, ультрафиолетовый свет или химические вещества склонны к образованию множественных участков объемных повреждений ДНК и двухцепочечных разрывов. Более того, агенты, повреждающие ДНК, могут повредить другие биомолекулы Такие как белки, углеводы, липиды, и РНК. Накопление повреждений, а именно двухцепочечных разрывов или аддуктов, останавливающих вилки репликации, являются одними из известных сигналов стимуляции глобального ответа на повреждение ДНК.[41] Глобальный ответ на повреждение - это действие, направленное на собственное сохранение клеток и запускающее несколько путей макромолекулярного восстановления, обхода поражения, толерантности или апоптоз. Общими чертами глобального ответа являются индукция множественных гены, клеточный цикл арест и подавление деление клеток.
Начальные шаги
Упаковка эукариотической ДНК в хроматин представляет собой барьер для всех основанных на ДНК процессов, которые требуют привлечения ферментов к участкам их действия. Чтобы позволить восстановление ДНК, хроматин должен быть реконструирован. У эукариот АТФ зависимый ремоделирование хроматина комплексы и ферменты, модифицирующие гистоны являются двумя преобладающими факторами, используемыми для выполнения этого процесса ремоделирования.[42]
Релаксация хроматина происходит быстро в месте повреждения ДНК.[43][44] На одном из самых ранних этапов стресс-активируемая протеинкиназа, c-Jun N-концевая киназа (JNK), фосфорилаты SIRT6 на серин 10 в ответ на двухцепочечные разрывы или другое повреждение ДНК.[45] Этот посттрансляционная модификация облегчает мобилизацию SIRT6 на участки повреждения ДНК и требуется для эффективного рекрутирования поли (АДФ-рибоза) полимеразы 1 (PARP1) на участки разрыва ДНК и для эффективной репарации DSB.[45] PARP1 белок начинает появляться в местах повреждения ДНК менее чем за секунду, с половиной максимального накопления в течение 1,6 секунды после повреждения.[46] PARP1 синтезирует полимерный аденозиндифосфат рибоза (поли (АДФ-рибоза) или PAR) цепи на себе. Далее ремоделирующий хроматин ALC1 быстро присоединяется к продукту действия PARP1, цепи поли-АДФ-рибозы, и ALC1 завершает прибытие к повреждению ДНК в течение 10 секунд после возникновения повреждения.[44] Примерно половина максимальной релаксации хроматина, предположительно из-за действия ALC1, происходит через 10 секунд.[44] Затем это позволяет задействовать фермент репарации ДНК. MRE11, чтобы начать восстановление ДНК в течение 13 секунд.[46]
γH2AX, фосфорилированная форма H2AX также участвует в ранних стадиях, ведущих к деконденсации хроматина после двухцепочечных разрывов ДНК. В гистон вариант H2AX составляет около 10% гистонов H2A в хроматине человека.[47] γH2AX (H2AX, фосфорилированный по серину 139) может быть обнаружен уже через 20 секунд после облучения клеток (с образованием двухцепочечного разрыва ДНК), а половинное максимальное накопление γH2AX происходит за одну минуту.[47] Размер хроматина с фосфорилированным γH2AX составляет около двух миллионов пар оснований на участке двухцепочечного разрыва ДНК.[47] γH2AX сам по себе не вызывает деконденсацию хроматина, но в течение 30 секунд после облучения RNF8 белок может быть обнаружен в ассоциации с γH2AX.[48] RNF8 опосредует обширную деконденсацию хроматина посредством его последующего взаимодействия с CHD4,[49] компонент ремоделирования нуклеосом и комплекса деацетилазы NuRD.
DDB2 встречается в гетеродимерном комплексе с DDB1. Этот комплекс далее комплексовался с убиквитинлигаза белок CUL4A[50] и с PARP1.[51] Этот более крупный комплекс быстро связывается с УФ-индуцированным повреждением хроматина, причем полумаксимальная связь завершается за 40 секунд.[50] Белок PARP1, присоединенный как к DDB1, так и к DDB2, затем PARylates (создает цепь поли-АДФ-рибозы) на DDB2, который привлекает белок ремоделирования ДНК ALC1.[51] Действие ALC1 расслабляет хроматин в месте повреждения ДНК ультрафиолетом. Это расслабление позволяет другим белкам в эксцизионная репарация нуклеотидов путь проникновения в хроматин и восстановления УФ-индуцированного димер циклобутана пиримидина убытки.
После быстрого ремоделирование хроматина, клеточный цикл контрольно-пропускные пункты активируются, чтобы позволить репарации ДНК происходить до того, как клеточный цикл прогрессирует. Первые два киназы, Банкомат и ATR активируются в течение 5-6 минут после повреждения ДНК. Затем следует фосфорилирование белка контрольной точки клеточного цикла. Chk1, инициируя свою функцию, примерно через 10 минут после повреждения ДНК.[52]
Контрольные точки повреждения ДНК
После повреждения ДНК клеточный цикл контрольно-пропускные пункты активированы. Активация контрольной точки приостанавливает клеточный цикл и дает клетке время на восстановление повреждений, прежде чем продолжить деление. Контрольные точки повреждения ДНК происходят в G1 /S и G2 /M границы. Внутри-S КПП тоже существует. Активация контрольной точки контролируется двумя мастерами. киназы, Банкомат и ATR. ATM реагирует на двухцепочечные разрывы ДНК и нарушения структуры хроматина,[53] тогда как ATR в первую очередь реагирует на остановку вилки репликации. Эти киназы фосфорилировать нижестоящие цели в преобразование сигнала каскад, в конечном итоге приводящий к остановке клеточного цикла. Класс белков-посредников контрольных точек, включая BRCA1, MDC1, и 53BP1 также был идентифицирован.[54] Эти белки, по-видимому, необходимы для передачи сигнала активации контрольной точки нижестоящим белкам.
Контрольная точка повреждения ДНК это путь передачи сигнала это блокирует клеточный цикл прогрессирование в G1, G2 и метафаза и замедляет скорость прогрессирования фазы S, когда ДНК поврежден. Это приводит к паузе в клеточном цикле, позволяя клетке время отремонтировать повреждение, прежде чем продолжить деление.
Белки контрольной точки можно разделить на четыре группы: фосфатидилинозитол-3-киназа (PI3K) -подобный протеинкиназа, ядерный антиген пролиферирующих клеток (PCNA) -подобная группа, две серин / треониновые (S / T) киназы и их адаптеры. Центральным во всех ответах контрольных точек, вызванных повреждением ДНК, является пара больших протеинкиназ, принадлежащих к первой группе PI3K-подобных протеинкиназ - ATM (Атаксия, телеангиэктазия, мутировавшая ) и ATR (родственные атаксии и Rad) киназы, последовательность и функции которых хорошо сохранились в процессе эволюции. Для любой реакции на повреждение ДНК требуется либо ATM, либо ATR, потому что они обладают способностью связываться с хромосомы в месте повреждения ДНК вместе с дополнительными белками, которые являются платформами, на которых могут быть собраны компоненты ответа на повреждение ДНК и комплексы репарации ДНК.
Важной целью нисходящего потока ATM и ATR является p53, так как это требуется для наведения апоптоз после повреждения ДНК.[55] В ингибитор циклин-зависимой киназы стр.21 индуцируется как p53-зависимыми, так и p53-независимыми механизмами и может останавливать клеточный цикл в контрольных точках G1 / S и G2 / M путем деактивации циклин /циклин-зависимая киназа комплексы.[56]
Прокариотический SOS-ответ
В SOS ответ изменения в экспрессия гена в кишечная палочка и другие бактерии в ответ на обширное повреждение ДНК. В прокариотический Система SOS регулируется двумя ключевыми белками: LexA и RecA. LexA гомодимер это транскрипционный репрессор что привязано к оператор Последовательности, обычно называемые SOS-сообщениями. В кишечная палочка известно, что LexA регулирует транскрипцию примерно 48 генов, включая гены lexA и recA.[57] Известно, что реакция SOS широко распространена в домене бактерий, но в большинстве случаев она отсутствует у некоторых бактериальных типов, таких как Спирохеты.[58]Наиболее распространенными клеточными сигналами, активирующими SOS-ответ, являются участки одноцепочечной ДНК (оцДНК), возникающие в результате остановки вилки репликации или двухниточные разрывы, которые обрабатываются ДНК-геликаза чтобы разделить две нити ДНК.[41] На этапе инициации белок RecA связывается с оцДНК в Гидролиз АТФ управляемая реакция, создающая филаменты RecA-ssDNA. Нити RecA – ssDNA активируют LexA autoпротеаза активность, которая в конечном итоге приводит к расщеплению димера LexA и последующей деградации LexA. Потеря репрессора LexA вызывает транскрипцию генов SOS и делает возможным дальнейшую индукцию сигнала, ингибирование деления клеток и повышение уровней белков, ответственных за обработку повреждений.
В кишечная палочка, SOS-боксы представляют собой 20-нуклеотидные последовательности рядом с промоторами с палиндромный структура и высокая степень сохранения последовательности. В других классах и типах последовательность SOS-боксов значительно различается, с разной длиной и составом, но она всегда высококонсервативна и является одним из самых сильных коротких сигналов в геноме.[58] Высокое информационное содержание SOS-боксов позволяет дифференцированно связывать LexA с разными промоторами и позволяет рассчитывать время для SOS-ответа. Гены восстановления повреждений индуцируются в начале SOS-ответа. Подверженные ошибкам полимеразы трансфузии, например, UmuCD'2 (также называемые ДНК-полимеразой V), индуцируются позже в крайнем случае.[59] После того, как повреждение ДНК репарируется или обходится с использованием полимераз или путем рекомбинации, количество одноцепочечной ДНК в клетках уменьшается, снижение количества волокон RecA снижает активность расщепления гомодимера LexA, который затем связывается с SOS-боксами рядом с промоторами и восстанавливает нормальная экспрессия генов.
Транскрипционные ответы эукариот на повреждение ДНК
Эукариотический клетки, подвергшиеся воздействию агентов, повреждающих ДНК, также активируют важные защитные пути, индуцируя множество белков, участвующих в репарации ДНК, контрольная точка клеточного цикла контроль, трафик и деградация белков. Такой транскрипционный ответ в масштабе всего генома очень сложен и жестко регулируется, что позволяет скоординировать глобальный ответ на повреждения. Контакт с дрожжи Saccharomyces cerevisiae к агентам, повреждающим ДНК, приводит к перекрывающимся, но различным профилям транскрипции. Сходства с экологическими шоковая реакция указывает на то, что на уровне транскрипционной активации существует общий глобальный путь ответа на стресс. Напротив, разные типы клеток человека по-разному реагируют на повреждения, что указывает на отсутствие общего глобального ответа. Вероятное объяснение этой разницы между дрожжевыми и человеческими клетками может заключаться в следующем. неоднородность из млекопитающее клетки. У животного разные типы клеток распределены между разными органами, которые развили разную чувствительность к повреждению ДНК.[60]
В целом глобальный ответ на повреждение ДНК включает экспрессию нескольких генов, ответственных за пострепликационный ремонт, гомологичная рекомбинация, эксцизионная репарация нуклеотидов, Контрольная точка повреждения ДНК, глобальная активация транскрипции, гены, контролирующие распад мРНК, и многие другие. Большой ущерб, нанесенный клетке, заставляет ее принять важное решение: подвергнуться апоптозу и умереть или выжить ценой жизни с измененным геномом. Повышение устойчивости к повреждениям может привести к увеличению выживаемости, что приведет к большему накоплению мутаций. Дрожжевой Rev1 и человеческая полимераза η являются членами транслезионной ДНК [семейства Y полимеразы присутствуют во время глобального ответа на повреждение ДНК и отвечают за усиленный мутагенез во время глобального ответа на повреждение ДНК у эукариот.[41]
Старение
Патологические эффекты плохой репарации ДНК

У экспериментальных животных с генетическим дефицитом репарации ДНК часто наблюдается сокращение продолжительности жизни и повышение заболеваемости раком.[15] Например, мыши, лишенные доминирующего пути NHEJ и механизмов поддержания теломер, получают лимфома и инфекции чаще и, как следствие, имеют более короткую продолжительность жизни, чем мыши дикого типа.[61] Точно так же у мышей, дефицитных по ключевому белку репарации и транскрипции, который раскручивает спирали ДНК, преждевременно начинаются заболевания, связанные со старением, и, как следствие, сокращается продолжительность жизни.[62] Однако не каждый дефицит репарации ДНК вызывает точно предсказанные эффекты; у мышей, дефицитных по пути NER, сокращалась продолжительность жизни без соответственно более высоких скоростей мутаций.[63]
Если скорость повреждения ДНК превышает способность клетки восстанавливать ее, накопление ошибок может подавить клетку и привести к раннему старению, апоптозу или раку. Унаследованные заболевания, связанные с нарушением функции восстановления ДНК, приводят к преждевременному старению,[15] повышенная чувствительность к канцерогенам и, соответственно, повышенный риск рака (см. ниже ). С другой стороны, организмы с улучшенными системами репарации ДНК, такими как Дейнококк радиодуранс, наиболее радиационно-устойчивый из известных организмов, проявляют замечательную устойчивость к двухцепочечному разрушающему действию радиоактивность, вероятно, из-за повышенной эффективности репарации ДНК и особенно NHEJ.[64]
Долголетие и ограничение калорийности

Было установлено, что ряд отдельных генов влияет на вариации продолжительности жизни в популяции организмов. Эффекты этих генов сильно зависят от окружающей среды, в частности, от диеты организма. Ограничение калорийности воспроизводимо приводит к увеличению продолжительности жизни у различных организмов, вероятно, за счет определение питательных веществ пути и уменьшились скорость метаболизма. Молекулярные механизмы, с помощью которых такое ограничение приводит к увеличению продолжительности жизни, пока неясны (см.[65] для обсуждения); однако поведение многих генов, которые, как известно, участвуют в репарации ДНК, изменяется в условиях ограничения калорийности. Было показано, что несколько агентов, обладающих антивозрастными свойствами, уменьшают основной уровень mTOR сигнализация, свидетельствующая о снижении метаболическая активность, и одновременно снизить конститутивный уровень Повреждение ДНК индуцируется эндогенно генерируемыми реактивными формами кислорода.[66]
Например, увеличение дозировка гена гена SIR-2, который регулирует упаковку ДНК у нематодного червя Caenorhabditis elegans, может значительно продлить срок службы.[67] Известно, что гомолог SIR-2 у млекопитающих индуцирует нижестоящие факторы репарации ДНК, участвующие в NHEJ, активность, которая особенно усиливается в условиях ограничения калорийности.[68] Ограничение калорий тесно связано со скоростью эксцизионной репарации оснований в ядерной ДНК грызунов.[69] хотя подобные эффекты не наблюдались в митохондриальной ДНК.[70]
В C. elegans Ген AGE-1, вышестоящий эффектор путей репарации ДНК, значительно увеличивает продолжительность жизни в условиях свободного питания, но приводит к снижению репродуктивной способности в условиях ограничения калорийности.[71] Это наблюдение подтверждает плейотропия теория биологические причины старения, что предполагает, что гены, дающие большое преимущество выживания в начале жизни, будут отбираться, даже если они несут соответствующий недостаток в конце жизни.
Медицина и модуляция восстановления ДНК
Наследственные нарушения репарации ДНК
Дефекты в механизме NER являются причиной нескольких генетических нарушений, в том числе:
- Пигментная ксеродермия: гиперчувствительность к солнечному свету / ультрафиолетовому излучению, что приводит к увеличению заболеваемости раком кожи и преждевременному старению
- Синдром Кокейна: гиперчувствительность к УФ и химическим веществам
- Трихотиодистрофия: чувствительная кожа, ломкие волосы и ногти.
Умственная отсталость часто сопровождает последние два расстройства, что указывает на повышенную уязвимость нейронов развития.
Другие нарушения репарации ДНК включают:
- Синдром Вернера: преждевременное старение и задержка роста
- Синдром Блума: гиперчувствительность к солнечному свету, высокая частота злокачественные новообразования (особенно лейкемии ).
- Атаксия телеангиэктазия: чувствительность к ионизирующему излучению и некоторым химическим веществам
Все вышеперечисленные заболевания часто называют «сегментарными». прогерия " ("болезни ускоренного старения "), потому что их жертвы выглядят пожилыми и страдают заболеваниями, связанными со старением, в аномально молодом возрасте, не проявляя при этом всех симптомов старости.
Другие заболевания, связанные со снижением функции репарации ДНК, включают: Анемия Фанкони, наследственный рак молочной железы и наследственный рак толстой кишки.
Рак
Из-за внутренних ограничений механизмов восстановления ДНК, если бы люди жили достаточно долго, у всех в конечном итоге разовьется рак.[72][73] Есть не менее 34 Унаследованные мутации гена репарации ДНК человека, повышающие риск рака. Многие из этих мутаций приводят к тому, что восстановление ДНК менее эффективно, чем обычно. Особенно, Наследственный неполипозный колоректальный рак (HNPCC) тесно связан со специфическими мутациями в пути репарации ошибочного спаривания ДНК. BRCA1 и BRCA2, два важных гена, мутации которых значительно повышают риск рака груди у носителей,[74] оба связаны с большим количеством путей репарации ДНК, особенно с NHEJ и гомологичной рекомбинацией.
Противораковые процедуры, такие как химиотерапия и лучевая терапия работают, подавляя способность клетки восстанавливать повреждения ДНК, что приводит к гибели клетки. Предпочтительно поражаются наиболее быстро делящиеся клетки - чаще всего раковые. Побочный эффект заключается в том, что поражаются и другие незлокачественные, но быстро делящиеся клетки, такие как клетки-предшественники в кишечнике, коже и кроветворной системе. Современные методы лечения рака пытаются локализовать повреждение ДНК в клетках и тканях, связанное только с раком, либо физическими средствами (концентрация терапевтического агента в области опухоли), либо биохимическими средствами (используя свойство, уникальное для раковых клеток в организме). . В контексте терапии, направленной на гены ответа на повреждение ДНК, последний подход получил название «синтетическая летальность».[75]
Возможно, наиболее известным из этих синтетических смертоносных препаратов является поли (АДФ-рибоза) полимераза 1 (PARP1 ) ингибитор олапариб, который был одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов в 2015 году для лечения рака яичников с дефектом BRCA у женщин. Опухолевые клетки с частичной потерей ответа на повреждение ДНК (в частности, гомологичная рекомбинация Repair) зависят от другого механизма - репарации одноцепочечного разрыва, который частично состоит из продукта гена PARP1.[76] Olaparib комбинируется с химиотерапевтическими средствами для ингибирования репарации одноцепочечных разрывов, вызванных повреждением ДНК, вызванным совместно вводимой химиотерапией. Опухолевые клетки, полагающиеся на этот механизм репарации остаточной ДНК, неспособны восстанавливать повреждения и, следовательно, не способны выживать и пролиферировать, тогда как нормальные клетки могут восстанавливать повреждение с помощью функционирующего механизма гомологичной рекомбинации.
Многие другие препараты для использования против других механизмов репарации остаточной ДНК, обычно обнаруживаемых при раке, в настоящее время исследуются. Тем не менее, синтетические подходы к лечению летальности были поставлены под сомнение из-за появляющихся доказательств приобретенной устойчивости, достигаемой за счет перестройки путей ответа на повреждение ДНК и реверсии ранее подавленных дефектов.[77]
Дефекты репарации ДНК при раке
За последние несколько лет стало очевидно, что реакция на повреждение ДНК действует как барьер для злокачественной трансформации пренеопластических клеток.[78] Предыдущие исследования показали повышенный ответ на повреждение ДНК в моделях клеточных культур с активацией онкогенов.[79] и пренеопластические аденомы толстой кишки.[80] Механизмы реакции на повреждение ДНК запускают остановку клеточного цикла и пытаются восстановить повреждения ДНК или способствовать гибели / старению клеток, если восстановление невозможно. Стресс репликации наблюдается в предопухолевых клетках из-за повышенных сигналов пролиферации от онкогенных мутаций. Репликационный стресс характеризуется: повышенным инициированием репликации / запуском ориджина; усиление транскрипции и коллизий комплексов транскрипция-репликация; нуклеотидная недостаточность; увеличение активных форм кислорода (АФК).[81]
Репликационный стресс, наряду с отбором инактивирующих мутаций в генах ответа на повреждение ДНК в процессе эволюции опухоли,[82] приводит к подавлению и / или потере некоторых механизмов ответа на повреждение ДНК и, следовательно, к потере репарации ДНК и / или старения / запрограммированной гибели клеток. В экспериментальных моделях мышей наблюдали потерю клеточного старения, опосредованного ответом на повреждение ДНК, после использования короткая шпилька РНК (shRNA) для ингибирования реакции двухцепочечного разрыва киназы атаксии телеангиэктазии (Банкомат ), что приводит к увеличению размера опухоли и инвазивности.[80] Люди, рожденные с наследственными дефектами механизмов восстановления ДНК (например, Синдром Ли-Фраумени ) имеют более высокий риск рака.[83]
Распространенность мутаций в ответ на повреждение ДНК различается в зависимости от типа рака; например, 30% инвазивных карцином груди имеют мутации в генах, участвующих в гомологичной рекомбинации.[78] При раке подавление наблюдается во всех механизмах ответа на повреждение ДНК (эксцизионная репарация оснований (BER), эксцизионная репарация нуклеотидов (NER), репарация несоответствия ДНК (MMR), репарация гомологичной рекомбинацией (HR), негомологичное соединение концов (NHEJ) и транслезионный синтез ДНК (TLS).[84] Помимо мутаций в генах восстановления повреждений ДНК, мутации также возникают в генах, ответственных за остановку клеточный цикл чтобы дать достаточно времени для репарации ДНК, и некоторые гены участвуют как в репарации повреждений ДНК, так и в контроле контрольных точек клеточного цикла, например ATM и киназа контрольной точки 2 (CHEK2) - опухолевый супрессор, который часто отсутствует или подавляется в немелких клеточный рак легкого.[85]
| HR | NHEJ | SSA | FA | BER | NER | MMR | |
|---|---|---|---|---|---|---|---|
| Банкомат | Икс | Икс | Икс | ||||
| ATR | Икс | Икс | Икс | ||||
| PAXIP | Икс | Икс | |||||
| RPA | Икс | Икс | Икс | ||||
| BRCA1 | Икс | Икс | |||||
| BRCA2 | Икс | Икс | |||||
| RAD51 | Икс | Икс | |||||
| RFC | Икс | Икс | Икс | ||||
| XRCC1 | Икс | Икс | |||||
| PCNA | Икс | Икс | Икс | ||||
| PARP1 | Икс | Икс | |||||
| ERCC1 | Икс | Икс | Икс | Икс | |||
| MSH3 | Икс | Икс | Икс |
Таблица: гены, участвующие в путях реакции на повреждение ДНК и часто мутирующие при раке (HR = гомологичная рекомбинация; NHEJ = негомологичное соединение концов; SSA = однонитевой отжиг; FA = путь анемии фанкони; BER = эксцизионная репарация оснований; NER = нуклеотид эксцизионная пластика; MMR = исправление несовпадений)
Эпигенетические дефекты репарации ДНК при раке
Классически рак рассматривался как набор заболеваний, которые вызваны прогрессирующими генетическими аномалиями, включая мутации в генах-супрессорах опухолей и онкогенов, а также хромосомные аберрации. Однако стало очевидно, что причиной рака также являютсяэпигенетические изменения.[86]
Эпигенетические изменения относятся к функционально значимым модификациям генома, которые не связаны с изменением нуклеотидной последовательности. Примерами таких модификаций являются изменения в Метилирование ДНК (гиперметилирование и гипометилирование) и гистоновая модификация,[87] изменения в архитектуре хромосом (вызванные несоответствующей экспрессией белков, таких как HMGA2 или же HMGA1 )[88] и изменения, вызванные микроРНК. Каждое из этих эпигенетических изменений служит для регулирования экспрессии генов без изменения лежащих в основе Последовательность ДНК. Эти изменения обычно сохраняются деления клеток, последние для нескольких поколений клеток и могут рассматриваться как эпимутации (эквивалент мутации).
Хотя при раке обнаруживается большое количество эпигенетических изменений, особенно важны эпигенетические изменения в генах репарации ДНК, вызывающие снижение экспрессии белков репарации ДНК. Считается, что такие изменения происходят на ранних стадиях прогрессирования рака и являются вероятной причиной генетический нестабильность, характерная для онкологических заболеваний.[89][90][91]
Сниженная экспрессия генов репарации ДНК вызывает недостаточную репарацию ДНК. Когда репарация ДНК недостаточна, повреждения ДНК остаются в клетках на более высоком, чем обычно, уровне, и эти избыточные повреждения вызывают повышенную частоту мутаций или эпимутаций. Скорость мутации существенно возрастает в клетках, дефектных по Ремонт несоответствия ДНК[92][93] или в гомологичный рекомбинационный ремонт (HRR).[94] Хромосомные перестройки и анеуплоидия также увеличиваются в клетках с дефектом HRR.[95]
Более высокие уровни повреждения ДНК не только вызывают усиление мутаций, но и вызывают усиление эпимутаций. Во время репарации двухцепочечных разрывов ДНК или репарации других повреждений ДНК не полностью очищенные участки репарации могут вызывать эпигенетическое молчание генов.[96][97]
Недостаточная экспрессия белков репарации ДНК из-за наследственной мутации может вызвать повышенный риск рака. Лица с наследственным нарушением любого из 34 генов репарации ДНК (см. Расстройство дефицита репарации ДНК ) имеют повышенный риск рака, при этом некоторые дефекты приводят к 100% вероятности возникновения рака на протяжении всей жизни (например, мутации p53).[98] Однако такие мутации зародышевой линии (которые вызывают синдромы высокопенетрантного рака) являются причиной только около 1 процента случаев рака.[99]
Частоты эпимутаций в генах репарации ДНК
Дефицит ферментов репарации ДНК иногда вызван вновь возникающей соматической мутацией в гене репарации ДНК, но гораздо чаще вызван эпигенетическими изменениями, которые снижают или заглушают экспрессию генов репарации ДНК. Например, когда 113 случаев рака прямой кишки были исследованы последовательно, только четыре из них имели миссенс-мутация в гене репарации ДНК MGMT, в то время как у большинства была снижена экспрессия MGMT из-за метилирования промоторной области MGMT (эпигенетическое изменение).[100] Пять различных исследований показали, что от 40% до 90% случаев колоректального рака снижают экспрессию MGMT из-за метилирования промоторной области MGMT.[101][102][103][104][105]
Аналогичным образом, из 119 случаев колоректального рака с недостаточностью репарации несоответствия, в которых отсутствовал ген репарации ДНК PMS2 экспрессии PMS2 был дефицит в 6 из-за мутаций в гене PMS2, в то время как в 103 случаях экспрессия PMS2 была недостаточной, потому что его партнер по спариванию MLH1 был репрессирован из-за метилирования промотора (белок PMS2 нестабилен в отсутствие MLH1).[106] В других 10 случаях потеря экспрессии PMS2, вероятно, была связана с эпигенетической сверхэкспрессией микроРНК, miR-155, который подавляет MLH1.[107]
В другом примере эпигенетические дефекты были обнаружены при различных формах рака (например, груди, яичников, колоректального рака, головы и шеи). Два или три недостатка в выражении ERCC1, XPF или PMS2 возникают одновременно в большинстве из 49 случаев рака толстой кишки, оцененных Facista et al.[108]
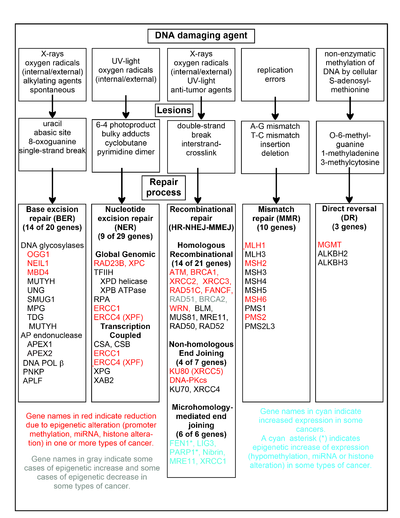
В таблице в этом разделе показаны некоторые часто встречающиеся агенты, повреждающие ДНК, примеры повреждений ДНК, которые они вызывают, и пути, которые имеют дело с этими повреждениями ДНК. По крайней мере, 169 ферментов либо непосредственно используются в репарации ДНК, либо влияют на процессы репарации ДНК.[109] Из них 83 непосредственно используются для восстановления 5 типов повреждений ДНК, показанных на диаграмме.
Некоторые из наиболее хорошо изученных генов, играющих ключевую роль в этих процессах восстановления, показаны на диаграмме. Обозначения генов, показанные красным, серым или голубым цветом, указывают на гены, которые часто эпигенетически изменяются при различных типах рака. Статьи в Википедии о каждом из генов, выделенных красным, серым или голубым цветом, описывают эпигенетические изменения и рак (ы), при которых обнаруживаются эти эпимутации. Обзорные статьи,[110] и широкие экспериментальные обзорные статьи[111][112] также документируют большинство этих недостатков эпигенетической репарации ДНК при раке.
Выделенные красным гены часто уменьшаются или заглушаются эпигенетическими механизмами при различных формах рака. Когда эти гены имеют низкую экспрессию или ее отсутствие, могут накапливаться повреждения ДНК. Ошибки репликации после этих повреждений (см. транслезионный синтез ) может привести к увеличению количества мутаций и, в конечном итоге, к раку. Эпигенетическая репрессия генов репарации ДНК в точный Пути репарации ДНК, по-видимому, играют центральную роль в канцерогенез.
Два выделенных серым гена RAD51 и BRCA2, необходимы для гомологичный рекомбинационный ремонт. Иногда они эпигенетически чрезмерно выражены, а иногда недостаточно выражены при некоторых формах рака. Как указано в статьях Википедии о RAD51 и BRCA2 такие виды рака обычно имеют эпигенетические дефекты в других генах репарации ДНК. Эти дефекты репарации, вероятно, вызовут увеличение нереставрированных повреждений ДНК. Чрезмерное выражение RAD51 и BRCA2 наблюдаемые при этих раковых заболеваниях могут отражать избирательное давление для компенсации RAD51 или же BRCA2 сверхэкспрессия и повышенная гомологичная рекомбинационная репарация, чтобы, по крайней мере, частично справиться с такими избыточными повреждениями ДНК. В тех случаях, когда RAD51 или же BRCA2 недоэкспрессированы, это само по себе привело бы к увеличению нерепарированных повреждений ДНК. Ошибки репликации после этих повреждений (см. транслезионный синтез ) может вызвать увеличение количества мутаций и рака, так что недостаточная экспрессия RAD51 или же BRCA2 сам по себе был бы канцерогенным.
Гены, выделенные голубым цветом, находятся в соединение концов, опосредованное микрогомологией (MMEJ) и активируются при раке. MMEJ является дополнительным подверженным ошибкам неточный путь восстановления для двухцепочечных разрывов. При репарации двухцепочечного разрыва MMEJ гомология 5-25 комплементарных пар оснований между обеими спаренными цепями достаточна для выравнивания цепей, но обычно присутствуют несовпадающие концы (лоскуты). MMEJ удаляет лишние нуклеотиды (створки) в местах соединения цепей, а затем лигирует цепи для создания неповрежденной двойной спирали ДНК. MMEJ почти всегда включает хотя бы небольшую делецию, так что это мутагенный путь.[113] FEN1, эндонуклеаза лоскута в MMEJ, эпигенетически увеличивается за счет гипометилирования промотора и сверхэкспрессируется в большинстве случаев рака молочной железы,[114] предстательная железа,[115] желудок,[116][117] нейробластомы,[118] поджелудочная железа[119] и легкое.[120] PARP1 также сверхэкспрессируется, когда его промоторная область ETS сайт эпигенетически гипометилирован, и это способствует прогрессированию рака эндометрия[121] и серозный рак яичников с мутацией BRCA.[122] Другие гены в MMEJ метаболические пути также чрезмерно экспрессируются при ряде видов рака (см. MMEJ для сводки), а также отображаются голубым цветом.
Распределение репарации ДНК в соматических клетках человека по всему геному
Различная активность путей репарации ДНК в различных областях генома человека приводит к тому, что мутации очень неравномерно распределяются в опухолевых геномах.[123][124] В частности, богатые генами, рано реплицирующиеся области человеческого генома демонстрируют более низкие частоты мутаций, чем бедные генами, поздно реплицирующиеся области. гетерохроматин. Один из механизмов, лежащих в основе этого, включает гистоновая модификация H3K36me3, который может набирать ремонт несоответствия белки,[125] тем самым снижая частоту мутаций в H3K36me3 -отмеченные регионы.[126] Другой важный механизм касается эксцизионная репарация нуклеотидов, которые могут быть задействованы аппаратом транскрипции, снижая частоту соматических мутаций в активных генах.[124] и другие области открытого хроматина.[127]
Эволюция
Основные процессы репарации ДНК очень высоки. консервированный среди обоих прокариоты и эукариоты и даже среди бактериофаги (вирусы которые заражают бактерии ); однако более сложные организмы с более сложными геномами имеют, соответственно, более сложные механизмы восстановления.[128] Способность большого количества белка структурные мотивы катализировать соответствующие химические реакции сыграли значительную роль в разработке механизмов репарации в ходе эволюции. Для чрезвычайно подробного обзора гипотез, касающихся эволюции репарации ДНК, см.[129]
В Окаменелости указывает на то, что одноклеточная жизнь начала размножаться на планете в какой-то момент во время Докембрийский период, хотя точно неясно, когда впервые появилась узнаваемая современная жизнь. Нуклеиновые кислоты стали единственным и универсальным средством кодирования генетической информации, требующим механизмов восстановления ДНК, которые в своей основной форме унаследованы всеми существующими формами жизни от их общего предка. Появление богатой кислородом атмосферы Земли (известной как "кислородная катастрофа ") из-за фотосинтетический организмов, а также наличие потенциально вредных свободные радикалы в камере из-за окислительного фосфорилирования, потребовали эволюции механизмов репарации ДНК, которые действуют конкретно, чтобы противодействовать типам повреждений, вызванных окислительный стресс.
Скорость эволюционного изменения
В некоторых случаях повреждение ДНК не восстанавливается или восстанавливается с помощью механизма, подверженного ошибкам, который приводит к изменению исходной последовательности. Когда это происходит, мутации может распространяться в геномах потомства клетки. Если такое событие произойдет в линия зародыша ячейка, которая в конечном итоге произведет гамета, мутация может передаваться потомству организма. Скорость эволюция в конкретном виде (или в конкретном гене) является функцией скорости мутации. Как следствие, скорость и точность механизмов репарации ДНК имеют влияние на процесс эволюционных изменений.[130] Защита от повреждений и репарация ДНК не влияет на скорость адаптации за счет регуляции генов, а также за счет рекомбинации и отбора аллелей. С другой стороны, восстановление и защита повреждений ДНК действительно влияет на скорость накопления непоправимых, полезных, расширяющих код наследуемых мутаций и замедляет эволюционный механизм расширения генома организмов с новыми функциями. Противоречие между эволюционируемостью и восстановлением и защитой мутаций требует дальнейшего изучения.
Технологии
Технология, получившая название кластеризованные с регулярными интервалами короткие палиндромные повторы (сокращенно до CRISPR -Cas9) была открыта в 2012 году. Новая технология позволяет любому, кто имеет подготовку в области молекулярной биологии, с точностью изменять гены любого вида, вызывая повреждение ДНК в определенной точке и затем изменяя механизмы восстановления ДНК для вставки новых генов.[131] Это дешевле, эффективнее и точнее, чем другие технологии. С помощью CRISPR – Cas9 ученые могут редактировать части генома путем удаления, добавления или изменения частей в последовательности ДНК.
Смотрите также
- Болезнь ускоренного старения
- Старение ДНК
- Клеточный цикл
- Повреждение ДНК (естественное)
- Теория повреждений ДНК старения
- Репликация ДНК
- Прямое повреждение ДНК
- Генная терапия
- Митохондриальная генетика человека
- Непрямое повреждение ДНК
- Продление жизни
- Прогерия
- Старение
- SiDNA
- Научный журнал Ремонт ДНК под Мутационные исследования
Рекомендации
- ^ «Серия обзоров природы: повреждение ДНК». Обзоры природы Молекулярная клеточная биология. 5 июля 2017 г.. Получено 7 ноября 2018.
- ^ а б Лодиш Х., Берк А., Мацудаира П., Кайзер Калифорния, Кригер М., Скотт М.П., Зипурски С.Л., Дарнелл Дж. (2004). Молекулярная биология клетки (5-е изд.). Нью-Йорк: WH Freeman. п. 963.
- ^ а б Ачарья П.В. (1971). «Выделение и частичная характеристика коррелированных с возрастом олиго-дезоксирибо-рибонуклеотидов с ковалентно связанными аспартил-глутамиловыми полипептидами». Медицинский журнал Джона Хопкинса. Добавка (1): 254–60. PMID 5055816.
- ^ а б Бьоркстен Дж, Ачарья П.В., Эшман С., Ветлауфер ДБ (июль 1971 г.). «Герогенные фракции у крыс, меченных тритием». Журнал Американского гериатрического общества. 19 (7): 561–74. Дои:10.1111 / j.1532-5415.1971.tb02577.x. PMID 5106728. S2CID 33154242.
- ^ Браунер WS, Кан А.Дж., Зив Э., Райнер А.П., Осима Дж., Коутон Р.М. и др. (Декабрь 2004 г.). «Генетика долголетия человека». Американский журнал медицины. 117 (11): 851–60. CiteSeerX 10.1.1.556.6874. Дои:10.1016 / j.amjmed.2004.06.033. PMID 15589490.
- ^ Broad WJ (7 октября 2015 г.). «Нобелевская премия по химии присуждена Томасу Линдалу, Полу Модричу и Азизу Санкару за исследования ДНК». Нью-Йорк Таймс. Получено 7 октября 2015.
- ^ Персонал (7 октября 2015 г.). «Нобелевская премия по химии 2015 года - восстановление ДНК - обеспечение химической стабильности на всю жизнь» (PDF). Нобелевская премия. Получено 7 октября 2015.
- ^ Рулстон А., Марселлус Р.К., Брантон П.Е. (1999). «Вирусы и апоптоз». Ежегодный обзор микробиологии. 53: 577–628. Дои:10.1146 / annurev.micro.53.1.577. PMID 10547702.
- ^ Мэдиган MT, Мартино JM (2006). Биология микроорганизмов Брока (11-е изд.). Пирсон. п. 136. ISBN 978-0-13-196893-6.
- ^ Охта Т., Токишита С.И., Мочизуки К., Кавасе Дж., Сакахира М., Ямагата Х. (2006). «Чувствительность к УФ-излучению и мутагенез чрезвычайно термофильных Eubacterium Thermus thermophilus HB27». Гены и окружающая среда. 28 (2): 56–61. Дои:10.3123 / jemsge.28.56.
- ^ Танака Т., Халика HD, Хуанг Х, Траганос Ф, Дарзинкевич З. (сентябрь 2006 г.). «Конститутивное фосфорилирование гистона H2AX и активация ATM, репортеры повреждения ДНК эндогенными оксидантами». Клеточный цикл. 5 (17): 1940–45. Дои:10.4161 / cc.5.17.3191. ЧВК 3488278. PMID 16940754.
- ^ Брейг М., Шмитт CA (март 2006 г.). «Онкоген-индуцированное старение: тормозит развитие опухоли». Исследования рака. 66 (6): 2881–84. Дои:10.1158 / 0008-5472.CAN-05-4006. PMID 16540631.
- ^ Линч, доктор медицины (февраль 2006 г.). «Как клеточное старение предотвращает рак?». ДНК и клеточная биология. 25 (2): 69–78. Дои:10.1089 / dna.2006.25.69. PMID 16460230.
- ^ Campisi J, d'Adda di Fagagna F (сентябрь 2007 г.). «Клеточное старение: когда с хорошими клетками случаются плохие вещи». Обзоры природы. Молекулярная клеточная биология. 8 (9): 729–40. Дои:10.1038 / nrm2233. PMID 17667954. S2CID 15664931.
- ^ а б c Лучший БП (июнь 2009 г.). «Повреждение ядерной ДНК как прямая причина старения» (PDF). Исследования омоложения. 12 (3): 199–208. CiteSeerX 10.1.1.318.738. Дои:10.1089 / rej.2009.0847. PMID 19594328. Архивировано из оригинал (PDF) 15 ноября 2017 г.. Получено 29 сентября 2009.
- ^ Санкар А. (июнь 2003 г.). «Структура и функция ДНК-фотолиазы и криптохромных фоторецепторов синего света». Химические обзоры. 103 (6): 2203–37. Дои:10.1021 / cr0204348. PMID 12797829.
- ^ Лукас-Льедо Дж. И., Линч М. (май 2009 г.). «Эволюция частоты мутаций: филогеномный анализ семейства фотолиазы / криптохрома». Молекулярная биология и эволюция. 26 (5): 1143–53. Дои:10.1093 / molbev / msp029. ЧВК 2668831. PMID 19228922.
- ^ а б c Уотсон Дж. Д., Бейкер Т. А., Белл С. П., Ганн А., Левин М., Лосик Р. (2004). Молекулярная биология гена (5-е изд.). Пирсон Бенджамин Каммингс; CSHL Press. Гл. 9, 10. OCLC 936762772.
- ^ Фолькерт MR (1988). «Адаптивный ответ Escherichia coli на повреждение алкилирования». Экологический и молекулярный мутагенез. 11 (2): 241–55. Дои:10.1002 / em.2850110210. PMID 3278898. S2CID 24722637.
- ^ а б c Уилли Дж, Шервуд Л., Вулвертон С. (2014). Микробиология Прескотта. Нью-Йорк: Макгроу Хилл. п. 381. ISBN 978-0-07-3402-40-6.
- ^ Рассел П. (2018). я генетика. Ченнаи: Пирсон. п. 186. ISBN 978-93-325-7162-4.
- ^ а б c d Рирдон Дж. Т., Санкар А. (2006). «Очистка и характеристика Escherichia coli и систем ферментов репарации эксцизионных нуклеотидов человека». Методы в энзимологии. 408: 189–213. Дои:10.1016 / S0076-6879 (06) 08012-8. ISBN 9780121828134. PMID 16793370.
- ^ Берг М., Тимочко Дж., Страйер Л. (2012). Биохимия 7-е издание. Нью-Йорк: W.H. Фримен и компания. п. 840. ISBN 9781429229364.
- ^ Лян Л., Дэн Л., Чен И., Ли Г.К., Шао С., Тишфилд Дж. А. (сентябрь 2005 г.). «Модуляция присоединения концов ДНК ядерными белками». Журнал биологической химии. 280 (36): 31442–49. Дои:10.1074 / jbc.M503776200. PMID 16012167.
- ^ а б Чыонг Л.Н., Ли И, Ши Л.З., Хванг ПЙ, Хе Дж, Ван Х и др. (Май 2013). «Опосредованное микрогомологией соединение концов и гомологичная рекомбинация разделяют начальный этап резекции концов для восстановления двухцепочечных разрывов ДНК в клетках млекопитающих». Труды Национальной академии наук Соединенных Штатов Америки. 110 (19): 7720–25. Bibcode:2013ПНАС..110.7720Т. Дои:10.1073 / pnas.1213431110. ЧВК 3651503. PMID 23610439.
- ^ Wilson TE, Grawunder U, Lieber MR (июль 1997 г.). «Дрожжевая ДНК-лигаза IV опосредует негомологичное соединение концов ДНК». Природа. 388 (6641): 495–98. Bibcode:1997 Натур.388..495Вт. Дои:10.1038/41365. PMID 9242411. S2CID 4422938.
- ^ Мур Дж. К., Хабер Дж. Э. (май 1996 г.). «Клеточный цикл и генетические потребности двух путей негомологичного репарации с присоединением концов двухцепочечных разрывов у Saccharomyces cerevisiae». Молекулярная и клеточная биология. 16 (5): 2164–73. Дои:10.1128 / mcb.16.5.2164. ЧВК 231204. PMID 8628283.
- ^ Бултон С.Дж., Джексон С.П. (сентябрь 1996 г.). «Saccharomyces cerevisiae Ku70 усиливает репарацию незаконных двухцепочечных разрывов ДНК и служит барьером для путей репарации ДНК, подверженных ошибкам». Журнал EMBO. 15 (18): 5093–103. Дои:10.1002 / j.1460-2075.1996.tb00890.x. ЧВК 452249. PMID 8890183.
- ^ Уилсон Т.Э., Либер М.Р. (август 1999 г.). «Эффективная обработка концов ДНК во время соединения негомологичных концов у дрожжей. Доказательства пути, зависимого от ДНК-полимеразы бета (Pol4)». Журнал биологической химии. 274 (33): 23599–609. Дои:10.1074 / jbc.274.33.23599. PMID 10438542.
- ^ Будман Дж., Чу Дж. (Февраль 2005 г.). «Обработка ДНК для негомологичного соединения концов бесклеточным экстрактом». Журнал EMBO. 24 (4): 849–60. Дои:10.1038 / sj.emboj.7600563. ЧВК 549622. PMID 15692565.
- ^ Ван Х, Перро А. Р., Такеда Й, Цинь В., Ван Х, Илиакис Дж. (Сентябрь 2003 г.). «Биохимические доказательства Ku-независимых резервных путей NHEJ». Исследования нуклеиновых кислот. 31 (18): 5377–88. Дои:10.1093 / нар / gkg728. ЧВК 203313. PMID 12954774.
- ^ Юнг Д., Альт Ф. В. (январь 2004 г.). «Раскрытие рекомбинации V (D) J; понимание регуляции генов». Клетка. 116 (2): 299–311. Дои:10.1016 / S0092-8674 (04) 00039-X. PMID 14744439. S2CID 16890458.
- ^ Шарма С., Джавадекар С.М., Пандей М., Шривастава М., Кумари Р., Рагхаван С.К. (март 2015 г.). «Гомология и ферментативные требования к альтернативному соединению концов в зависимости от микрогомологии». Смерть и болезнь клеток. 6 (3): e1697. Дои:10.1038 / cddis.2015.58. ЧВК 4385936. PMID 25789972.
- ^ Декоттиньи А (2013). «Альтернативные механизмы соединения концов: историческая перспектива». Границы генетики. 4: 48. Дои:10.3389 / fgene.2013.00048. ЧВК 3613618. PMID 23565119.
- ^ Zahradka K, Slade D, Bailone A, Sommer S, Averbeck D, Petranovic M и др. (Октябрь 2006 г.). «Повторная сборка разрушенных хромосом у Deinococcus radiodurans». Природа. 443 (7111): 569–73. Bibcode:2006Натура.443..569Z. Дои:10.1038 / природа05160. PMID 17006450. S2CID 4412830.
- ^ Waters LS, Minesinger BK, Wiltrout ME, D'Souza S, Woodruff RV, Walker GC (март 2009 г.). «Эукариотические транслезионные полимеразы, их роль и регуляция в толерантности к повреждению ДНК». Обзоры микробиологии и молекулярной биологии. 73 (1): 134–54. Дои:10.1128 / MMBR.00034-08. ЧВК 2650891. PMID 19258535.
- ^ Colis LC, Raychaudhury P, Basu AK (август 2008 г.). «Мутационная специфичность индуцированных гамма-излучением гуанин-тимина и тимин-гуанина внутрицепочечных сшивок в клетках млекопитающих и трансфузионный синтез за пределы гуанин-тиминового поражения ДНК-полимеразой человека эта». Биохимия. 47 (31): 8070–79. Дои:10.1021 / bi800529f. ЧВК 2646719. PMID 18616294.
- ^ Райчаудхури П., Басу А.К. (март 2011 г.). «Генетическая потребность в мутагенезе поперечной сшивки G [8,5-Me] T в Escherichia coli: ДНК-полимеразы IV и V конкурируют за способный к ошибкам обходной путь». Биохимия. 50 (12): 2330–38. Дои:10.1021 / bi102064z. ЧВК 3062377. PMID 21302943.
- ^ «Транслезионный синтез». Research.chem.psu.edu. Архивировано из оригинал 10 марта 2012 г.. Получено 14 августа 2012.
- ^ Ван Зи (июль 2001 г.). «Транслейсионный синтез семейством ДНК-полимераз UmuC». Мутационные исследования. 486 (2): 59–70. Дои:10.1016 / S0921-8777 (01) 00089-1. PMID 11425512.
- ^ а б c Friedberg EC, Walker GC, Siede W, Wood RD, Schultz RA, Ellenberger T. (2006). Ремонт ДНК и мутагенез, часть 3. ASM Press. 2-е изд.
- ^ Лю Б., Ип РК, Чжоу З. (ноябрь 2012 г.). «Ремоделирование хроматина, восстановление повреждений ДНК и старение». Текущая геномика. 13 (7): 533–47. Дои:10.2174/138920212803251373. ЧВК 3468886. PMID 23633913.
- ^ Halicka HD, Zhao H, Podhorecka M, Traganos F, Darzynkiewicz Z (июль 2009 г.). «Цитометрическое определение релаксации хроматина, ранний репортер ответа на повреждение ДНК». Клеточный цикл. 8 (14): 2233–37. Дои:10.4161 / cc.8.14.8984. ЧВК 3856216. PMID 19502789.
- ^ а б c Sellou H, Lebeaupin T, Chapuis C., Smith R, Hegele A, Singh HR, et al. (Декабрь 2016 г.). «Поли (АДФ-рибоза) -зависимый ремоделер хроматина Alc1 индуцирует локальную релаксацию хроматина при повреждении ДНК». Молекулярная биология клетки. 27 (24): 3791–99. Дои:10.1091 / mbc.E16-05-0269. ЧВК 5170603. PMID 27733626.
- ^ а б Ван Метер М., Саймон М., Томблайн Дж., Мэй А., Морелло Т.Д., Хаббард Б.П. и др. (Сентябрь 2016 г.). «JNK фосфорилирует SIRT6, чтобы стимулировать репарацию двухцепочечных разрывов ДНК в ответ на окислительный стресс, привлекая PARP1 к разрывам ДНК». Отчеты по ячейкам. 16 (10): 2641–50. Дои:10.1016 / j.celrep.2016.08.006. ЧВК 5089070. PMID 27568560.
- ^ а б Haince JF, McDonald D, Rodrigue A, Déry U, Masson JY, Hendzel MJ, Poirier GG (январь 2008 г.). «PARP1-зависимая кинетика рекрутирования белков MRE11 и NBS1 на множественные участки повреждения ДНК». Журнал биологической химии. 283 (2): 1197–208. Дои:10.1074 / jbc.M706734200. PMID 18025084.
- ^ а б c Rogakou EP, Pilch DR, Orr AH, Иванова VS, Боннер WM (март 1998 г.). «Двухцепочечные разрывы ДНК индуцируют фосфорилирование гистона H2AX по серину 139». Журнал биологической химии. 273 (10): 5858–68. Дои:10.1074 / jbc.273.10.5858. PMID 9488723.
- ^ Mailand N, Bekker-Jensen S, Faustrup H, Melander F, Bartek J, Lukas C, Lukas J (ноябрь 2007 г.). «RNF8 убиквитилирует гистоны в двухцепочечных разрывах ДНК и способствует сборке белков репарации». Клетка. 131 (5): 887–900. Дои:10.1016 / j.cell.2007.09.040. PMID 18001824. S2CID 14232192.
- ^ Luijsterburg MS, Acs K, Ackermann L, Wiegant WW, Bekker-Jensen S, Larsen DH и др. (Май 2012 г.). «Новая некаталитическая роль убиквитинлигазы RNF8 в раскрытии структуры хроматина более высокого порядка». Журнал EMBO. 31 (11): 2511–27. Дои:10.1038 / emboj.2012.104. ЧВК 3365417. PMID 22531782.
- ^ а б Luijsterburg MS, Goedhart J, Moser J, Kool H, Geverts B, Houtsmuller AB и др. (Август 2007 г.). «Динамическое взаимодействие in vivo убиквитинлигазы DDB2 E3 с поврежденной УФ-излучением ДНК не зависит от белка распознавания повреждений XPC». Журнал клеточной науки. 120 (Pt 15): 2706–16. Дои:10.1242 / jcs.008367. PMID 17635991.
- ^ а б Pines A, Vrouwe MG, Marteijn JA, Typas D, Luijsterburg MS, Cansoy M и др. (Октябрь 2012 г.). «PARP1 способствует эксцизионной репарации нуклеотидов за счет стабилизации DDB2 и привлечения ALC1». Журнал клеточной биологии. 199 (2): 235–49. Дои:10.1083 / jcb.201112132. ЧВК 3471223. PMID 23045548.
- ^ Джазайери А., Фальк Дж., Лукас С., Бартек Дж., Смит Г.К., Лукас Дж., Джексон С.П. (январь 2006 г.). «ATM- и зависимая от клеточного цикла регуляция ATR в ответ на двухцепочечные разрывы ДНК». Природа клеточной биологии. 8 (1): 37–45. Дои:10.1038 / ncb1337. PMID 16327781. S2CID 9797133.
- ^ Баккенист CJ, Кастан МБ (январь 2003 г.). «Повреждение ДНК активирует АТМ посредством межмолекулярного аутофосфорилирования и диссоциации димеров». Природа. 421 (6922): 499–506. Bibcode:2003Натура.421..499Б. Дои:10.1038 / природа01368. PMID 12556884. S2CID 4403303.
- ^ Вэй Кью, Ли Л., Чен Д. (2007). Ремонт ДНК, генетическая нестабильность и рак. World Scientific. ISBN 978-981-270-014-8.[страница нужна ]
- ^ Шонталь AH (2004). Контрольно-пропускные пункты и рак. Humana Press. ISBN 978-1-58829-500-2.[страница нужна ]
- ^ Гартель А.Л., Тайнер А.Л. (июнь 2002 г.). «Роль ингибитора циклин-зависимой киназы p21 в апоптозе». Молекулярная терапия рака. 1 (8): 639–49. PMID 12479224.
- ^ Янион С (2001). «Некоторые аспекты системы экстренного реагирования - критический обзор». Acta Biochimica Polonica. 48 (3): 599–610. Дои:10.18388 / abp.2001_3894. PMID 11833768.
- ^ а б Эрилл I, Кампой С., Барбе Дж. (Ноябрь 2007 г.). «Эоны бедствий: эволюционная перспектива бактериального SOS-ответа». Обзоры микробиологии FEMS. 31 (6): 637–56. Дои:10.1111 / j.1574-6976.2007.00082.x. PMID 17883408.
- ^ Schlacher K, Pham P, Cox MM, Goodman MF (февраль 2006 г.). «Роль ДНК-полимеразы V и белка RecA в мутации, вызванной повреждением SOS». Химические обзоры. 106 (2): 406–19. Дои:10.1021 / cr0404951. PMID 16464012.
- ^ Фрай Р.К., Бегли Т.Дж., Самсон Л.Д. (2004). «Общегеномные ответы на агентов, повреждающих ДНК». Ежегодный обзор микробиологии. 59: 357–77. Дои:10.1146 / annurev.micro.59.031805.133658. PMID 16153173.
- ^ Эспехель С., Мартин М., Клатт П., Мартин-Кабальеро Дж., Флорес Дж. М., Бласко М. А. (май 2004 г.). «Более короткие теломеры, ускоренное старение и увеличение лимфомы у мышей с дефицитом ДНК-PKcs». Отчеты EMBO. 5 (5): 503–09. Дои:10.1038 / sj.embor.7400127. ЧВК 1299048. PMID 15105825.
- ^ де Бур Дж., Андрессоо Дж. О., де Вит Дж., Хейманс Дж., Бимс Р. Б., ван Стиг Х. и др. (Май 2002 г.). «Преждевременное старение у мышей с дефицитом репарации ДНК и транскрипции». Наука. 296 (5571): 1276–79. Bibcode:2002Научный ... 296.1276D. Дои:10.1126 / science.1070174. PMID 11950998. S2CID 41930529.
- ^ Dollé ME, Busuttil RA, Garcia AM, Wijnhoven S, van Drunen E, Niedernhofer LJ, et al. (Апрель 2006 г.). «Повышенная нестабильность генома не является предпосылкой для сокращения продолжительности жизни мышей с дефицитом репарации ДНК». Мутационные исследования. 596 (1–2): 22–35. Дои:10.1016 / j.mrfmmm.2005.11.008. PMID 16472827.
- ^ Кобаяши Ю., Наруми И., Сато К., Фунаяма Т., Кикучи М., Китайма С., Ватанабэ Х. (ноябрь 2004 г.). «Механизмы радиационного ответа чрезвычайно радиорезистентной бактерии Deinococcus radiodurans». Учу Сэйбуцу Кагаку. 18 (3): 134–35. PMID 15858357.
- ^ Spindler SR (сентябрь 2005 г.). «Быстрая и обратимая индукция долголетия, противораковые и геномные эффекты ограничения калорийности». Механизмы старения и развития. 126 (9): 960–66. Дои:10.1016 / j.mad.2005.03.016. PMID 15927235. S2CID 7067036.
- ^ Halicka HD, Zhao H, Li J, Lee YS, Hsieh TC, Wu JM, Darzynkiewicz Z (декабрь 2012 г.). «Потенциальные антивозрастные агенты подавляют уровень конститутивной передачи сигналов mTOR- и повреждений ДНК». Старение. 4 (12): 952–65. Дои:10.18632 / старение.100521. ЧВК 3615161. PMID 23363784.
- ^ Тиссенбаум HA, Guarente L (март 2001 г.). «Повышенная доза гена sir-2 продлевает продолжительность жизни Caenorhabditis elegans». Природа. 410 (6825): 227–30. Bibcode:2001Натура.410..227Т. Дои:10.1038/35065638. PMID 11242085. S2CID 4356885.
- ^ Коэн Х.Й., Миллер С., Биттерман К.Дж., Уолл Н.Р., Хеккинг Б., Кесслер Б. и др. (Июль 2004 г.). «Ограничение калорийности способствует выживанию клеток млекопитающих за счет индукции деацетилазы SIRT1». Наука. 305 (5682): 390–92. Bibcode:2004Наука ... 305..390C. Дои:10.1126 / science.1099196. PMID 15205477. S2CID 33503081.
- ^ Cabelof DC, Yanamadala S, Raffoul JJ, Guo Z, Soofi A, Heydari AR (март 2003 г.). «Ограничение калорийности способствует стабильности генома за счет индукции эксцизионной репарации оснований и обращения вспять его возрастного снижения». Ремонт ДНК. 2 (3): 295–307. Дои:10.1016 / S1568-7864 (02) 00219-7. PMID 12547392.
- ^ Стюарт Дж. А., Карахалил Б., Хог Б. А., Соуза-Пинто, Северная Каролина, Бор В. А. (март 2004 г.). «Ограничение калорий по-разному влияет на эксцизионную репарацию оснований митохондриальной и ядерной ДНК». Журнал FASEB. 18 (3): 595–97. Дои:10.1096 / fj.03-0890fje. PMID 14734635. S2CID 43118901.
- ^ Уокер Д.В., Макколл Дж., Дженкинс Н.Л., Харрис Дж., Литгоу Дж. Дж. (Май 2000 г.). «Эволюция продолжительности жизни C. elegans». Природа. 405 (6784): 296–97. Дои:10.1038/35012693. PMID 10830948. S2CID 4402039.
- ^ Джонсон Дж. (28 декабря 2010 г.). «Выявление доисторических опухолей и дебаты». Нью-Йорк Таймс.
Если бы мы прожили достаточно долго, рано или поздно все мы заболели бы раком.
- ^ Альбертс Б., Джонсон А., Льюис Дж. И др. (2002). «Предотвратимые причины рака». Молекулярная биология клетки (4-е изд.). Нью-Йорк: Наука Гарланд. ISBN 978-0-8153-4072-0.
Невзирая на обстоятельства, следует ожидать некоторую неснижаемую фоновую заболеваемость раком: мутаций нельзя полностью избежать, потому что они являются неизбежным следствием фундаментальных ограничений точности репликации ДНК, как обсуждалось в главе 5. Если бы человек мог жить долго Достаточно того, что по крайней мере одна из его или ее клеток неизбежно накопит набор мутаций, достаточный для развития рака.
- ^ Friedenson B (август 2007 г.). «Путь BRCA1 / 2 предотвращает гематологический рак в дополнение к раку груди и яичников». BMC Рак. 7: 152. Дои:10.1186/1471-2407-7-152. ЧВК 1959234. PMID 17683622.
- ^ Гаванде Н.С., Вандервер-Карозза П.С., Хиншоу HD, Джалал С.И., Сирс С.Р., Павелчак К.С., Турчи Дж.Дж. (апрель 2016 г.). "Таргетная терапия восстановления ДНК: прошлое или будущее лечения рака?". Фармакология и терапия. 160: 65–83. Дои:10.1016 / j.pharmthera.2016.02.003. ЧВК 4811676. PMID 26896565.
- ^ Bryant HE, Schultz N, Thomas HD, Parker KM, Flower D, Lopez E, et al. (Апрель 2005 г.). «Специфическое уничтожение BRCA2-дефицитных опухолей с помощью ингибиторов поли (АДФ-рибоза) полимеразы». Природа. 434 (7035): 913–17. Bibcode:2005Натура.434..913Б. Дои:10.1038 / природа03443. PMID 15829966. S2CID 4391043.
- ^ Гольдштейн М, Кастан МБ (2015). «Ответ на повреждение ДНК: последствия для реакции опухоли на радиацию и химиотерапию». Ежегодный обзор медицины. 66: 129–43. Дои:10.1146 / annurev-med-081313-121208. PMID 25423595.
- ^ а б Jeggo PA, Pearl LH, Carr AM (январь 2016 г.). «Восстановление ДНК, стабильность генома и рак: историческая перспектива» (PDF). Обзоры природы. Рак. 16 (1): 35–42. Дои:10.1038 / nrc.2015.4. PMID 26667849. S2CID 14941857.
- ^ Барткова Дж., Хорейси З., Коед К., Кремер А., Торт Ф., Зигер К. и др. (Апрель 2005 г.). «Ответ на повреждение ДНК как кандидат противоракового барьера в раннем онкогенезе человека». Природа. 434 (7035): 864–70. Bibcode:2005Натура.434..864Б. Дои:10.1038 / природа03482. PMID 15829956. S2CID 4398393.
- ^ а б Барткова Дж., Резаи Н., Лионтос М., Каракайдос П., Клецас Д., Исаева Н. и др. (Ноябрь 2006 г.). «Онкоген-индуцированное старение является частью барьера туморогенеза, налагаемого контрольными точками повреждения ДНК». Природа. 444 (7119): 633–37. Bibcode:2006Натура.444..633Б. Дои:10.1038 / природа05268. PMID 17136093. S2CID 4406956.
- ^ Гайяр Х., Гарсия-Муза Т, Агилера А (май 2015 г.). «Репликационный стресс и рак». Обзоры природы. Рак. 15 (5): 276–89. Дои:10.1038 / nrc3916. HDL:10261/123721. PMID 25907220. S2CID 11342123.
- ^ Halazonetis TD, Gorgoulis VG, Bartek J (март 2008 г.). «Модель индуцированного онкогеном повреждения ДНК для развития рака». Наука. 319 (5868): 1352–55. Bibcode:2008Sci ... 319.1352H. Дои:10.1126 / наука.1140735. PMID 18323444. S2CID 16426080.
- ^ де Бур Дж., Hoeijmakers JH (март 2000 г.). «Эксцизионная репарация нуклеотидов и синдромы человека» (PDF). Канцерогенез. 21 (3): 453–60. Дои:10.1093 / carcin / 21.3.453. PMID 10688865.
- ^ Брустас CG, Либерман HB (февраль 2014 г.). «Гены реакции на повреждение ДНК и развитие метастазов рака». Радиационные исследования. 181 (2): 111–30. Bibcode:2014РадР..181..111Б. Дои:10.1667 / RR13515.1. ЧВК 4064942. PMID 24397478.
- ^ Чжан П., Ван Дж., Гао В., Юань Б.З., Роджерс Дж., Рид Э. (май 2004 г.). «Экспрессия киназы CHK2 подавляется из-за метилирования промотора при немелкоклеточном раке легкого». Молекулярный рак. 3 (4): 14. Дои:10.1186/1476-4598-3-14. ЧВК 419366. PMID 15125777.
- ^ Байлин С.Б., Ohm JE (февраль 2006 г.). «Эпигенетическое молчание генов при раке - механизм ранней зависимости от онкогенного пути?». Обзоры природы. Рак. 6 (2): 107–16. Дои:10.1038 / nrc1799. PMID 16491070. S2CID 2514545.
- ^ Канвал Р., Гупта С. (апрель 2012 г.). «Эпигенетические модификации рака». Клиническая генетика. 81 (4): 303–11. Дои:10.1111 / j.1399-0004.2011.01809.x. ЧВК 3590802. PMID 22082348.
- ^ Baldassarre G, Battista S, Belletti B, Thakur S, Pentimalli F, Trapasso F и др. (Апрель 2003 г.). «Отрицательная регуляция экспрессии гена BRCA1 белками HMGA1 объясняет снижение уровней белка BRCA1 при спорадической карциноме молочной железы». Молекулярная и клеточная биология. 23 (7): 2225–38. Дои:10.1128 / MCB.23.7.2225-2238.2003. ЧВК 150734. PMID 12640109.
- ^ Хасинто Ф.В., Эстеллер М (июль 2007 г.). «Пути мутатора, вызванные эпигенетическим молчанием при раке человека». Мутагенез. 22 (4): 247–53. Дои:10.1093 / mutage / gem009. PMID 17412712.
- ^ Lahtz C, Pfeifer GP (февраль 2011 г.). «Эпигенетические изменения генов репарации ДНК при раке». Журнал молекулярной клеточной биологии. 3 (1): 51–58. Дои:10.1093 / jmcb / mjq053. ЧВК 3030973. PMID 21278452. Эпигенетические изменения генов репарации ДНК при раке
- ^ Бернштейн С., Нфонсам В., Прасад А. Р., Бернштейн Н. (март 2013 г.). «Дефекты эпигенетического поля в прогрессировании рака». Всемирный журнал онкологии желудочно-кишечного тракта. 5 (3): 43–49. Дои:10.4251 / wjgo.v5.i3.43. ЧВК 3648662. PMID 23671730.
- ^ Нараянан Л., Фритцелл Дж. А., Бейкер С. М., Лискай Р. М., Глейзер П. М. (апрель 1997 г.). «Повышенные уровни мутации во многих тканях мышей с дефицитом гена репарации несоответствия ДНК Pms2». Труды Национальной академии наук Соединенных Штатов Америки. 94 (7): 3122–27. Bibcode:1997ПНАС ... 94.3122Н. Дои:10.1073 / пнас.94.7.3122. ЧВК 20332. PMID 9096356.
- ^ Хеган Д.К., Нараянан Л., Джирик FR, Эдельманн В., Лискай Р.М., Глейзер П.М. (декабрь 2006 г.). «Различия в паттернах генетической нестабильности у мышей, лишенных генов репарации несовпадений Pms2, Mlh1, Msh2, Msh3 и Msh6». Канцерогенез. 27 (12): 2402–08. Дои:10.1093 / carcin / bgl079. ЧВК 2612936. PMID 16728433.
- ^ Тутт А.Н., ван Остром К.Т., Росс Г.М., ван Стиг Х., Эшворт А. (март 2002 г.). «Нарушение Brca2 увеличивает скорость спонтанных мутаций in vivo: синергизм с ионизирующим излучением». Отчеты EMBO. 3 (3): 255–60. Дои:10.1093 / embo-reports / kvf037. ЧВК 1084010. PMID 11850397.
- ^ Герман Дж. (Март 1969 г.). «Синдром Блума. I. Генетические и клинические наблюдения у первых двадцати семи пациентов». Американский журнал генетики человека. 21 (2): 196–227. ЧВК 1706430. PMID 5770175.
- ^ О'Хаган Х.М., Мохаммад Х.П., Бейлин С.Б. (август 2008 г.). «Двухцепочечные разрывы могут инициировать сайленсинг генов и SIRT1-зависимое начало метилирования ДНК в экзогенном промоторном островке CpG». PLOS Genetics. 4 (8): e1000155. Дои:10.1371 / journal.pgen.1000155. ЧВК 2491723. PMID 18704159.
- ^ Куоццо С., Порселлини А., Ангрисано Т., Морано А., Ли Б., Ди Пардо А. и др. (Июль 2007 г.). «Повреждение ДНК, гомологически направленная репарация и метилирование ДНК». PLOS Genetics. 3 (7): e110. Дои:10.1371 / journal.pgen.0030110. ЧВК 1913100. PMID 17616978.
- ^ Малкин Д (апрель 2011). «Синдром Ли-Фраумени». Гены и рак. 2 (4): 475–84. Дои:10.1177/1947601911413466. ЧВК 3135649. PMID 21779515.
- ^ Fearon ER (ноябрь 1997 г.). «Синдромы рака человека: ключи к разгадке происхождения и природы рака». Наука. 278 (5340): 1043–50. Bibcode:1997Sci ... 278.1043F. Дои:10.1126 / science.278.5340.1043. PMID 9353177.
- ^ Halford S, Rowan A, Sawyer E, Talbot I, Tomlinson I (июнь 2005 г.). «О (6) -метилгуанинметилтрансфераза при колоректальном раке: обнаружение мутаций, потеря экспрессии и слабая связь с переходами G: C> A: T». Кишечник. 54 (6): 797–802. Дои:10.1136 / гут.2004.059535. ЧВК 1774551. PMID 15888787.
- ^ Шен Л., Кондо Й., Роснер Г.Л., Сяо Л., Эрнандес Н.С., Вилайтонг Дж. И др. (Сентябрь 2005 г.). «Метилирование промотора MGMT и дефект поля при спорадическом колоректальном раке». Журнал Национального института рака. 97 (18): 1330–38. Дои:10.1093 / jnci / dji275. PMID 16174854.
- ^ Псофаки В., Калогера С., Цамбурас Н., Стефану Д., Цианос Е., Сефериадис К., Колиос Г. (июль 2010 г.). «Статус метилирования промотора hMLH1, MGMT и CDKN2A / p16 в колоректальных аденомах». Всемирный журнал гастроэнтерологии. 16 (28): 3553–60. Дои:10.3748 / wjg.v16.i28.3553. ЧВК 2909555. PMID 20653064.
- ^ Ли К. Х., Ли Дж. С., Нам Дж. Х., Чхве С., Ли МС, Пак С. С. и др. (Октябрь 2011 г.). «Статус метилирования промотора генов hMLH1, hMSH2 и MGMT при колоректальном раке, ассоциированном с последовательностью аденома-карцинома». Архив хирургии Лангенбека. 396 (7): 1017–26. Дои:10.1007 / s00423-011-0812-9. PMID 21706233. S2CID 8069716.
- ^ Амату А., Сарторе-Бьянки А., Моутинью С., Белотти А., Бенкардино К., Кирико Дж. И др. (Апрель 2013). «Промотор CpG-островка гиперметилирование фермента репарации ДНК MGMT предсказывает клинический ответ на дакарбазин в исследовании II фазы метастатического колоректального рака». Клинические исследования рака. 19 (8): 2265–72. Дои:10.1158 / 1078-0432.CCR-12-3518. PMID 23422094.
- ^ Мокаррам П., Замани М., Кавусипур С., Нагибалхоссаини Ф., Ираджи С., Моради Сараби М., Хоссейни С.В. (май 2013 г.). «Различные паттерны метилирования ДНК двух различных областей промотора O6-метилгуанин-ДНК-метилтрансферазы (O6-MGMT) при колоректальном раке». Отчеты по молекулярной биологии. 40 (5): 3851–57. Дои:10.1007 / s11033-012-2465-3. PMID 23271133. S2CID 18733871.
- ^ Truninger K, Menigatti M, Luz J, Russell A, Haider R, Gebbers JO и др. (Май 2005 г.). «Иммуногистохимический анализ показывает высокую частоту дефектов PMS2 при колоректальном раке». Гастроэнтерология. 128 (5): 1160–71. Дои:10.1053 / j.gastro.2005.01.056. PMID 15887099.
- ^ Валери Н., Гаспарини П., Фаббри М., Бракони С., Веронезе А., Ловат Ф. и др. (Апрель 2010 г.). «Модуляция репарации несовпадений и стабильности генома с помощью miR-155». Труды Национальной академии наук Соединенных Штатов Америки. 107 (15): 6982–87. Bibcode:2010ПНАС..107.6982В. Дои:10.1073 / pnas.1002472107. ЧВК 2872463. PMID 20351277.
- ^ Фасиста А., Нгуен Х., Льюис С., Прасад А.Р., Рэмси Л., Зейтлин Б. и др. (Апрель 2012 г.). «Недостаточная экспрессия ферментов репарации ДНК на ранней стадии развития спорадического рака толстой кишки». Целостность генома. 3 (1): 3. Дои:10.1186/2041-9414-3-3. ЧВК 3351028. PMID 22494821.
- ^ Гены восстановления ДНК человека, 15 апреля 2014 г., Онкологический центр доктора медицины Андерсона, Техасский университет
- ^ Джин Б., Робертсон К.Д. (2013). «ДНК-метилтрансферазы, восстановление повреждений ДНК и рак». Достижения экспериментальной медицины и биологии. 754: 3–29. Дои:10.1007/978-1-4419-9967-2_1. ISBN 978-1-4419-9966-5. ЧВК 3707278. PMID 22956494.
- ^ Кришнан К., Степто А.Л., Мартин Х.С., Вани С., Нонс К., Уодделл Н. и др. (Февраль 2013). «MicroRNA-182-5p нацелена на сеть генов, участвующих в репарации ДНК». РНК. 19 (2): 230–42. Дои:10.1261 / rna.034926.112. ЧВК 3543090. PMID 23249749.
- ^ Чайсаингмонгкол Дж., Попанда О, Варта Р., Дайкхофф Дж., Херпель Е, Гейзельхарт Л. и др. (Декабрь 2012 г.). «Эпигенетический скрининг генов репарации ДНК человека выявляет аберрантное метилирование промотора NEIL1 при плоскоклеточной карциноме головы и шеи». Онкоген. 31 (49): 5108–16. Дои:10.1038 / onc.2011.660. PMID 22286769.
- ^ Лян Л., Дэн Л., Чен И., Ли Г.К., Шао С., Тишфилд Дж. А. (сентябрь 2005 г.). «Модуляция присоединения концов ДНК ядерными белками». Журнал биологической химии. 280 (36): 31442–49. Дои:10.1074 / jbc.M503776200. PMID 16012167.
- ^ Сингх П., Ян М., Дай Х, Ю Д., Хуанг К., Тан В. и др. (Ноябрь 2008 г.). «Сверхэкспрессия и гипометилирование гена эндонуклеазы 1 лоскута при раке груди и других формах рака». Молекулярные исследования рака. 6 (11): 1710–17. Дои:10.1158 / 1541-7786.MCR-08-0269 (неактивно 25 октября 2020 г.). ЧВК 2948671. PMID 19010819.CS1 maint: DOI неактивен по состоянию на октябрь 2020 г. (связь)
- ^ Лам Дж. С., Селигсон Д. Б., Ю Х, Ли А., Ива М., Пантак А. Дж. И др. (Август 2006 г.). «Эндонуклеаза лоскута 1 сверхэкспрессируется при раке простаты и связана с высоким показателем Глисона». BJU International. 98 (2): 445–51. Дои:10.1111 / j.1464-410X.2006.06224.x. PMID 16879693. S2CID 22165252.
- ^ Kim JM, Sohn HY, Yoon SY, Oh JH, Yang JO, Kim JH и др. (Январь 2005 г.). «Идентификация генов, связанных с раком желудка, с использованием микроматрицы кДНК, содержащей новые метки экспрессированной последовательности, экспрессируемые в клетках рака желудка». Клинические исследования рака. 11 (2 Pt 1): 473–82. PMID 15701830.
- ^ Ван К., Се С, Чен Д. (май 2014 г.). «Эндонуклеаза лоскута 1 является многообещающим кандидатом в биомаркеры рака желудка и участвует в пролиферации клеток и апоптозе». Международный журнал молекулярной медицины. 33 (5): 1268–74. Дои:10.3892 / ijmm.2014.1682. PMID 24590400.
- ^ Краузе А, Комбаре V, Яконо I, Лакруа Б, Компаньон С, Бержерон С и др. (Июль 2005 г.). «Полногеномный анализ экспрессии генов в нейробластомах, обнаруженных с помощью массового скрининга» (PDF). Письма о раке. 225 (1): 111–20. Дои:10.1016 / j.canlet.2004.10.035. PMID 15922863.
- ^ Якобуцио-Донахью, Калифорния, Майтра А., Олсен М., Лоу А.В., ван Хик Н.Т., Рости С. и др. (Апрель 2003 г.). «Исследование глобальных паттернов экспрессии генов в аденокарциноме поджелудочной железы с использованием микрочипов кДНК». Американский журнал патологии. 162 (4): 1151–62. Дои:10.1016 / S0002-9440 (10) 63911-9. ЧВК 1851213. PMID 12651607.
- ^ Сато М., Жирар Л., Секин И., Сунага Н., Рамирес Р. Д., Камибаяси С., Минна Д. Д. (октябрь 2003 г.). «Повышенная экспрессия и отсутствие мутации гена эндонуклеазы лоскута (FEN1) при раке легких человека». Онкоген. 22 (46): 7243–46. Дои:10.1038 / sj.onc.1206977. PMID 14562054.
- ^ Би Ф.Ф., Ли Д., Ян Кью (2013). «Гипометилирование сайтов связывания фактора транскрипции ETS и усиление экспрессии PARP1 при раке эндометрия». BioMed Research International. 2013: 946268. Дои:10.1155/2013/946268. ЧВК 3666359. PMID 23762867.
- ^ Би Ф.Ф., Ли Д., Ян Ц. (февраль 2013 г.). «Гипометилирование промотора, особенно вокруг мотива, специфичного для трансформации E26, и повышенная экспрессия поли (АДФ-рибоза) полимеразы 1 при серозном раке яичников с мутацией BRCA». BMC Рак. 13: 90. Дои:10.1186/1471-2407-13-90. ЧВК 3599366. PMID 23442605.
- ^ Супек Ф., Ленер Б. (май 2015 г.). «Дифференциальная репарация несовпадений ДНК лежит в основе вариаций скорости мутаций в геноме человека». Природа. 521 (7550): 81–84. Bibcode:2015Натура.521 ... 81S. Дои:10.1038 / природа14173. ЧВК 4425546. PMID 25707793.
- ^ а б Zheng CL, Wang NJ, Chung J, Moslehi H, Sanborn JZ, Hur JS, et al. (Ноябрь 2014 г.). «Транскрипция восстанавливает репарацию ДНК гетерохроматина, определяя частоту региональных мутаций в геномах рака». Отчеты по ячейкам. 9 (4): 1228–34. Дои:10.1016 / j.celrep.2014.10.031. ЧВК 4254608. PMID 25456125.
- ^ Ли Ф, Мао Г, Тонг Д, Хуанг Дж, Гу Л, Ян В, Ли ГМ (апрель 2013 г.). «Гистоновая метка H3K36me3 регулирует репарацию ошибочного спаривания ДНК человека посредством взаимодействия с MutSα». Клетка. 153 (3): 590–600. Дои:10.1016 / j.cell.2013.03.025. ЧВК 3641580. PMID 23622243.
- ^ Супек Ф., Ленер Б. (июль 2017 г.). «Кластерные сигнатуры мутаций показывают, что подверженная ошибкам репарация ДНК нацелена на мутации активных генов». Клетка. 170 (3): 534–547.e23. Дои:10.1016 / j.cell.2017.07.003. HDL:10230/35343. PMID 28753428.
- ^ Полак П., Лоуренс М.С., Хауген Э., Столетцкий Н., Стоянов П., Турман Р.Э. и др. (Январь 2014). «Снижение плотности локальных мутаций в регуляторной ДНК раковых геномов связано с репарацией ДНК». Природа Биотехнологии. 32 (1): 71–75. Дои:10.1038 / nbt.2778. ЧВК 4116484. PMID 24336318.
- ^ Кроми Г. А., Коннелли Дж. С., Лич Д. Р. (декабрь 2001 г.). «Рекомбинация на двухцепочечных разрывах и концах ДНК: консервативные механизмы от фага к человеку». Молекулярная клетка. 8 (6): 1163–74. Дои:10.1016 / S1097-2765 (01) 00419-1. PMID 11779493.
- ^ О'Брайен П.Дж. (февраль 2006 г.). «Каталитическая неразборчивость и дивергентная эволюция ферментов репарации ДНК». Химические обзоры. 106 (2): 720–52. Дои:10.1021 / cr040481v. PMID 16464022.
- ^ Мареска Б., Шварц Дж. Х. (январь 2006 г.). «Внезапное происхождение: общий механизм эволюции, основанный на концентрации стрессового белка и быстрых изменениях окружающей среды». Анатомическая запись. Часть B, новый анатом. 289 (1): 38–46. Дои:10.1002 / ar.b.20089. PMID 16437551.
- ^ «Инструмент редактирования генов CRISPR взволновал ученых, но нервничал» Новости CBC. Автор Келли Кроу. 30 ноября 2015 года.
внешняя ссылка
| Библиотечные ресурсы о Ремонт ДНК |
 СМИ, связанные с Ремонт ДНК в Wikimedia Commons
СМИ, связанные с Ремонт ДНК в Wikimedia Commons- Лекции по восстановлению ДНК в Институте рака Розуэл-Парка
- Полный список генов восстановления ДНК человека
- 3D-структуры некоторых ферментов репарации ДНК
- Болезни восстановления ДНК человека
- Группа особого интереса по восстановлению ДНК
- Ремонт ДНК
- Повреждение ДНК и восстановление ДНК
- Сегментарная прогерия
- Восстановление повреждений ДНК; Хороший, плохой, злой

