Урацил-ДНК гликозилаза - Uracil-DNA glycosylase
Урацил-ДНК гликозилаза, также известен как UNG или UDG. Его наиболее важная функция - предотвращение мутагенеза путем удаления урацила из ДНК молекулы путем разрыва N-гликозидной связи и инициирования базисно-эксцизионная пластика (BER) путь.
Функция
Ген человека кодирует одну из нескольких гликозилаз урацил-ДНК. Использование альтернативного промотора и сплайсинг этого гена приводит к двум различным изоформам: митохондриальной UNG1 и ядерной UNG2.[5] Одной из важных функций урацил-ДНК-гликозилаз является предотвращение мутагенеза путем удаления урацила из ДНК молекулы путем разрыва N-гликозидной связи и инициирования базисно-эксцизионная пластика (BER) путь. Урацил базы происходят из цитозин дезаминирование или неправильное включение дамп остатки. После мутации мутагенная угроза урацила распространяется через все последующие Репликация ДНК шаги.[6] После распаковки несоответствие гуанин и урацил пары разделены, и ДНК-полимераза вставляет комплементарные основания с образованием пары гуанин-цитозин (GC) в одну дочернюю цепь и аденин пара -урацил (AU) в другом.[7] Половина всей ДНК потомства, полученной из мутировавшей матрицы, наследует сдвиг от GC к AU в сайте мутации.[7] UDG удаляет урацил как в парах AU, так и в GU, чтобы предотвратить распространение несоответствия оснований ниже по течению. транскрипция и перевод процессы.[7] Обладая высокой эффективностью и специфичностью, эта гликозилаза восстанавливает более 10 000 оснований, ежедневно повреждаемых в клетке человека.[8] Клетки человека экспрессируют от пяти до шести типов ДНК гликозилазы, все они имеют общий механизм выворота и вырезания оснований как средства репарации ДНК.[9]
Структура
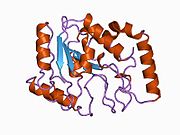
УДГ выполнен из четырехжильного параллельного β-лист в окружении восьми α-спирали.[10] В активный сайт состоит из пяти очень консервированный мотивы, которые в совокупности катализируют гликозидная связь расщепление:[11][12]
- Водоактивирующая петля: 63-QDPYH-67[12]
- Pro -богатый шлейф: 165-PPPPS-169[10]
- Мотив, связывающий урацил: 199-GVLLLN-204[10][11]
- Gly -Сер петля: 246-ГС-247[10]
- Малая канавка вставка петля: 268-HPSPLS-273[10][11]
Механизм
Расщепление гликозидной связи происходит по механизму «пинч-толкай-тяни» с использованием пяти консервативных мотивов.[10]
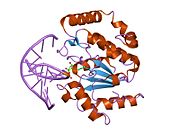
Ущипнуть: UDG сканирует ДНК на наличие урацила путем неспецифического связывания с цепью и создания акинка в основной цепи, тем самым позиционируя выбранную основу для обнаружения. Петли Pro-rich и Gly-Ser образуют полярные контакты с 3 ’и 5’ фосфатами, фланкирующими исследуемое основание.[11] Это сжатие ДНК позвоночник или «защемление» обеспечивает тесный контакт между UDG и интересующей базой.[10]
От себя: Чтобы полностью оценить идентичность нуклеотидов, петля интеркаляции проникает или проталкивается в малую бороздку ДНК и вызывает конформационные изменения, чтобы перевернуть нуклеотид из спирали.[13] Компрессия остова способствует выворачиванию теперь внеспирального нуклеотида, который позиционируется для распознавания мотивом, связывающим урацил.[10] Сочетание интеркаляции и эверсии помогает компенсировать нарушение благоприятных взаимодействий стэкинга оснований внутри спирали ДНК. Лея 272 заполняет пустоту, оставленную перевернутым нуклеотидом, чтобы создать дисперсионные взаимодействия с соседними основаниями и восстановить стабильность стэкинга.[11]
Вытащить: Теперь доступный для активного сайта нуклеотид взаимодействует с мотивом связывания урацила. Форма активного сайта дополняет вывернутую структуру урацила, что обеспечивает высокую субстратную специфичность. Пурины слишком велики, чтобы поместиться в активном центре, в то время как неблагоприятные взаимодействия с другими пиримидинами препятствуют связыванию альтернативных субстратов.[9] Боковая цепь Тюр 147 стерически мешает тимин C5 метильная группа, а конкретный водородная связь между урацилом O2 карбонил и Gln 144 дискриминирует цитозиновый субстрат, в котором отсутствует необходимый карбонил.[9] После распознавания урацила расщепление гликозидной связи происходит в соответствии с механизмом, описанным ниже.



Положение остатков, активирующих воду нуклеофил и протонировать урацил уходящая группа широко обсуждаются, хотя наиболее часто применяемый механизм использует цикл активации воды, подробно описанный в структуре фермента.[12][14] Независимо от должности, личности аспарагиновая кислота и гистидин остатки согласуются в ходе каталитических исследований.[10][11][12][14][15]
Лабораторное использование
Урацил N-гликозилаза (UNG) - это фермент, который используется в мощном методе устранения уноса полимеразной цепной реакции (ПЦР) продуктов в ПЦР в реальном времени. Этот метод модифицирует продукты ПЦР таким образом, что в новой реакции любые остаточные продукты от предыдущих амплификаций ПЦР будут расщеплены и предотвращены от амплификации, но истинные матрицы ДНК не будут затронуты.[16] ПЦР синтезирует обильные продукты амплификации каждый цикл, но загрязнение последующих циклов ПЦР следовыми количествами этих продуктов, называемое переходящим загрязнением, дает ложноположительные результаты. Переносное загрязнение из некоторых предыдущих ПЦР может быть значительной проблемой как из-за обилия продуктов ПЦР, так и из-за идеальной структуры загрязняющего материала для повторной амплификации. Однако переносимое загрязнение можно контролировать с помощью следующих двух этапов: (i) включение dUTP во все продукты ПЦР (путем замены dUTP на dTTP или путем включения урацила во время синтеза праймеров; и (ii) обработки всех последующих полностью предварительно собранных стартовых реакций с урацил-ДНК-гликозилазой (UDG) с последующей термической инактивацией UDG. UDG отщепляет урациловое основание от фосфодиэфирного остова урацилсодержащей ДНК, но не влияет на природную (т. е. содержащую тимин) ДНК. В результате блокируются апиримидиновые сайты репликации ДНК-полимеразами и очень лабильны к кислотному / основному гидролизу.Поскольку UDG не реагирует с dTTP, а также инактивируется тепловой денатурацией перед фактической ПЦР, переносимое загрязнение ПЦР можно эффективно контролировать, если примеси содержат урацилы вместо тиминов.[6]
Урацил N-гликозилаза также использовалась в исследовании для выявления свидетельств продолжающейся низкой метаболической активности и Ремонт ДНК у древних бактерий.[17] Долгосрочное выживание бактерий может происходить либо через эндоспора образование (при котором бактерия входит в состояние полного покоя, при этом никакая метаболическая активность не происходит, и, таким образом, не происходит репарация ДНК), или же посредством снижения метаболической активности до очень низкой скорости, достаточной только для продолжения репарации ДНК и предотвратить истощение других нестабильных молекул (таких как АТФ ), при котором микроб способен восстанавливать поврежденную ДНК, но при этом продолжает медленно потреблять питательные вещества.[17] Последовательности ДНК бактерий в вечная мерзлота были амплифицированы с помощью ПЦР. В одной серии прогонов амплифицировались последовательности ДНК как есть (для обнаружения всей живой бактериальной ДНК в образцах), в то время как в другой серии проводился поиск ДНК, которая подвергалась продолжающемуся восстановлению; Для этого ДНК обрабатывали УНГ для удаления урацилов. Это предотвратило амплификацию нерепарированной ДНК двумя способами: во-первых, базовые сайты образовавшиеся в результате удаления урацилов предотвращали прохождение ДНК-полимеразы, используемой в ПЦР, мимо места повреждения, в то время как эти базовые сайты также непосредственно ослабляли ДНК и повышали вероятность ее фрагментирования при нагревании.[17] Таким образом, исследователи смогли продемонстрировать доказательства продолжающегося восстановления ДНК в высокий GC Грамположительные бактерии до 600000 лет.[17]
Урацил-N-гликозилаза также использовалась в способе клонирования амплифицированных с помощью ПЦР фрагментов ДНК. В этом методе праймеры, используемые в ПЦР, синтезируются с остатками урацила вместо тимина. Когда эти праймеры включаются в фрагменты, амплифицированные ПЦР, последовательность праймера становится восприимчивой к расщеплению урацил-N-гликозилазой и дает 3'-выступающие концы, которые можно отжигать с соответствующим образом приготовленной векторной ДНК. Образовавшиеся химерные молекулы можно с высокой эффективностью трансформировать в компетентные клетки без необходимости лигирования in vitro.[18]
Взаимодействия
Было показано, что урацил-ДНК-гликозилаза взаимодействовать с участием RPA2.[19]
использованная литература
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000076248 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000029591 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ «Энтрез Ген: урацил-ДНК гликозилаза UNG». Ncbi.nlm.nih.gov. Получено 29 декабря 2017.
- ^ а б Лонго М.С., Бернингер М.С., Хартли Д.Л. (сентябрь 1990 г.). «Использование урацил ДНК-гликозилазы для контроля переходящего загрязнения в полимеразных цепных реакциях». Ген. 93 (1): 125–8. Дои:10.1016 / 0378-1119 (90) 90145-Н. PMID 2227421.
- ^ а б c Pearl LH (август 2000 г.). «Структура и функция в суперсемействе урацил-ДНК-гликозилазы». Мутационные исследования. 460 (3–4): 165–81. Дои:10.1016 / S0921-8777 (00) 00025-2. PMID 10946227.
- ^ Slupphaug G, Mol CD, Kavli B, Arvai AS, Krokan HE, Tainer JA (ноябрь 1996 г.). «Механизм переворота нуклеотидов из структуры человеческой урацил-ДНК-гликозилазы, связанной с ДНК». Природа. 384 (6604): 87–92. Bibcode:1996Натура 384 ... 87С. Дои:10.1038 / 384087a0. PMID 8900285. S2CID 4310250.
- ^ а б c Lindahl T (апрель 2000 г.). «Подавление спонтанного мутагенеза в клетках человека путем эксцизионного восстановления оснований ДНК». Мутационные исследования. 462 (2–3): 129–35. Дои:10.1016 / S1383-5742 (00) 00024-7. PMID 10767624.
- ^ а б c d е ж г час я Парих С.С., Putnam CD, Тайнер Дж. А. (август 2000 г.). «Уроки, извлеченные из структурных результатов по урацил-ДНК-гликозилазе». Мутационные исследования. 460 (3–4): 183–99. Дои:10.1016 / S0921-8777 (00) 00026-4. PMID 10946228.
- ^ а б c d е ж Жарков Д.О., Мечетин Г.В., Невинский Г.А. (март 2010 г.). «Урацил-ДНК-гликозилаза: структурные, термодинамические и кинетические аспекты поиска и распознавания повреждений». Мутационные исследования. 685 (1–2): 11–20. Дои:10.1016 / j.mrfmmm.2009.10.017. ЧВК 3000906. PMID 19909758.
- ^ а б c d Ачарья Н., Кумар П., Варшней У. (июль 2003 г.). «Комплексы белка-ингибитора урацил-ДНК-гликозилазы, Ugi, с урацил-ДНК-гликозилазами Mycobacterium smegmatis и Mycobacterium tuberculosis». Микробиология. 149 (Pt 7): 1647–58. Дои:10.1099 / мик. 0.26228-0. PMID 12855717.
- ^ Mol CD, Arvai AS, Slupphaug G, Kavli B, Alseth I, Krokan HE, Tainer JA (март 1995 г.). «Кристаллическая структура и мутационный анализ урацил-ДНК-гликозилазы человека: структурные основы специфичности и катализа». Ячейка. 80 (6): 869–78. Дои:10.1016/0092-8674(95)90290-2. PMID 7697717. S2CID 14851787.
- ^ а б Шорманн Н., Григорян А., Самал А., Кришнан Р., ДеЛукас Л., Чаттопадхьяй Д. (2007). «Кристаллическая структура урацил-ДНК-гликозилазы вируса осповакцины выявляет димерную сборку». BMC Структурная биология. 7: 45. Дои:10.1186/1472-6807-7-45. ЧВК 1936997. PMID 17605817.
- ^ Савва Р., Маколи-Хехт К., Браун Т., Жемчуг Л. (февраль 1995 г.). «Структурные основы специфической эксцизионной репарации оснований с помощью урацил-ДНК-гликозилазы». Природа. 373 (6514): 487–93. Bibcode:1995Натура.373..487С. Дои:10.1038 / 373487a0. PMID 7845459. S2CID 4315434.
- ^ «Центры поддержки - Thermo Fisher Scientific». Abcommunity.thermofisher.com. Получено 29 декабря 2017.
- ^ а б c d Джонсон СС; Hebsgaard MB; Christensen TR; Мастепанов М; Nielsen R; Мунк К; Марка Т; Gilbert MT; Zuber MT; Bunce M; Rønn R; Гиличинский Д; Froese D; Виллерслев Э. (сентябрь 2007 г.). «Древние бактерии демонстрируют доказательства восстановления ДНК». PNAS. 104 (36): 14401–5. Bibcode:2007PNAS..10414401J. Дои:10.1073 / pnas.0706787104. ЧВК 1958816. PMID 17728401.
- ^ Аналитическая биохимия 1992; 206 (1): 91-7.
- ^ Нагельхус Т.А., Хауг Т., Сингх К.К., Кешав К.Ф., Скорпен Ф., Оттерлей М., Бхарати С., Линдмо Т., Бенишоу С., Бенарус Р., Крокан Х.Э. (март 1997 г.). «Последовательность в N-концевой области урацил-ДНК гликозилазы человека с гомологией XPA взаимодействует с C-концевой частью субъединицы 34 кДа репликационного белка A». Журнал биологической химии. 272 (10): 6561–6. Дои:10.1074 / jbc.272.10.6561. PMID 9045683.