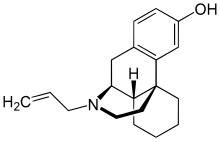
Декстраллорфан - Dextrallorphan
 | |
| Клинические данные | |
|---|---|
| Маршруты администрация | Устный |
| Код УВД |
|
| Легальное положение | |
| Легальное положение |
|
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| ChemSpider | |
| Химические и физические данные | |
| Формула | C19ЧАС25NО |
| Молярная масса | 283.415 г · моль−1 |
| 3D модель (JSmol ) | |
| |
Декстраллорфан (DXA) является опиоидным производным химического морфинан класс, который используется в научное исследование. Он действует как σ1 рецептор агонист и Рецептор NMDA антагонист.[1][2][3][4] Не имеет существенного близость для σ2, μ-опиоид, или же δ-опиоидный рецептор, или для серотонин или же переносчик норэпинефрина.[2][5]Как антагонист рецепторов NMDA, in vivo, это примерно вдвое больше мощный в качестве декстрометорфан, и в пять раз менее мощный, чем декстрорфан.[3]
Использование в научных исследованиях
Маскировка рецептора сигма-1
Декстраллорфан часто используется в исследованиях для блокировки σ1 рецептор сайты так что σ2 рецептор сайты (которые еще не были клонированы[когда? ]) можно изучить.[6][7][8] Было высказано предположение, что оба этих сигма (σ) рецептора были опиоидными рецепторами из-за их сродства к психоактивным препаратам. Однако теперь стало понятно, что это неопиоидные рецепторы, которые связываются с некоторыми психоактивными препаратами, такими как декстраллорфан.[9] Один из примеров использования декстраллорфана для маскировки σ1 рецептор сайтов было замечено в исследовании по локализации σ2 рецептор в устойчивых к детергентам доменах липидных рафтов.[6] Он также использовался для маскировки σ1 рецептор сайты так что σ2 рецептор характеристики связывания в печени крысы могут быть определены путем маркировки σ2 рецептор сайты с [3H] 1,3-ди-о-толилгуанидин (DTG) в присутствии 1 мкМ раствора декстраллорфана.[8]
Исследования на животных
Декстраллорфан использовали на крысах Spraque-Dawley для изучения электрофизических ответов нейронов Пуркинье мозжечка на лекарство, когда он применялся ионтофоретически в качестве лиганда сигма (σ) рецептора. Декстраллорфан увеличивал частоту возбуждения на 14%, предполагая, что сигма (σ) лиганды (например, декстраллорфан) изменяют спонтанное возбуждение нейронов Пуркинье и вызывают двигательные эффекты.[10]
В другом исследовании было обнаружено, что декстраллорфан, наряду с другими производными опиоидов, является мощным ингибитором недоступных для эторфина (EI) участков в мозге морской свинки. Декстраллорфан входил в тройку самых сильных ингибиторов опиоидов из исследованных, с концентрацией 67 нМ, необходимой для 50% ингибирования.[1]
История
Эта секция слишком полагается на Рекомендации к основные источники. (Декабрь 2014 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
В 1955 году декстраллорфан был использован для изучения ингибирования холинэстеразы и изучения взаимосвязи между анальгетиками и метаболизмом ацетилхолина.[11]Было обнаружено, что декстраллорфан ингибирует 25% холинэстеразы эритроцитов крупного рогатого скота в дозе 10−3 моль / литр, что соответствует концентрации до 0,2 мг / кг в кишечнике собаки. Однако в этой дозе препарат не оказал влияния на тонус кишечника. Декстраллорфан был классифицирован как мощный ингибитор холинэстеразы кишечника и эритроцитов на основании концентрации лекарственного средства, необходимого для ингибирования этих ферментов в препаратах холинэстеразы используемых животных систем. Одновременно с этим декстраллорфан не оказывал анальгезии и не изменял тонус кишечника. С этими результатами декстраллорфан помог доказать отсутствие корреляции между ингибированием систем холинэстеразы и анальгетическим или кишечным действием.[12]
В 1979 году было обнаружено, что декстраллорфан имеет половину максимальной ингибирующей концентрации (IC50) для связывания с рецепторами гипофиза и головного мозга 10 000 ± 1000 нМ и 10 000 ± 1500 нМ соответственно. В то время как его стереоизомер, леваллорфан, имел в 10 000 раз более мощную дозу, что доказывает, что связывание с этими рецепторами является стереоспецифическим.[13]
Смотрите также
Рекомендации
- ^ а б Су ТП (ноябрь 1982 г.). «Доказательства сигма-опиоидного рецептора: связывание [3H] SKF-10047 с недоступными для эторфина участками мозга морской свинки» (PDF). Журнал фармакологии и экспериментальной терапии. 223 (2): 284–90. PMID 6290634.
- ^ а б Кодд Е.Е., Шанк Р.П., Щупский Дж.Дж., Раффа РБ (сентябрь 1995 г.). «Активность анальгетиков центрального действия, ингибирующая захват серотонина и норэпинефрина: структурные детерминанты и роль в антиноцицепции» (PDF). Журнал фармакологии и экспериментальной терапии. 274 (3): 1263–70. PMID 7562497.
- ^ а б Шукла В.К., Lemaire S (январь 1997 г.). «Антагонистическая активность N-метил-D-аспартата альфа- и бета-сульфаллорфанов» (PDF). Журнал фармакологии и экспериментальной терапии. 280 (1): 357–65. PMID 8996216.
- ^ Шеннон HE (апрель 1983 г.). «Фармакологическая оценка N-аллинорметазоцина (SKF 10 047) на основе его свойств различительного стимула у крыс». Журнал фармакологии и экспериментальной терапии. 225 (1): 144–52. PMID 6834266.
- ^ He XS, Bowen WD, Lee KS, Williams W, Weinberger DR, de Costa BR (март 1993). «Синтез и характеристики связывания потенциальных агентов визуализации SPECT для сайтов связывания сигма-1 и сигма-2». Журнал медицинской химии. 36 (5): 566–71. Дои:10.1021 / jm00057a006. PMID 8496936.
- ^ а б Гебреселасси Д., Боуэн В. Д. (июнь 2004 г.). «Сигма-2 рецепторы специфически локализованы на липидных рафтах в мембранах печени крыс». Европейский журнал фармакологии. 493 (1–3): 19–28. Дои:10.1016 / j.ejphar.2004.04.005. PMID 15189760.
- ^ Маэда Д. Ю., Уильямс В., Боуэн В. Д., Куп А. (январь 2000 г.). «Селективный аналог сигма-1 рецептора BD1008. Возможный заменитель (+) - опиоидов в анализах связывания сигма-рецептора». Письма по биоорганической и медицинской химии. 10 (1): 17–8. Дои:10.1016 / s0960-894x (99) 00590-9. PMID 10636233.
- ^ а б Торренс-Кэмпбелл К., Боуэн В.Д. (май 1996 г.). «Дифференциальная солюбилизация сигма-1 и сигма-2 рецепторов печени крысы: сохранение сайтов сигма 2 во фракциях твердых частиц». Европейский журнал фармакологии. 304 (1–3): 201–10. Дои:10.1016/0014-2999(96)00109-4. PMID 8813603.
- ^ Хаяси Т., Су Т. (октябрь 2005 г.). «Сигма-рецептор: эволюция концепции в нейропсихофармакологии». Современная нейрофармакология. 3 (4): 267–80. Дои:10.2174/157015905774322516. ЧВК 2268997. PMID 18369400.
- ^ Мартин В. Дж., Де Коста Б. Р., Уокер Дж. М. (1994). «Эффекты сигма-лигандов на нейрон Пуркинье мозжечка крысы: ионтофоретическое исследование». Бюллетень исследований мозга. 35 (4): 303–9. Дои:10.1016/0361-9230(94)90106-6. PMID 7850479.
- ^ Эйкенбург, округ Колумбия, Стикни Дж. Л. (1979). «Антихолинэстеразная активность 1-альфа-ацетилметадола: связь с брадикардией». Общая фармакология. 10 (3): 195–200. Дои:10.1016/0306-3623(79)90089-2. PMID 467958.
- ^ Молодой округ Колумбия, Плоег Р.А., Фезерстоун Р.М., Гросс ЭГ (май 1955 г.). «Взаимосвязь между центральными, периферическими и антихолинэстеразными эффектами некоторых производных морфинана» (pdf). Журнал фармакологии и экспериментальной терапии. 114 (1): 33–7. PMID 14392568.
- ^ Симантов Р., Снайдер Ш. (март 1977 г.). «Связывание опиатных рецепторов в гипофизе». Исследование мозга. 124 (1): 178–84. Дои:10.1016/0006-8993(77)90877-0. PMID 191146.
