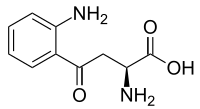
Кинуренин - Kynurenine
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК (S) -2-амино-4- (2-аминофенил) -4-оксобутановая кислота | |
| Другие имена (S) -Кинуренин | |
| Идентификаторы | |
| |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| MeSH | Кинуренин |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C10ЧАС12N2О3 | |
| Молярная масса | 208.217 г · моль−1 |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
л-Кинуренин это метаболит аминокислоты л-триптофан используется в производстве ниацин.
Кинуренин синтезируется ферментом триптофандиоксигеназой, который вырабатывается в основном, но не исключительно в печени, и индоламин-2,3-диоксигеназа, который вырабатывается во многих тканях в ответ на активацию иммунной системы.[1] Кинуренин и продукты его дальнейшего распада выполняют разнообразные биологические функции, включая расширение кровеносных сосудов во время воспаления.[2] и регулирование иммунного ответа.[3] Некоторые виды рака увеличивают выработку кинуренина, что увеличивает рост опухоли.[1]
Данные свидетельствуют о том, что повышенная выработка кинуренина может спровоцировать депрессивные симптомы, связанные с интерферон лечение для гепатит С.[4] Когнитивный дефицит в шизофрения связаны с дисбалансом ферментов, расщепляющих кинуренин.[5] Производство кинуренина увеличивается при болезни Альцгеймера[6] и сердечно-сосудистые заболевания[7] где его метаболиты связаны с когнитивным дефицитом[8] и депрессивные симптомы.[9] Кинуренин также ассоциируется с тики.[10][11]
Кинурениназа катаболизирует превращение кинуренина в антраниловая кислота[12] пока кинуренин-оксоглутарат трансаминаза катаболизирует его превращение в кинуреновая кислота. Кинуренин-3-гидроксилаза превращает кинуренин в 3-гидроксикинуренин.[13]
Дисфункция кинуренинового пути
Дисфункциональные состояния отдельных этапов кинуренинового пути (таких как кинуренин, кинуреновая кислота, хинолиновая кислота, антраниловая кислота, 3-гидроксикинуренин) были описаны для ряда заболеваний, включая:[14]
- Деменция ВИЧ
- синдром Туретта
- Тики
- Психиатрические расстройства (Такие как шизофрения, большая депрессия, тревожные расстройства )
- Рассеянный склероз
- болезнь Хантингтона
- Энцефалопатии
- Липидный обмен
- Обмен жиров в печени
- Системная красная волчанка
- Глутаровая ацидурия
- Витамин B6 недостаток
- Синдром эозинофилии-миалгии
Подавление кинуренин-3-монооксигеназа (KMO) может быть вызвано генетическим полиморфизмы, цитокины, или оба.[15][16] Дефицит KMO приводит к накоплению кинуренина и сдвигу в триптофане. метаболический путь по отношению к кинурениновой кислоте и антраниловая кислота.[17] Дефицит кинуренин-3-монооксигеназы связан с заболеваниями головного мозга (например, большое депрессивное расстройство, биполярное расстройство, шизофрения, тиковые расстройства) [18] и печени.[10][19][20][21][22]
Смотрите также
- Индолеамин 2,3-диоксигеназа (Я ДЕЛАЮ)
- Триптофан-2,3-диоксигеназа (TDO)
- N′ -Formylkynurenine
- Кинуренинский путь
Рекомендации
- ^ а б Opitz CA, Litzenburger UM, Sahm F, Ott M, Tritschler I, Trump S, Schumacher T., Jestaedt L, Schrenk D, Weller M, Jugold M, Guillemin GJ, Miller CL, Lutz C, Radlwimmer B, Lehmann I, von Deimling А, Вик В., Платтен М. (2011). «Эндогенный опухолевый лиганд человеческого арилуглеводородного рецептора». Природа. 478 (7368): 197–203. Bibcode:2011Натура.478..197O. Дои:10.1038 / природа10491. PMID 21976023.
- ^ Ван И, Лю Х., Маккензи Дж., Виттинг П.К., Сташ Дж. П., Хан М., Чангсириватханатхамронг Д., Ву Б.Дж., Болл Х.Д., Томас С.Р., Капур В., Келермайер Д.С., Меллор А.Л., Кини Дж.Ф., Хант Н.Х., Стокер Р. (2010) . «Кинуренин - это релаксирующий фактор эндотелия, вырабатываемый во время воспаления». Природа Медицина. 16 (3): 279–85. Дои:10,1038 / нм.2092. ЧВК 3556275. PMID 20190767.
- ^ Нгуен Н.Т., Кимура А., Накахама Т., Чинен И., Масуда К., Нохара К., Фуджи-Курияма Ю., Кишимото Т. (2010). «Арилуглеводородный рецептор отрицательно регулирует иммуногенность дендритных клеток посредством кинуренин-зависимого механизма». Труды Национальной академии наук. 107 (46): 19961–6. Bibcode:2010PNAS..10719961N. Дои:10.1073 / pnas.1014465107. ЧВК 2993339. PMID 21041655.
- ^ Capuron L, Neurauter G, Musselman DL, Lawson DH, Nemeroff CB, Fuchs D, Miller AH (2003). «Интерферон-альфа-индуцированные изменения метаболизма триптофана». Биологическая психиатрия. 54 (9): 906–14. Дои:10.1016 / S0006-3223 (03) 00173-2. PMID 14573318. S2CID 24079984.
- ^ Воноди И., Стайн О.К., Сатьясайкумар К.В., Робертс Р.К., Митчелл Б.Д., Хонг Л.Е., Каджии Ю., Такер Г.К., Шварц Р. (2011). «Подавление экспрессии гена кинуренин-3-монооксигеназы и ферментативной активности при шизофрении и генетической ассоциации с эндофенотипами шизофрении». Архив общей психиатрии. 68 (7): 665–74. Дои:10.1001 / archgenpsychiatry.2011.71. ЧВК 3855543. PMID 21727251.
- ^ Гиллемин Г.Дж., Брю Б.Дж., Нунан К.Э., Такикава О., Каллен К.М. (2005). «Иммунореактивность индолеамин-2,3-диоксигеназы и хинолиновой кислоты в гиппокампе при болезни Альцгеймера». Невропатология и прикладная нейробиология. 31 (4): 395–404. Дои:10.1111 / j.1365-2990.2005.00655.x. PMID 16008823.
- ^ Вирляйтнер Б., Рудзите В., Нейраутер Г., Мурр С., Калниньш Ю., Эрглис А., Трусинскис К., Фукс Д. (2003). «Иммунная активация и деградация триптофана при ишемической болезни сердца». Европейский журнал клинических исследований. 33 (7): 550–4. Дои:10.1046 / j.1365-2362.2003.01186.x. PMID 12814390.
- ^ Гуладж Э, Павлак К., Бьен Б., Павлак Д. (2010). «Кинуренин и его метаболиты у пациентов с болезнью Альцгеймера». Достижения в медицинских науках. 55 (2): 204–11. Дои:10.2478 / v10039-010-0023-6. PMID 20639188.
- ^ Swardfager W, Herrmann N, Dowlati Y, Oh PI, Kiss A, Walker SE, Lanctôt KL (2009). «Активация индолеамин-2,3-диоксигеназы и депрессивные симптомы у пациентов с ишемической болезнью сердца». Психонейроэндокринология. 34 (10): 1560–6. Дои:10.1016 / j.psyneuen.2009.05.019. PMID 19540675. S2CID 36687413.
- ^ а б Хукстра П.Дж., Андерсон Г.М., Трост П.В., Калленберг К.Г., Миндераа РБ (2007). «Плазменный кинуренин и связанные с ним меры у пациентов с тиковым расстройством». Европейская детская и подростковая психиатрия. 16: 71–7. Дои:10.1007 / s00787-007-1009-1. PMID 17665285. S2CID 39150343.
- ^ Маккрири А.С., Хэндли С.Л. (1995). «Кинуренин усиливает дрожание головы у мышей». Журнал психофармакологии. 9 (1): 69–70. Дои:10.1177/026988119500900112. PMID 22298697. S2CID 28700510.
- ^ Кинурениназа, Европейский институт биоинформатики
- ^ Сайто Ю., Хаяиши О., Ротберг С. (1957-12-01). «Исследования оксигеназ». Журнал биологической химии. 229 (2): 921–34. PMID 13502353.
- ^ Камень TW (2001). «Кинуренины в ЦНС: от эндогенной неизвестности до терапевтического значения». Прогресс в нейробиологии. 64 (2): 185–218. Дои:10.1016 / s0301-0082 (00) 00032-0. PMID 11240212. S2CID 6446144.
- ^ «Нейробиохимия» (на немецком).
- ^ Мюллер Н., Мьинт AM, Шварц MJ (2011). «Воспалительные биомаркеры и депрессия». Neurotox Res. 19 (2): 308–18. Дои:10.1007 / s12640-010-9210-2. PMID 20658274. S2CID 3225744.
- ^ Воноди И., Стайн О.К., Сатьясайкумар К.В., Робертс Р.К., Митчелл Б.Д., Хонг Л.Е., Каджии Ю., Такер Г.К., Шварц Р. (2011). «Снижение экспрессии гена кинуренин-3-монооксигеназы и активности ферментов при шизофрении и генетическая ассоциация с эндофенотипами шизофрении». Arch. Генеральная психиатрия. 68 (7): 665–74. Дои:10.1001 / archgenpsychiatry.2011.71. ЧВК 3855543. PMID 21727251.
- ^ Маркс В., МакГиннесс А.Дж., Рокс Т., Руусунен А., Клеминсон Дж., Уокер А.Дж., Гомеш-да-Коста С., Лейн М, Санчес М., Диас А.П., Ценг П.Т., Лин ПЙ, Берк М., Кларк Дж., О'Нил А. , Джака Ф., Стаббс Б., Карвалью А.Ф., Кеведо Дж., Соарес Дж.С., Фернандес Б.С. (2020). «Путь кинуренина при большом депрессивном расстройстве, биполярном расстройстве и шизофрении: метаанализ 101 исследования». Молекулярная психиатрия - через DOI: 10.1038 / s41380-020-00951-9. PMID: 33230205.CS1 maint: несколько имен: список авторов (связь)
- ^ Holtze M, Saetre P, Engberg G, Schwieler L, Werge T, Andreassen OA, Hall H, Terenius L, Agartz I, Jönsson EG, Schalling M, Erhardt S (2012). «Полиморфизмы кинуренин-3-монооксигеназы: значение для синтеза кинуреновой кислоты у пациентов с шизофренией и здоровых людей». J Psychiatry Neurosci. 37 (1): 53–7. Дои:10.1503 / jpn.100175. ЧВК 3244499. PMID 21693093.
- ^ Кэмпбелл Б.М., Чарыч Э., Ли А.В., Мёллер Т. (2014). «Кинуренины при заболевании ЦНС: регуляция воспалительными цитокинами». Front Neurosci. 8: 12. Дои:10.3389 / fnins.2014.00012. ЧВК 3915289. PMID 24567701.
- ^ Бунесс А., Рот А., Херрманн А., Шмитц О, Камп Х, Буш К., Сутер Л. (2014). «Идентификация метаболитов, маркеров клинической химии и транскриптов, связанных с гепатотоксичностью». PLOS ONE. 9 (5): e97249. Bibcode:2014PLoSO ... 997249B. Дои:10.1371 / journal.pone.0097249. ЧВК 4023975. PMID 24836604.
- ^ Хирата Ю., Кавачи Т., Сугимура Т. (1967). «Жирная печень, вызванная инъекцией L-триптофана». Биохим. Биофиз. Acta. 144 (2): 233–41. Дои:10.1016/0005-2760(67)90153-1. PMID 4168935.
