Вориностат - Vorinostat
 | |
| Клинические данные | |
|---|---|
| Произношение | /vɒˈрɪпoʊsтæт/ ворр-В-oh-stat |
| Торговые наименования | Zolinza |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a607050 |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | Устный (капсулы ) |
| Код УВД | |
| Легальное положение | |
| Легальное положение |
|
| Фармакокинетический данные | |
| Биодоступность | 1.8–11%[1] |
| Связывание с белками | ~71% |
| Метаболизм | Печеночный глюкуронизация и β-окисление CYP система не задействована |
| Метаболиты | вориностат О-глюкуронид, 4-анилино-4-оксобутановая кислота (оба неактивны)[2] |
| Устранение период полураспада | ~ 2 часа (вориностат и О-глюкуронид), 11 часов (4-анилино-4-оксобутановая кислота) |
| Экскреция | Почечный (незначительно) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.207.822 |
| Химические и физические данные | |
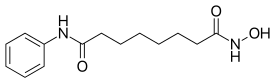
| Формула | C14ЧАС20N2О3 |
| Молярная масса | 264.325 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| | |
Вориностат (rINN )[3] также известный как суберанилогидроксамовая кислота (субероил +анилид +гидроксамовая кислота сокращенно САХА) является членом более широкого класса соединений, которые ингибируют гистоновые деацетилазы (HDAC). Ингибиторы гистон-деацетилазы (HDI) имеют широкий спектр эпигенетический виды деятельности.
Вориностат продается под названием Zolinza (/zoʊˈлɪпzə/ зох-LIN-zə ) к Merck для лечения кожных проявлений у пациентов с кожная Т-клеточная лимфома (CTCL), когда болезнь сохраняется, ухудшается или возвращается во время или после двух системных терапий.[2][4] Состав был разработан химиком из Колумбийского университета. Рональд Бреслоу и исследователь Мемориала Слоуна-Кеттеринга Пол Маркс.[5][6]
Медицинское использование
Вориностат был первым ингибитор гистондеацетилазы[7] одобрено США Управление по контролю за продуктами и лекарствами (FDA) для лечения CTCL 6 октября 2006 г.[8] Также не удалось продемонстрировать эффективность в лечении острый миелоидный лейкоз в исследовании фазы II.[9]
Механизм действия
Было показано, что вориностат связывается с активным сайтом гистоновые деацетилазы и действуют как хелатор для ионов цинка, также обнаруженных в активном центре деацетилаз гистонов.[10] Ингибирование гистон-деацетилаз вориностатом приводит к накоплению ацетилированных гистонов и ацетилированных белков, включая факторы транскрипции, имеющие решающее значение для экспрессии генов, необходимых для индукции дифференцировки клеток.[10] Он действует на I, II и IV классы гистондеацетилазы.
Клинические испытания
Вориностат также использовался для лечения Синдром Сезари, другой тип лимфомы, тесно связанный с CTCL.[11]
Недавнее исследование показало, что вориностат также обладает некоторой активностью против рецидивирующих мультиформная глиобластома, что привело к средней общей выживаемости 5,7 месяца (по сравнению с 4–4,4 месяца в более ранних исследованиях).[12] Планируются дальнейшие исследования опухолей головного мозга, в которых вориностат будет сочетаться с другими препаратами.
Включение вориностата в лечение продвинутых немелкоклеточный рак легкого (НМРЛ) показали улучшение показателей ответа и увеличение средней выживаемости без прогрессирования заболевания и общей выживаемости.[13]
Это дало обнадеживающие результаты в испытании фазы II для миелодиспластические синдромы в комбинации с идарубицин и цитарабин.[14]
Доклинические исследования
Вориностат исследуется как потенциальный ВИЧ агент, обращающий латентный период (LRA), как часть исследовательской терапевтической стратегии, известной как «шокируй и убей».[15] Было показано, что вориностат реактивирует ВИЧ у латентно ВИЧ-инфицированных. Т-клетки, обе in vitro и in vivo.[16][17]
Вориностат также показал некоторую активность против патофизиологических изменений в α1-антитрипсин дефицит[18] и кистозный фиброз.[19]Недавние данные также свидетельствуют о том, что вориностат может быть терапевтическим средством при Тип Ниманна-Пика C1 (NPC1), редкое лизосомное заболевание накопления липидов.[20]
Доклинические эксперименты, проведенные исследователями Университета Алабамы в Бирмингеме, позволяют предположить, что лекарства от рака - вориностат, белиностат и панобиностат может быть перепрофилирован для лечения инфекций, вызванных вирус папилломы человека, или ВПЧ.[21]
Смотрите также
Рекомендации
- ^ «Отчет об оценке отмены препарата Vorinostat MSD, 100 мг твердых капсул (вориностат)» (PDF). Европейское агентство по лекарственным средствам. 23 октября 2008 г. с. 9. Получено 1 сентября 2016.
- ^ а б "Золинза (вориностат) капсулы. Полная информация по назначению" (PDF). Merck & Co., Inc., Whitehouse Station, NJ 08889, США. Получено 1 сентября 2016.
- ^ «Международные непатентованные наименования фармацевтических субстанций (МНН). Рекомендуемые международные непатентованные наименования: Список 56» (PDF). Информация ВОЗ о лекарствах. 20 (3): 232. 2006. Получено 1 сентября 2016.
- ^ «ZOLINZA, подразделение Merck's Investigational Medicine for Advanced T-Cell Lymphoma (CTCL), для получения приоритетного обзора от Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США» (Пресс-релиз). Merck & Co. 7 июня 2006 г. Архивировано с оригинал 14 сентября 2006 г.. Получено 6 октября, 2006.
- ^ Ли Дж. Х., Махендран А., Яо Й, Нго Л., Вента-Перес Дж., Чой М. Л. и др. (Сентябрь 2013). «Разработка ингибитора гистондеацетилазы 6 и его биологические эффекты». Труды Национальной академии наук Соединенных Штатов Америки. 110 (39): 15704–9. Bibcode:2013ПНАС..11015704Л. Дои:10.1073 / pnas.1313893110. ЧВК 3785767. PMID 24023063.
- ^ Marks PA, Breslow R (январь 2007 г.). «От диметилсульфоксида к вориностату: разработка этого ингибитора гистондеацетилазы в качестве противоракового препарата». Природа Биотехнологии. 25 (1): 84–90. Дои:10.1038 / nbt1272. PMID 17211407.
- ^ База ингибиторов HDAC (вориностат)
- ^ «Дозирование золинзы (вориностата), показания, взаимодействия, побочные эффекты и многое другое». Ссылка на Medscape. WebMD. Получено 16 февраля 2014.
- ^ Schaefer EW, Loaiza-Bonilla A, Juckett M, DiPersio JF, Roy V, Slack J и др. (Октябрь 2009 г.). «Фаза 2 исследования вориностата при остром миелоидном лейкозе». Haematologica. 94 (10): 1375–82. Дои:10.3324 / haematol.2009.009217. ЧВК 2754953. PMID 19794082.
- ^ а б Маркс П.А., Докманович М. (декабрь 2005 г.). «Ингибиторы гистондеацетилазы: открытие и разработка в качестве противораковых агентов». Заключение эксперта по исследуемым препаратам. 14 (12): 1497–511. Дои:10.1038 / sj.bjc.6603463. ЧВК 2360770. PMID 16307490.
- ^ Кунео А. С. «Грибовидный микоз / синдром Сезари». Получено 2008-02-15.
- ^ «Вориностат проявляет противораковую активность при рецидивирующих глиомах» (Пресс-релиз). Клиника Майо. 3 июня 2007 г.. Получено 2007-06-03.
- ^ Рамалингам С.С., Мейтленд М.Л., Франкель П., Аргирис А.Е., Кочивас М., Гитлитц Б. и др. (Январь 2010 г.). «Карбоплатин и паклитаксел в комбинации с вориностатом или плацебо для терапии первой линии распространенного немелкоклеточного рака легкого». Журнал клинической онкологии. 28 (1): 56–62. Дои:10.1200 / JCO.2009.24.9094. ЧВК 2799233. PMID 19933908.
- ^ «Комбинация золинзы, идарубицина и цитарабина дает высокие показатели ответа у пациентов с МДС (ASH 2011)».
- ^ Номер клинического исследования NCT01319383 для «Влияние вориностата на экспрессию РНК ВИЧ в покоящихся CD4 + Т-клетках ВИЧ + пациентов на стабильной АРТ» на ClinicalTrials.gov
- ^ Арчин Н.М., Эспесет А., Паркер Д., Чима М., Хазуда Д., Марголис Д.М. (февраль 2009 г.). «Экспрессия латентного ВИЧ, индуцированная мощным ингибитором HDAC субероиланилид гидроксамовой кислотой». Исследования СПИДа и ретровирусы человека. 25 (2): 207–12. Дои:10.1089 / помощь.2008.0191. ЧВК 2853863. PMID 19239360.
- ^ Контрерас X, Швенекер М., Чен С.С., МакКьюн Дж.М., Дикс С.Г., Мартин Дж., Петерлин Б.М. (март 2009 г.). «Субероиланилид гидроксамовая кислота реактивирует ВИЧ из латентно инфицированных клеток». Журнал биологической химии. 284 (11): 6782–9. Дои:10.1074 / jbc.M807898200. ЧВК 2652322. PMID 19136668.
- ^ Bouchecareilh M, Hutt DM, Szajner P, Flotte TR, Balch WE (ноябрь 2012 г.). «Коррекция дефицита α1-антитрипсина, опосредованная ингибитором гистондеацетилазы (HDACi) субероиланилид гидроксамовой кислотой (SAHA)». Журнал биологической химии. 287 (45): 38265–78. Дои:10.1074 / jbc.M112.404707. ЧВК 3488095. PMID 22995909.
- ^ Хатт Д.М., Герман Д., Родригес А.П., Ноэль С., Пилевски Дж. М., Маттесон Дж. И др. (Январь 2010 г.). «Снижение активности гистондеацетилазы 7 восстанавливает функцию неправильно свернутого CFTR при муковисцидозе». Природа Химическая Биология. 6 (1): 25–33. Дои:10.1038 / nchembio.275. ЧВК 2901172. PMID 19966789.
- ^ Алам М.С., Гетц М., Халдар К. (февраль 2016 г.). «Хроническое введение ингибитора HDAC лечит как неврологическое, так и системное заболевание Ниманна-Пика типа C на мышиной модели». Научная трансляционная медицина. 8 (326): 326ra23. Дои:10.1126 / scitranslmed.aad9407. PMID 26888431.
- ^ «Лекарство от рака может помочь в лечении инфекций, вызванных вирусом папилломы человека». Получено 2018-11-30.
