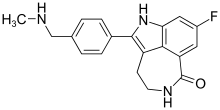
Рукапариб - Rucaparib
 | |
| Клинические данные | |
|---|---|
| Произношение | /рuˈkæпərɪб/ ру-КАП-ər-ib |
| Торговые наименования | Rubraca |
| Другие имена | AG014699 |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a617002 |
| Данные лицензии | |
| Беременность категория |
|
| Маршруты администрация | Устно (таблетки ) |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетический данные | |
| Биодоступность | 30–45% (ТМаксимум = 1,9 часа) |
| Связывание с белками | 70% (in vitro) |
| Метаболизм | Печень (в первую очередь CYP2D6; 1A2 и 3A4 в меньшей степени) |
| Устранение период полураспада | 17–19 часов[2] |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank |
|
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Лиганд PDB | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.247.490 |
| Химические и физические данные | |
| Формула | C19ЧАС18FN3О |
| Молярная масса | 323.371 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
Рукапариб, продается под торговой маркой Rubraca, это Ингибитор PARP используется как противораковое средство. Рукапариб - это первый в своем классе фармацевтический препарат, нацеленный на фермент репарации ДНК. поли-АДФ-рибоза-полимераза-1 (ПАРП-1). Он одобрен в США и Европе в качестве препарата третьей линии в BRCA -мутированный рак яичников.[3][4][5]
Его можно принимать внутрь в форме таблеток.[2][6]
Наиболее частые побочные эффекты включают усталость или слабость, тошноту (плохое самочувствие), повышенный уровень креатинина (который может указывать на проблемы с почками) и ферментов печени в крови (что может указывать на повреждение печени), рвоту, анемию (низкий уровень эритроцитов). ), снижение аппетита, дисгевзия (нарушение вкуса), диарея, тромбоцитопения (низкий уровень тромбоцитов) и боли в животе (боль в животе).[7][2]
Медицинское использование
Рукапариб показан в качестве монотерапии для поддерживающего лечения взрослых с чувствительным к платине рецидивом эпителиального рака яичников высокой степени злокачественности, фаллопиевых труб или первичным раком брюшины, которые находятся в ответе (полном или частичном) на химиотерапию на основе платины.[7][2][8]
Рукапариб показан в качестве монотерапевтического лечения взрослых с чувствительным к платине, рецидивным или прогрессирующим, мутированным BRCA (зародышевым и / или соматическим), эпителиальным раком яичников, фаллопиевой трубы или первичным раком брюшины высокой степени злокачественности, которые лечились двумя или более предыдущими линиями химиотерапии на основе платины и которые не могут переносить дальнейшую химиотерапию на основе платины.[7][2]
Разработка
Он был обнаружен в результате сотрудничества ученых, работающих в Северном институте исследования рака и Медицинской школе Ньюкаслский университет и Agouron Pharmaceuticals в Сан-Диего, Калифорния.[9] Это было развитый к Онкология Хлодвига.
В декабре 2016 г. Управление по контролю за продуктами и лекарствами (FDA) предоставила ускоренное утверждение для использования в случаях предварительной обработки рак яичников.[10][11]
В Европейском Союзе он был признан сирота лекарственного средства 10 октября 2012 г. 22 марта 2018 г. Комитет по лекарственным средствам для человека (CHMP) принял положительное заключение, рекомендуя предоставить условное разрешение на продажу, предназначенное для лечения рецидивирующего или прогрессирующего рака яичников.[12][7] Он был одобрен для медицинского использования в Европейском Союзе в мае 2018 года.[7]
Фармакология
Механизм действия
Рукапариб подавляет «сокращение изолированной гладкой мускулатуры сосудов, в том числе опухолей больных раком. Он также снижает миграцию некоторых раковых и нормальных клеток в культуре».[13]
Как Ингибитор PARP, ожидается, что рукапариб будет более эффективным в 9% случаев рака поджелудочной железы с BRCA мутация (BRCA1 или BRCA2).[14]
Клинические испытания
После одобрения FDA были начаты исследования mCRPC TRITON2 и TRITON3, чтобы определить, как пациенты с раком простаты будут реагировать на препарат рукапариб. Исследования этих двух испытаний все еще продолжаются, и предполагаемые даты первых результатов находятся в диапазоне между 2019 и 2022 годами.[15]
ARIEL3 и ARIEL4 - это два рандомизированных двойных слепых исследования фазы III. Исследование ARIEL3 было разработано для оценки эффекта исследуемого агента в качестве поддерживающего лечения для пациентов с прогрессирующим чувствительным к платине раком яичников по сравнению с плацебо после их ответа как минимум на два предшествующих химиотерапевтических лечения. Основные результаты исследования были представлены на конгрессе ESMO 2017, и сразу после этого оно было опубликовано в журнале Lancet в сентябре 2017 года. Результаты показали значительное улучшение выживаемости без прогрессирования (ВБП) у пациентов, получавших Rubraca, чем плацебо. Недавно, в октябре 2017 года, в FDA был подан дополнительный sNDA для поддерживающей терапии рукапарибом ARIEL3.[16]
Испытание ARIEL4 все еще продолжается[когда? ] чтобы оценить, как пациенты будут лучше реагировать на лечение руккапарибом по сравнению с химиотерапией. Ориентировочная дата сбора данных для измерения первичных результатов - июнь 2022 года.[17]
Смотрите также
Рекомендации
- ^ «Таблетки, покрытые пленочной оболочкой Rubraca 200 мг - Сводка характеристик продукта (SmPC)». (emc). 19 июн 2019. Получено 17 мая 2020.
- ^ а б c d е «Рубрака-рукапариб таблетка, покрытая пленочной оболочкой». DailyMed. 6 апреля 2018 г.. Получено 17 мая 2020.
- ^ Коломбо I, Lheureux S, Oza AM (2018). «Распространенный рак яичников BRCA». Дизайн, разработка и терапия лекарств. 12: 605–617. Дои:10.2147 / DDDT.S130809. ЧВК 5868608. PMID 29606854.
- ^ Musella A, Bardhi E, Marchetti C, Vertechy L, Santangelo G, Sassu C и др. (Май 2018). «Рукапариб: новый ингибитор parp для лечения рецидивирующего рака яичников». Отзывы о лечении рака. 66: 7–14. Дои:10.1016 / j.ctrv.2018.03.004. PMID 29605737.
- ^ Ширли М. (апрель 2019 г.). «Рукапариб: обзор рака яичников». Таргетированная онкология. 14 (2): 237–246. Дои:10.1007 / s11523-019-00629-5. PMID 30830551. S2CID 71147857.
- ^ «Онкологические исследования запускают новое испытание лекарств». netdoctor.co.uk. Hearst Magazines UK. 10 января 2012 г.. Получено 20 декабря 2016.
- ^ а б c d е "Rubraca EPAR". Европейское агентство по лекарствам (EMA). Получено 17 мая 2020. Текст был скопирован из этого источника © European Medicines Agency. Воспроизведение разрешено при условии указания источника.
- ^ «FDA одобряет рукапариб». НАС. Управление по контролю за продуктами и лекарствами (FDA) (Пресс-релиз). 6 апреля 2018 г.. Получено 17 мая 2020.
 Эта статья включает текст из этого источника, который находится в всеобщее достояние.
Эта статья включает текст из этого источника, который находится в всеобщее достояние. - ^ White AW, Almassy R, Calvert AH, Curtin NJ, Griffin RJ, Hostomsky Z, et al. (Ноябрь 2000 г.). «Агенты, модифицирующие резистентность. 9. Синтез и биологические свойства бензимидазольных ингибиторов фермента репарации ДНК поли (АДФ-рибоза) полимеразы». Журнал медицинской химии. 43 (22): 4084–97. Дои:10.1021 / jm000950v. PMID 11063605.
- ^ Bankhead C (19 декабря 2016 г.). «Ингибитор PARP получил одобрение FDA от рака яичников». MedPage Today, ООО. Получено 20 декабря 2016.
- ^ «Рубрака (рукаапариб) в таблетках». НАС. Управление по контролю за продуктами и лекарствами (FDA). 30 января 2017 г.. Получено 17 мая 2020.
- ^ «Рубрака». Европейское Медицинское Агентство. 22 марта 2018. Архивировано с оригинал 29 мая 2018 г.
- ^ «Действует ли ингибитор PARP AG014699 через нуклеотидный рецептор P2?» (PDF). Школа фармацевтики - кандидатские проекты 2009 г.. Архивировано из оригинал (PDF) 13 июня 2011 г.. Получено 17 ноября 2009.
- ^ «Рукапариб показывает клиническую пользу у больных раком поджелудочной железы с мутацией BRCA». sciencedaily.com.
- ^ "«Клинический обзор Рукапариба» (PDF). Онкология Хлодвига. Архивировано из оригинал (PDF) 13 апреля 2018 г.
- ^ Коулман Р.Л., Оза А.М., Лоруссо Д., Агаджанян К., Оакнин А., Дин А. и др. (Октябрь 2017 г.). «Поддерживающая терапия рукапарибом при рецидивирующей карциноме яичников после ответа на терапию платиной (ARIEL3): рандомизированное, двойное слепое, плацебо-контролируемое исследование фазы 3» (PDF). Ланцет. 390 (10106): 1949–1961. Дои:10.1016 / S0140-6736 (17) 32440-6. ЧВК 5901715. PMID 28916367.
- ^ "Ледерманн Дж., Оза А.М., Лоруссо Д. (ноябрь 2017 г.). «ARIEL3: фаза 3, рандомизированное, двойное слепое исследование рукапариба по сравнению с плацебо после ответа на химиотерапию на основе платины при рецидивной карциноме яичников (ОК)» (PDF): 28. Цитировать журнал требует
| журнал =(помощь)
внешняя ссылка
- «Рукапариб». Портал информации о наркотиках. Национальная медицинская библиотека США.
- Номер клинического исследования NCT01968213 для «Исследования Рукапариба в качестве поддерживающей терапии после химиотерапии на основе платины у пациентов с чувствительным к платине, серозным или эндометриоидным эпителиальным раком яичников высокой степени, первичным раком брюшины или фаллопиевых труб (ARIEL3)» в ClinicalTrials.gov
