Кандоксатрил - Candoxatril
 | |
| Имена | |
|---|---|
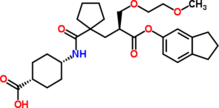
| Название ИЮПАК 4 - {[(1- {3- (2,3-дигидро-1H-инден-5-илокси) -2 - [(2-метоксиэтокси) метил] -3-оксопропил} циклопентил) карбонил] амино} циклогексанкарбоновая кислота | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭМБЛ | |
| ChemSpider | |
| DrugBank | |
| MeSH | кандоксатрил |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C29ЧАС41НЕТ7 | |
| Молярная масса | 515.638 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Кандоксатрил является перорально активным пролекарством[1] кандоксатрилата (UK-73967) нейтральной эндопептидазы человека (Неприлысин ) как нейтральная эндопептидаза 24.11[2] комплексный (РБ-101 ) с фосфорамидоном деградирует и инактивирует[3] ряд биоактивных пептидов. Две многосвязные складчатые области[3] локуса нейтральной эндопептидазы[3] сплайсинг экзонов 1, 2a или 2b с общим экзоном 3, состоящим из 24 экзонов гена CALLA / NEP человека[2] содержащий активный сайт, он известен как семейство пептидаз M13 (семейство неприлизинов, клан MA (E)) глюцинцины слабое, но значимое структурное родство метцинцинов[4][5][6][7] к термолизин -подобные ферменты,[5] Цинцин - простейший дескриптор биологического пространства.[8] В структуре обнаружены два многосвязных складчатых домена, которые охватывают большую центральную полость, содержащую активный центр пролекарства 5-инданилового эфира кандоксатрила.[9] и отличается от фосфорамидон [N- (N - ((((6-дезокси-α-L-маннопиранозил) окси) гидроксифосфинил) -L-лейцил) -L-триптофан ] в нескольких отношениях строение человеческого нейтральная эндопептидаза в комплексе с фосфорамидоном теряется из-за десольватации[9] фермента и лиганда на образование комплекса Кандоксатрил.
Исследования
Кандоксатрил - первое в своем роде лекарство, выпущенное для клинических испытаний сердечной недостаточности. Это связано с тем, что кандоксатрил оказывает благоприятные гемодинамические эффекты у пациентов с хронической сердечной недостаточностью. Было продемонстрировано, что кандоксатрил связан с благоприятным гемодинамическим эффектом, который полезен как при отдыхе, так и при физических упражнениях. В нескольких различных исследованиях было показано, что кандоксатрил улучшает работоспособность у людей с сердечной недостаточностью. В одном исследовании были отобраны 12 разных пациентов, все с сердечной недостаточностью средней степени тяжести. В первый день этого исследования кандоксатрил увеличивал уровни ПНП в плазме, подавлял альдостерон и снижал давление клина в правом предсердии и легочных капиллярах. После лечения в течение 10 дней состояние здоровья пациентов улучшилось за счет увеличения базального ПНП и снижения альдостерона, а также снижения массы тела, что могло быть отражением хронического натрийуретического, мочегонного эффектов или обоих. Было решено, что на 10-й день исследования эффекты кандоксатрила были такими же, как и в первый день.[10]
В отдельном исследовании были собраны пациенты из 16 различных центров Соединенного Королевства. В течение четырех недель пациенты получали кандоксатрил или плацебо в течение 84 дней, и каждые 28 дней пациенты подвергались повторной оценке. 56 из 110 пациентов получали кандоксатрил и 54 получали плацебо. За время исследования у пациентов, принимавших кандоксатрил, наблюдалось общее улучшение времени выполнения упражнений по сравнению с пациентами, принимавшими плацебо.[11]
В третьем исследовании только один пациент испытал ухудшение сердечной недостаточности во время этого конкретного исследования. Однако частота статистически значимо не отличалась от другой наблюдаемой группы, принимавшей плацебо. В совокупности результаты этого исследования показывают, что кандоксатрил предлагает новое эффективное терапевтическое средство для лечения людей с легкой сердечной недостаточностью. Благоприятные эффекты могут начать улучшать самочувствие пациентов во время повседневной деятельности.[12]
Смотрите также
Рекомендации
- ^ Мо Г.Н., Стоби А., Планкен С., Прайд, округ Колумбия, Сандерсон В., Платтс М.Ю., Корлесс М., Стейси П., Уэйман С., Ван дер Грааф П., Кол С., Коггон С., Бомонт К. (январь 2006 г.). «Открытие низкомолекулярных ингибиторов нейтральной эндопептидазы. Исследования структуры и активности функционализированных глутарамидов». Chem Biol Drug Des. 67 (1): 74–77. Дои:10.1111 / j.1747-0285.2005.00320.x. PMID 16492151.
- ^ а б Д'Адамио Л., Шипп М.А., Мастеллер Е.Л., Рейнхерц Е.Л. (сентябрь 1989 г.). «Организация гена, кодирующего общий антиген острого лимфобластного лейкоза (нейтральная эндопептидаза 24.11): несколько миниексонов и отдельные 5'-нетранслируемые области». Proc Natl Acad Sci U S A. 86 (18): 7103–7107. Bibcode:1989PNAS ... 86.7103D. Дои:10.1073 / пнас.86.18.7103. ЧВК 298003. PMID 2528730.
- ^ а б c Oefner C; Д'Арси А; Hennig M; Винклер Ф.К .; Дейл Г.Е. (февраль 2000 г.). «Структура человеческой нейтральной эндопептидазы (Неприлизина) в комплексе с фосфорамидоном». J. Mol. Биол. 296 (2): 341–349. Дои:10.1006 / jmbi.1999.3492. PMID 10669592.
- ^ Найджел М. Хупер (октябрь 1994 г.). «Семейства металлопротеиназ цинка». FEBS Lett. 354 (1): 1–6. Дои:10.1016 / 0014-5793 (94) 01079-X. PMID 7957888. S2CID 25374738.
- ^ а б Стёкер В., Грамс Ф., Бауманн Ю., Райнемер П., Гомис-Рют Ф.С., МакКей Д. Б., Боде В. (май 1995 г.). «Метцинцины - топологические и последовательные отношения между астацинами, адамализинами, серрализинами и матрицинами (коллагеназами) определяют суперсемейство цинк-пептидаз». Белковая наука. 4 (5): 823–840. Дои:10.1002 / pro.5560040502. ЧВК 2143131. PMID 7663339.
- ^ «Нейтральные металлопептидазы цинка, сигнатура цинк-связывающей области в качестве суперсемейства, известная как метцинцины (EC 3.4.15.1). ExPASy: PDOC00129».
- ^ «EC 3.4.15.1 - Пептидил-дипептидаза A в отличие от EC 3.4.15.4 атриопептина. EMBL-EBI: PDOC00129».
- ^ Макардл Б.М., Куинн Р.Дж. (апрель 2007 г.). «Идентификация топологии белковой складки, общей для разных складок, ингибируемой натуральными продуктами». ChemBioChem. 8 (7): 788–798. Дои:10.1002 / cbic.200700035. PMID 17429823.
- ^ а б Holland, D.R .; Barclay, P.L .; Danilewicz, J.C .; Matthews, B.W .; Джеймс, К. (январь 1994 г.). «Ингибирование термолизина и нейтральной эндопептидазы 24.11 новым производным глутарамида: определение структуры комплекса термолизин-ингибитор с помощью рентгеновских лучей». Биохимия. 33 (1): 51–56. Дои:10.1021 / bi00167a007. PMID 8286362.
- ^ «Фильтры результатов». Национальный центр биотехнологической информации. Национальная медицинская библиотека США, n.d. Интернет. 23 ноября 2015 г.
- ^ Макдауэлл, Г., У. Коути, К. Шоу, К. Д. Бьюкенен, А. Д. Стратерс и Д. П. Николлс. «Влияние лекарственного средства нейтрального ингибитора эндопептидазы, Candoxatril, на уровни циркуляции двух наиболее сильных вазоактивных пептидов». Британский журнал клинической фармакологии. Национальная медицинская библиотека США, n.d. Интернет. 23 ноября 2015 г.
- ^ МакМюррей, Джон. «Клиническая кардиология: новые рубежи». Американская Ассоциация Сердца. Американская кардиологическая ассоциация, n.d. Интернет.
