Wee1 - Wee1
| Wee1 | |||||||
|---|---|---|---|---|---|---|---|
 Кристаллическая структура человека Wee1 | |||||||
| Идентификаторы | |||||||
| Символ | Ингибитор митоза протеинкиназа Wee1 | ||||||
| Альт. символы | Wee1 протеинкиназа двойной специфичности Wee1 | ||||||
| Ген NCBI | 2539123 | ||||||
| UniProt | P07527 | ||||||
| Прочие данные | |||||||
| Номер ЕС | 2.7.11.1 | ||||||
| |||||||
Wee1 ядерный киназа принадлежащий к Семья Ser / Thr протеинкиназ в делящихся дрожжах Schizosaccharomyces pombe (С. Помбе). Wee1 имеет молекулярная масса из 96кДа и является ключевым регулятором клеточный цикл прогрессия. Он влияет на размер клеток, препятствуя проникновению в митоз, подавляя Cdk1. Wee1 имеет гомологи у многих других организмов, включая млекопитающих.
Вступление
Регулирование размер ячейки имеет решающее значение для обеспечения работоспособности ячейки. Помимо факторов окружающей среды, таких как питательные вещества, факторы роста и функциональная нагрузка, размер клетки также контролируется контрольной точкой размера клетки.
Wee1 является составной частью этой контрольной точки. Это киназа определение момента времени вступления в митоз, тем самым влияя на размер дочерних клеток. Потеря функции Wee1 приведет к образованию дочерних клеток меньшего размера, чем нормальные, потому что деление клеток происходит преждевременно.
Его название происходит от Шотландский диалект слово Ви, означающее маленький - его первооткрыватель Пол Медсестра во время открытия работал в Эдинбургском университете в Шотландии.[1][2]
Функция
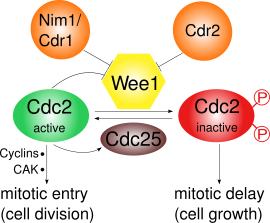
Wee1 подавляет Cdk1 фосфорилируя его по двум разным сайтам, Tyr15 и Thr14.[3] Cdk1 имеет решающее значение для циклин-зависимого прохождения различных контрольных точек клеточного цикла. Существует как минимум три контрольных точки, для которых важно ингибирование Cdk1 с помощью Wee1:
- КПП G2 / M: Wee1 фосфорилирует аминокислоты Tyr15 и Thr14 в Cdk1, что поддерживает низкую киназную активность Cdk1 и предотвращает проникновение в митоз; в С. Помбе может происходить дальнейший рост клеток. Инактивация Cdk1, опосредованная Wee1, оказалась сверхчувствительный в результате конкуренции субстратов.[4] Во время митотического входа активность Wee1 снижается несколькими регуляторами и, таким образом, активность Cdk1 увеличивается. В С. Помбе, Пом1, протеинкиназа, локализуется на полюсах клетки. Это активирует путь, в котором Cdr2 ингибирует Wee1 через Cdr1. Сам Cdk1 негативно регулирует Wee1 путем фосфорилирования, что приводит к положительной петле обратной связи. Одного только снижения активности Wee1 недостаточно для митотического входа: синтез циклины и активирующее фосфорилирование с помощью активирующей киназы Cdk (САК) также необходимы.[5]
- Контрольная точка размера клетки: есть свидетельства существования контрольной точки размера клетки, которая предотвращает попадание мелких клеток в митоз. Wee1 играет роль в этой контрольной точке, координируя размер клетки и развитие клеточного цикла.[6]
- Контрольная точка повреждения ДНК: эта контрольная точка также контролирует переход G2 / M. В С. Помбе эта контрольная точка задерживает вход в митоз клеток с повреждением ДНК (например, вызванным гамма-излучение ). Удлинение фазы G2 зависит от Wee1; wee1 мутанты не имеют продолжительной фазы G2 после гамма-облучения.[7]
Также сообщалось об эпигенетической функции киназы Wee1. Было показано, что Wee1 фосфорилирует гистон H2B по остатку тирозина 37, который регулирует глобальную экспрессию гистонов.[8][9]
Гомологи
| гомолог WEE1 человека (С. Помбе) | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | WEE1 | ||||||
| Ген NCBI | 7465 | ||||||
| HGNC | 12761 | ||||||
| OMIM | 193525 | ||||||
| RefSeq | NM_003390 | ||||||
| UniProt | P30291 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 11 п15.3-15.1 | ||||||
| |||||||
| человеческий WEE1 гомолог 2 (С. Помбе) | |||||||
|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||
| Символ | WEE2 | ||||||
| Ген NCBI | 494551 | ||||||
| HGNC | 19684 | ||||||
| RefSeq | NM_001105558 | ||||||
| UniProt | P0C1S8 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 7 q32-q32 | ||||||
| |||||||
WEE1 ген имеет два известных гомолога у людей: WEE1 (также известный как WEE1A) и WEE2 (WEE1B). Соответствующие белки Wee1-подобная протеинкиназа и Wee1-подобная протеинкиназа 2 которые действуют на гомолог Cdk1 человека Cdk1.
Гомолог Wee1 у почкующихся дрожжей Saccharomyces cerevisiae называется Swe1.
Регулирование
В С. Помбе, Wee1 фосфорилируется
Cdk1 и циклин B составить фактор, способствующий созреванию (MPF), который способствует вступлению в митоз. Он инактивируется фосфорилированием через Wee1 и активируется фосфатазой. Cdc25C. Cdc25C, в свою очередь, активируется Поло киназа и инактивирован Chk1.[6] Таким образом, в С. Помбе Регулирование Wee1 в основном находится под контролем фосфорилирование через киназу полярности, Пом1 путь, включающий Cdr2 и Cdr1.[10][11][12][13]
При переходе G2 / M Cdk1 активируется с помощью Cdc25 посредством дефосфорилирования Tyr15. В то же время Wee1 инактивируется за счет фосфорилирования на своем C-терминал каталитический домен Nim1 / Cdr1.[12] Кроме того, активный MPF будет продвигать свою собственную активность, активируя Cdc25 и инактивируя Wee1, создавая петля положительной обратной связи, хотя это еще не изучено в деталях.[6]
Высшие эукариоты регулируют Wee1 через фосфорилирование и деградацию
В высшем эукариоты, Инактивация Wee1 происходит как путем фосфорилирования, так и деградация.[14] Белковый комплекс[nb 1] SCFβ-TrCP1 / 2 это E3 убиквитинлигаза что функционирует в Wee1A убиквитинирование. В M-фаза киназы Поло-подобная киназа (Plk1) и Cdc2 фосфорилируют два сериновых остатка в Wee1A, которые распознаются SCFβ-TrCP1 / 2.[15]
С. cerevisiae гомолог Swe1
В С. cerevisiae, циклин-зависимая киназа Cdc28 (Гомолог Cdk1) фосфорилируется Swe1 (гомолог Wee1) и дефосфорилируется Mih1 (гомолог Cdc25). Гомолог Nim1 / Cdr1 в С. cerevisiae, Hsl1 вместе с родственными ему киназами Gin4 и Kcc4 локализуют Swe1 в бутон-шейка. Киназы, связывающие почковидную шейку, Cla4 и Cdc5 (гомолог полокиназы) фосфорилируют Swe1 на разных стадиях клеточного цикла. Swe1 также фосфорилируется Clb2-Cdc28, который служит распознаванием для дальнейшего фосфорилирования Cdc5.
В С. cerevisiae белок Swe1 также регулируется деградацией. Swe1 гиперфосфорилируется Clb2-Cdc28 и Cdc5, что может быть сигналом для убиквитинирования и деградации посредством SCF Комплекс убиквитин-лигазы Е3, как у высших эукариот.[16]
Роль в раке
Фактор, способствующий митозу, MPF также регулирует Повреждение ДНК индуцированный апоптоз. Отрицательная регуляция MPF с помощью WEE1 вызывает аберрантный митоз и, таким образом, устойчивость к апоптозу, вызванному повреждением ДНК. Фактор Круппеля 2 (KLF2) негативно регулирует человеческий WEE1, тем самым повышая чувствительность к апоптозу, вызванному повреждением ДНК, в раковых клетках.[17]
Мутантный фенотип
Wee1 действует как дозозависимый ингибитор митоза.[18] Таким образом, количество белка Wee1 коррелирует с размером клеток:
Делящиеся дрожжи мутант wee1, также называемый wee1−, делится со значительно меньшим размером клеток, чем клетки дикого типа. Поскольку Wee1 ингибирует вступление в митоз, его отсутствие приведет к преждевременному делению и к субнормальному размеру клеток. Напротив, когда экспрессия Wee1 увеличивается, митоз задерживается, и клетки вырастают до больших размеров перед делением.
Смотрите также
Примечания
- ^ белок 1/2, содержащий повторы β-трансдуцина (β-TrCP1 / 2) F-бокс-белок, содержащий белок SKP1 / Cul1 / F-бокс-белковый комплекс
Рекомендации
- ^ Медсестра П. (декабрь 2004 г.). "Маленькие звери". Природа. 432 (7017): 557. Дои:10.1038 / 432557a. PMID 15577889. S2CID 29840746.
- ^ Медсестра П., Тюрио П. (ноябрь 1980 г.). «Регулирующие гены, контролирующие митоз у делящихся дрожжей Schizosaccharomyces pombe». Генетика. 96 (3): 627–37. ЧВК 1214365. PMID 7262540.
- ^ Ден Хезе Г.Дж., Уолворт Н., Карр А.М., Гулд К.Л. (1995). «Протеинкиназа Wee1 регулирует фосфорилирование T14 делящихся дрожжей Cdc2». Клетка Mol Biol. 6 (4): 371–85. Дои:10.1091 / mbc.6.4.371. ЧВК 301198. PMID 7626804.
- ^ Kim, SY; Феррелл Дж. Э. младший (23 марта 2007 г.). «Конкуренция субстратов как источник сверхчувствительности при инактивации Wee1». Клетка. 128 (6): 1133–45. Дои:10.1016 / j.cell.2007.01.039. PMID 17382882. S2CID 14138576.
- ^ Коулман Т.Р., Данфи В.Г. (1994). «Регулирующие факторы Cdc2». Текущее мнение в области клеточной биологии. 6 (6): 877–82. Дои:10.1016/0955-0674(94)90060-4. PMID 7880537.
- ^ а б c Келлог Д.Р. (2003). «Wee1-зависимые механизмы, необходимые для координации роста и деления клеток». J Cell Sci. 116 (24): 4883–90. Дои:10.1242 / jcs.00908. PMID 14625382.
- ^ Роули Р., Хадсон Дж., Янг П.Г. (1992). «Протеинкиназа wee1 необходима для радиационно-индуцированной задержки митоза». Природа. 356 (6367): 353–5. Дои:10.1038 / 356353a0. PMID 1549179. S2CID 4280074.
- ^ Махаджан К., Фанг Б., Кумен Дж. М., Махаджан Н. П. (2012). «Фосфорилирование H2B Tyr37 подавляет экспрессию зависимых от репликации генов гистонов ядра». Структурная и молекулярная биология природы. 19 (9): 930–7. Дои:10.1038 / nsmb.2356. ЧВК 4533924. PMID 22885324.
- ^ Махаджан К., Махаджан Н.П. (2013). «Тирозинкиназа WEE1, новый эпигенетический модификатор». Тенденции Genet. 29 (7): 394–402. Дои:10.1016 / j.tig.2013.02.003. ЧВК 3700603. PMID 23537585.
- ^ Бодди М.Н., Фурнари Б., Мондесерт О, Рассел П. (май 1998 г.). «Контрольная точка репликации обеспечивается киназами Cds1 и Chk1». Наука. 280 (5365): 909–12. Дои:10.1126 / science.280.5365.909. PMID 9572736.
- ^ Ву Л., Рассел П. (июнь 1993 г.). «Киназа Nim1 способствует митозу, инактивируя тирозинкиназу Wee1». Природа. 363 (6431): 738–41. Дои:10.1038 / 363738a0. PMID 8515818. S2CID 4320080.
- ^ а б Коулман Т.Р., Тан З., Данфи В.Г. (март 1993 г.). «Отрицательная регуляция протеинкиназы wee1 путем прямого действия митотического индуктора nim1 / cdr1». Клетка. 72 (6): 919–29. Дои:10.1016 / 0092-8674 (93) 90580-Дж. PMID 7681363. S2CID 42256641.
- ^ Тан З., Коулман Т.Р., Данфи В.Г. (сентябрь 1993 г.). «Два различных механизма отрицательной регуляции протеинкиназы Wee1». EMBO J. 12 (9): 3427–36. Дои:10.1002 / j.1460-2075.1993.tb06017.x. ЧВК 413619. PMID 7504624.
- ^ Ватанабэ Н., Брум М., Хантер Т. (май 1995 г.). «Регулирование человеческой тирозин-15-киназы WEE1Hu CDK во время клеточного цикла». EMBO J. 14 (9): 1878–91. Дои:10.1002 / j.1460-2075.1995.tb07180.x. ЧВК 398287. PMID 7743995.
- ^ Ватанабе Н., Араи Х., Нишихара Й. и др. (Март 2004 г.). «Киназы M-фазы индуцируют фосфо-зависимое убиквитинирование соматического Wee1 с помощью SCFbeta-TrCP». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 101 (13): 4419–24. Дои:10.1073 / pnas.0307700101. ЧВК 384762. PMID 15070733.
- ^ Ли К.С., Асано С., Пак Дж. Э., Сакчайсри К., Эриксон Р. Л. (октябрь 2005 г.). «Мониторинг клеточного цикла с помощью мультикиназозависимой регуляции Swe1 / Wee1 у почкующихся дрожжей». Клеточный цикл. 4 (10): 1346–9. Дои:10.4161 / cc.4.10.2049. PMID 16123596.
- ^ Ван Ф, Чжу Й, Хуанг И и др. (Июнь 2005 г.). «Репрессия транскрипции WEE1 с помощью Kruppel-подобного фактора 2 участвует в апоптозе, вызванном повреждением ДНК». Онкоген. 24 (24): 3875–85. Дои:10.1038 / sj.onc.1208546. PMID 15735666.
- ^ Рассел П., медсестра П. (май 1987 г.). «Отрицательная регуляция митоза с помощью We1 +, гена, кодирующего гомолог протеинкиназы». Клетка. 49 (4): 559–67. Дои:10.1016/0092-8674(87)90458-2. PMID 3032459. S2CID 42801276.
