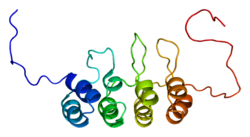P16 - P16
| Ингибитор циклин-зависимой киназы 2a p19Arf N-конец | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 структура раствора n-концевых 37 аминокислот белка супрессора опухоли arf мыши | |||||||||
| Идентификаторы | |||||||||
| Символ | P19Arf_N | ||||||||
| Pfam | PF07392 | ||||||||
| ИнтерПро | IPR010868 | ||||||||
| SCOP2 | 1хн3 / Объем / СУПФАМ | ||||||||
| |||||||||
p16 (также известен как p16INK4a, ингибитор циклинзависимой киназы 2А, CDKN2A, подавитель множественных опухолей 1 и множество других синонимов), является белок это замедляется деление клеток замедляя прогрессирование клеточного цикла от Фаза G1 к Фаза S, тем самым действуя как подавитель опухолей. Он закодирован CDKN2A ген. А удаление (пропуск части последовательности ДНК во время репликации) в этом гене может привести к недостаточному или нефункциональному p16, ускорению клеточного цикла и возникновению многих типов рака.[5][6][7]
p16 можно использовать как биомаркер для повышения гистологической точности диагностики 3 степени цервикальная интраэпителиальная неоплазия (КИН). p16 также участвует в предотвращении меланома, плоскоклеточный рак ротоглотки, рак шейки матки, рак вульвы и рак пищевода.
p16 был открыт в 1993 году. Это белок, содержащий 148 аминокислот и молекулярный вес из 16 кДа это включает четыре Анкирин повторяет.[8] Название p16 происходит от его молекулярный вес, а альтернативное имя p16INK4a относится к его роли в подавлении циклин-зависимая киназа CDK4.[8]
Номенклатура
p16 также известен как:
- p16INK4A
- p16Чернила4
- Ингибитор циклинзависимой киназы 2A (CDKN2A)
- CDKN2
- CDK 4 ингибитор
- Подавитель множественных опухолей 1 (MTS1)
- TP16
- АРФ
- MLM
- P14
Ген
У человека p16 кодируется CDKN2A ген, расположенный на хромосома 9 (9п21.3). Этот ген генерирует несколько стенограмма варианты, которые отличаются по первому экзоны. Не менее трех альтернативно сращенный сообщалось о вариантах, кодирующих различные белки, два из которых кодируют структурно родственные изоформы известен как ингибиторы из CDK4. Остающийся транскрипт включает альтернативный экзон 1, расположенный в 20 kb перед остальной частью гена; эта стенограмма содержит альтернативная открытая рамка считывания (ARF) который определяет белок, структурно не связанный с продуктами других вариантов.[9] Продукт ARF действует как стабилизатор белка-супрессора опухоли. p53, поскольку он может взаимодействовать и изолировать MDM2, белок, ответственный за деградацию p53.[10][11] Несмотря на их структурные и функциональные различия, изоформы ингибиторов CDK и продукт ARF, кодируемый этим геном, через регуляторные роли CDK4 и p53 в клеточный цикл G1 прогрессия, имеют общие функции по контролю фазы G1 клеточного цикла. Этот ген часто мутируют или делетируют в большом количестве опухолей и, как известно, является важным геном-супрессором опухоли.[5]
Когда организмы стареют, экспрессия p16 увеличивается, чтобы уменьшить распространение стволовые клетки.[12] Это уменьшение деления и производства стволовых клеток защищает от рак при увеличении рисков, связанных с клеточное старение.
Функция
p16 - ингибитор циклинзависимых киназ (CDK). Он замедляет клеточный цикл, запрещая переход от фазы G1 к фазе S. В противном случае CDK4 / 6 связывает циклин D и образует активный белковый комплекс, который фосфорилирует белок ретинобластомы (pRB). После фосфорилирования pRB отделяется от фактора транскрипции. E2F1. Это высвобождает E2F1 из связанного состояния в цитоплазме и позволяет ему проникать в ядро. Попадая в ядро, E2F1 способствует транскрипции генов-мишеней, которые необходимы для перехода от G1 к S-фазе.[13][14]
Этот путь связывает процессы онкогенеза и старения опухоли, фиксируя их на противоположных концах спектра. С одной стороны, гиперметилирование, мутация или делеция p16 приводит к подавлению активности гена и может привести к раку из-за нарушения регуляции развития клеточного цикла. И наоборот, активация p16 через активные формы кислорода, Повреждение ДНК или старение приводит к накоплению p16 в тканях и участвует в старении клеток.[13]
Регулирование
Регуляция p16 сложна и включает взаимодействие нескольких факторов транскрипции, а также нескольких белков, участвующих в эпигенетической модификации посредством метилирования и репрессии промоторной области.[13]
PRC1 и PRC2 представляют собой два белковых комплекса, которые модифицируют экспрессию p16 посредством взаимодействия различных факторов транскрипции, которые выполняют паттерны метилирования, которые могут репрессировать транскрипцию p16. Эти пути активируются в клеточном ответе, чтобы уменьшить старение.[15][16]
Клиническое значение
Роль в канцерогенезе
Мутации, приводящие к делеции или снижению функции гена CDKN2A, связаны с повышенным риском развития широкого спектра видов рака, а изменения гена часто наблюдаются при раке. Сотовые линии.[17][18] Примеры включают:
Аденокарцинома поджелудочной железы часто ассоциируется с мутациями в гене CDKN2A.[19][20][21]
Носители мутаций зародышевой линии в CDKN2A имеют, помимо высокого риска меланомы, также повышенный риск рака поджелудочной железы, легких, гортани и ротоглотки. Курение табака увеличивает восприимчивость носителей к таким немеланомным видам рака.[22]
Гомозиготные делеции p16 часто встречаются в рак пищевода и рак желудка Сотовые линии.[23]
Мутации зародышевой линии в CDKN2A связаны с повышенной восприимчивостью к развитию рак кожи.[24]
Гиперметилирование генов-супрессоров опухолей вовлечено в различные виды рака. В 2013 году метаанализ выявил повышенную частоту метилирования ДНК гена p16 при раке пищевода. По мере увеличения степени дифференцировки опухоли увеличивалась и частота метилирования ДНК p16.
Образцы тканей первичной плоскоклеточной карциномы полости рта (OSCC) часто обнаруживают гиперметилирование в промоторных областях p16. Раковые клетки обнаруживают значительное увеличение накопления метилирования в CpG-островках в промоторной области p16. Этот эпигенетический изменение приводит к потере функции гена-супрессора опухоли посредством двух возможных механизмов: во-первых, метилирование может физически ингибировать транскрипцию гена, а во-вторых, метилирование может привести к рекрутированию факторов транскрипции, которые подавляют транскрипцию. Оба механизма вызывают один и тот же конечный результат: подавление экспрессии генов, что приводит к снижению уровня белка p16. Было высказано предположение, что этот процесс отвечает за развитие различных форм рака, выступая в качестве альтернативного процесса делеции или мутации гена.[25][26][27][28][29][30]
Показано, что положительный результат по p16 является благоприятным прогностическим фактором при плоскоклеточной карциноме ротоглотки.[31] В ретроспективном исследовании пациентов с раком ротоглотки III и IV стадии был оценен статус ВПЧ, и было обнаружено, что 3-летняя общая выживаемость составила 82,4% (95% ДИ от 77,2 до 87,6) в подгруппе с ВПЧ-положительной реакцией. и 57,1% (95% ДИ, от 48,1 до 66,1) в подгруппе с отрицательным результатом ВПЧ, а 3-летняя выживаемость без прогрессирования составила 73,7% (95% ДИ, 67,7-79,8) и 43,4% (95% ДИ, 34,4 - 52,4) соответственно. Статус p16 является настолько прогностическим, что система стадирования AJCC была пересмотрена, чтобы включить статус p16 в групповую стадию плоскоклеточного рака ротоглотки.[32]

Клиническое использование
Биомаркер типов рака
Экспрессия p16 используется в качестве прогностического биомаркера для определенных типов рака. Причина этого в том, что разные типы рака могут по-разному влиять на экспрессию p16: рак, сверхэкспрессирующий p16, обычно вызывается вирус папилломы человека (ВПЧ), тогда как рак, при котором уровень p16 снижается, обычно имеет другие причины. Было показано, что для пациентов с плоскоклеточным раком ротоглотки использование иммуногистохимии для обнаружения биомаркера p16 является наиболее сильным индикатором течения заболевания. Присутствие биомаркера связано с более благоприятным прогнозом, который измеряется с помощью специфической для рака выживаемости (CSS), выживаемости без рецидивов (RFS), локорегионального контроля (LRC), а также других измерений. Появление гиперметилирования p16 также оценивается как потенциальный прогностический биомаркер рака простаты.[33][34][35]
p16 РЫБА
p16 удаление обнаружен РЫБЫ в поверхностных эпителиальных мезотелиальных разрастаниях является прогностическим признаком инвазивного мезотелиома.[36]
p16 иммунохимия

По мере того, как растет консенсус относительно силы p16 как биомаркера для обнаружения и определения прогнозов рака, важность иммуногистохимии p16 возрастает.[13][33][37]
гинекологический рак
p16 - широко используемый иммуногистохимический маркер при гинекологической патологии. Сильная и диффузная цитоплазматическая и ядерная экспрессия p16 в плоскоклеточный рак (SCC) женских половых путей тесно связаны с высоким риском вирус папилломы человека (ВПЧ) инфекции и новообразования шейки матки. Большинство ПКР шейки матки экспрессируют p16. Однако p16 может экспрессироваться в других новообразованиях и в некоторых нормальных тканях человека.[38]
SCC мочевого пузыря
Более трети SCC мочевого пузыря экспрессируют p16. SCC мочевого пузыря экспрессируют p16 независимо от пола. Сама по себе иммуногистохимическая экспрессия p16 не может быть использована для различения SCC, возникающих из шейки матки и мочевого пузыря.[38]
Роль в клеточном старении
Концентрация p16INK4a резко возрастает с возрастом ткани. p16INK4a вместе с связанная со старением бета-галактозидаза, считается биомаркер из клеточное старение.[39] Следовательно, p16INK4a потенциально может использоваться в качестве анализа крови, который измеряет, насколько быстро ткани организма стареют на молекулярном уровне.[40] Примечательно, что недавнее исследование клеточного старения, вызванного множественными обработками нескольких клеточных линий, не идентифицирует p16 как принадлежащую к «основной сигнатуре» маркеров старения.[41]
Его использовали в качестве мишени для замедления некоторых изменений старения у мышей.[42]
Роль в нейрогенезе
Было показано, что p16INK4a предотвращает истощение во время старения нервных стволовых и клеток-предшественников в одной из нейрогенных ниш взрослого мозга, то есть в субвентрикулярной зоне, которая генерирует на протяжении всей жизни новые нейроны, мигрирующие в обонятельную луковицу. [43]. Делеция p16INK4a не влияет на нейрогенез в другой нейрогенной нише взрослых, зубчатые извилины гиппокампа [43]. Однако недавно было продемонстрировано, что p16INK4a защищает от истощения после мощного пронейрогенного стимула - т. Е. Бега - также стволовые клетки и клетки-предшественники старой зубчатой извилины. [44]. Фактически, после делеции p16INK4a стволовые клетки зубчатой извилины в значительной степени активируются при беге, в то время как у p16INK4a дикого типа на стволовые клетки зубчатой извилины бег не влияет.[44] Следовательно, p16Ink4a играет роль в поддержании стволовых клеток зубчатой извилины после стимула, сохраняя резерв их способности к самообновлению во время старения. Поскольку зубчатая извилина играет ключевую роль в формировании пространственной и контекстной памяти, p16INK4a участвует в поддержании когнитивных функций во время старения.
Открытие
Исследователи Мануэль Серрано, Грегори Дж. Хэннон и Дэвид Бич открыли p16 в 1993 году и правильно охарактеризовали этот белок как ингибитор циклин-зависимой киназы.
Роль в канцерогенезе
С момента своего открытия p16 приобрел важное значение в области исследований рака. Предполагалось, что белок участвует в канцерогенезе из-за наблюдения, что мутация или делеция в гене участвуют в линиях раковых клеток человека. Обнаружение инактивации p16 при семейной меланоме дало дополнительные доказательства. В настоящее время делеция, мутация, гиперметилирование или избыточная экспрессия p16 связаны с различными видами рака. Можно ли считать мутации в p16 мутациями драйвера, требует дальнейшего изучения.[17]
Взаимодействия
p16 был показан взаимодействовать с:
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000147889 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000044303 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ «Ссылка на Mouse PubMed:». Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ а б «Ген Entrez: CDKN2A, ингибитор циклин-зависимой киназы 2A (меланома, p16, ингибирует CDK4)».
- ^ Нобори Т., Миура К., Ву Диджей, Лоис А., Такабаяши К., Карсон Д.А. (апрель 1994 г.). «Делеции гена ингибитора циклин-зависимой киназы-4 при множественных раковых заболеваниях человека». Природа. 368 (6473): 753–6. Дои:10.1038 / 368753a0. PMID 8152487. S2CID 13199401.
- ^ Стоун С., Цзян П., Даянант П., Тавтиджан С.В., Катчер Х., Парри Д., Петерс Дж., Камб А. (июль 1995 г.). «Сложная структура и регуляция локуса P16 (MTS1)». Исследования рака. 55 (14): 2988–94. PMID 7606716.
- ^ а б c Серрано М., Хэннон Г.Дж., Пляж D (декабрь 1993 г.). «Новый регуляторный мотив в контроле клеточного цикла, вызывающий специфическое ингибирование циклина D / CDK4». Природа. 366 (6456): 704–7. Дои:10.1038 / 366704a0. PMID 8259215. S2CID 4368128.
- ^ Хамош, Ада. «Ингибитор циклин-зависимой киназы 2A; CDKN2A». OMIM. Получено 10 декабря 2013.
- ^ «Молекулярная биология рака», Oxford University Press, 2005 г., ISBN 978-0-19-926472-8, Раздел 5.3
- ^ Руссель М.Ф. (сентябрь 1999 г.). «Семейство ингибиторов клеточного цикла INK4 при раке». Онкоген. 18 (38): 5311–7. Дои:10.1038 / sj.onc.1202998. PMID 10498883.
- ^ Кришнамурти Дж., Рэмси М.Р., Лигон К.Л., Торрис С., Кох А., Боннер-Вейр С., Шарплесс, штат Нью-Йорк (сентябрь 2006 г.). «p16INK4a вызывает возрастное снижение регенеративного потенциала островков». Природа. 443 (7110): 453–7. Дои:10.1038 / природа05092. PMID 16957737. S2CID 4402013.
- ^ а б c d Райесс Х., Ван МБ, Сриватсан Э.С. (апрель 2012 г.). «Клеточное старение и ген супрессора опухолей p16». Международный журнал рака. 130 (8): 1715–25. Дои:10.1002 / ijc.27316. ЧВК 3288293. PMID 22025288.
- ^ Хара Э., Смит Р., Парри Д., Тахара Х, Стоун С., Петерс Дж. (Март 1996 г.). «Регулирование экспрессии p16CDKN2 и ее значение для иммортализации и старения клеток». Молекулярная и клеточная биология. 16 (3): 859–67. Дои:10.1128 / mcb.16.3.859. ЧВК 231066. PMID 8622687.
- ^ Цао Р., Ван Л., Ван Х., Ся Л., Эрдджумент-Бромаж Х, Темпст П., Джонс Р. С., Чжан Ю. (ноябрь 2002 г.). «Роль метилирования гистона H3 лизина 27 в сайленсинге Polycomb-группы». Наука. 298 (5595): 1039–43. Дои:10.1126 / science.1076997. PMID 12351676. S2CID 6265267.
- ^ Bracken AP, Kleine-Kohlbrecher D, Dietrich N, Pasini D, Gargiulo G, Beekman C, Theilgaard-Mönch K, Minucci S, Porse BT, Marine JC, Hansen KH, Helin K (март 2007 г.). «Белки группы Polycomb связываются по всему локусу INK4A-ARF и диссоциируют в стареющих клетках». Гены и развитие. 21 (5): 525–30. Дои:10.1101 / gad.415507. ЧВК 1820894. PMID 17344414.
- ^ а б Лиггетт У.Х., Сидранский Д. (март 1998 г.). «Роль гена супрессора опухоли p16 при раке». Журнал клинической онкологии. 16 (3): 1197–206. Дои:10.1200 / JCO.1998.16.3.1197. PMID 9508208.
- ^ Рокко Дж. В., Сидранский Д. (март 2001 г.). «p16 (MTS-1 / CDKN2 / INK4a) при прогрессировании рака». Экспериментальные исследования клеток. 264 (1): 42–55. Дои:10.1006 / exc.2000.5149. PMID 11237522.
- ^ Caldas C, Hahn SA, da Costa LT, Redston MS, Schutte M, Seymour AB, Weinstein CL, Hruban RH, Yeo CJ, Kern SE (сентябрь 1994 г.). «Частые соматические мутации и гомозиготные делеции гена p16 (MTS1) при аденокарциноме поджелудочной железы». Природа Генетика. 8 (1): 27–32. Дои:10.1038 / ng0994-27. PMID 7726912. S2CID 23195660.
- ^ Барч Д., Шевлин Д.В., Тунг В.С., Кискер О., Уэллс С.А., Гудфеллоу П.Дж. (ноябрь 1995 г.). «Частые мутации CDKN2 в первичных аденокарциномах поджелудочной железы». Гены, хромосомы и рак. 14 (3): 189–95. Дои:10.1002 / gcc.2870140306. PMID 8589035. S2CID 22823227.
- ^ Лю Л., Лассам Нью-Джерси, Слингерленд Дж. М., Бейли Д., Коул Д., Дженкинс Р., Хогг Д. (июль 1995 г.). «Мутация зародышевой линии p16INK4A и дисфункция белка в семье с наследственной меланомой». Онкоген. 11 (2): 405–12. PMID 7624155.
- ^ Helgadottir H, Höiom V, Jönsson G, Tuominen R, Ingvar C, Borg A, Olsson H, Hansson J (август 2014 г.). «Высокий риск рака, связанного с курением, в семьях меланомы с положительной мутацией CDKN2A». Журнал медицинской генетики. 51 (8): 545–52. Дои:10.1136 / jmedgenet-2014-102320. ЧВК 4112445. PMID 24935963.
- ^ Игаки Х., Сасаки Х., Киши Т., Сакамото Х., Тачимори Й., Като Х., Ватанабе Х., Сугимура Т., Терада М. (сентябрь 1994 г.). «Очень частая гомозиготная делеция гена p16 в клеточных линиях рака пищевода». Сообщения о биохимических и биофизических исследованиях. 203 (2): 1090–5. Дои:10.1006 / bbrc.1994.2294. PMID 8093026.
- ^ Пуиг-Бутилле Х.А., Эскамес М.Дж., Гарсия-Гарсия Ф., Телль-Марти Г., Фабра А., Мартинес-Сантамария Л., Баденас С., Агилера П., Певида М., Допасо Д., дель Рио М., Пуч С. (март 2014 г.). «Определение биологического воздействия генов CDKN2A и MC1R как раннего предрасполагающего события к меланоме и немеланомному раку кожи». Oncotarget. 5 (6): 1439–51. Дои:10.18632 / oncotarget.1444. ЧВК 4039222. PMID 24742402.
- ^ Хор Г.Х., Фремминг Г.Р., Заин РБ, Абрахам М.Т., Омар Э., Тан С.К., Тан А.С., Винсент-Чонг В.К., Тонг К.Л. (2013). «Профилирование метилирования ДНК выявило индуцированное гиперметилированием промотора молчание p16, DDAH2 и DUSP1 в первичной плоскоклеточной карциноме полости рта». Международный журнал медицинских наук. 10 (12): 1727–39. Дои:10.7150 / ijms.6884. ЧВК 3805925. PMID 24155659.
- ^ Демокан С., Чуанг А., Суоглу Ю., Улусан М., Ялныз З., Калифано Дж. А., Далай Н. (октябрь 2012 г.). «Метилирование промотора и потеря экспрессии гена p16 (INK4a) при раке головы и шеи». Голова и шея. 34 (10): 1470–5. Дои:10.1002 / хед.21949. PMID 22106032. S2CID 11512476.
- ^ Шоу Р.Дж., Лилоглу Т., Роджерс С.Н., Браун Дж.С., Воган Э.Д., Лоу Д., Филд Дж. К., Риск Дж. М. (февраль 2006 г.). «Промоторное метилирование P16, RARbeta, E-кадгерина, циклина A1 и цитоглобина при раке полости рта: количественная оценка с использованием пиросеквенирования». Британский журнал рака. 94 (4): 561–8. Дои:10.1038 / sj.bjc.6602972. ЧВК 2361183. PMID 16449996.
- ^ Шарма Г., Мирза С., Прасад С. П., Шривастава А., Гупта С. Д., Ралхан Р. (апрель 2007 г.). «Промотор гиперметилирования p16INK4A, p14ARF, CyclinD2 и Slit2 в сыворотке и опухолевой ДНК от пациентов с раком груди». Науки о жизни. 80 (20): 1873–81. Дои:10.1016 / j.lfs.2007.02.026. PMID 17383681.
- ^ Jabłonowski Z, Reszka E, Gromadzińska J, Wąsowicz W, Sosnowski M (июнь 2011 г.). «Гиперметилирование участков промоторных генов p16 и DAPK у пациентов с неинвазивным раком мочевого пузыря». Архив медицинской науки. 7 (3): 512–6. Дои:10.5114 / aoms.2011.23421. ЧВК 3258754. PMID 22295037.
- ^ Сюй Р, Ван Ф, Ву Л, Ван Дж, Лу Ц (январь 2013 г.). «Систематический обзор гиперметилирования гена p16 при раке пищевода». Биомаркеры рака. 13 (4): 215–26. Дои:10.3233 / CBM-130355. PMID 24240582.
- ^ Ang KK, et al. (2010). «Вирус папилломы человека и выживаемость больных раком ротоглотки». Медицинский журнал Новой Англии. 363 (1): 24–35. Дои:10.1056 / NEJMoa0912217. ЧВК 2943767. PMID 20530316.
- ^ Lydiatt WM и др. (2017). «Рак головы и шеи - основные изменения в восьмом издании руководства по стадированию рака Американского объединенного комитета по раку». КА: Онкологический журнал для клиницистов. 67 (2): 122–137. Дои:10.3322 / caac.21389. PMID 28128848.
- ^ а б Oguejiofor KK, Hall JS, Mani N, Douglas C, Slevin NJ, Homer J, Hall G, West CM (ноябрь 2013 г.). «Прогностическое значение биомаркера p16 в плоскоклеточной карциноме ротоглотки». Клиническая онкология. 25 (11): 630–8. Дои:10.1016 / j.clon.2013.07.003. PMID 23916365.
- ^ Balgkouranidou I, Liloglou T, Lianidou ES (февраль 2013 г.). «Эпигенетика рака легких: новые биомаркеры». Биомаркеры в медицине. 7 (1): 49–58. Дои:10.2217 / bmm.12.111. PMID 23387484.
- ^ Синха П., Торстад В. Т., Нуссенбаум Б., Хоги Б. Х., Адкинс Д. Р., Каллогжери Д., Льюис Дж. С. (январь 2014 г.). «Отдаленные метастазы при плоскоклеточной карциноме ротоглотки, положительной по p16: критический анализ закономерностей и результатов». Оральная онкология. 50 (1): 45–51. Дои:10.1016 / j.oraloncology.2013.10.007. ЧВК 3942323. PMID 24211084.
- ^ Hwang H, Tse C, Rodriguez S, Gown A, Churg A (май 2014 г.). «Делеция p16 FISH в мезотелиальных пролиферациях поверхностного эпителия является предиктором инвазивной мезотелиомы». Американский журнал хирургической патологии. 38 (5): 681–8. Дои:10.1097 / PAS.0000000000000176. PMID 24503757. S2CID 28068784.
- ^ Дрейер Дж. Х., Хаук Ф., Оливейра-Силва М., Баррос М. Х., Ниедобитек Дж. (Апрель 2013 г.). «Выявление инфекции ВПЧ при плоскоклеточном раке головы и шеи: практическое предложение». Вирховский архив. 462 (4): 381–9. Дои:10.1007 / s00428-013-1393-5. PMID 23503925. S2CID 7469046.
- ^ а б Cioffi-Lavina M, Chapman-Fredricks J, Gomez-Fernandez C, Ganjei-Azar P, Manoharan M, Jorda M (июль 2010 г.). «Экспрессия P16 в плоскоклеточном раке шейки матки и мочевого пузыря». Прикладная иммуногистохимия и молекулярная морфология. 18 (4): 344–7. Дои:10.1097 / PAI.0b013e3181d2bbd7. PMID 20571342. S2CID 5065484.
- ^ Холл Б.М., Балан В., Глейберман А.С., Стром Э., Краснов П., Виртуоз Л.П., Рыдкина Е., Вуйчич С., Балан К., Гитлин И., Леонова К., Полинский А., Чернова О.Б., Гудков А.В. (июль 2016). «Старение мышей связано с накоплением p16 (Ink4a) и β-галактозидаза-положительных макрофагов, которое может быть индуцировано у молодых мышей стареющими клетками». Старение. 8 (7): 1294–315. Дои:10.18632 / старение.100991. ЧВК 4993332. PMID 27391570.
- ^ Лю Й., Санофф Х.К., Чо Х., Бурд С.Е., Торрис К., Ибрагим Дж. Г., Томас Н. Э., Шарплесс Н. Э. (август 2009 г.). «Экспрессия p16 (INK4a) в Т-клетках периферической крови является биомаркером старения человека». Ячейка старения. 8 (4): 439–48. Дои:10.1111 / j.1474-9726.2009.00489.x. ЧВК 2752333. PMID 19485966.
- ^ Эрнандес-Сегура А., де Йонг ТВ, Мелов С., Гурьев В., Кампизи Дж., Демария М. (август 2017 г.). «Разоблачение транскрипционной гетерогенности в стареющих клетках». Текущая биология. 27 (17): 2652–2660.e4. Дои:10.1016 / j.cub.2017.07.033. ЧВК 5788810. PMID 28844647.
- ^ Baker DJ, Wijshake T, Tchkonia T, LeBrasseur NK, Childs BG, van de Sluis B, Kirkland JL, van Deursen JM (ноябрь 2011 г.). «Удаление p16Ink4a-позитивных стареющих клеток задерживает нарушения, связанные со старением». Природа. 479 (7372): 232–6. Дои:10.1038 / природа10600. ЧВК 3468323. PMID 22048312.
- ^ а б Молофский А.В., Слуцкий С.Г., Джозеф Н.М., Хе С., Пардал Р., Кришнамурти Дж. И др. (Сентябрь 2006 г.). «Повышение экспрессии p16INK4a снижает количество предшественников в переднем мозге и нейрогенез во время старения». Природа. 443 (7110): 448–52. Дои:10.1038 / природа05091. ЧВК 2586960. PMID 16957738.
- ^ а б Микели Л., Д'Андреа Г., Чеккарелли М., Ферри А., Скардигли Р., Тироне Ф (2019). «p16Ink4a предотвращает активацию состаренных покоящихся стволовых клеток зубчатой коры с помощью физических упражнений». Границы клеточной неврологии. 13:10: 10. Дои:10.3389 / fncel.2019.00010. ISSN 1662-5102. ЧВК 6374340. PMID 30792628.
- ^ Zhao L, Samuels T, Winckler S, Korgaonkar C, Tompkins V, Horne MC, Quelle DE (январь 2003 г.). «Циклин G1 обладает активностью ингибирования роста, связанной с путями подавления опухоли ARF-Mdm2-p53 и pRb». Молекулярные исследования рака. 1 (3): 195–206. PMID 12556559.
- ^ а б Ли Дж., Мелвин В.С., Цай, доктор медицины, Muscarella P (апрель 2004 г.). «Ядерный белок p34SEI-1 регулирует киназную активность циклин-зависимой киназы 4 в зависимости от концентрации». Биохимия. 43 (14): 4394–9. CiteSeerX 10.1.1.386.140. Дои:10.1021 / bi035601s. PMID 15065884.
- ^ а б Сугимото М., Накамура Т., Отани Н., Хэмпсон Л., Хэмпсон И. Н., Шимамото А., Фуруичи Ю., Окумура К., Нива С., Тая Ю., Хара Е. (ноябрь 1999 г.). «Регулирование активности CDK4 с помощью нового CDK4-связывающего белка, p34 (SEI-1)». Гены и развитие. 13 (22): 3027–33. Дои:10.1101 / gad.13.22.3027. ЧВК 317153. PMID 10580009.
- ^ Юинг Р.М., Чу П., Элизма Ф., Ли Х., Тейлор П., Клими С. и др. (2007). «Крупномасштабное картирование белок-белковых взаимодействий человека с помощью масс-спектрометрии». Молекулярная системная биология. 3: 89. Дои:10.1038 / msb4100134. ЧВК 1847948. PMID 17353931.
- ^ а б Fåhraeus R, Paramio JM, Ball KL, Laín S, Lane DP (январь 1996 г.). «Ингибирование фосфорилирования pRb и прогрессирования клеточного цикла пептидом из 20 остатков, полученным из p16CDKN2 / INK4A» (PDF). Текущая биология. 6 (1): 84–91. Дои:10.1016 / S0960-9822 (02) 00425-6. PMID 8805225. S2CID 23024663.
- ^ Коулман К.Г., Уотлет Б.С., Моррисси Д., Малхерон Дж., Седман С.А., Бринкли П., Прайс С., Вебстер К.Р. (июль 1997 г.). «Идентификация последовательностей CDK4, участвующих в связывании циклина D1 и p16». Журнал биологической химии. 272 (30): 18869–74. Дои:10.1074 / jbc.272.30.18869. PMID 9228064.
- ^ Руссо А.А., Тонг Л., Ли Джо, Джеффри П.Д., Павлетич Н.П. (сентябрь 1998 г.). «Структурная основа для ингибирования циклин-зависимой киназы Cdk6 опухолевым супрессором p16INK4a». Природа. 395 (6699): 237–43. Дои:10.1038/26155. PMID 9751050. S2CID 204997058.
- ^ Калдис П., Ояла П.М., Тонг Л., Мякеля Т.П., Соломон М.Дж. (декабрь 2001 г.). «САК-независимая активация CDK6 вирусным циклином». Молекулярная биология клетки. 12 (12): 3987–99. Дои:10.1091 / mbc.12.12.3987. ЧВК 60770. PMID 11739795.
- ^ а б Иванчук С.М., Мондал С, Рутка Ю.Т. (июнь 2008 г.). «p14ARF взаимодействует с DAXX: влияет на HDM2 и p53». Клеточный цикл. 7 (12): 1836–50. Дои:10.4161 / cc.7.12.6025. PMID 18583933.
- ^ а б Ризос Х., Дифенбах Э., Бадхвар П., Вудрафф С., Беккер TM, Руни Р.Дж., Кеффорд РФ (февраль 2003 г.). «Ассоциация p14ARF с репрессором транскрипции p120E4F усиливает ингибирование клеточного цикла». Журнал биологической химии. 278 (7): 4981–9. Дои:10.1074 / jbc.M210978200. PMID 12446718.
- ^ а б c Чжан Ю., Вольф Г. В., Бхат К., Джин А., Аллио Т., Буркхарт В. А., Сюн Ю. (декабрь 2003 г.). «Рибосомный белок L11 отрицательно регулирует онкопротеин MDM2 и опосредует p53-зависимый путь контрольной точки рибосомного стресса». Молекулярная и клеточная биология. 23 (23): 8902–12. Дои:10.1128 / MCB.23.23.8902-8912.2003. ЧВК 262682. PMID 14612427.
- ^ а б Чжан Ю., Сюн Ю., Ярбро В.Г. (март 1998 г.). «ARF способствует деградации MDM2 и стабилизирует p53: делеция локуса ARF-INK4a нарушает пути подавления опухоли Rb и p53». Клетка. 92 (6): 725–34. Дои:10.1016 / S0092-8674 (00) 81401-4. PMID 9529249. S2CID 334187.
- ^ Кларк П.А., Льянос С., Петерс Г. (июль 2002 г.). «Множественные взаимодействующие домены способствуют опосредованному p14ARF ингибированию MDM2». Онкоген. 21 (29): 4498–507. Дои:10.1038 / sj.onc.1205558. PMID 12085228.
- ^ Померанц Дж., Шрайбер-Агус Н., Льежуа Нью-Джерси, Сильверман А., Алланд Л., Чин Л., Потес Дж., Чен К., Орлоу И., Ли Х. В., Кордон-Кардо C, ДеПиньо РА (март 1998 г.). «Продукт гена-супрессора опухоли Ink4a, p19Arf, взаимодействует с MDM2 и нейтрализует ингибирование p53 MDM2». Клетка. 92 (6): 713–23. Дои:10.1016 / S0092-8674 (00) 81400-2. PMID 9529248. S2CID 17190271.
- ^ Vivo M, Calogero RA, Sansone F, Calabrò V, Parisi T, Borrelli L, Saviozzi S, La Mantia G (апрель 2001 г.). «Человеческий опухолевый супрессор arf взаимодействует со спинофилином / нейрабином II, белком, связывающим протеин-фосфатазу 1 типа». Журнал биологической химии. 276 (17): 14161–9. Дои:10.1074 / jbc.M006845200. PMID 11278317.
внешняя ссылка
- Гены, + p16 в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- CDKN2A расположение человеческого гена в Браузер генома UCSC.
- CDKN2A детали человеческого гена в Браузер генома UCSC.