Анталармин - Antalarmin
 | |
| Клинические данные | |
|---|---|
| Другие имена | Анталармин |
| Код УВД |
|
| Легальное положение | |
| Легальное положение |
|
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| ChemSpider | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| Химические и физические данные | |
| Формула | C24ЧАС34N4 |
| Молярная масса | 378.564 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| (проверять) | |
Анталармин (CP-156,181) это препарат, который действует как CRH1 антагонист.
Кортикотропин-рилизинг-гормон (CRH), также известный как Кортикотропин-рилизинг-фактор, представляет собой эндогенный пептидный гормон, высвобождающийся в ответ на различные триггеры, такие как хронический стресс и наркомания. Такие триггеры приводят к высвобождению кортикотропин (АКТГ), еще один гормон, участвующий в физиологической реакции на стресс. Считается, что хроническое высвобождение CRH и ACTH прямо или косвенно участвует во многих вредных физиологических эффектах хронического стресса, таких как чрезмерное глюкокортикоид релиз, язва желудка, беспокойство, сахарный диабет, остеопороз, депрессия, и развитие высокое кровяное давление и последующие сердечно-сосудистые проблемы.[1]
Анталармин - это непептидный препарат, который блокирует рецептор CRH1 и, как следствие, снижает высвобождение АКТГ в ответ на хронический стресс.[2] Это было продемонстрировано на животных, чтобы уменьшить поведенческие реакции на стрессовые ситуации,[3] и предполагается, что сам Анталармин или, что более вероятно, новые препараты-антагонисты CRH1 все еще находятся в стадии разработки,[4] может быть полезным для уменьшения неблагоприятных последствий для здоровья хронического стресса у людей, а также для возможного использования при лечении таких состояний, как тревога, депрессия и наркомания.[5]
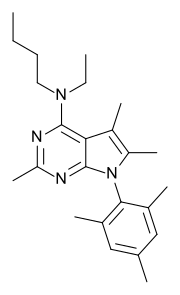
Химическая структура
Синтез CP-154,526, непептидного антагониста рецептора CRH1, был впервые описан в 1997 году.[6] Анталармин, или CP-156,181, является близким аналогом, который очень похож по структуре и, как было показано, легче синтезировать.[2] Результаты нескольких химических, фармакокинетических и фармакологических исследований показывают, что эти два соединения обладают очень схожими свойствами.

Механизм действия
Связывание рецептора
Как показано в таблице 1, Аденилилциклаза и лагерь Анализы использовались в различных функциональных исследованиях для определения степени ингибирования цАМФ двумя антагонистами рецептора CRH1: анталармином и CP-154 526.
| Ткань | Тип анализа | Сложный | Параметр |
|---|---|---|---|
| SH-SY5Y человека (нейробластома) | лагерь | Анталармин | pKb = 9.19 [7] |
| Клетки Y79 человека (ретинобластома) | лагерь | Анталармин | IC50 = 0,8 нМ [8] |
| Человек SH-SY5Y | лагерь | CP-154 526 | pKb = 7,76 [7] |
| Кора головного мозга крысы | Циклаз | CP-154 526 | Ki = 3,7 нМ [9] |
Несколько исследований связывания рецепторов показали, что Анталармин и CP-154 526 обладают высоким сродством к рецепторам CRH1 с очень похожими профилями. В таблице 2 показаны аффинности связывания каждого соединения в различных клеточных линиях.
| Ткань | Сложный | Ki (нМ) | IC50 (нМ) |
|---|---|---|---|
| Гипофиз крысы | Анталармин | 1.9 [2] | 0.04 [10] |
| Фронтальная кора головного мозга крысы | Анталармин | 1.4 [2] | |
| Клон человека | Анталармин | 6 [8] | 5 [10] |
| Гипофиз крысы | CP-154 526 | 1.4 [9] | |
| Кора головного мозга крысы | CP-154 526 | 5.7 [9] | |
| Клон человека | CP-154 526 | 10 [11] |
Фармакокинетика (ADME)
Фармакокинетика CP-154 526, близкий аналог анталармина, были исследованы на самцах крыс Sprauge-Dawley с помощью внутривенный (i.v.) и устный (p.o.) маршруты.[12] После введения 5 мг / кг (в / в) СР-154,526 концентрации лекарства со временем снижались на двухфазную величину. CP-154,526 также продемонстрировал большой объем распределения (Vd) при 6,7 л / кг, что указывает на обширное связывание лекарственного средства с тканью у крыс Sprauge-Dawley. Плазменный клиренс 82 мл / мин / кг наблюдался с расчетным периодом полувыведения 1,5 часа. После п.о. введение в дозе 10 мг / кг, средняя пиковая концентрация в плазме (Cmax ) 367 нг / мл было определено в течение 0,5-1 часа после введения. Устный биодоступность был рассчитан на 37%, в результате чего предполагаемый печеночный клиренс составил 63%.[12]
У самцов крыс Wistar, получавших дозу 5 мг / кг (перорально) СР-154,526, была определена пероральная биодоступность 27% и высокий объем распределения 105 л / кг с расчетным общим клиренсом (CLt ) 36 мл / мин / кг. Также наблюдалось, что CP-154,526 пересекает гематоэнцефалический барьер с хорошей пенетрантностью при соотношении мозг: плазма 2,5 через 8 часов после перорального приема.[13] Обширное фармакокинетическое исследование анталармина, проведенное на макаках, показало, что пероральная биодоступность составляет 19%, общий клиренс составляет 4,5 л / час / кг, а период полувыведения составляет 7,8 часов после приема 20 мг / кг (перорально). Эта же доза также привела к средним уровням анталармина в плазме 76 нг / мл и уровням CSF 9,8 нг / мл через 3 часа после введения.[14]
В пробирке и В естественных условиях Исследование
Результаты до сих пор имели ограниченный успех: тестировались различные антагонисты CRF, которые показали некоторые антидепрессивные эффекты, но не дали эффекта, сравнимого с обычными антидепрессантами.[15] Однако более положительные результаты были получены при сочетании анталармина с антидепрессантом из группы СИОЗС, что свидетельствует о возможности синергического эффекта.[16] Обнадеживающие результаты также наблюдались при использовании Анталармина в качестве потенциального средства от беспокойства.[17][18] и гипертония, вызванная стрессом.[19]
Первоначальные исследования CP-154,526 показали, что соединение с высоким сродством связывается с кортикальными и гипофизарными рецепторами CRH у нескольких видов. Кроме того, системное введение СР-154,526 полностью антагонизирует эффекты экзогенного КРГ на уровни АКТГ, активируя клетки в голубое пятно и потенцирование страха на животных моделях.[9] Однако это сильнодействующее и селективное соединение продемонстрировало низкую биодоступность при пероральном приеме, а исследования in vitro с использованием микросом печени человека предсказывали высокий печеночный клиренс, считая соединение непригодным для клинической разработки. Тем не менее, многие исследователи продолжают изучать CP-154,526 и его близкие аналоги (например, анталармин), используя их в качестве инструментов для изучения физиологии рецепторов CRH и CRH, а также для определения потенциальной терапевтической ценности антагонистов CRH1 в некоторых ЦНС и периферических органах. расстройства.[20]
Стресс и тревога
Исследования in vitro, изучающие влияние антагонистов CRH1 на Гипотальмогипофиз надпочечников (HPA) ось показала, что анталармин ингибировал высвобождение АКТГ в клетках передней доли гипофиза крыс,[21] а также ингибирует синтез и высвобождение кортизола в клетках надпочечников человека.[22] яИсследования n vivo показали, что предварительная обработка крыс анталармином ингибировала повышение уровня АКТГ в плазме после инъекции CRH (в / в), не влияя на исходные уровни.[2] Однако другое исследование показало, что 8-недельный прием Анталармина дважды в день (i.p. ) у крыс значительно снизили базальные уровни АКТГ и кортикостерона, что привело к снижению чувствительности коры надпочечников к АКТГ.[23] Когда анталармин вводили приматам, он также подавлял повышение уровня АКТГ в плазме, а также предотвращал тревожную реакцию, вызванную социальным стрессором (например, появление другого самца в незнакомой среде).[14]
Что касается нейрохимических эффектов, то было показано, что анталармин ингибирует увеличение внеклеточного кортикального норадреналина, вызванное защемлением хвоста крысы.,[24] предполагая, что рецепторы CHR1 могут быть вовлечены в вызванное стрессом высвобождение норэпинефрина в коре головного мозга. Было также показано, что анталармин оказывает электрофизиологические эффекты, частично обращая ингибирование возбуждения нейронов в ядро дорсального шва что происходит после интрацеребровентрикулярный (i.c.v) введение CRH.[25]
Исследования с использованием антагонистов рецепторов CRH, таких как анталармин, на моделях тревожности показали, что эти агенты производят эффекты, подобные клинически эффективным анксиолитикам.[26][27] В моделях условного страха Анталармин уменьшал условное замораживание, предполагая, что он блокирует развитие и выражение условного страха, и вовлекает рецепторы CRH1 в оба процесса..[28] Пероральное введение анталармина (3–30 мг / кг) также значительно уменьшало неподвижность на модели поведенческого отчаяния на крысах с эффектами, аналогичными эффекту СИОЗС флуоксетин.[26][29]
Нейродегенерация
Также было показано, что CRH способствует нейродегенерация, предполагая, что антагонисты CRH1 могут оказывать нейропротекторное действие. PC12 клетки происходят из мозгового вещества надпочечников крысы и широко используются для изучения нейральной дифференцировки. Клетки PC12, обработанные CRH (1-10 нМ), показали повышенное количество апоптозных клеток и повышенную регуляцию Fas лиганд через стр.38 активации, демонстрируя проапоптотические эффекты CRH. Введение анталармина (10 нМ) полностью блокировало индуцированный CRH ответ апоптоза и подавляло экспрессию лиганда Fas.[30]
Воспаление
Анталармин также широко использовался для изучения роли CRH в воспалении. Внутрибрюшинный (i.p.) введение анталармина крысам значительно подавляло воспаление, вызванное подкожным введением каррагинан (известная воспалительная пищевая добавка), измеренная по концентрации лейкоцитов.[2] В модели активации тучных клеток кожи крыс предварительная обработка анталармином (10 мг / кг, в / в) ингибировала индуцированную CRH индукцию дегрануляции тучных клеток.,[31] предполагая провоспалительные свойства CRH. Анталармин также блокировал проницаемость сосудов и реакцию дегрануляции тучных клеток, вызванную внутрикожным введением. Урокортин (10 нМ).[31] В совокупности эти результаты указывают на то, что во время стресса CRH приводит к активации тучных клеток кожи через рецептор CRH1, который запускает расширение сосудов и увеличивает проницаемость сосудов.
Хроническое лечение анталармином также показало противовоспалительное действие и было предложено как имеющее потенциальное применение при лечении воспалительных состояний, таких как артрит,[32] а также язвы желудочно-кишечного тракта, вызванные стрессом[33] и синдром раздраженного кишечника.[34][35]
Зависимость
Смешанные результаты были замечены в исследованиях использования анталармина и других антагонистов CRF-1 при лечении наркозависимых расстройств. Испытания Анталармина на употребление кокаина на обезьянах, страдающих кокаиновой зависимостью, показали лишь незначительное сокращение употребления, которое не было статистически значимым.[36] однако в тестах на крысах, зависимых от кокаина, Анталармин действительно предотвращал повышение дозы при длительном применении, предполагая, что он может стабилизировать употребление кокаина и предотвратить его увеличение с течением времени, хотя и без последовательного его снижения.[37]
Анталармин также показал положительные эффекты в снижении синдрома отмены от хронического употребления опиоидов,[38] и значительно уменьшило самостоятельное введение этанола грызунам, зависимым от этанола.[39][40][41]
В целом, необходимы дополнительные исследования для определения терапевтической эффективности анталармина и других непептидных антагонистов CRH при тревоге, депрессии, воспалении, нейродегенеративных заболеваниях и зависимости.[20]
Смотрите также
Рекомендации
- ^ Зумакис Э., Райс К.С., Gold PW, Chrousos GP (ноябрь 2006 г.). «Возможное использование антагонистов кортикотропин-рилизинг-гормона». Летопись Нью-Йоркской академии наук. 1083 (1): 239–51. Bibcode:2006НЯСА1083..239Z. Дои:10.1196 / летопись.1367.021. PMID 17148743.
- ^ а б c d е ж Webster EL, Lewis DB, Torpy DJ, Zachman EK, Rice KC, Chrousos GP (декабрь 1996 г.). «Исследование in vivo и in vitro анталармина, непептидного антагониста рецептора кортикотропин-рилизинг-гормона (CRH): подавление высвобождения АКТГ гипофизом и периферическое воспаление». Эндокринология. 137 (12): 5747–50. Дои:10.1210 / endo.137.12.8940412. PMID 8940412.
- ^ Деак Т., Нгуен К.Т., Эрлих А.Л., Уоткинс Л.Р., Спенсер Р.Л., Майер С.Ф. и др. (Январь 1999 г.). «Влияние непептидного антагониста рилизинг-гормона кортикотропина анталармина на поведенческие и эндокринные реакции на стресс». Эндокринология. 140 (1): 79–86. Дои:10.1210 / эндо.140.1.6415. PMID 9886810.
- ^ Нильсен Д.М., Кэри Г.Дж., Gold LH (сентябрь 2004 г.). «Антидепрессант-подобная активность антагонистов рецептора кортикотропин-рилизинг-фактора типа 1 у мышей». Европейский журнал фармакологии. 499 (1–2): 135–46. Дои:10.1016 / j.ejphar.2004.07.091. PMID 15363960.
- ^ Маккарти-младший, Хайнрихс СК, Григориадис Д.Е. (май 1999 г.). «Последние достижения в области рецептора CRF1: разработка низкомолекулярных ингибиторов, подтипы рецепторов и клинические показания». Текущий фармацевтический дизайн. 5 (5): 289–315. PMID 10213797.
- ^ Чен Ю.Л., Мансбах Р.С., Винтер С.М., Брукс Э., Коллинз Дж., Корман М.Л. и др. (Май 1997 г.). «Синтез и пероральная эффективность 4- (бутилэтиламино) пирроло [2,3-d] пиримидина: центрально-активный антагонист рецептора рилизинг-фактора 1 кортикотропина». Журнал медицинской химии. 40 (11): 1749–54. Дои:10.1021 / jm960861b. PMID 9171885.
- ^ а б Шеффтер П., Фейербах Д., Бобирнак И., Гази Л., Лонгато Р. (1999). «Функциональная, эндогенно экспрессируемая экспрессия рецептора рилизинг-фактора кортикотропина типа 1 (CRF1) и мРНК рецептора CRF1 в клетках нейробластомы человека SH-SY5Y». Фундаментальная и клиническая фармакология. 13 (4): 484–9. Дои:10.1111 / j.1472-8206.1999.tb00007.x. PMID 10456290.
- ^ а б Овраг Д., Геслин М., Серва Л., Фонтейн Е., Роджер П., Лэр С. и др. (Апрель 2002 г.). "4- (2-Хлор-4-метокси-5-метилфенил) -N - [(1S) -2-циклопропил-1- (3-фтор-4-метилфенил) этил] 5-метил-N- (2- пропинил) -1,3-тиазол-2-амина гидрохлорид (SSR125543A): мощный и селективный антагонист рецептора рилизинг-фактора кортикотропина (1). I. Биохимическая и фармакологическая характеристика ". Журнал фармакологии и экспериментальной терапии. 301 (1): 322–32. Дои:10.1124 / jpet.301.1.322. PMID 11907190.
- ^ а б c d Schulz DW, Mansbach RS, Sprouse J, Braselton JP, Collins J, Corman M и др. (Сентябрь 1996 г.). «CP-154,526: мощный и селективный непептидный антагонист рецепторов рилизинг-фактора кортикотропина». Труды Национальной академии наук Соединенных Штатов Америки. 93 (19): 10477–82. Bibcode:1996PNAS ... 9310477S. Дои:10.1073 / пнас.93.19.10477. ЧВК 38410. PMID 8816826.
- ^ а б Лундквист Дж., Чай З., Тегеранский Р., Хасанван Х., Бартфай Т., Дженк Ф. и др. (Август 1996 г.). «Непептидный антагонист рецептора рилизинг-фактора кортикотропина снижает жар и проявляет анксиолитическую активность». Европейский журнал фармакологии. 309 (2): 195–200. Дои:10.1016/0014-2999(96)00337-8. PMID 8874139.
- ^ Gottowik J, Goetschy V, Henriot S, Kitas E, Fluhman B, Clerc RG и др. (Октябрь 1997 г.). «Мечение рецепторов CRF1 и CRF2 с использованием нового радиолиганда, [3H] -урокортина». Нейрофармакология. 36 (10): 1439–46. Дои:10.1016 / S0028-3908 (97) 00098-1. PMID 9423932.
- ^ а б Чен Ю.Л., Мансбах Р.С., Винтер С.М., Брукс Э., Коллинз Дж., Корман М.Л. и др. (Май 1997 г.). «Синтез и пероральная эффективность 4- (бутилэтиламино) пирроло [2,3-d] пиримидина: центрально активный антагонист рецептора рилизинг-фактора 1 кортикотропина». Журнал медицинской химии. 40 (11): 1749–54. Дои:10.1021 / jm960861b. PMID 9171885.
- ^ Келлер С., Брюлизауэр А., Лемер М., Энц А. (февраль 2002 г.). «Фармакокинетика мозга непептидного антагониста рецептора рилизинг-фактора кортикотропина». Метаболизм и утилизация лекарств. 30 (2): 173–6. Дои:10.1124 / dmd.30.2.173. PMID 11792687.
- ^ а б Habib KE, Weld KP, Rice KC, Pushkas J, Champoux M, Listwak S и др. (Май 2000 г.). «Пероральное введение антагониста рецепторов кортикотропин-рилизинг-гормона значительно ослабляет поведенческие, нейроэндокринные и вегетативные реакции на стресс у приматов». Труды Национальной академии наук Соединенных Штатов Америки. 97 (11): 6079–84. Bibcode:2000PNAS ... 97.6079H. Дои:10.1073 / pnas.97.11.6079. ЧВК 18561. PMID 10823952.
- ^ Юткевич Е.М., Вуд С.К., Хушьяр Х., Синь Л.В., Райс К.С., Вудс Дж. Х. (июль 2005 г.). «Влияние антагонистов CRF, анталармина, CP154,526, LWH234 и R121919, в тесте принудительного плавания и на вызванное плаванием повышение адренокортикотропина у крыс». Психофармакология. 180 (2): 215–23. Дои:10.1007 / s00213-005-2164-z. ЧВК 1315297. PMID 15696320.
- ^ Ducottet C, Griebel G, Belzung C (июнь 2003 г.). «Эффекты селективного непептидного антагониста рецептора 1 рилизинг-фактора кортикотропина анталармина в модели хронического легкого стресса депрессии у мышей». Прогресс в нейропсихофармакологии и биологической психиатрии. 27 (4): 625–31. Дои:10.1016 / S0278-5846 (03) 00051-4. PMID 12787849.
- ^ Zorrilla EP, Valdez GR, Nozulak J, Koob GF, Markou A (октябрь 2002 г.). «Эффекты анталармина, антагониста рецептора CRF типа 1, на тревожное поведение и моторную активацию у крыс». Исследование мозга. 952 (2): 188–99. Дои:10.1016 / S0006-8993 (02) 03189-X. PMID 12376179.
- ^ Habib KE, Weld KP, Rice KC, Pushkas J, Champoux M, Listwak S и др. (Май 2000 г.). «Пероральное введение антагониста рецепторов кортикотропин-рилизинг-гормона значительно ослабляет поведенческие, нейроэндокринные и вегетативные реакции на стресс у приматов». Труды Национальной академии наук Соединенных Штатов Америки. 97 (11): 6079–84. Bibcode:2000PNAS ... 97.6079H. Дои:10.1073 / пнас.97.11.6079. ЧВК 18561. PMID 10823952.
- ^ Briscoe RJ, Cabrera CL, Baird TJ, Rice KC, Woods JH (октябрь 2000 г.). «Анталарминная блокада артериальной гипертензии, вызванной рилизинг-гормоном кортикотропина, у крыс». Исследование мозга. 881 (2): 204–7. Дои:10.1016 / S0006-8993 (00) 02742-6. PMID 11036160.
- ^ а б Сеймур PA, Schmidt AW, Schulz DW (2003). «Фармакология CP-154,526, непептидного антагониста рецептора CRH1: обзор». Обзоры препаратов для ЦНС. 9 (1): 57–96. Дои:10.1111 / j.1527-3458.2003.tb00244.x. ЧВК 6741649. PMID 12595912.
- ^ Маккарти-младший, Хайнрихс СК, Григориадис Д.Е. (май 1999 г.). «Последние достижения в области рецептора CRF1: разработка низкомолекулярных ингибиторов, подтипы рецепторов и клинические показания». Текущий фармацевтический дизайн. 5 (5): 289–315. PMID 10213797.
- ^ Willenberg HS, Bornstein SR, Hiroi N, Päth G, Goretzki PE, Scherbaum WA, Chrousos GP (март 2000 г.). «Влияние нового антагониста рецептора кортикотропин-рилизинг-гормона типа I на функцию надпочечников человека». Молекулярная психиатрия. 5 (2): 137–41. Дои:10.1038 / sj.mp.4000720. PMID 10822340.
- ^ Wong ML, Webster EL, Spokes H, Phu P, Ehrhart-Bornstein M, Bornstein S и др. (1999). «Хроническое введение непептидного антагониста рецептора CRH типа 1 анталармина не притупляет ответы оси гипоталамус-гипофиз-надпочечники на острый иммобилизационный стресс». Науки о жизни. 65 (4): PL53-8. Дои:10.1016 / с0024-3205 (99) 00268-4. PMID 10421433.
- ^ Грибель Г., Симианд Дж., Стейнберг Р., Юнг М., Галли Д., Роджер П. и др. (Апрель 2002 г.). "4- (2-Хлор-4-метокси-5-метилфенил) -N - [(1S) -2-циклопропил-1- (3-фтор-4-метилфенил) этил] 5-метил-N- (2- пропинил) -1,3-тиазол-2-амина гидрохлорид (SSR125543A), мощный и селективный антагонист рецептора кортикотропин-рилизинг-фактора (1). II. Характеристика на грызунах, моделирующих расстройства, связанные со стрессом ». Журнал фармакологии и экспериментальной терапии. 301 (1): 333–45. Дои:10.1124 / jpet.301.1.333. PMID 11907191.
- ^ Кирби LG, Райс KC, Валентино RJ (февраль 2000 г.). «Влияние фактора высвобождения кортикотропина на активность нейронов в серотонинергическом ядре дорсального шва». Нейропсихофармакология. 22 (2): 148–62. Дои:10.1016 / S0893-133X (99) 00093-7. PMID 10649828.
- ^ а б Грибель Г. (апрель 1999 г.). «Есть ли будущее у лигандов нейропептидных рецепторов в лечении тревожных расстройств?». Фармакология и терапия. 82 (1): 1–61. Дои:10.1016 / S0163-7258 (98) 00041-2. PMID 10341356.
- ^ Бриттон К. Т., Ли Дж., Вэйл В., Ривье Дж., Куб Г. Ф. (март 1986 г.). «Антагонист рецептора рилизинг-фактора кортикотропина (CRF) блокирует активирующее и« анксиогенное »действие CRF у крыс». Исследование мозга. 369 (1–2): 303–6. Дои:10.1016/0006-8993(86)90539-1. PMID 3008937.
- ^ Деак Т., Нгуен К.Т., Эрлих А.Л., Уоткинс Л.Р., Спенсер Р.Л., Майер С.Ф. и др. (Январь 1999 г.). «Влияние непептидного антагониста рилизинг-гормона кортикотропина анталармина на поведенческие и эндокринные реакции на стресс». Эндокринология. 140 (1): 79–86. Дои:10.1210 / эндо.140.1.6415. PMID 9886810.
- ^ Порсолт Р.Д., Бертен А., Джалфр М. (октябрь 1977 г.). «Поведенческое отчаяние у мышей: первичный скрининговый тест на антидепрессанты». Archives Internationales de Pharmacodynamie et de Therapie. 229 (2): 327–36. PMID 596982.
- ^ Дермитзаки Э., Цацанис Ц., Граванис А., Маргиорис А.Н. (апрель 2002 г.). «Кортикотропин-рилизинг-гормон индуцирует продукцию лиганда Fas и апоптоз в клетках PC12 посредством активации митоген-активируемой протеинкиназы p38». Журнал биологической химии. 277 (14): 12280–7. Дои:10.1074 / jbc.M111236200. PMID 11790788.
- ^ а б Теохаридес Т.С., Сингх Л.К., Бушер В., Панг Х, Летурно Р., Вебстер Е., Хрусос Г. (январь 1998 г.). «Кортикотропин-рилизинг-гормон вызывает дегрануляцию тучных клеток кожи и увеличивает проницаемость сосудов, что является возможным объяснением его провоспалительных эффектов». Эндокринология. 139 (1): 403–13. Дои:10.1210 / эндо.139.1.5660. PMID 9421440.
- ^ Webster EL, Barrientos RM, Contoreggi C, Isaac MG, Ligier S, Gabry KE и др. (Июнь 2002 г.). «Антагонист рилизинг-гормона кортикотропина (CRH) ослабляет индуцированный адъювантом артрит: роль CRH в периферическом воспалении». Журнал ревматологии. 29 (6): 1252–61. PMID 12064844.
- ^ Габри К.Э., Хрусос Г.П., Райс К.С., Мостафа Р.М., Штернберг Э., Неграо А.Б. и др. (2002). «Заметное подавление ульцерогенеза желудка и ответов кишечника на стресс с помощью нового класса лекарств». Молекулярная психиатрия. 7 (5): 474–83, 433. Дои:10.1038 / sj.mp.4001031. PMID 12082565.
- ^ Гринвуд-Ван Меервельд Б., Джонсон А.С., Кокрейн С., Шулкин Дж., Майерс Д.А. (июнь 2005 г.). «Механизмы, опосредованные рецептором рилизинг-фактора 1 кортикотропина, подавляют гиперчувствительность толстой кишки у крыс». Нейрогастроэнтерология и моторика. 17 (3): 415–22. Дои:10.1111 / j.1365-2982.2005.00648.x. PMID 15916629.
- ^ Мартинес В., Таше И (2006). «Рецепторы CRF1 как терапевтическая мишень для синдрома раздраженного кишечника». Текущий фармацевтический дизайн. 12 (31): 4071–88. Дои:10.2174/138161206778743637. PMID 17100612.
- ^ Мелло Н.К., Негус СС, Райс К.С., Мендельсон Дж. Х. (декабрь 2006 г.). «Эффекты антагониста CRF1 анталармина на самоуправление кокаина и дискриминацию у макак-резусов». Фармакология, биохимия и поведение. 85 (4): 744–51. Дои:10.1016 / j.pbb.2006.11.008. PMID 17182090.
- ^ Specio SE, Wee S, O'Dell LE, Boutrel B, Zorrilla EP, Koob GF (февраль 2008 г.). «Антагонисты рецептора CRF (1) ослабляют повышенное самовведение кокаина у крыс». Психофармакология. 196 (3): 473–82. Дои:10.1007 / s00213-007-0983-9. ЧВК 2769571. PMID 17965976.
- ^ Stinus L, Cador M, Zorrilla EP, Koob GF (январь 2005 г.). «Бупренорфин и антагонист CRF1 блокируют приобретение у крыс обусловленного отменой опиатов условного отвращения к месту». Нейропсихофармакология. 30 (1): 90–8. Дои:10.1038 / sj.npp.1300487. PMID 15138444.
- ^ Funk CK, Zorrilla EP, Lee MJ, Rice KC, Koob GF (январь 2007 г.). «Антагонисты кортикотропин-рилизинг фактора 1 избирательно снижают самовведение этанола у этанолзависимых крыс». Биологическая психиатрия. 61 (1): 78–86. Дои:10.1016 / j.biopsych.2006.03.063. ЧВК 2741496. PMID 16876134.
- ^ Чу К., Куб Г.Ф., Коул М., Зоррилла Е.П., Робертс А.Дж. (апрель 2007 г.). «Вызванное зависимостью увеличение самовведения этанола у мышей блокируется антагонистом рецептора CRF1 анталармином и нокаутом рецептора CRF1». Фармакология, биохимия и поведение. 86 (4): 813–21. Дои:10.1016 / j.pbb.2007.03.009. ЧВК 2170886. PMID 17482248.
- ^ Маринелли П. У., Фанк Д., Юзитч В., Хардинг С., Райс К. К., Шахам Ю., Ле А. Д. (декабрь 2007 г.). «Антагонист рецептора CRF1, анталармин, ослабляет вызванное йохимбином увеличение самоуправления оперантного алкоголя и возобновление поиска алкоголя у крыс». Психофармакология. 195 (3): 345–55. Дои:10.1007 / s00213-007-0905-x. PMID 17705061.
