Орексин - Orexin
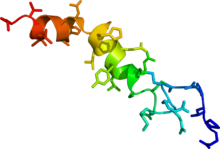
| Препроорексин | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| Идентификаторы | |||||||||
| Символ | Орексин | ||||||||
| Pfam | PF02072 | ||||||||
| ИнтерПро | IPR001704 | ||||||||
| SCOP2 | 1cq0 / Объем / СУПФАМ | ||||||||
| OPM суперсемейство | 145 | ||||||||
| Белок OPM | 1wso | ||||||||
| |||||||||
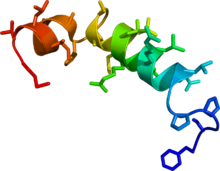
| орексин (гипокретин) нейропептид-предшественник | |||||||
|---|---|---|---|---|---|---|---|
 | |||||||
| Идентификаторы | |||||||
| Символ | HCRT | ||||||
| Альт. символы | PPOX, OX | ||||||
| Ген NCBI | 3060 | ||||||
| HGNC | 4847 | ||||||
| OMIM | 602358 | ||||||
| RefSeq | NM_001524 | ||||||
| UniProt | O43612 | ||||||
| Прочие данные | |||||||
| Locus | Chr. 17 q21 | ||||||
| |||||||
Орексин (/ɒˈрɛksɪп/), также известный как гипокретин, это нейропептид что регулирует возбуждение, бодрствование, и аппетит.[1] Наименее распространенная форма нарколепсия, тип 1, при котором пациент испытывает кратковременную потерю мышечного тонуса (катаплексия ), вызвано нехваткой орексина в головном мозге из-за разрушения клеток, которые его производят.[2][3]
Есть только 10 000–20 000 производящих орексин. нейроны в человеческом мозгу,[2] расположены преимущественно в районе Калифорнии и боковой гипоталамус.[1][4] Они широко распространяются по центральной нервной системе, регулируя бодрствование, кормление и другие формы поведения.[1] Есть два типа орексина пептид и два типа орексина рецептор.[5][4]
Орексин был открыт в 1998 году почти одновременно двумя независимыми группами исследователей, работающими над крыса мозг.[6][7] Одна группа назвала это орексин, из орексис означает «аппетит» по-гречески; другая группа назвала это гипокретин, потому что он производится в гипоталамус и имеет слабое сходство с секретин, еще один пептид.[2] Официально, гипокретин (HCRT) используется для обозначения гены и стенограммы, пока орексин используется для обозначения закодированного пептиды.[8] Между системой орексина в мозге крысы и мозгом человека существует большое сродство.[5]
Открытие
В 1998 году почти одновременно были опубликованы отчеты об открытии орексина / гипокретина. Луис де Леса, Томас Килдафф, и его коллеги сообщили об открытии системы гипокретина одновременно с Такеши Сакураи из Масаси Янагисава лаборатория в Юго-западный медицинский центр Техасского университета в Далласе сообщил об открытии орексины отражать орексигенную (стимулирующую аппетит) активность этих пептидов. В своей статье 1998 года, описывающей эти нейропептиды, они также сообщили об открытии двух рецепторов орексина, получивших название OX1R и OX2Р.[6]
Обе группы также использовали разные подходы к своему открытию. Одна команда была заинтересована в поиске новых генов, которые экспрессировались в гипоталамусе. В 1996 году ученые из Научно-исследовательский институт Скриппса сообщили об открытии нескольких генов в мозге крысы, в том числе одного, которого они назвали «клоном 35». Их работа показала, что экспрессия клона 35 ограничена латеральным гипоталамусом.[9] Они извлекли селективную ДНК, обнаруженную в боковом гипоталамусе. Они клонировали эту ДНК и изучили ее с помощью электронной микроскопии. Нейротрансмиттеры, обнаруженные в этой области, были странно похожи на гормон кишечника секретин, член инкретин семейство, поэтому они назвали гипокретином, чтобы обозначить гипоталамический член семейства инкретинов.[10] Первоначально считалось, что эти клетки находятся и работают только в боковой области гипоталамуса, но методы иммуноцитохимии показали, что эта область действительно имеет различные проекции на другие части мозга. Большинство этих проекций достигали лимбической системы и связанных с ней структур (включая миндалину, перегородку и базальную область переднего мозга).
С другой стороны, Сакураи и его коллеги изучали систему орексинов как сиротские рецепторы. С этой целью они использовали трансгенные клеточные линии, которые экспрессировали отдельные орфанные рецепторы, а затем подвергали их воздействию различных потенциальных лигандов. Они обнаружили, что пептиды орексина активировали клетки, экспрессирующие рецепторы орексина, и продолжили обнаружение экспрессии пептида орексина именно в гипоталамусе. Кроме того, когда крысам вводили любой из пептидов орексина, это стимулировало кормление, что дало название «орексин».[6]
Номенклатура системы орексин / гипокретин теперь учитывает историю ее открытия. «Гипокретин» относится к гену или генетическим продуктам, а «орексин» относится к белку, что отражает различные подходы, которые привели к его открытию. Использование обоих терминов также является практической необходимостью, поскольку "HCRT" является стандартным символом гена в таких базах данных, как GenBank и «OX» используется для обозначения фармакологии пептидной системы Международный союз фундаментальной и клинической фармакологии.[8]
Изоформы
Есть два типа орексина: орексин-А и -B (гипокретин-1 и -2).[11] Они возбуждающие нейропептиды с приблизительно 50% идентичностью последовательности, полученной расщеплением одного белка-предшественника.[11] Орексин-A состоит из 33 аминокислотных остатков и имеет два внутрицепочечных дисульфидные связи; орексин-B представляет собой линейный пептид из 28 аминокислотных остатков.[11] Хотя эти пептиды продуцируются очень небольшой популяцией клеток в латеральном и заднем отделах. гипоталамус, они посылают проекции по всему мозгу. Пептиды орексина связываются с двумя Связанный с G-белком рецепторы орексина, OX1 и OX2, со связыванием орексина-A как с OX1 и OX2 примерно с равным сродством, в то время как орексин-B связывается в основном с OX2 и в 5 раз менее эффективен на OX1.[12]
Орексины - это строго консервативные пептиды, обнаруженные у всех основных классов позвоночных.[13]
Функция
Первоначально предполагалось, что система орексина в первую очередь участвует в стимуляции приема пищи, на основании открытия, что центральное введение орексина-A и -B увеличивает потребление пищи. Кроме того, он стимулирует бодрствование, регулирует энергия расход и модулирует висцеральную функцию.
Активация бурого жира
Многие исследования подтверждают, что нейроны орексина регулируют коричневая жировая ткань (BAT) активность через симпатическую нервную систему для увеличения расхода энергии.[14][15]Хотя орексин нокаутные мыши сообщалось о недоразвитии коричневая жировая ткань (ЛЕТУЧАЯ МЫШЬ),[16] последующий отчет показал нормальное развитие НДТ.[17]
Бодрствование
Орексин, кажется, способствует бодрствованию. Недавние исследования показывают, что основная роль системы орексинов заключается в интеграции метаболических, циркадных и недосыпание влияет на определение того, должно ли животное спать или бодрствовать и быть активным. Орексиновые нейроны сильно возбуждают различные ядра мозга, играющие важную роль в бодрствовании, включая дофамин, норэпинефрин, гистамин и ацетилхолин системы[18][19] и, по-видимому, играют важную роль в стабилизации бодрствования и сна.
Открытие того, что мутация рецептора орексина вызывает расстройство сна собачий нарколепсия[20] в Доберман-пинчер впоследствии указали на важную роль этой системы в спать регулирование. Сообщалось, что у мышей с генетическим нокаутом, лишенных гена орексина, наблюдалась нарколепсия.[21] Часто и быстро переходя между сном и бодрствованием, эти мыши проявляют многие симптомы нарколепсии. Исследователи используют эту животную модель нарколепсии для изучения болезни.[22] Нарколепсия приводит к повышенная дневная сонливость, неспособность закрепить бодрствование днем (и спать ночью), и катаплексия, то есть потеря мышечного тонуса в ответ на сильные, обычно положительные эмоции. У собак, у которых отсутствует функциональный рецептор орексина, наблюдается нарколепсия, в то время как животные и люди, у которых отсутствует сам нейропептид орексина, также страдают нарколепсией.
Центральное введение орексина-A сильно способствует бодрствованию, повышает температуру тела и движения, а также вызывает резкое увеличение расхода энергии. Недосыпание также увеличивает передачу орексина-А. Таким образом, система орексина может играть более важную роль в регулировании расхода энергии, чем прием пищи. Фактически, у пациентов с нарколепсией с дефицитом орексина ожирение увеличивается, а не уменьшается. ИМТ, как и следовало ожидать, если бы орексин был в первую очередь пептидом, стимулирующим аппетит. Другим признаком того, что дефицит орексина вызывает нарколепсию, является то, что лишение обезьян сна на 30–36 часов с последующим введением им нейрохимических веществ снижает когнитивные нарушения, обычно наблюдаемые при таком недосыпании.[23][24]
У людей нарколепсия связана с определенным вариантом человеческий лейкоцитарный антиген (HLA) комплекс.[25] Более того, полногеномный анализ показывает, что, помимо варианта HLA, нарколептики также обладают специфическим генетическим мутация в Т-клетка рецептор альфа-локус.[26] В сочетании эти генетические аномалии заставляют иммунную систему атаковать и убивать критические нейроны орексина. Следовательно, отсутствие продуцирующих орексин нейроны у нарколептиков может быть результатом аутоиммунный беспорядок.[27]
Прием пищи
Орексин увеличивает тягу к еде и коррелирует с функцией веществ, которые способствуют его выработке. Также показано, что орексин увеличивает размер еды, подавляя тормозную постингестивную обратную связь.[28] Однако некоторые исследования показывают, что стимулирующее действие орексина на кормление может быть связано с общим возбуждением, но не обязательно с увеличением общего потребления пищи.[29]
Результаты обзора показывают, что гипергликемия это происходит у мышей из-за привычной диеты с высоким содержанием жиров, что приводит к снижению передачи сигналов рецептором орексина-2, и эти рецепторы могут стать терапевтической мишенью в будущем.[30]
Лептин это гормон, вырабатываемый жировыми клетками, который действует как долгосрочное внутреннее средство измерения энергетического состояния. Грелин является кратковременным фактором, выделяемым желудком непосредственно перед ожидаемым приемом пищи, и сильно способствует приему пищи.
Недавно было показано, что клетки, продуцирующие орексин, ингибируются лептином (через путь рецептора лептина), но активируются грелином и гипогликемия (глюкоза подавляет выработку орексина). Орексин, по состоянию на 2007 год, считается очень важным связующим звеном между метаболизмом и регуляцией сна.[31][32] Такая взаимосвязь давно подозревалась на основании наблюдения, что длительное лишение сна у грызунов резко увеличивает потребление пищи и энергетический обмен, т. Е. катаболизм, со смертельным исходом в долгосрочной перспективе. Таким образом, недосыпание приводит к нехватке энергии. Чтобы восполнить эту нехватку энергии, многие люди употребляют продукты с высоким содержанием углеводов и жиров, что в конечном итоге может привести к ухудшению здоровья и увеличению веса. Другие пищевые питательные вещества, аминокислоты, также могут активировать нейроны орексина, и они могут подавлять глюкозный ответ нейронов орексина при физиологической концентрации, в результате чего энергетический баланс, который поддерживает орексин, нарушается.[33]
Зависимость
Предварительные исследования показали потенциал блокаторов орексина при лечении кокаина, опиоидов и алкоголь зависимость.[34][35][36] Например, лабораторные крысы Учитывая, что лекарства, нацеленные на систему орексина, потеряли интерес к алкоголю, несмотря на то, что им предоставили бесплатный доступ в экспериментах.[37][38]
Исследования участия орексина в никотиновой зависимости дали неоднозначные результаты. Например, блокирование рецептора орексина-1 селективным антагонист орексина SB-334,867 пониженный никотин самоуправление у крыс и курильщиков, пострадавших от островок область мозга, которая регулирует тягу и содержит рецепторы орексина-1, потеряла желание курить.[39] Однако другие исследования на крысах с использованием двойного антагониста рецепторов орексина TCS 1102 не обнаружили подобных эффектов.[40]
Липидный обмен
Недавно было продемонстрировано, что орексин-A (OXA) оказывает прямое влияние на один из аспектов липид метаболизм. ОКСА стимулирует глюкоза поглощение в 3T3-L1 адипоциты и что повышенное потребление энергии сохраняется в виде липидов (триацилглицерин ). Таким образом, OXA увеличивает липогенез. Он также подавляет липолиз и стимулирует секрецию адипонектин. Считается, что эти эффекты в основном передаются через PI3K пути, потому что этот ингибитор пути (LY294002) полностью блокирует эффекты OXA в адипоцитах.[41] Связь между ОКСА и метаболизмом липидов является новой и в настоящее время находится в стадии дополнительных исследований.
Настроение
Высокий уровень орексина-А ассоциируется у людей с ощущением счастья, а низкий - с печалью.[42] Открытие предполагает, что повышение уровня орексина-A может улучшить настроение у людей, что, таким образом, является возможным будущим лечением таких расстройств, как депрессия.
Орексиновые нейроны
Нейротрансмиттеры
Было показано, что орексинергические нейроны чувствительны к сигналам группы III. метаботропные рецепторы глутамата,[43] каннабиноидный рецептор 1 и CB1 – OX1 рецепторные гетеродимеры,[44][45][46] аденозин А1 рецепторы,[47] мускариновый M3 рецепторы,[48] серотонин 5-HT1А рецепторы,[49] нейропептид Y рецепторы,[50] рецепторы холецистокинина А,[51] и катехоламины,[52][53] а также грелин, лептин, и глюкоза.[54] Орексинергические нейроны сами регулируют высвобождение ацетилхолин,[55][56] серотонин, и норадреналин.[57]
Орексинергические нейроны можно разделить на две группы в зависимости от связности и функциональности. Орексинергические нейроны в боковой гипоталамический группы тесно связаны с функциями, связанными с вознаграждением, такими как предпочтение условного места. Эти нейроны преимущественно иннервируют вентральная тегментальная область и вентромедиальная префронтальная кора. В отличие от латеральных нейронов гипоталамуса перифорно-дорсальная группа орексинергических нейронов участвует в функциях, связанных с возбуждением и вегетативной реакцией. Эти нейроны проецируются межгипоталамически, а также в ствол мозга, где высвобождение орексина модулирует различные вегетативные процессы.[58][59]
Клиническое использование
Система орексин / гипокретин является мишенью для лечения бессонницы. суворексант, который работает, блокируя оба рецептора орексина. Суворексант прошел три испытания фазы III и был одобрен в 2014 г. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) после отказа в одобрении годом ранее.[60] это проданный в качестве Белсомра.[61]
В 2016 г. Научный центр здоровья Техасского университета зарегистрировали клиническое исследование применения суворексанта для людей с кокаиновая зависимость. Они планируют измерить реактивность, тревогу и стресс.[62]
Другое возможное использование
Интраназальный орексин способен улучшить познавательные способности у приматов, особенно в условиях недосыпания,[63] что может предоставить возможность лечения чрезмерной дневной сонливости.[64]
В исследовании сообщалось, что трансплантация нейронов орексина в мостик ретикулярная формация у крыс возможно, что указывает на разработку альтернативных терапевтических стратегий в дополнение к фармакологическим вмешательствам для лечения нарколепсии.[65]
Рекомендации
- ^ а б c Дэвис Дж. Ф., Чой Д. Л., Бенуа С. К. (2011). «24. Орексигенные гипоталамические пептиды, поведение и питание - орексин 24,5». В Preedy VR, Watson RR, Martin CR (ред.). Справочник по поведению, питанию и питанию. Springer. С. 361–2. ISBN 9780387922713.
- ^ а б c Стэнфордский центр нарколепсии Часто задаваемые вопросы (Дата обращения 27 марта 2012)
- ^ Sutcliffe JG, de Lecea L (октябрь 2000 г.). «Гипокретины: возбуждающие нейромодулирующие пептиды для множества гомеостатических систем, включая сон и питание». Журнал неврологических исследований. 62 (2): 161–8. Дои:10.1002 / 1097-4547 (20001015) 62: 2 <161 :: AID-JNR1> 3.0.CO; 2-1. PMID 11020209.
- ^ а б Маркус Дж. Н., Элмквист Дж. К. (2006). «3. Проекции орексина и локализация рецепторов орексина». В Nishino S, Sakurai T (ред.). Система орексин / гипокретин: физиология и патофизиология. Springer. п. 195. ISBN 9781592599509.
- ^ а б Boss C, Roch C (август 2015 г.). «Последние тенденции в исследованиях орексинов - с 2010 по 2015 годы». Письма по биоорганической и медицинской химии. 25 (15): 2875–87. Дои:10.1016 / j.bmcl.2015.05.012. PMID 26045032.
- ^ а б c Сакураи Т., Амемия А., Исии М., Мацузаки И., Чемелли Р.М., Танака Х., Уильямс С.К., Ричардсон Дж.А., Козловски Г.П., Уилсон С., Арч-младший, Бакингем Р.Э., Хейнс А.С., Карр С.А., Аннан Р.С., МакНалти Д.Е., Лю В.С. , Террет Дж. А., Эльшурбаджи Н. А., Бергсма Д. Д., Янагисава М. (февраль 1998 г.). «Орексины и рецепторы орексина: семейство нейропептидов гипоталамуса и рецепторов, связанных с G-белком, которые регулируют пищевое поведение». Клетка. 92 (4): 573–85. Дои:10.1016 / S0092-8674 (00) 80949-6. PMID 9491897. S2CID 16294729.
- ^ de Lecea L, Kilduff TS, Peyron C, Gao X, Foye PE, Danielson PE, Fukuhara C, Battenberg EL, Gautvik VT, Bartlett FS, Frankel WN, van den Pol AN, Bloom FE, Gautvik KM, Sutcliffe JG (январь 1998 г. ). «Гипокретины: гипоталамус-специфические пептиды с нейровозбуждающей активностью». Труды Национальной академии наук Соединенных Штатов Америки. 95 (1): 322–7. Дои:10.1073 / пнас.95.1.322. ЧВК 18213. PMID 9419374.
- ^ а б Готтер А.Л., Уэббер А.Л., Коулман П.Дж., Ренгер Дж.Дж., Уинроу С.Дж. (июль 2012 г.). "Международный союз фундаментальной и клинической фармакологии. LXXXVI. Функция рецептора орексина, номенклатура и фармакология". Фармакологические обзоры. 64 (3): 389–420. Дои:10.1124 / пр.111.005546. PMID 22759794. S2CID 2038246.
- ^ Гаутвик К.М., де Лесеа Л., Гаутвик В.Т., Дэниэлсон П.Е., Транк П., Допазо А., Блум Ф. Е., Сатклифф Дж. Г. (август 1996 г.). «Обзор наиболее распространенных мРНК, специфичных для гипоталамуса, по данным направленного вычитания ПЦР с метками». Труды Национальной академии наук Соединенных Штатов Америки. 93 (16): 8733–8. Дои:10.1073 / пнас.93.16.8733. ЧВК 38742. PMID 8710940.
- ^ Эбрагим И.О., Ховард Р.С., Копельман, доктор медицины, Шариф М.К., Уильямс А.Дж. (май 2002 г.). «Система гипокретин / орексин». Журнал Королевского медицинского общества. 95 (5): 227–30. Дои:10.1177/014107680209500503. ЧВК 1279673. PMID 11983761.
- ^ а б c Инуцука А., Яманака А. (2013). «Физиологическая роль нейронов орексина / гипокретина в регуляции сна / бодрствования и нейроэндокринных функций». Фронт-эндокринол (Лозанна). 4: 18. Дои:10.3389 / fendo.2013.00018. ЧВК 3589707. PMID 23508038.
- ^ Лэнгмид CJ, Джерман JC, Бро SJ, Скотт C, Портер Р.А., Хердон HJ (январь 2004 г.). «Характеристика связывания [3H] -SB-674042, нового непептидного антагониста, с рецептором орексина-1 человека». Британский журнал фармакологии. 141 (2): 340–6. Дои:10.1038 / sj.bjp.0705610. ЧВК 1574197. PMID 14691055.
- ^ Вонг К.К., Нг С.И., Ли Л.Т., Нг Г.К., Чоу Б.К. (апрель 2011 г.). «Орексины и их рецепторы от рыб к млекопитающим: сравнительный подход». Общая и сравнительная эндокринология. 171 (2): 124–30. Дои:10.1016 / j.ygcen.2011.01.001. PMID 21216246.
- ^ Мартинс Л., Сеоан-Колласо П., Контрерас С., Гонсалес-Гарсия I, Мартинес-Санчес Н., Гонсалес Ф., Зальвиде Дж., Гальего Р., Диегес С., Ногейрас Р., Тена-Семпере М., Лопес М. (август 2016 г.). «Функциональная связь между AMPK и орексином опосредует влияние BMP8B на энергетический баланс». Отчеты по ячейкам. 16 (8): 2231–42. Дои:10.1016 / j.celrep.2016.07.045. ЧВК 4999418. PMID 27524625.
- ^ Tupone D, Madden CJ, Cano G, Morrison SF (ноябрь 2011 г.). "Орексинергическая проекция от перифорниального гипоталамуса до бледного шва увеличивает термогенез коричневой жировой ткани крыс". Журнал неврологии. 31 (44): 15944–55. Дои:10.1523 / JNEUROSCI.3909-11.2011. ЧВК 3224674. PMID 22049437.
- ^ Селлайах Д., Бхарадж П., Сикдер Д. (октябрь 2011 г.). «Орексин необходим для развития, дифференциации и функционирования коричневой жировой ткани». Клеточный метаболизм. 14 (4): 478–90. Дои:10.1016 / j.cmet.2011.08.010. PMID 21982708.
- ^ Какидзаки М., Цунэока Й, Такасе К., Ким С.Дж., Чой Дж., Иккю А., Абэ М., Сакимура К., Янагисава М., Фунато Х. (сентябрь 2019 г.). «Дифференциальная роль каждого сигнального рецептора орексина при ожирении». iScience. 20: 1–13. Дои:10.1016 / j.isci.2019.09.003. ЧВК 6817686. PMID 31546102.
- ^ Шерин Дж. Э., Элмквист Дж., Торреальба Ф., Сапер CB (июнь 1998 г.). «Иннервация гистаминергических туберомаммиллярных нейронов ГАМКергическими и галанинергическими нейронами в вентролатеральном преоптическом ядре крысы». Журнал неврологии. 18 (12): 4705–21. Дои:10.1523 / JNEUROSCI.18-12-04705.1998. ЧВК 6792696. PMID 9614245.
- ^ Лу Дж., Бьоркум А.А., Сюй М., Гаус С.Е., Широмани П.Дж., Сапер С.Б. (июнь 2002 г.). «Избирательная активация расширенного вентролатерального преоптического ядра во время сна с быстрым движением глаз». Журнал неврологии. 22 (11): 4568–76. ЧВК 6758802. PMID 12040064.
- ^ Линь Л., Фарако Дж., Ли Р., Кадотани Х., Роджерс В., Линь Икс, Цю Х, де Йонг П. Дж., Нишино С., Миньот Е. (август 1999 г.). «Нарколепсия собак, вызванная нарушением сна, вызвана мутацией в гене рецептора 2 гипокретина (орексина)». Клетка. 98 (3): 365–76. Дои:10.1016 / S0092-8674 (00) 81965-0. PMID 10458611. S2CID 902666.
- ^ Чемелли Р.М., Уилли Дж. Т., Синтон К. М., Элмквист Дж. К., Скаммелл Т., Ли С., Ричардсон Дж. А., Уильямс С. К., Сюн Й., Кисануки И., Fitch TE, Наказато М., Хаммер Р. Э., Сапер С. Б., Янагисава М. (август 1999 г.). «Нарколепсия у мышей с нокаутом орексина: молекулярная генетика регуляции сна». Клетка. 98 (4): 437–51. Дои:10.1016 / S0092-8674 (00) 81973-X. PMID 10481909. S2CID 89799178.
- ^ Мочизуки Т., Крокер А., Маккормак С., Янагисава М., Сакураи Т., Скаммелл Т.Э. (июль 2004 г.). «Нестабильность поведенческого состояния у мышей с нокаутом орексина». Журнал неврологии. 24 (28): 6291–300. Дои:10.1523 / JNEUROSCI.0586-04.2004. ЧВК 6729542. PMID 15254084.
- ^ Алексис Мадригал (2007-12-28). «Нюхание химического вещества в мозгу может заменить сон». Wired News, Condé Nast. Получено 2008-02-05.
- ^ Deadwyler SA, Porrino L, Siegel JM, Hampson RE (декабрь 2007 г.). «Системная и назальная доставка орексина-А (гипокретина-1) снижает влияние недосыпания на когнитивные функции у нечеловеческих приматов». Журнал неврологии. 27 (52): 14239–47. Дои:10.1523 / JNEUROSCI.3878-07.2007. ЧВК 6673447. PMID 18160631.
- ^ Кляйн Дж., Сато А. (сентябрь 2000 г.). «Система HLA. Вторая из двух частей». Медицинский журнал Новой Англии. 343 (11): 782–6. Дои:10.1056 / NEJM200009143431106. PMID 10984567.
- ^ Халлмайер Дж., Фарако Дж., Лин Л., Хессельсон С., Винкельманн Дж., Кавашима М., Майер Дж., Плацци Дж., Невсималова С., Бурджин П., Хонг СК, Хонг СС, Хонда Й, Хонда М, Хёгль Б., Лонгстрет В. Т., Монплезир Дж. , Kemlink D, Einen M, Chen J, Musone SL, Akana M, Miyagawa T., Duan J, Desautels A, Erhardt C, Hesla PE, Poli F, Frauscher B, Jeong JH, Lee SP, Ton TG, Kvale M, Kolesar L, Dobrovolná M, Nepom GT, Salomon D, Wichmann HE, Rouleau GA, Gieger C, Levinson DF, Gejman PV, Meitinger T, Young T, Peppard P, Tokunaga K, Kwok PY, Risch N, Mignot E (июнь 2009 г.) . «Нарколепсия прочно связана с альфа-локусом Т-клеточного рецептора». Природа Генетика. 41 (6): 708–11. Дои:10,1038 / нг.372. ЧВК 2803042. PMID 19412176.
- ^ «Нарколепсия - это аутоиммунное заболевание, - говорит исследователь из Стэнфорда».. EurekAlert. Американская ассоциация развития науки. 2009-05-03. Получено 2009-05-31.
- ^ Бэрд Дж. П., Чоу А., Лавленд Дж. Л., Бек Дж., Махони К. Э., Лорд Дж. С., Григг Л. А. (март 2009 г.). «Гиперфагия орексина-А: участие заднего мозга в ответных реакциях на питание». Эндокринология. 150 (3): 1202–16. Дои:10.1210 / en.2008-0293. ЧВК 2654731. PMID 19008313.
- ^ Ида Т., Накахара К., Катаяма Т., Мураками Н., Накадзато М. (март 1999 г.). «Эффект латеральной церебровентрикулярной инъекции нейропептида, стимулирующего аппетит, орексина и нейропептида Y, на различные поведенческие активности крыс». Исследование мозга. 821 (2): 526–9. Дои:10.1016 / S0006-8993 (99) 01131-2. PMID 10064841. S2CID 39775146.
- ^ Цунэки Х., Вада Т., Сасаока Т. (март 2010 г.). «Роль орексина в регуляции гомеостаза глюкозы». Acta Physiologica. 198 (3): 335–48. Дои:10.1111 / j.1748-1716.2009.02008.x. PMID 19489767. S2CID 23346403.
- ^ Brisbare-Roch C, Dingemanse J, Koberstein R, Hoever P, Aissaoui H, Flores S, Mueller C, Nayler O, van Gerven J, de Haas SL, Hess P, Qiu C, Buchmann S, Scherz M, Weller T., Fischli W, Clozel M, Jenck F (февраль 2007 г.). «Улучшение сна путем воздействия на систему орексина у крыс, собак и людей». Природа Медицина. 13 (2): 150–5. Дои:10,1038 / нм 1544. PMID 17259994. S2CID 40999737.
- ^ Сакураи Т. (март 2007 г.). «Нейронная цепь орексина (гипокретина): поддержание сна и бодрствования». Обзоры природы. Неврология. 8 (3): 171–81. Дои:10.1038 / номер 2092. PMID 17299454. S2CID 8932862.
- ^ Инуцука А., Яманака А. (2013-03-06). «Физиологическая роль нейронов орексина / гипокретина в регуляции сна / бодрствования и нейроэндокринных функций». Границы эндокринологии. 4 (18): 18. Дои:10.3389 / fendo.2013.00018. ЧВК 3589707. PMID 23508038.
- ^ «Нейротрансмиттер орексин, связанный с путями получения удовольствия и вознаграждения в мозгу». ScienceDaily. Получено 2018-05-08.
- ^ Харрис Г.К., Виммер М., Астон-Джонс Г. (сентябрь 2005 г.). «Роль латеральных нейронов орексина гипоталамуса в поиске вознаграждения». Природа. 437 (7058): 556–9. Дои:10.1038 / природа04071. PMID 16100511. S2CID 4386257.
- ^ Смит Р.Дж., см. RE, Aston-Jones G (август 2009 г.). «Передача сигналов орексина / гипокретина на рецепторе орексина 1 регулирует поиск кокаина, вызванный сигналом». Европейский журнал нейробиологии. 30 (3): 493–503. Дои:10.1111 / j.1460-9568.2009.06844.x. ЧВК 2771107. PMID 19656173.
- ^ Хелен Путтик (26 декабря 2006 г.). «Надежда в борьбе с алкоголизмом». Вестник. Архивировано из оригинал на 2012-02-10. Получено 2007-02-11.
- ^ Лоуренс А.Дж., Коуэн М.С., Ян Х.Дж., Чен Ф., Олдфилд Б. (июль 2006 г.). «Орексиновая система регулирует поиск алкоголя у крыс». Британский журнал фармакологии. 148 (6): 752–9. Дои:10.1038 / sj.bjp.0706789. ЧВК 1617074. PMID 16751790.
- ^ «Блокирование нейропептидного рецептора снижает никотиновую зависимость». ScienceDaily LLC. 2008-12-01. Получено 2009-02-11.
- ^ Ху С.Ю., МакНалли Г.П., Клеменс К.Дж. (2017). «Двойной антагонист рецептора орексина TCS1102 не влияет на возобновление поиска никотина». PLOS ONE. 12 (3): e0173967. Дои:10.1371 / journal.pone.0173967. ЧВК 5351999. PMID 28296947.
- ^ Skrzypski M, T Le T, Kaczmarek P, Pruszynska-Oszmalek E, Pietrzak P, Szczepankiewicz D, Kolodziejski PA, Sassek M, Arafat A, Wiedenmann B, Nowak KW, Strowski MZ (июль 2011 г.). «Орексин A стимулирует захват глюкозы, накопление липидов и секрецию адипонектина адипоцитами 3T3-L1 и изолированными первичными адипоцитами крысы». Диабетология. 54 (7): 1841–52. Дои:10.1007 / s00125-011-2152-2. PMID 21505958.
- ^ Блуин А.М., Фрид I, Уилсон К.Л., Стаб Р.Дж., Бенке Э.Дж., Лам Х.А., Мейдмент Н.Т., Карлссон Ко, Лапьер Дж. Л., Сигель Дж. «Уровни человеческого гипокретина и меланин-концентрирующего гормона связаны с эмоциями и социальным взаимодействием». Nature Communications. 4: 1547. Дои:10.1038 / ncomms2461. ЧВК 3595130. PMID 23462990. Сложить резюме – Science Daily.
- ^ Acuna-Goycolea C, Li Y, Van Den Pol AN (март 2004 г.). «Метаботропные рецепторы глутамата группы III поддерживают тоническое ингибирование возбуждающего синаптического входа в нейроны гипокретина / орексина». Журнал неврологии. 24 (12): 3013–22. Дои:10.1523 / JNEUROSCI.5416-03.2004. ЧВК 6729849. PMID 15044540.
- ^ Флорес А., Мальдонадо Р., Беррендеро Ф. (декабрь 2013 г.). «Перекрестный разговор между каннабиноидом и гипокретином в центральной нервной системе: что мы знаем до сих пор». Границы неврологии. 7: 256. Дои:10.3389 / fnins.2013.00256. ЧВК 3868890. PMID 24391536.
Прямое взаимодействие CB1-HcrtR1 было впервые предложено в 2003 г. (Hilairet et al., 2003). Действительно, 100-кратное увеличение активности гипокретина-1 для активации передачи сигналов ERK наблюдалось, когда CB1 и HcrtR1 были совместно экспрессированы ... В этом исследовании более высокая эффективность гипокретина-1 в регулировании гетеромера CB1-HcrtR1 по сравнению с с гомомером HcrtR1-HcrtR1 (Ward et al., 2011b). Эти данные позволяют однозначно идентифицировать гетеромеризацию CB1-HcrtR1, которая оказывает существенное функциональное влияние. ... Существование перекрестной связи между гипокретинергической и эндоканнабиноидной системами убедительно подтверждается их частично перекрывающимся анатомическим распределением и общей ролью в нескольких физиологических и патологических процессах. Однако мало что известно о механизмах, лежащих в основе этого взаимодействия.
• Рисунок 1: Схема экспрессии CB1 мозга и орексинергических нейронов, экспрессирующих OX1 или OX2
• Рисунок 2: Синаптические сигнальные механизмы в каннабиноидных и орексиновых системах.
• Рисунок 3: Схема мозговых путей, участвующих в приеме пищи. - ^ Томпсон, доктор медицины, Хаард Х, Сакурай Т., Райнеро И., Кукконен Дж. П. (2014). «Фармакогенетика рецепторов орексина / гипокретина OX1 и OX2». Границы неврологии. 8: 57. Дои:10.3389 / fnins.2014.00057. ЧВК 4018553. PMID 24834023.
Было высказано предположение, что димеризация OX1-CB1 сильно усиливает передачу сигналов рецептора орексина, но вероятное объяснение усиления сигнала вместо этого предлагается способностью передачи сигналов рецептора OX1 продуцировать 2-арахидоноилглицерин, лиганд рецептора CB1, и последующий со- передача сигналов рецепторов (Haj-Dahmane, Shen, 2005; Turunen et al., 2012; Jäntti et al., 2013). Однако это не исключает димеризации.
- ^ Янтти М.Х., Мандрика I, Кукконен Дж.П. (март 2014 г.). «Рецепторы орексина / гипокретина человека образуют конститутивные гомо- и гетеромерные комплексы друг с другом и с каннабиноидными рецепторами CB1 человека». Сообщения о биохимических и биофизических исследованиях. 445 (2): 486–90. Дои:10.1016 / j.bbrc.2014.02.026. PMID 24530395.
Подтипы рецепторов орексина легко образуют гомо- и гетеро (ди) меры, о чем свидетельствуют значимые сигналы BRET. Рецепторы CB1 образуют гомодимеры, а также гетеродимеризуются с обоими рецепторами орексина. ... В заключение, рецепторы орексина имеют значительную склонность к образованию гомо- и гетероди / олигомерных комплексов. Однако неясно, влияет ли это на их передачу сигналов. Поскольку рецепторы орексина эффективно передают сигнал через продукцию эндоканнабиноидов рецепторам CB1, димеризация может быть эффективным способом образования сигнальных комплексов с оптимальными концентрациями каннабиноидов, доступных для рецепторов каннабиноидов.
- ^ Лю ZW, Гао XB (январь 2007 г.). «Аденозин подавляет активность нейронов гипокретина / орексина посредством рецептора A1 в боковом гипоталамусе: возможно, стимулирующий сон эффект». Журнал нейрофизиологии. 97 (1): 837–48. Дои:10.1152 / ян.00873.2006. ЧВК 1783688. PMID 17093123.
- ^ Оно К., Хондо М., Сакураи Т. (март 2008 г.). «Холинергическая регуляция нейронов орексина / гипокретина через М (3) мускариновый рецептор у мышей». Журнал фармакологических наук. 106 (3): 485–91. Дои:10.1254 / jphs.FP0071986. PMID 18344611.
- ^ Мураки Ю., Яманака А., Цуджино Н., Килдафф Т.С., Гото К., Сакураи Т. (август 2004 г.). «Серотонинергическая регуляция нейронов орексина / гипокретина через рецептор 5-HT1A». Журнал неврологии. 24 (32): 7159–66. Дои:10.1523 / JNEUROSCI.1027-04.2004. ЧВК 6729168. PMID 15306649.
- ^ Fu LY, Acuna-Goycolea C, van den Pol AN (октябрь 2004 г.). «Нейропептид Y подавляет нейроны гипокретина / орексина с помощью множества пресинаптических и постсинаптических механизмов: тоническая депрессия системы возбуждения гипоталамуса». Журнал неврологии. 24 (40): 8741–51. Дои:10.1523 / JNEUROSCI.2268-04.2004. ЧВК 6729969. PMID 15470140.
- ^ Цудзино Н., Яманака А., Итики К., Мураки Ю., Килдафф Т. С., Ягами К., Такахаши С., Гото К., Сакураи Т. (август 2005 г.). «Холецистокинин активирует нейроны орексина / гипокретина через рецептор холецистокинина А». Журнал неврологии. 25 (32): 7459–69. Дои:10.1523 / JNEUROSCI.1193-05.2005. ЧВК 6725310. PMID 16093397.
- ^ Li Y, van den Pol AN (январь 2005 г.). «Прямое и косвенное ингибирование катехоламинами гипокретиновых / орексиновых нейронов». Журнал неврологии. 25 (1): 173–83. Дои:10.1523 / JNEUROSCI.4015-04.2005. ЧВК 6725201. PMID 15634779.
- ^ Яманака А., Мураки Ю., Итики К., Цуджино Н., Килдафф Т.С., Гото К., Сакураи Т. (июль 2006 г.). «Орексиновые нейроны прямо и косвенно регулируются катехоламинами сложным образом». Журнал нейрофизиологии. 96 (1): 284–98. CiteSeerX 10.1.1.320.260. Дои:10.1152 / ян.01361.2005. PMID 16611835.
- ^ Оно К., Сакураи Т. (январь 2008 г.). «Орексин нейронная схема: роль в регуляции сна и бодрствования». Границы нейроэндокринологии. 29 (1): 70–87. Дои:10.1016 / j.yfrne.2007.08.001. PMID 17910982. S2CID 7888110.
- ^ Бернард Р., Лидик Р., Багдоян Х.А. (октябрь 2003 г.). «Гипокретин-1 вызывает активацию G-белка и увеличивает высвобождение ACh в мостах крысы» (PDF). Европейский журнал нейробиологии. 18 (7): 1775–85. Дои:10.1046 / j.1460-9568.2003.02905.x. HDL:2027.42/75751. PMID 14622212. S2CID 18515164.
- ^ Фредерик-Дуус Д., Гайтон М.Ф., Фадель Дж. (Ноябрь 2007 г.). «Повышение выработки кортикального ацетилхолина, вызванное пищей, требует передачи орексина». Неврология. 149 (3): 499–507. Дои:10.1016 / j.neuroscience.2007.07.061. PMID 17928158. S2CID 19452926.
- ^ Соффин Е.М., Гилл СН, Бро С.Дж., Джерман Дж.С., Дэвис СН (июнь 2004 г.). «Фармакологическая характеристика подтипа рецептора орексина, опосредующего постсинаптическое возбуждение в ядре дорсального шва крысы». Нейрофармакология. 46 (8): 1168–76. Дои:10.1016 / j.neuropharm.2004.02.014. PMID 15111023. S2CID 45872346.
- ^ Aston-Jones G, Smith RJ, Sartor GC, Moorman DE, Massi L, Tahsili-Fahadan P, Richardson KA (февраль 2010 г.). «Боковые нейроны орексина / гипокретина гипоталамуса: роль в поиске вознаграждения и зависимости». Исследование мозга. 1314: 74–90. Дои:10.1016 / j.brainres.2009.09.106. ЧВК 2819557. PMID 19815001.
- ^ Гримальди Д., Сильвани А., Бенарроч Е. Е., Кортелли П. (январь 2014 г.). «Система орексин / гипокретин и вегетативный контроль: новые идеи и клинические корреляции». Неврология. 82 (3): 271–8. Дои:10.1212 / WNL.0000000000000045. PMID 24363130. S2CID 9209963.
- ^ Вентура, Джефф, изд. (2014-08-31). «FDA одобрило новый вид снотворного - Белсомра». Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA). Получено 2015-10-31.
- ^ «БЕЛСОМРА® (суворексант) С-IV». Белсомра. Получено 2015-10-31.
- ^ «Роль системы рецепторов орексина в стрессе, сне и употреблении кокаина (NCT02785406)». ClinicalTrials.gov. Получено 2017-07-08.
- ^ Никсон Дж. П., Маванджи В., Баттерик Т. А., Биллингтон С. Дж., Коц С. М., Теске Дж. А. (март 2015 г.). «Нарушения сна, ожирение и старение: роль орексина». Обзоры исследований старения. 20: 63–73. Дои:10.1016 / j.arr.2014.11.001. ЧВК 4467809. PMID 25462194.
- ^ Бильярд М (июнь 2008 г.). «Нарколепсия: современные варианты лечения и будущие подходы». Психоневрологические заболевания и лечение. 4 (3): 557–66. ЧВК 2526380. PMID 18830438.
- ^ Ариас-Каррион О, Мурильо-Родригес Э., Сюй М., Бланко-Центурион С., Друкер-Колин Р., Широмани П.Дж. (декабрь 2004 г.). «Трансплантация гипокретиновых нейронов в ретикулярную формацию моста: предварительные результаты» (PDF). Спать. 27 (8): 1465–70. Дои:10.1093 / сон / 27.8.1465. ЧВК 1201562. PMID 15683135. Архивировано из оригинал (PDF) на 03.03.2016.
внешняя ссылка
- орексины в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Сравните разные снотворные, Национальный фонд сна
- Антагонисты рецепторов орексина: новый класс снотворных, Национальный фонд сна
