Хлористый водород - Hydrogen chloride
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Хлористый водород[1] | |||
| Другие имена Газообразная соляная кислота Соляной газ | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| 1098214 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.028.723 | ||
| Номер ЕС |
| ||
| 322 | |||
| КЕГГ | |||
| MeSH | Соляная + кислота | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1050 | ||
| |||
| |||
| Характеристики | |||
| HCl | |||
| Молярная масса | 36,46 г / моль | ||
| Внешность | Бесцветный газ | ||
| Запах | острый; острый и жгучий | ||
| Плотность | 1,49 г / л[2] | ||
| Температура плавления | -114,22 ° С (-173,60 ° F, 158,93 К) | ||
| Точка кипения | -85,05 ° С (-121,09 ° F, 188,10 К) | ||
| 823 г / л (0 ° С) 720 г / л (20 ° С) 561 г / л (60 ° С) | |||
| Растворимость | растворим в метанол, этиловый спирт, эфир | ||
| Давление газа | 4352 кПа (при 21,1 ° C)[3] | ||
| Кислотность (пKа) | −3.0;[4] −5.9 (±0.4)[5] | ||
| Основность (пKб) | 17.0 | ||
| Конъюгированная кислота | Хлороний | ||
| Основание конъюгата | Хлористый | ||
| 1.0004456 (газ) 1,254 (жидкость) | |||
| Вязкость | 0,311 сП (-100 ° С) | ||
| Структура | |||
| линейный | |||
| 1.05 D | |||
| Термохимия | |||
Теплоемкость (C) | 0,7981 Дж / (К · г) | ||
Стандартный моляр энтропия (S | 186,902 Дж / (К · моль) | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | −92,31 кДж / моль | ||
Станд. Энтальпия горение (ΔcЧАС⦵298) | -95,31 кДж / моль | ||
| Фармакология | |||
| A09AB03 (ВОЗ) B05XA13 (ВОЗ) | |||
| Опасности | |||
| Паспорт безопасности | Паспорт безопасности данных JT Baker | ||
| Пиктограммы GHS |   | ||
| Сигнальное слово GHS | Опасность | ||
| H280, H314, H331 | |||
| P261, P280, P305 + 351 + 338, P310, P410 + 403 | |||
| NFPA 704 (огненный алмаз) | |||
| Смертельная доза или концентрация (LD, LC): | |||
LD50 (средняя доза ) | 238 мг / кг (крыса, перорально) | ||
LC50 (средняя концентрация ) | 3124 частей на миллион (крыса, 1час ) 1108 частей на миллион (мышь, 1 ч)[7] | ||
LCLo (самый низкий опубликованный ) | 1300 частей на миллион (человек, 30мин ) 4416 частей на миллион (кролик, 30 мин) 4416 частей на миллион (морская свинка, 30 мин) 3000 частей на миллион (человек, 5 мин)[7] | ||
| NIOSH (Пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | C 5 частей на миллион (7 мг / м3)[6] | ||
REL (Рекомендуемые) | C 5 частей на миллион (7 мг / м3)[6] | ||
IDLH (Непосредственная опасность) | 50 частей на миллион[6] | ||
| Родственные соединения | |||
Родственные соединения | Фтористый водород Бромистый водород Йодистый водород Водородный астатид | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
В сложный хлористый водород имеет химическая формула ЧАСCl и как таковой галогенид водорода. В комнатная температура, это бесцветный газ, который образует белые пары соляная кислота при контакте с атмосферным водяной пар. Газообразный хлористый водород и соляная кислота важны в технологии и промышленности. Соляная кислота, водный раствор хлористого водорода, также обычно дают формулу HCl.
Реакции

Хлороводород - это двухатомная молекула, состоящий из водород атом H и a хлор атом Cl, связанный полярная ковалентная связь. Атом хлора намного больше электроотрицательный чем атом водорода, что делает эту связь полярной. Следовательно, молекула имеет большой дипольный момент с отрицательным частичная оплата (δ−) у атома хлора и положительный частичный заряд (δ +) у атома водорода.[8] Отчасти из-за своей высокой полярности HCl очень растворимый в воды (и в других полярных растворители ).
При контакте, H2O и HCl объединяются с образованием гидроксоний катионы ЧАС3О+ и хлористый анионы Cl− через обратимый химическая реакция:
- HCl + H2O → H3О+ + Cl−
Полученное решение называется соляная кислота и является сильная кислота. В кислотная диссоциация или константа ионизации, Kа, является большим, что означает, что HCl практически полностью диссоциирует или ионизируется в воде. Даже в отсутствие воды хлористый водород может действовать как кислота. Например, хлористый водород может растворяться в некоторых других растворителях, таких как метанол и протонировать молекулы или ионы, а также могут служить кислотойкатализатор для химических реакций, где безводный (безводные) условия желательны.
- HCl + CH3ОН → СН3О+ЧАС2 + Cl−
Из-за своей кислой природы хлористый водород коррозионное вещество, особенно в присутствии влаги.
Структура и свойства
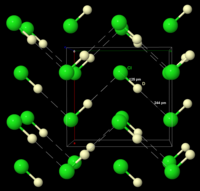

Замороженная HCl претерпевает фазовый переход при 98,4 К. Порошковая дифракция рентгеновских лучей замороженного материала показывает, что материал изменяется от ромбический структура к кубический один во время этого перехода. В обеих структурах атомы хлора находятся в гранецентрированный массив. Однако определить местонахождение атомов водорода не удалось.[9] Анализ спектроскопических и диэлектрических данных, а также определение структуры DCl (хлорида дейтерия) показывает, что HCl образует зигзагообразные цепочки в твердом теле, как и HF (см. рисунок справа).[10]
| Температура (° C) | 0 | 20 | 30 | 50 |
|---|---|---|---|---|
| Вода | 823 | 720 | 673 | 596 |
| Метанол | 513 | 470 | 430 | |
| Этиловый спирт | 454 | 410 | 381 | |
| Эфир | 356 | 249 | 195 |


В инфракрасный спектр газообразного хлористого водорода, показанный слева, состоит из ряда резких линий поглощения, сгруппированных около 2886 см−1 (длина волны ~ 3,47 мкм). При комнатной температуре практически все молекулы находятся в основном колебательном состоянии. v = 0. С учетом ангармонизма колебательную энергию можно записать как.
Для продвижения молекулы HCl из v = 0 в v = 1, мы ожидаем увидеть инфракрасное поглощение около νо = νе + 2Иксеνе = 2880 см−1. Однако это поглощение, соответствующее Q-ветви, не наблюдается из-за его запрета по симметрии. Вместо этого видны два набора сигналов (P- и R-ветви) из-за одновременного изменения вращательного состояния молекул. Из-за квантово-механических правил отбора разрешены только определенные вращательные переходы. Состояния характеризуются вращательным квантовым числом J = 0, 1, 2, 3, ... правила выбора гласят, что ΔJ может принимать только значения ± 1.
Значение вращательной постоянной B намного меньше колебательного νо, так что для вращения молекулы требуется гораздо меньшее количество энергии; для типичной молекулы это находится в микроволновом диапазоне. Однако колебательная энергия молекулы HCl помещает свое поглощение в инфракрасную область, что позволяет легко собирать спектр, показывающий колебательные переходы этой молекулы, используя инфракрасный спектрометр с газовой ячейкой. Последний может быть даже изготовлен из кварца, так как поглощение HCl находится в окне прозрачности для этого материала.
Обильный хлор состоит из двух изотопов: 35Cl и 37Cl в соотношении приблизительно 3: 1. Хотя пружинные постоянные почти идентичны, разнородные уменьшенные массы из H35Cl и H37Cl вызывает измеримые различия во вращательной энергии, поэтому при внимательном рассмотрении каждой линии поглощения наблюдаются дублеты, взвешенные в том же соотношении 3: 1.
Производство
Большая часть хлористого водорода, производимого в промышленных масштабах, используется для соляная кислота производство.[12]
Прямой синтез
Очень чистый хлористый водород получают путем объединения хлор и водород:
- Cl2 + H2 → 2 HCl
Поскольку реакция экзотермический, установка называется HCl печь или горелка HCl. Образующийся газообразный хлористый водород поглощен в деионизированная вода, в результате чего получается химически чистая соляная кислота. Эта реакция может дать очень чистый продукт, например для использования в пищевой промышленности.
Органический синтез
Промышленное производство хлористого водорода часто объединяют с образованием хлорированный и фторированный органический соединения, например, Тефлон, Фреон, и другие ХФУ, а также хлоруксусная кислота и ПВХ. Часто это производство соляной кислоты совмещается с ее использованием на месте. в химические реакции, водород атомы на углеводороде замещаются атомами хлора, после чего освобожденный атом водорода рекомбинирует с запасным атомом молекулы хлора, образуя хлористый водород. Фторирование - это последующая реакция замещения хлора, снова производящая хлористый водород:
- R − H + Cl2 → R − Cl + HCl
- R − Cl + HF → R − F + HCl
Образующийся хлористый водород либо используется повторно, либо поглощается водой, в результате чего получается соляная кислота технического или промышленного класса.
Лабораторные методы
Небольшие количества хлористого водорода для лабораторного использования могут образовываться в Генератор HCl путем дегидратации соляной кислоты либо серная кислота или безводный хлорид кальция. В качестве альтернативы HCl можно получить реакцией серной кислоты с хлоридом натрия:[13]
- NaCl + H2ТАК4 → NaHSO4 + HCl
Эта реакция происходит при комнатной температуре. При условии, что в генераторе остается NaCl и он нагревается выше 200 ° C, реакция протекает дальше:
- NaCl + NaHSO4 → HCl + Na2ТАК4
Для работы таких генераторов реагенты должны быть сухими.
Хлористый водород также может быть получен гидролиз некоторых реактивных хлоридных соединений, таких как хлориды фосфора, тионилхлорид (SOCl2), и ацилхлориды. Например, холодную воду можно постепенно капать на пентахлорид фосфора (PCl5) для получения HCl:
- PCl5 + H2O → POCl3 + 2 HCl
Приложения
Большая часть хлористого водорода используется в производстве соляной кислоты. Это также важный реагент в других промышленных химических превращениях, например:
- Гидрохлорирование резины
- Производство винил- и алкилхлоридов
В полупроводниковой промышленности он используется как для травления полупроводниковых кристаллов, так и для очистки кремний через трихлорсилан (SiHCl3).
История
Алхимики из Средний возраст узнал, что соляная кислота (тогда известная как дух соли или же Acidum Salis) выделяется парообразный хлористый водород, который получил название морской кислотный воздух. В 17 веке Иоганн Рудольф Глаубер использованная соль (хлорид натрия ) и серная кислота для подготовки сульфат натрия, выделяя газообразный хлористый водород (см. производство выше). В 1772 г. Карл Вильгельм Шееле также сообщил об этой реакции и иногда приписывают ее открытие. Джозеф Пристли приготовил хлористый водород в 1772 г., а в 1810 г. Хэмфри Дэви установлено, что он состоит из водород и хлор.[14]
Вовремя Индустриальная революция, спрос на щелочной такие вещества как кальцинированной соды увеличился, и Николя Леблан разработал новый промышленный процесс производства кальцинированной соды. в Процесс Леблана, соль была преобразована в кальцинированную соду с использованием серной кислоты, известняка и угля, с получением хлористого водорода в качестве побочного продукта. Первоначально этот газ выпускался в воздух, но Щелочной акт 1863 г. запретил такой выпуск, поэтому производители кальцинированной соды абсорбировали отработанный газ HCl в воде, производя соляную кислоту в промышленных масштабах. Позже Процесс Харгривза был разработан, который похож на процесс Леблана, за исключением диоксид серы, вода и воздух используются вместо серной кислоты в реакции, которая в целом является экзотермической. В начале 20 века процесс Леблана был фактически заменен Сольвеевский процесс, который не давал HCl. Однако производство хлористого водорода продолжалось как стадия производства соляной кислоты.
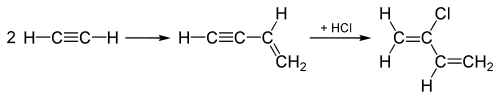
Историческое использование хлористого водорода в 20 веке включает гидрохлорирование алкины в производстве хлорированных мономеры хлоропрен и винилхлорид, которые впоследствии полимеризованный сделать полихлоропрен (Неопрен ) и поливинил хлорид (ПВХ) соответственно. При производстве винилхлорида, ацетилен (C2ЧАС2) гидрохлорируют путем добавления HCl через тройная связь C2ЧАС2 молекула, превращая тройку в двойная связь, давая винилхлорид.
«Ацетиленовый процесс», использовавшийся до 1960-х годов для производства хлоропрен, начинается с объединения двух ацетилен молекул, а затем добавляет HCl к соединенному промежуточному продукту через тройная связь чтобы преобразовать его в хлоропрен, как показано здесь:
Этот «ацетиленовый процесс» был заменен процессом, который добавляет Cl2 к одной из двойных связей в 1,3-бутадиен вместо этого и последующее удаление вместо этого производит HCl, а также хлоропрен.
Безопасность
Хлористый водород образует агрессивную соляную кислоту при контакте с водой, содержащейся в тканях тела. Вдыхание паров может вызвать кашляющий, задыхаясь, воспаление носа, горла и верхних дыхательные пути, а в тяжелых случаях отек легких, сердечно-сосудистая система неудача и смерть. Контакт с кожей может вызвать покраснение, боль, и суровый химические ожоги. Хлористый водород может вызвать серьезные ожоги глаз и необратимые повреждения глаз.
Соединенные штаты. Управление по охране труда и Национальный институт охраны труда и здоровья установили пределы профессионального воздействия хлористого водорода на уровне 5 частей на миллион (7 мг / м3),[15] и собрал обширную информацию о проблемах безопасности на рабочем месте с использованием хлористого водорода.[16]
Смотрите также
- Желудочный сок, соляная кислота секретируется в желудок помочь пищеварение из белки
- Хлористый, соли хлористого водорода
- Гидрохлорид, органические соли соляной кислоты
- Гидрохлорирование, реакция присоединения с алкенами
Рекомендации
- ^ «хлористый водород (CHEBI: 17883)». Химические объекты, представляющие биологический интерес (ChEBI). Великобритания: Европейский институт биоинформатики.
- ^ Хейнс, Уильям М. (2010). Справочник по химии и физике (91 изд.). Бока-Ратон, Флорида, США: CRC Press. п. 4–67. ISBN 978-1-43982077-3.
- ^ Хлористый водород. Газовая энциклопедия. Air Liquide
- ^ Типпинг, Э. (2002) [1]. Издательство Кембриджского университета, 2004.
- ^ Trummal, A .; Губа, L .; Кальюранд, I .; Koppel, I.A .; Лейто, И. "Кислотность сильных кислот в воде и диметилсульфоксиде" J. Phys. Chem. А. 2016, 120, 3663-3669. Дои:10.1021 / acs.jpca.6b02253
- ^ а б c Карманный справочник NIOSH по химической опасности. "#0332". Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б «Хлороводород». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ Ouellette, Роберт Дж .; Рон, Дж. Дэвид (2015). Принципы органической химии. Elsevier Science. С. 6–. ISBN 978-0-12-802634-2.
- ^ Натта, Г. (1933). "Struttura e polimorfismo degli acidi alogenidrici". Gazzetta Chimica Italiana (на итальянском). 63: 425–439.
- ^ Sándor, E .; Фэрроу, Р.Ф.К. (1967). «Кристаллическая структура твердого хлористого водорода и хлорида дейтерия». Природа. 213 (5072): 171–172. Bibcode:1967Натура.213..171С. Дои:10.1038 / 213171a0. S2CID 4161132.
- ^ Соляная кислота - Резюме соединения. Pubchem
- ^ Остин, Северин; Гловацки, Арндт (2000). "Соляная кислота". Энциклопедия промышленной химии Ульмана. Дои:10.1002 / 14356007.a13_283. ISBN 3527306730.
- ^ Франсиско Дж. Арнслиз (1995). «Удобный способ получения хлорида водорода в лаборатории первокурсников». J. Chem. Educ. 72 (12): 1139. Bibcode:1995JChEd..72.1139A. Дои:10.1021 / ed072p1139.
- ^ Хартли, Гарольд (1960). "Лекция Уилкинса. Сэр Хэмфри Дэви, Британская Колумбия, 1778–1829 гг.". Труды Королевского общества А. 255 (1281): 153–180. Bibcode:1960RSPSA.255..153H. Дои:10.1098 / RSPA.1960.0060. S2CID 176370921.
- ^ CDC - Карманный справочник NIOSH по химической опасности
- ^ «Хлористый водород». CDC - Тема безопасности и гигиены труда NIOSH. 5 марта 2012 г.. Получено 15 июля 2016.
внешняя ссылка
- Международная карта химической безопасности 0163
- Темза и Космос Chem C2000 Руководство по эксперименту