Аминорадикал - Amino radical
| |||
| Имена | |||
|---|---|---|---|
| Систематическое название ИЮПАК | |||
| Другие имена Амидоген; Аминильный радикал; Азанил радикал | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
PubChem CID | |||
| |||
| |||
| Характеристики | |||
| NH 2• | |||
| Молярная масса | 16,0226 г моль−1 | ||
| Термохимия | |||
Стандартный моляр энтропия (S | 194,71 Дж К−1 моль−1 | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | 190,37 кДж моль−1 | ||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
В амино- радикальный, •
NH
2, также известный как аминильный радикал или же азанильный радикал, является нейтральной формой амид-ион (NH−
2). Аминилы обладают высокой реакционной способностью и, следовательно, недолговечны. как большинство радикалов; однако они составляют важную часть химии азота. При достаточно высокой концентрации амино-радикалы димеризуются с образованием гидразин. Хотя NH2 как функциональная группа распространено в природа, входящие в состав многих соединений (например, фенэтиламины ) радикал не может быть выделен в свободном виде.[2]
Синтез
Реакция 1: образование аминорадикала из аммиака.
Аминорадикалы могут быть получены реакцией радикала ОН с аммиаком в облученных водных растворах. Эта реакция сформулирована как реакция отвода водорода.[3]
- NH3 + • OH → • NH2 + H2О
Константа скорости (k1) для этой реакции было определено как 1.0 × 108 M−1 s−1, а параллельная реакция OH с NH+
4 оказался намного медленнее. Эта скорость была повторно определена с использованием двух конкурентных методов импульсного радиолиза с ионами бензоата и тиоцианата при pH 11,4. Ценность k1 = (9 + 1) × 107 M−1 s−1 был получен из обеих систем. Находясь в кислом растворе, соответствующая реакция • OH с NH+
4 слишком медленный, чтобы его можно было наблюдать с помощью импульсного радиолиза.
Реакция 2: образование аминорадикала из гидроксиламина.
Аминорадикал также может быть получен реакцией e−(водн.) с NH2ОЙ. В нескольких исследованиях также использовалась окислительно-восстановительная система TiIII—NH2ОН для производства амино-радикалов с использованием спектроскопии электронного парамагнитного резонанса (ЭПР) и полярографии.[3]
- TiIII + NH2OH → TiIV + • NH2 + ОН−
Реакция 3: образование аминорадикала из аммониила.
Восстановление гидроксиламина по e−Предполагается, что (водн.) также образует аминорадикал в следующей реакции.[3]
- •NH+
3 ⇌ • NH2 + H+
Ожидается, что реакционная способность амино-радикала в этой реакции будет зависеть от pH и должна иметь место в области pH 3–7.
Характеристики
Электронные состояния
Аминорадикал имеет два характерных электронных состояния:
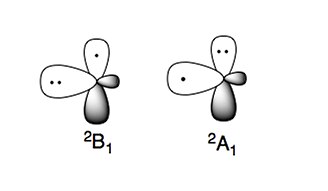
Более стабильное электронное состояние 2B1, где неспаренный электрон находится в п-орбиталь, перпендикулярная плоскости молекулы (радикал π-типа). Электронное состояние высокой энергии, 2А1, имеет два электрона в п-орбитальный и неспаренный электрон в sp2 орбитальный (радикал типа σ).[4][5]
Азотцентрированные соединения, такие как амины, являются нуклеофильный в природе. Этот характер также наблюдается в амино-радикалах, которые можно рассматривать как нуклеофильные.[4][5]
Спектральные свойства
Аминорадикал демонстрирует очень низкое оптическое поглощение только в видимой области (λМаксимум 530 нм, εМаксимум 81 млн−1 s−1), в то время как его поглощение в УФ (<260 нм) похоже на поглощение ОН. В связи с этим непрактично определять скорость реакции амино-радикала с органическими соединениями по распаду амино-радикала.
Реактивность
Обычно аминорадикалы обладают высокой реакционной способностью и недолговечны; однако это не тот случай, когда он реагирует с некоторыми органическими молекулами. Сообщалось об относительной реакционной способности амино-радикала с несколькими органическими соединениями, но абсолютные константы скорости таких реакций остаются неизвестными. В реакции 1 была высказана гипотеза, что аминорадикал может реагировать с NH3 быстрее, чем ОН, и может окисляться NH+
4 для образования амино-радикала в кислых растворах, учитывая, что радикалы являются более сильными окислителями, чем ОН. Чтобы проверить это, использовали сульфатные и фосфатные анион-радикалы. Сульфатный и фосфатный анионы-радикалы медленнее реагируют с NH3 чем амино-радикал, и они реагируют с аммиаком за счет отрыва водорода, а не за счет окисления с переносом электрона.[3]
Когда амино-радикал реагирует с бензоат ионов, константа скорости очень мала и наблюдается только слабое поглощение в УФ-спектрах, что указывает на то, что амино-радикалы не реагируют быстро с бензолом. Фенол с другой стороны, было обнаружено, что он быстрее реагирует с амино-радикалом. В экспериментах при pH 11,3 и 12 с использованием 1,5 M NH3 и варьируя концентрации фенола от 4 до 10 мМ, образование абсорбции феноксильного радикала наблюдали с константой скорости (3 + 0,4) × 106 M−1 s−1. Эта реакция может производить феноксильные радикалы по двум возможным механизмам:[3]
- Добавление в кольцо с последующим удалением NH3, или же
- Окисление прямым переносом электрона

В то время как амино-радикал, как известно, является слабореактивным, процесс рекомбинации двух амино-радикалов с образованием гидразин кажется одним из самых быстрых. В результате он часто конкурирует с другими NH.2 реакции.
- NH2 + NH2 → N2ЧАС4
При низких давлениях эта реакция является наиболее быстрой и, следовательно, основной модой NH2 исчезновение.[6]
Смотрите также
- Амид
- Амин
- Радикал (химия)
- Гидразин (димер)
Рекомендации
- ^ а б «аминил (CHEBI: 29318)». Химические объекты, представляющие биологический интерес (ChEBI). Великобритания: Европейский институт биоинформатики. Имена ИЮПАК.
- ^ die.net. «Амидоген». Архивировано из оригинал 21 февраля 2013 г.. Получено 16 мая, 2012.
- ^ а б c d е ж Neta, P .; Maruthamuthu, P .; Картон, П. М .; Фессенден, Р. В. (1978). «Образование и реакционная способность аминорадикала». Журнал физической химии. 82 (17): 1875–1878. Дои:10.1021 / j100506a004. ISSN 0022-3654.
- ^ а б "Аминорадикал". Интернет-книга NIST по химии. Национальный институт науки и технологий. 2017 г.. Получено 15 июн 2018.
- ^ а б Koenig, T .; Hoobler, J. A .; Klopfenstein, C.E .; Hedden, G .; Sunderman, F .; Рассел Б. Р. (1974). «Электронные конфигурации амид радикалов». Журнал Американского химического общества. 96 (14): 4573–4577. Дои:10.1021 / ja00821a036. ISSN 0002-7863.
- ^ Khe, P. V .; Soulignac, J.C .; Лескло, Р. (1977). «Зависимость константы скорости рекомбинации аминорадикалов от давления и температуры». Журнал физической химии. 81 (3): 210–214. Дои:10.1021 / j100518a006.
дальнейшее чтение
- Дэвис, П. (2008). «Обнаружение амино-радикала NH2 методом лазерной магнитно-резонансной спектроскопии». Журнал химической физики. 62 (9): 3739. Дои:10.1063/1.430970.
- Баттнер, Т. (2005). «Стабильный комплекс металла аминильного радикала». Наука. 307 (5707): 235–8. Bibcode:2005Наука ... 307..235B. Дои:10.1126 / science.1106070. PMID 15653498.
- Джон, Сили (1977). «Зависимость константы скорости реакции HO2 + NO от температуры и давления». Журнал физической химии. 81 (10): 210–214. Дои:10.1021 / jp952553f.
- Кениг, Хублер (1974). «Электронные конфигурации амино радикалов». Журнал Американского химического общества. 96 (14): 4573–4577. Дои:10.1021 / ja00821a036.



